5 липня, 2018
Смертность при применении пероральных антикоагулянтов: данные FDA
Выбор оптимального антикоагулянта, в частности для предупреждения инсульта при фибрилляции предсердий, остается нерешенной проблемой. Инновационные пероральные антикоагулянты (НОАК) дабигатран, ривароксабан, апиксабан, эдоксабан сравнивались с варфарином в нескольких крупных рандомизированных клинических исследованиях, однако сопоставления НОАК между собой практически не проводились. Метаанализ C. T. Ruff и соавт. (2014) продемонстрировал снижение смертности от всех причин на фоне применения НОАК по сравнению с варфарином – относительный риск 0,90 (95% доверительный интервал (ДИ) 0,85-0,95; p<0,001).
Методологические различия не позволяют напрямую сравнивать НОАК, основываясь на результатах разных исследований (RE-LY, ROCKET-AF, ARISTOTLE, ENGAGE), поэтому авторы сопоставили показатели смертности на фоне приема различных НОАК, проанализировав базу нежелательных явлений Управления по контролю за качеством продуктов питания и лекарственных средств (FDA) (FDA Adverse Event Reporting System – FAERS). FAERS – это пассивная система контроля, которая предусматривает добровольное предоставление информации работниками здравоохранения и пациентами, а также обязательные сообщения производителей фармпрепаратов (в т. ч. о нежелательных явлениях, произошедших в ходе клинических испытаний).
В ходе анализа FAERS изучены все сообщения о смерти, ассоциированные с приемом НОАК или варфарина. В исследование было включено 283217 случаев приема НОАК или варфарина, среди них – 34546 (12,2%) смертельных исходов. Данные учитывались, начиная с первой записи о препарате (варфарин – 02.11.1997, дабигатран – 15.03.2005, ривароксабан – 09.10.2007, апиксабан – 21.09.2006, эдоксабан – 21.05.2012) и до 31.12.2015 для всех медикаментов. Если пациент принимал два антикоагулянта, этот случай засчитывался в обе группы, поэтому суммарное количество случаев для всех НОАК (128267) несколько меньше, чем сумма отдельных показателей для дабигатрана, ривароксабана, апиксабана и эдоксабана (129306). Прием варфарина был зафиксирован в >60% проанализированных случаев. Среди НОАК наиболее часто применялся ривароксабан, далее – дабигатран, апиксабан, эдоксабан (в порядке убывания частоты). Авторы указывают, что объем выборки и количество смертей для всех препаратов, кроме относительно недавно внедренного в клиническую практику эдоксабана, более чем достаточен для проведения достоверного анализа.
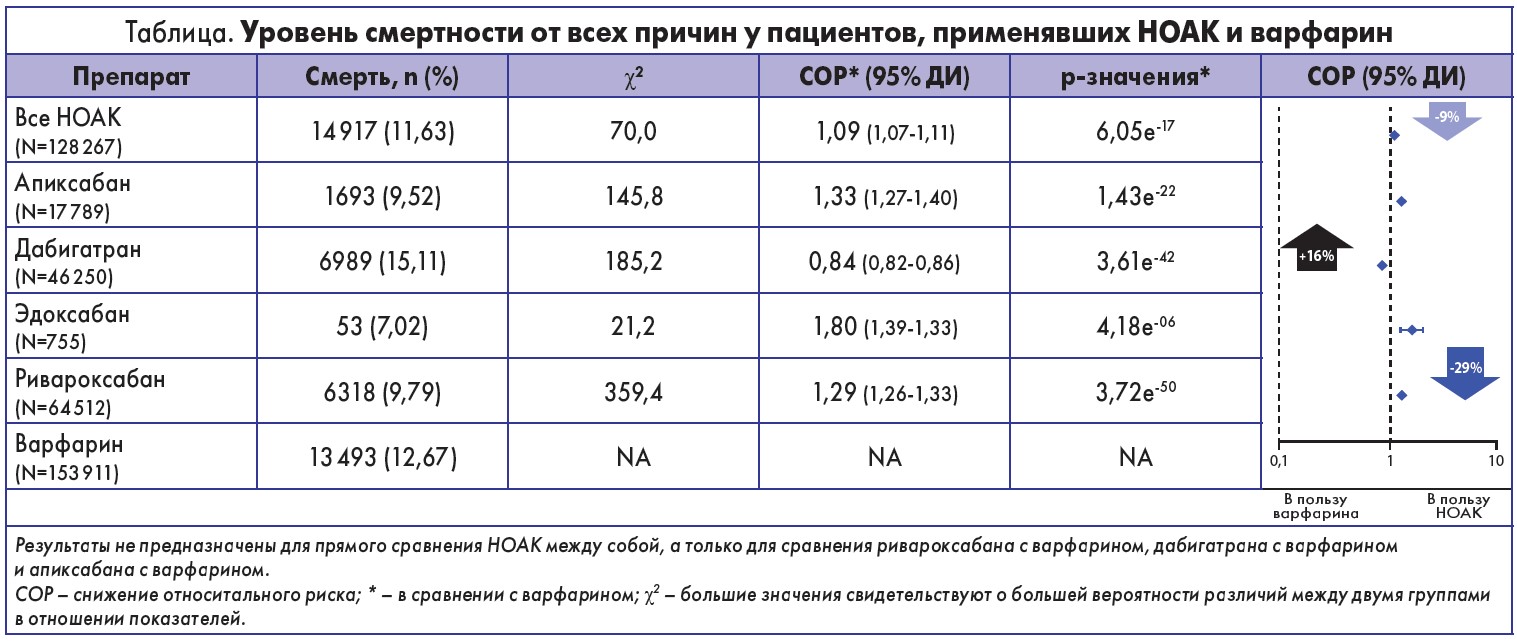
Этот анализ продемонстрировал общее умеренное преимущество от применения НОАК перед варфарином в более низком риске смерти с одним исключением: при сравнении дабигатрана с варфарином и другими НОАК наблюдался непропорционально высокий уровень смертности (табл.). Авторы отметили, что этот результат может быть следствием различий в популяциях участников, принимавших разные НОАК, поэтому необходимо трактовать его крайне осторожно.
Данный анализ касался исключительно показателей смертности по трем причинам: во‑первых, смертность – наиболее важный показатель эффективности любого медикамента в целом и в частности НОАК; во‑вторых, особенности базы FAERS таковы, что об одном случае нежелательного явления могут поступить несколько сообщений, в то время как смертельный случай учитывается лишь однократно; в‑третьих, достоверное снижение риска смерти наблюдалось только в одном исследовании с варфарином без каких-либо сравнений НОАК между собой.
В общем, согласно результатам данного анализа, НОАК превосходят варфарин в отношении смертности, что совпадает с результатами предыдущих метаанализов клинических исследований. Однако авторы обнаружили, что дабигатран связан с непропорционально большим количеством сообщений о смерти в системе FAERS, в то время как ривароксабан, апиксабан и эдоксабан ассоциируются со значительно меньшим риском смерти по сравнению с варфарином.
База данных FAERS позволяет мониторировать исходы в реальной жизни, которые могли не быть представлены в контролированных исследованиях, поскольку последние не всегда могут охватить весь спектр пациентов. Сообщения о нежелательных явлениях в подобных базах позволяют проводить скрининг больших популяций, большого количества препаратов и различных типов неблагоприятных явлений, а также сопоставлять профили безопасности разных медикаментов.
Многие недавние публикации рекомендуют учитывать результаты анализа таких баз данных при принятии решений о выборе лечения. Однако выявленные диспропорции следует трактовать осторожно, поскольку возможны различные нарушения объективности этих показателей. Гипотезы, созданные на основе диспропорций анализа различных препаратов, необходимо проверять более точными методами и лишь тогда внедрять в практику принятия решений.
Тем не менее база данных FAERS обеспечивает реалистичное отображение действия антикоагулянтов в клинических условиях, хотя возможно некоторое искажение, например существование сообщений-дубликатов, характеризующих одни и те же случаи. Что касается летальных показателей, случай смерти можно рассматривать и как нежелательное явление, и как исход (окончательное событие, возникшее вследствие нежелательного явления), поэтому установить причинно-следственную связь крайне тяжело, поскольку сложные обстоятельства каждого отдельного клинического случая редко позволяют четко связать смерть с приемом какого-либо медикамента.
При дальнейших исследованиях следует отдельно анализировать кардиоваскулярные и другие смерти, а также случаи фатальных кровотечений.
Недостатком подобного сравнения является то, что нельзя учесть исходные отличия в популяциях, подлежавших лечению разными НОАК. В связи с этим такие сравнения подходят для создания гипотез, проверка которых требует учета многих других параметров.
Преимущество данного анализа заключается в том, что он был проведен на основе государственной базы данных независимыми специалистами, а также с достаточным для достоверной статистики количеством сообщений о смерти.
Таким образом, значимость преимущества НОАК перед варфарином в отношении риска смерти достаточно велика. Риски летального исхода при приеме НОАК демонстрируют благоприятные тенденции для ингибиторов фактора Xa (ривароксабан, апиксабан, эдоксабан) и неблагоприятные – для прямого ингибитора тромбина дабигатрана. Эти результаты следует интерпретировать с осторожностью, а для лучшего понимания профилей безопасности НОАК необходимы дальнейшие исследования.
Serebruany V., Cherepanov V., Fortmann S. et al. Mortality and oral anticoagulants in the Food and Drug Administration Adverse Event Reporting System. Open Heart 2017; 4: e000629. doi:10.1136.
Перевела с англ. Лариса Стрильчук
Медична газета «Здоров’я України 21 сторіччя» № 11-12 (432-433), червень 2018 р.