18 липня, 2018
Конгрес Асоціації урологів України: акцент на оригінальні вітчизняні дослідження
14-16 червня відбувся черговий конгрес Асоціації урологів України, який став місцем зустрічі провідних практикуючих фахівців країни. Програма та атмосфера заходу не відступали від традиції: були представлені цікаві майстер-класи, велика кількість інформації щодо оперативних технік, школа ендоурології та доповіді зарубіжних спікерів. Надзвичайно інформативною була секція, у ході якої з результатами власних досліджень виступили представники різних наукових шкіл України.
 Так, у своїй доповіді член-кореспондент НАМН України, професор кафедри урології Національної медичної академії післядипломної освіти ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор С.О. Возіанов представив результати дослідження функцій єдиної нирки в пацієнтів із сечокам’яною хворобою (СКХ) на тлі цукрового діабету (ЦД) 2 типу.
Так, у своїй доповіді член-кореспондент НАМН України, професор кафедри урології Національної медичної академії післядипломної освіти ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор С.О. Возіанов представив результати дослідження функцій єдиної нирки в пацієнтів із сечокам’яною хворобою (СКХ) на тлі цукрового діабету (ЦД) 2 типу.
– Актуальність проблеми єдиної нирки полягає в тому, що, незважаючи на впровадження в урологію нових малоінвазивних та органозберігаючих методів хірургічного лікування, рівень нефректомій, які виконуються в більшості випадків у пацієнтів найбільш активного соціального й трудового віку, залишається досить високим. Так, у період з 2014 по 2017 рік в Україні щорічно було виконано близько 3 тис нефректомій. Після такого втручання в нирці, що залишилася, часто виникають пієлонефрит (ПН) (47-89%) і нефролітіаз (12-50%). СКХ нерідко виявляється вже через 1-4 роки після нефректомії, тобто в період функціональної реабілітації єдиної нирки.
Ще одним ускладнюючим фактором, що сприяє розвитку нефролітіазу, є ЦД, поширеність якого в нашій країні за останні 15 років збільшилася на 45,5%, а захворюваність – на 89%. Згідно з дослідженням A.E. Weinberg і співавт. (2014), рівень глікозильованого гемоглобіну (HbA1c) 5,7-6,4% і більше в осіб із ЦД 2 типу підвищує ризик утворення каменів у нирках.
В оригінальному дослідженні, проведеному в Україні, представлені дані обстеження 211 хворих на СКХ, серед них 71 (33%) пацієнт мав єдину набуту нирку, 140 (67%) – дві функціонуючі нирки, а 114 хворих мали супутній ЦД 2 типу, що стало основою в розподілі пацієнтів на 4 групи:
- група 1 – пацієнти з нефролітіазом єдиної нирки та супутнім ЦД 2 типу;
- група 2 – пацієнти з нефролітіазом єдиної нирки;
- група 3 – пацієнти з однобічним нефролітіазом та супутнім ЦД 2 типу;
- група 4 – пацієнти з однобічним нефролітіазом.
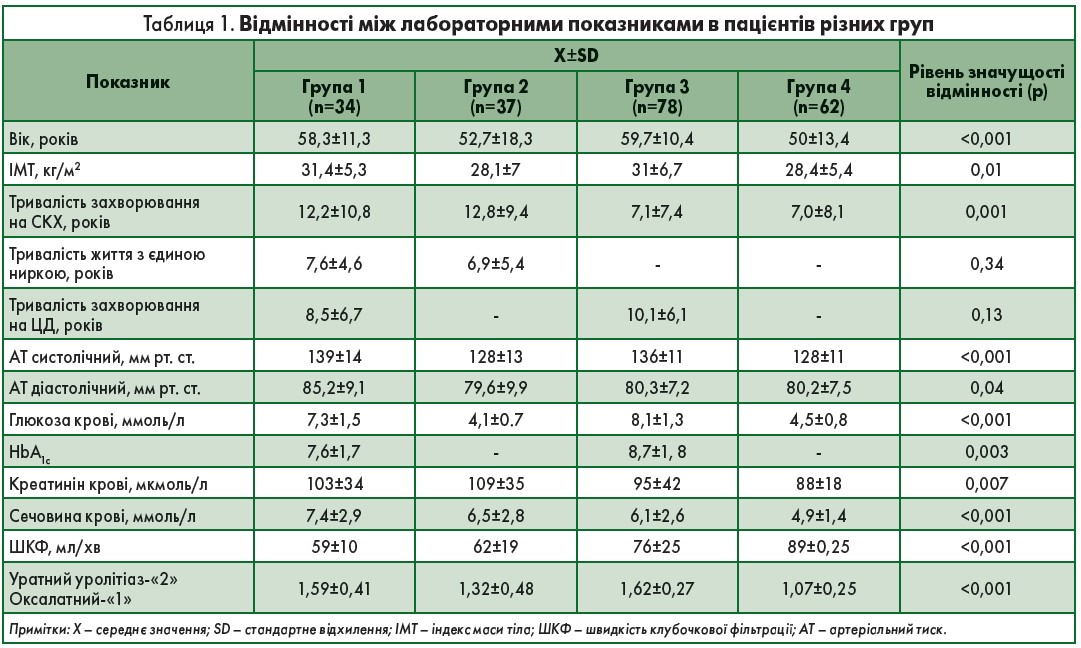
Відмінності між лабораторними показниками у хворих різних груп представлені в таблиці 1.
Також було встановлено, що середньорічна втрата фільтраційної функції нирки при тривалості життя з єдиною набутою ниркою до 10 років склала близько 0,9 мл/хв, на тлі ЦД 2 типу – 1,4 мл/хв на рік, а при тривалості понад 10 років – 1,6 мл/хв і 2,4 мл/хв на рік відповідно.
Різноманіття вже відомих та нових етіологічних чинників захворювань єдиної нирки (ожиріння, гіпертонія, ЦД, гіподинамія, гормональний дисбаланс) показує, що сучасне патогенетичне вирішення проблеми ранньої діагностики та профілактики захворювань єдиної нирки слід шукати тільки на стику різних медичних спеціальностей.
 Про результати ще одного оригінального дослідження, метою якого було з’ясувати питому вагу інфікованості біоматеріалу із сечових та статевих шляхів збудниками різного таксономічного положення у хворих на гострий неускладнений ПН; визначити їхній вплив на клінічний перебіг захворювання, стан місцевого імунітету сечових та статевих шляхів для подальшого обґрунтування персоніфікованої антибактеріальної терапії з впливом на всі джерела інфекції та корекції порушень мукозального імунітету розповів старший науковий співробітник відділу запальних захворювань ДУ «Інститут урології НАМН України» (м. Київ), кандидат медичних наук М.В. Мітчєнко.
Про результати ще одного оригінального дослідження, метою якого було з’ясувати питому вагу інфікованості біоматеріалу із сечових та статевих шляхів збудниками різного таксономічного положення у хворих на гострий неускладнений ПН; визначити їхній вплив на клінічний перебіг захворювання, стан місцевого імунітету сечових та статевих шляхів для подальшого обґрунтування персоніфікованої антибактеріальної терапії з впливом на всі джерела інфекції та корекції порушень мукозального імунітету розповів старший науковий співробітник відділу запальних захворювань ДУ «Інститут урології НАМН України» (м. Київ), кандидат медичних наук М.В. Мітчєнко.
– Нещодавно ми провели власне дослідження з вивчення складу мікрофлори та рівня антибіотикорезистентності у хворих урологічного профілю. У 246 хворих на неускладнений гострий ПН (ГПН) віком від 18 до 49 років проводили забір сечі, сироватки крові, зскрібків зі слизової оболонки сечівника, цервікального каналу, мазків або змивів із піхви. Були проведені клінічні, мікробіологічні (посів на середовища, культурально-ферментативний метод, КФМ), полімеразна ланцюгова реакція, ПЛР), серологічні та імунологічні дослідження.
Згідно з отриманими даними, загальна інфікованість сечових шляхів дорівнювала 91,9%, а статевих – 84,5% (рис.).
Серед молікутів частота виявлення уреаплазми в сечових шляхах склала 63,8% за даними ПЛР та КФМ (50,4% – лише за ПЛР), а мікоплазми – 35,8% (17% – за ПЛР). Схожа картина спостерігалася і при дослідженні статевих шляхів. Поширеність уреаплазми склала 62,6% за даними ПЛР та КФМ (46,9% – лише за ПЛР), а мікоплазми – 31,7% (15,6% – за ПЛР).
Напруженість специфічного імунітету до молікулітів визначалася за титром IgG-антитіл, який у більшості хворих був діагностично значущим та підтверджувався наявністю цих збудників у сечових та статевих шляхах. Первинне інфікування молікутами було зафіксовано у чверті хворих (27,6% та 26,8%), коли антитіла до них не визначалися.
При встановленні кореляції між видом переважного збудника та ступенем тяжкості захворювання було виявлено, що збільшення кількості бактерій та молікутів у структурі мікрофлори погіршує клінічний перебіг ПН, знижуючи показники місцевого імунітету.
Лікування хворих на неускладнений ГПН згідно з протоколом МОЗ України не враховує високий ступінь інфікованості мікоплазмами та уреаплазмами сечових та статевих шляхів. Подальша персистенція цих збудників призводить до погіршення стану місцевого імунітету, що є причинним фактором рецидивного перебігу ПН і підтверджено при подальшому спостереженні за хворими, які не отримували спрямовану протиуреплазмену та протимікоплазмену терапію після атаки ПН. Результати мікробіологічних та імунологічних досліджень стали науковою основою для обґрунтованої розробки та впровадження додаткової терапії, спрямованої на ерадикацію молікутів і корекцію порушень місцевого імунітету сечових і статевих шляхів, що й було виконано та запатентовано дослідниками.
 Катетер-зумовлені інфекції органів сечової та статевої систем в умовах урологічного стаціонару стали темою дослідження, результати якого представив загалу професор кафедри урології і нефрології Одеського національного медичного університету, доктор медичних наук, професор М.І. Ухаль.
Катетер-зумовлені інфекції органів сечової та статевої систем в умовах урологічного стаціонару стали темою дослідження, результати якого представив загалу професор кафедри урології і нефрології Одеського національного медичного університету, доктор медичних наук, професор М.І. Ухаль.
– Катетер-асоційована інфекція у всьому світі є однією з найбільш актуальних проблем охорони здоров’я. Одним із основних завдань Глобального дослідження поширеності нозокоміальної інфекції в урології (Global Prevalence Study on Nosocomial UTI in Urology – GPUI), яке розпочалося в Європі і продовжується в країнах Азії, стало визначення частоти й ролі уретральних катетерів у розвитку нозокоміальних катетер-асоційованих інфекційних запальних процесів органів сечової та статевої систем, а також розробка методів їх профілактики та ефективного лікування.
Найпоширенішими збудниками внутрішньолікарняних інфекцій є P. aeruginosa, Klebsiella spp., Acinetobacter spp., S. aureus, MRSA, Enterococcus spp. та, рідко, Candida spp. Збудники можуть потрапляти в сечовий міхур крізь простір між зовнішньою поверхнею катетера та слизовою оболонкою сечовипускального каналу (найчастіше), заноситися разом із катетером та потрапляти в катетер із відвідних дренажів.
В основі патогенезу лежить адгезія бактерій до слизової оболонки сечового міхура з наступним розмноженням і розвитком бактеріального запалення і формуванням біоплівки на стінці катетера та слизовій оболонці сечового міхура. При спаданні стінка сечового міхура утворює безліч крипт (складок), в яких знижується дезінфікуюча дія сечі та захисного муцина, і саме тут відбувається адгезія бактерій та формування біоплівок. За відсутності самостійного сечовипускання сеча не змиває бактерії з уретри, що створює сприятливі умови для адгезії бактерій із біоплівки катетера і розвитку уретриту.
У поточному дослідженні частоти розвитку катетер-зумовленої інфекції органів сечової та статевої систем в умовах урологічного стаціонару у 65 хворих віком від 58 до 76 років ознаки додаткового інфікування були виявлені у 25 (37,7%) пацієнтів. Тривалість захворювання до моменту госпіталізації коливалася від 3 до 7 днів. У 17 пацієнтів був супутній ЦД. У більшості хворих при поступленні в стаціонар із сечі були висіяні E. coli (76,8%), Enterobacteriaceae (16%), Staphylococcus spp. (4,2%) та Р. mirabilis (3%).
У зв’язку з усуненням обструкції сечових шляхів катетери були негайно видалені. Для ліквідації катетер-зумовленого бактеріального запального процесу наявну антибактеріальну терапію замінили на комбінацію сучасних антибактеріальних препаратів третього покоління – захищений інгібітором β-лактамаз (сульбактамом) цефалоспорин цефоперазон (по 2 г 2 р/день) та амікацина сульфат (по 0,5 г 2 р/день). Тривалість лікування становила 7-8 днів.
Ліквідація обструкції та своєчасне видалення катетерів у комбінації з комплексною антибактеріальною терапією з використанням сучасних антибіотиків дозволило попередити розвиток уросепсису та прогресування інфекційного запалення органів сечової та статевої систем.
 Надзвичайно інформативною була доповідь, присвячена диференційній діагностиці видів гіперкальціурії та її ролі в метафілактиці кальцій-оксалатного нефролітіазу (КОН), яку представив завідувач відділу сечокам’яної хвороби ДУ «Інститут урології НАМН України», доктор медичних наук, професор В.В. Черненко.
Надзвичайно інформативною була доповідь, присвячена диференційній діагностиці видів гіперкальціурії та її ролі в метафілактиці кальцій-оксалатного нефролітіазу (КОН), яку представив завідувач відділу сечокам’яної хвороби ДУ «Інститут урології НАМН України», доктор медичних наук, професор В.В. Черненко.
– Сечокам’яна хвороба посідає одне з лідуючих місць у патології урологічних хворих. Найпоширенішими видами СКХ є КОН (35-70%) та кальцій-фосфатний нефролітіаз (33%). В Україні цей показник становить від 65,4 до 70,2% і має тенденцію до зростання. Важливим моментом є перебіг хвороби протягом наступних 5 років після першого епізоду, тому запобігання рецидивам є однією з ключових цілей у лікуванні СКХ.
Згідно з рекомендаціями Європейської асоціації урологів (EАU) стосовно уролітіазу видалення конкрементів або їх самостійне відходження не призводить до виліковування від СКХ, а лише створює сприятливі умови для ефективної терапії запального рубцево-склеротичного процесу в нирці та сечовивідних шляхах, корекції метаболічних порушень і запобігання рецидивному каменеутворенню.
У всіх випадках первинної діагностики СКХ необхідно проводити аналіз складу конкременту за допомогою достовірного аналітичного метода (дифракції рентгенівських променів або інфрачервоної спектроскопії). Повторний аналіз складу конкременту слід проводити в пацієнтів із:
- рецидивом на тлі медикаментозної профілактики;
- раннім рецидивом після повного видалення конкременту;
- пізнім рецидивом після тривалої відсутності каменів, оскільки склад конкременту може змінитися.
Пацієнтам із резидуальними каменями особливо показана метафілактика СКХ, яка полягає в діагностиці метаболічних порушень, ідентифікації біохімічних факторів ризику та проведенні відповідної немедикаментозної та медикаментозної корекції.
В основі розвитку вторинної гіперкальціурії та формуванні КОН лежить надмірне споживання продуктів із високим вмістом щавлевої кислоти та вітаміну С, зниження кількості та активності кишкової мікрофлори (Oxalobacter formigenes), дефіцит вітаміну В6 та порушення активності ферментів печінки (аланін-гідроксил-амінотрансферази).
Основи метафілактики КОН включають зниження концентрації в сечі каменеутворюючих солей (при КОН – солей кальцію та сечової кислоти), збільшення в сечі інгібіторів каменеутворення, корекцію рівня рН сечі, відновлення функції нирки та пасажу сечі.
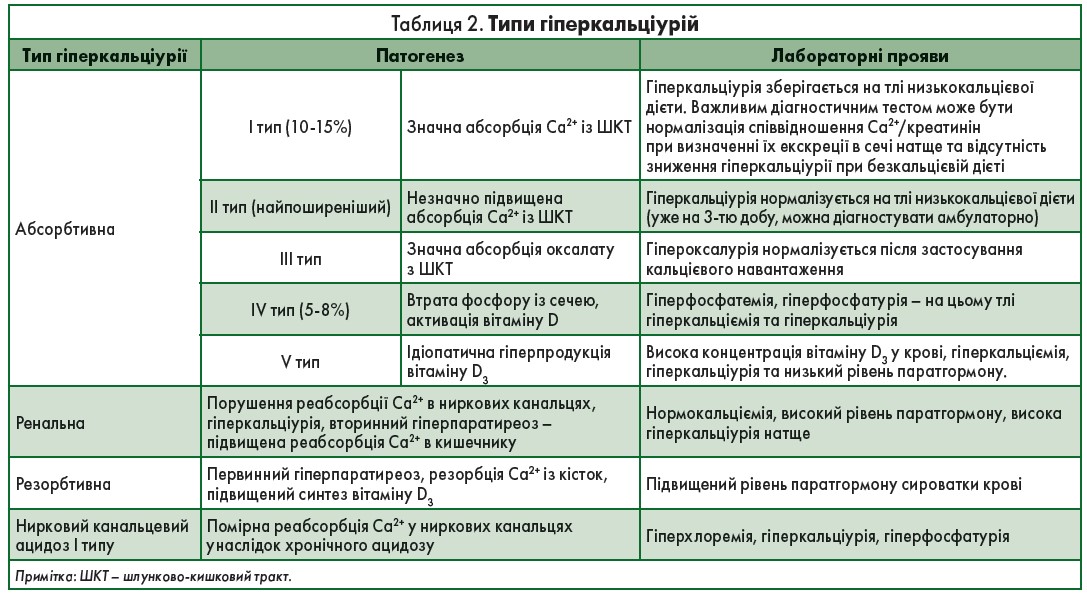
Гіперкальціурія (збільшення рівня добової екскреції кальцію із сечею >6,2 ммоль/добу в жінок та >7,5 ммоль/добу в чоловіків) є основним літогенним агентом у 65% пацієнтів із рецидивними кальцій-оксалатними каменями. Високий рівень кальцію в сечі та її насиченість знижує рівень інгібіторів цитрарату та хондроїтин-сульфату, що сприяє гіперкристалізації, утворенню мікролітів та каменів. Залежно від патогенетичних механізмів виділяють декілька типів гіперкальціурій (табл. 2).
В основі диференційної діагностики типів гіперкальціурії лежать наступні лабораторні обстеження:
 Біохімічні показники крові: креатинін, сечовина, Са, К, Р, Mg, Na, сечова кислота.
Біохімічні показники крові: креатинін, сечовина, Са, К, Р, Mg, Na, сечова кислота.- Біохімічні показники добової сечі з визначенням рівня екскреції Са, Р, сечової кислоти, оксалатів, цитратів, Na, К, креатиніну.
- Коливання рН у добовій сечі.
- Посів сечі на флору та чутливість до антибіотиків.
- Визначення мінерального (хімічного) складу каменя.
- Рівень паратгормону та активної форми вітаміну D3 у крові.
- Низькокальцієва проба: протягом 3 діб призначається дієта з виключенням молока, кефіру, йогуртів, сирів (бринза, кисломолочний сир), кави, какао, шоколаду, бобових, сметани, горіхів, фісташок, гірчиці, вівсянки, томатів, салату, шпинату. При зниженні рівня Са до 6,25-6,3 ммоль/л діагностується абсорбтивний тип гіперкальціурії. При аналізі проб абсорбтивної гіперкальціурії ІІІ типу у 25-30% хворих встановлено значне підвищення рівня оксалатів у сечі: до 76 мг/л при добовому діурезі до 1,5 л при нормі 20-40 мг/мл або добовому 114 мг/добу. Збільшення діурезу до 2,5-3 л призводить до значного зниження оксалатурії до 44,5 мг/л, але гіпероксалурія залишається високою.
Багаторічне вивчення пацієнтів із КОН дозволило прийти до нової нозологічної форми – гіпероксалурії. Встановлення діагнозу абсорбтивної гіпероксалурії передбачає застосування кальцієвого навантаження (глюконат кальцію 0,5 г 3 р/день протягом 3 днів). При контролі рівня оксалатурії визначається зниження рівня оксалату в сечі до верхніх меж норми (38-45 мг/л), що доводить необхідність призначення кальцієвої (іноді з високим вмістом кальцію) дієти для цієї популяції хворих. Якщо після проведення проби рівень оксалурії не змінюється, встановлюється діагноз вродженої тубулопатії-гіпероксалурії.
Після встановлення типу гіперкальціурії необхідне призначення метафілактики, яка включає:
1. Тіазидні діуретики – трихлорметиазид 4 мг/добу. У 8-10% хворих на тлі діуретичної терапії може виникати гіперурикемія, що є промотором гіперкристалізації – рекомендовано алопуринол 100 мг 2 р/день протягом 2-3 міс.
2. Канефрон Н – 2 таблетки 3 р/добу.
3. Питний режим – 2,5 л/добу.
4. Протизапальна терапія (за показаннями).
Терапія проводиться курсами по 3 міс із перервою в 1 місяць. На цей період рекомендовано прийом піридоксину 40 мг/добу, який метаболізується печінкою з утворенням активних метаболітів, запобігає утворенню альдегіду й формуванню надлишку щавлевої кислоти. Метафілактика проводиться постійно під контролем лікаря протягом 3-5 років з амбулаторним контролем кожні 3-6 місяців.
Запропонована диференційна діагностика типів гіперкальціурії дає можливість науково обґрунтовувати протирецидивне лікування найбільш поширеного нефролітіазу з високою його ефективністю (92-95%) безрецидивного періоду протягом ≥5 років і може широко використовуватися в практичній діяльності лікарів.
Конгрес Асоціації урологів України вкотре підтвердив свій статус однієї з найбільш важливих й інформаційно насичених подій у вітчизняній урології, яка дала змогу учасникам заходу ознайомитися із сучасними світовими тенденціями в діагностиці, лікуванні й профілактиці урологічних захворювань, поспілкуватися з корифеями галузі та сформулювати чіткі алгоритми реалізації отриманих знань у своїй практичній діяльності.
Підготувала Ганна Кирпач
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2 (13), червень 2018 р.