29 серпня, 2018
VIII Научно-практическая конференция Ассоциации аритмологов Украины: в поиске терапевтических резервов
17-18 мая в г. Киеве состоялась VIII научно-практическая конференция ассоциации аритмологов Украины. Научные заседания проходили в эти дни в нескольких залах отеля «Русь» – и каждый из них был полон. В рамках конференции состоялось уже традиционное совместное заседание Ассоциации аритмологов Украины и Европейской ассоциации ритма сердца (EHRA), в ходе которого выступили специалисты из Бельгии (профессор Том де Поттер), Словакии (профессор Роберт Хатала) и Польши (профессор Микаэль Худзик).
Вопросы антиаритмической, антитромботической, up-stream терапии у пациентов с нарушениями ритма сердца; ургентная помощь и долгосрочное лечение аритмий; ведение больных с имплантированными автоматическими устройствами – кажется, не осталось ни одной проблемы, которая не была бы затронута в ходе лекций и дискуссий. Основой всех обсуждений были современные рекомендации по диагностике и лечению аритмий.
Европейские и американские экспертные рекомендации, основанные на непредвзятом анализе доказательной базы, безусловно, являются надежными ориентирами для эффективной диагностики и терапии, в том числе в аритмологии. Так, в 2016 г. увидели свет обновленные рекомендации Европейского общества кардиологов по ведению пациентов с фибрилляцией предсердий (ФП). Однако не все положения европейских рекомендаций можно напрямую перенести в отечественную клиническую практику, поэтому работа по их адаптации ведется по сей день. Одна из задач конференции состояла в том, чтобы в ходе дискуссий экспертов с врачами выработать оптимальные решения для терапии нарушений ритма сердца с учетом доказательно обоснованных рекомендаций и реалий повседневной практики.

Сопредседатель Ассоциации аритмологов Украины, руководитель отдела нарушений ритма сердца ГУ «ННЦ «Институт кардиологии им. акад. Н.Д. Стражеско» НАМН Украины» (г. Киев), доктор медицинских наук, профессор Олег Сергеевич Сычев открыл работу конференции лекцией «Фибрилляция предсердий: резервы терапии». Лечение пациентов с ФП, которые, как правило, пожилого возраста, имеют фоновую сердечно-сосудистую патологию и груз сопутствующих заболеваний, остается одной из важнейших проблем клинической кардиологии как за рубежом, так и в Украине.
В лекции были рассмотрены все современные возможности терапии ФП, начиная от антиаритмических препаратов (ААП) для восстановления и удержания синусового ритма и заканчивая использованием полезных свойств полиненасыщенных жирных кислот.
В частности, профессор О.С. Сычев прокомментировал современные возможности терапии вагусной формы ФП с учетом особенностей украинского рынка ААП и предыдущего отечественного опыта. При анализе европейских рекомендаций обращает на себя внимание тот факт, что практически все рекомендованные ААП (амиодарон, дронедарон, пропафенон, соталол) в той или иной степени замедляют проведение в атриовентрикулярном узле и снижают частоту сердечных сокращений (ЧСС). Вместе с тем есть пациенты, у которых пароксизмы ФП возникают ночью, в состоянии покоя, во время еды, при нормальной или низкой ЧСС.
В предыдущей версии европейских рекомендаций (2010) присутствовала классификация ФП по вегетативному статусу, в соответствии с которой выделяют адренергически опосредованную ФП (20% пациентов), вагус-опосредованную ФП (24%) и смешанную ФП (56%). Выделение вегетативного статуса, предложенное Р. Coumel и соавт., несомненно, улучшило как понимание факторов, способствующих развитию аритмии, так и терапевтическую тактику при пароксизмах.
 При адренергически опосредованной ФП пароксизмы начинаются преимущественно днем, после физических нагрузок и психоэмоциональных стрессов, аритмии обычно предшествует тахикардия >90 уд/мин. Аритмия может сочетаться с тиреотоксикозом или кардиомиопатиями. Если приступы аритмии связаны с повышением активности симпатической системы, β-адреноблокаторы являются препаратами выбора первой линии, а при их неэффективности применяются пропафенон, обладающий относительно выраженными β-блокирующими свойствами, и соталол.
При адренергически опосредованной ФП пароксизмы начинаются преимущественно днем, после физических нагрузок и психоэмоциональных стрессов, аритмии обычно предшествует тахикардия >90 уд/мин. Аритмия может сочетаться с тиреотоксикозом или кардиомиопатиями. Если приступы аритмии связаны с повышением активности симпатической системы, β-адреноблокаторы являются препаратами выбора первой линии, а при их неэффективности применяются пропафенон, обладающий относительно выраженными β-блокирующими свойствами, и соталол.
Вагус-опосредованная ФП чаще развивается у мужчин (80%) с дебютом в возрасте 40-50 лет. Аритмия обычно носит пароксизмальный характер, приступ начинается ночью, в покое, после еды, после приема алкоголя, ему предшествует брадикардия. В качестве препарата выбора при вагус-опосредованной ФП европейские эксперты рекомендуют дизопирамид. Однако этот ААП в Украине не зарегистрирован, поэтому оптимальным вариантом для начала долгосрочного контроля ритма является ААП ІС класса этацизин, хорошо знакомый кардиологам в нашей стране.
Учитывая многолетний положительный опыт применения, украинские эксперты решили оставить этацизин в национальных рекомендациях по ФП с формулировкой «для лечения пациентов с вагусной формой ФП и без выраженной органической патологии сердца» (рекомендация класса I, уровень доказательств С). Этацизин также эффективен для лечения желудочковых аритмий у пациентов без структурного поражения сердца.
Резолюция совета экспертов от 26.10.2017 г. содержит следующие положения:
- Этацизин – безопасный и эффективный ААП для терапии ФП и желудочковой экстрасистолии у пациентов без тяжелой органической патологии сердца, с возможностью длительного приема.
- Следует использовать алгоритм контроля за приемом препарата Этацизин при его длительном применении.
- При достижении терапевтического эффекта рекомендуется снизить дозу препарата до минимальной эффективной.
- Этацизин – препарат выбора для лечения аритмий, которые развиваются на фоне брадикардии.
- Этацизин эффективен в виде моно- и комбинированной (с β-адреноблокаторами) терапии нарушений ритма сердца.
 Лектор обратил внимание на некоторые ограничения и лекарственные взаимодействия. Противопоказано применение этацизина одновременно с другими ААП IC класса (флекаинидом, пропафеноном), а также с дронедароном. Вместе с тем допускается сочетание с амиодароном и соталолом в низких дозах. Комбинация этацизина с β-адреноблокаторами является рациональной, особенно при адренергических формах аритмий.
Лектор обратил внимание на некоторые ограничения и лекарственные взаимодействия. Противопоказано применение этацизина одновременно с другими ААП IC класса (флекаинидом, пропафеноном), а также с дронедароном. Вместе с тем допускается сочетание с амиодароном и соталолом в низких дозах. Комбинация этацизина с β-адреноблокаторами является рациональной, особенно при адренергических формах аритмий.
При тщательном соблюдении критериев отбора пациентов этацизин является высокоэффективным и безопасным ААП, что демонстрирует клинический опыт ННЦ «Институт кардиологии им. Н.Д. Стражеско».
О нем более подробно рассказала старший научный сотрудник отдела аритмий сердца, кандидат медицинских наук Елена Николаевна Романова. Также в ее докладе была озвучена важная информация об особенностях применения этацизина.
Непременным условием при назначении этацизина (как и других ААП I класса) является отсутствие органического поражения сердца, что подразумевает:
– отсутствие инфаркта миокарда с зубцом Q в анамнезе;
– отсутствие гипертрофической или дилатационной кардиомиопатии;
– фракция выброса левого желудочка >45%;
– отсутствие застойной или прогрессирующей сердечной недостаточности (СН), стадия СН не более ІІА;
– отсутствие врожденных или ревматических пороков сердца;
– отсутствие выраженной гипертрофии левого желудочка (толщина одной из стенок левого желудочка ≥14 мм).
 Если пациент начинает лечение этацизином впервые, необходимо снять электрокардиограмму (ЭКГ) и при отсутствии противопоказаний назначить первую таблетку (50 мг) под контролем врача. Через 1-2 ч следует повторно выполнить ЭКГ для исключения проаритмогенного эффекта препарата.
Если пациент начинает лечение этацизином впервые, необходимо снять электрокардиограмму (ЭКГ) и при отсутствии противопоказаний назначить первую таблетку (50 мг) под контролем врача. Через 1-2 ч следует повторно выполнить ЭКГ для исключения проаритмогенного эффекта препарата.
Его признаками могут быть: расширение комплекса QRS более чем на 25%, уменьшение его амплитуды, увеличение продолжительности зубца Р более 0,12 с, появление блокад, брадикардии, усиление имеющейся экстрасистолии, трансформация ФП в трепетание предсердий (ТП).
Если пациент хорошо перенес первую дозу, назначается поддерживающая доза 50 мг 3 раза в сутки. Через три дня необходима повторная консультация с контролем ЭКГ. При достижении антиаритмического эффекта проводится поддерживающая терапия в индивидуально подобранных дозах (1/2-1 таблетка 2-4 раза в сутки).
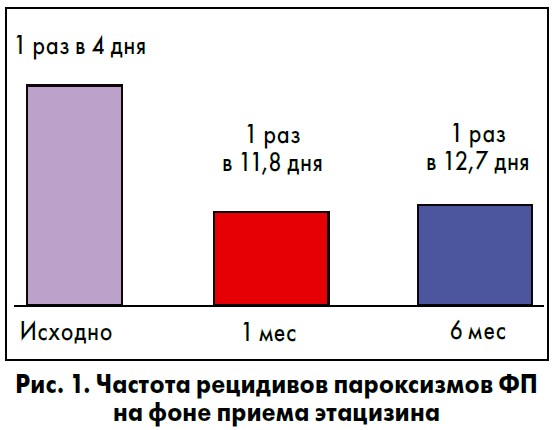
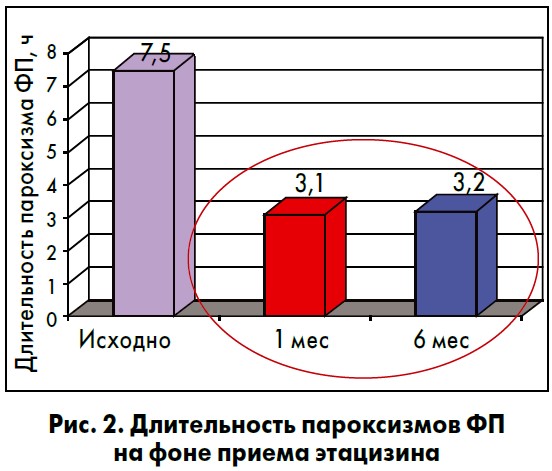 В докладе были представлены данные отдела аритмий сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины относительно эффективности и безопасности этацизина для лечения ФП у пациентов без выраженных органических изменений сердца. Очень показательна динамика частоты рецидивов пароксизмов ФП на фоне приема этацизина: за 6 мес лечения она уменьшилась более чем в 3 раза (рис. 1). Также обращает на себя внимание существенное сокращение длительности пароксизмов (рис. 2).
В докладе были представлены данные отдела аритмий сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины относительно эффективности и безопасности этацизина для лечения ФП у пациентов без выраженных органических изменений сердца. Очень показательна динамика частоты рецидивов пароксизмов ФП на фоне приема этацизина: за 6 мес лечения она уменьшилась более чем в 3 раза (рис. 1). Также обращает на себя внимание существенное сокращение длительности пароксизмов (рис. 2).
Из кардиальных побочных эффектов этацизина отмечали развитие блокады правой ножки пучка Гиса у 2% пациентов, расширение комплекса QRS более чем на 25% от исходного – у 1,2% и трансформацию ФП в ТП – у 1,8%.
Некоторые пациенты отмечали экстракардиальные побочные эффекты препарата: диплопию (12%), головную боль и/или головокружение (3%), онемение языка за счет местного анестезирующего действия препарата (2%), тошноту (2%), шум в ушах (1%).
На основании представленных данных были сделаны следующие выводы:
- При корректном отборе пациентов согласно критериям «без выраженной структурной патологии сердца» и типу ФП (вагусная/адренергическая/смешанная) этацизин является эффективным и безопасным ААП при лечении суправентрикулярных нарушений ритма.
- Этацизин также эффективен для лечения желудочковой экстрасистолии у обследованных больных.
- Этацизин не терял эффективности при длительном приеме.
 Профессор кафедры терапии и семейной медицины учебно-научного института последипломного образования Тернопольского государственного медицинского университета им. И.Я. Горбачевского, доктор медицинских наук Марьян Васильевич Гребеник представил результаты локального реестра нарушений сердечного ритма у ургентно госпитализированных пациентов. Лектор прокомментировал различия в характеристиках пациентов, тактике лечения и исходах между когортами, набранными в реестр с 2000 по 2006 г. и с 2010 по 2017 г.
Профессор кафедры терапии и семейной медицины учебно-научного института последипломного образования Тернопольского государственного медицинского университета им. И.Я. Горбачевского, доктор медицинских наук Марьян Васильевич Гребеник представил результаты локального реестра нарушений сердечного ритма у ургентно госпитализированных пациентов. Лектор прокомментировал различия в характеристиках пациентов, тактике лечения и исходах между когортами, набранными в реестр с 2000 по 2006 г. и с 2010 по 2017 г.
За прошедший период времени доля нарушений ритма в структуре причин ургентных госпитализаций несколько увеличилась, хотя и не достоверно, с 19,6 до 21,3%. Увеличился средний возраст больных: с 59,89±1,05 до 62,36±2,01 года. Также вырос индекс коморбидности Чарлсона: в когорте 2010-2017 гг. он превысил 3.
Наиболее распространенным основным диагнозом была и остается ишемическая болезнь сердца – 76,5%. Среди вероятных ведущих факторов развития аритмии доминировала артериальная гипертензия (37,3%). Постинфарктный кардиосклероз как фактор аритмогенного ремоделирования миокарда занимал 11,7%, СН – 9,8%, кардиомиопатии – 7,9%.
Комментируя особенности терапии нарушений сердечного ритма, докладчик обратил внимание на сокращение количества препаратов, которые применялись с 2010 по 2017 г. по сравнению с более ранней когортой 2000-2006 гг. Практически ушли со сцены такие препараты, как лидокаин, новокаинамид, хинидин и дифенин. Лидером по частоте назначений с выраженной динамикой роста является амиодарон: его назначили 36,36% пациентов в первой когорте и 72,45% – во второй. За ним следуют β-блокаторы: 13,56 и 18,26% соответственно.
 Наблюдается ренессанс этацизина, который является безальтернативным ААП для пациентов с вагусными формами аритмий. В когорте 2000-2006 гг. этацизин принимали 12,6% пациентов, в когорте 2010-2017 гг. – 6,44%. Дигоксин не сдает позиций, несмотря на противоречивую и неполную доказательную базу: 5,93% назначений в когорте 2000-2006 гг. и 18,6% назначений в когорте 2010-2017 гг. Электроимпульсную терапию применяли у 8,47 и 7,8% пациентов соответственно. Также докладчик отметил очень низкий показатель применения радиочастотной абляции – 1,14%.
Наблюдается ренессанс этацизина, который является безальтернативным ААП для пациентов с вагусными формами аритмий. В когорте 2000-2006 гг. этацизин принимали 12,6% пациентов, в когорте 2010-2017 гг. – 6,44%. Дигоксин не сдает позиций, несмотря на противоречивую и неполную доказательную базу: 5,93% назначений в когорте 2000-2006 гг. и 18,6% назначений в когорте 2010-2017 гг. Электроимпульсную терапию применяли у 8,47 и 7,8% пациентов соответственно. Также докладчик отметил очень низкий показатель применения радиочастотной абляции – 1,14%.
Анализ выживаемости пациентов после выписки из стационара за период с 01.2000 по 31.12.2017 г., проведенный по методу Каплана – Мейера, показал значительные различия между пациентами с пароксизмальной или персистирующей формой ФП (11,36 года) и пациентами с хронической (перманентной) ФП (6,44 года). Таким образом, смертность в указанных подгруппах отличалась в 1,76 раза (р=0,008) при исходно сопоставимых демографических и клинических характеристиках на момент включения в реестр в 2000 г.
По данным регрессионного анализа предикторов сердечно-сосудистой смертности на модели пропорциональных рисков Кокса единственным фактором, который достоверно влиял на выживаемость больных, был возраст. Подводя итог, докладчик отметил, что показанные в исследовании тенденции свидетельствуют о преимуществах стратегии контроля ритма над стратегией контроля ЧСС.
Подготовил Дмитрий Молчанов
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (58) червень 2018 р.



