30 серпня, 2018
Застосування голімумабу при псоріатичному артриті: огляд літератури та власні спостереження
Псоріатичний артрит (ПсА) належить до групи серонегативних спондилоартропатій та є хронічним запальним захворюванням із вираженою гетерогенністю клінічних проявів, включаючи ураження шкіри, нігтів, периферичних суглобів, хребта, сакроіліальних з’єднань, розвитком ентезитів, дактилітів тощо. Поширеність ПсА в популяції становить близько 1,5%. У 70% випадків псоріаз передує ураженню суглобів і хребта, в 15% – ураження шкіри й опорно-рухового апарату розвиваються одночасно, в деяких хворих типові ураження шкіри відсутні чи псоріаз мають кровні родичі. У США щорічна захворюваність на ПсА становить 7,2 на 100 тис. осіб (F.C. Wilson et al., 2009). 30% хворих на псоріаз мають ПсА; крім того, близько 15% пацієнтів із псоріазом можуть мати недіагностований ПсА (P.J. Mease, 2013; A.P. Villani et al., 2015). Слід зазначити, що ПсА значно знижує функціональну активність та якість життя хворих, а за відсутності адекватного лікування прогресує, що призводить до швидкої втрати працездатності.
Метою терапії ПсА, як і інших ревматичних захворювань, є «treat to target», тобто досягнення й утримання стійкої клініко-лабораторної ремісії. Оцінювати настання ремісії пропонується з огляду на п’ять кінцевих точок, а саме: синовіт, ентезит, дактиліт, спондиліт і псоріаз шкіри/нігтів на підставі розрахунку відповідних інтегральних показників активності (P.J. Mease, L.C. Coates et al., 2018).
У 2015 році оновлено рекомендації Європейської протиревматичної ліги (EULAR) із лікування ПсА. Основними постулатами оновлених рекомендацій є такі: при ПсА з переважанням аксіальних проявів та ентезитів рекомендовано призначення біологічних хворобомодифікувальних протиревматичних препаратів (ХМПРП) без попереднього застосування традиційних синтетичних ХМПРП. У разі переважно периферичної форми ПсА за неефективності традиційних синтетичних ХМПРП біологічні агенти також рекомендовані.
Як біологічним ХМПРП першої лінії цілковиту перевагу віддають інгібіторам фактора некрозу пухлин-α (ФНП-α). У разі наявності протипоказань до інгібіторів ФНП-α рекомендовано використовувати інгібітори інтерлейкінів‑12/23 або інтерлейкіну‑17. За наявності протипоказань до біологічних ХМПРП слід застосовувати інгібітори фосфодіестерази‑4.
Для лікування ПсА починаючи з 2012 року Управлінням із контролю якості продуктів харчування та лікарських засобів США (FDA) схвалено інгібітор ФНП-α голімумаб. Ефективність препарату доведена в клінічних дослідженнях GO-REVEAL та GO-VIBRANT.
GO-REVEAL – багатоцентрове плацебо-контрольоване дослідження ІІІ фази, що проводилося з 2005 по 2012 рік (A. Kavanaugh, I.B. McInnes, P. Mease еt al., 2014). У дослідження включили 405 пацієнтів з активним ПсА (≥3 набряклих і болючих суглобів та активний псоріаз шкіри), яких рандомізовували на три групи: підшкірно (п/ш) голімумаб 50 мг, голімумаб 100 мг або плацебо кожні 4 тиж до 252-го тижня лікування. Після останньої ін’єкції спостереження тривало ще 16 тиж. Близько половини пацієнтів приймали метотрексат у терапевтичній дозі.
За результатами проведеного дослідження на 256-му тижні голімумаб виявився ефективним для утримання клінічної відповіді. Так, відповідь ACR20 становила 62,8; 65,8; 69,9%; ACR50 – 43,4; 47,9; 50,7%; ACR70 – 32,7; 30,8; 35,6% у групах плацебо, голімумаб 50 мг і голімумаб 100 мг відповідно.
Індекс DAS28-CRP на 256-му тижні зменшився до 2,8±1,2 у групах голімумабу 50 і 100 мг порівняно з вихідними рівнями (5,0±1,1 та 4,9±1,1 відповідно). Серед рандомізованих пацієнтів з ураженням ≥3% поверхні тіла псоріазом індекс PASI на 256-му тижні в групах голімумабу 50 і 100 мг зменшився з 9,8±8,6 до 2,7±4,5 та з 11,1±9,5 до 2,2±3,9 відповідно. Відповідь PASI75 мали 61,5 та 72,2% пацієнтів. Достовірну позитивну динаміку також реєстрували за індексом ураження нігтів, кількістю ентезитів і дактилітів.
Покращення фізичної активності за шкалою HAQ-DI спостерігали в 54,1% пацієнтів у групі голімумабу 50 мг і в 58,2% – у групі голімумабу 100 мг. Значення індексу HAQ-DI на 256-му тижні становило 0,6±0,6 для обох груп проти вихідних значень 1,0±0,6 та 1,1±0,6 відповідно.
Рентгенологічне прогресування оцінювали за ПсА-модифікованою шкалою Sharp / van der Heijde, що на 256-му тижні порівняно з вихідним значенням становило ≤0,3. Достовірне сповільнення рентгенологічних змін виявили в пацієнтів, які отримували метотрексат.
Антитіла до голімумабу виявляли в 6% пацієнтів, серед яких 1,8% – приймали метотрексат і 10,5% – не приймали. 126 (31%) пацієнтів припинили участь у дослідженні через небажані побічні явища. Експерти визнали, що зареєстровані побічні ефекти подібні та не відрізнялися від можливих побічних ефектів інших інгібіторів ФНП-α.
На підставі проведеного дослідження зроблено висновок, що прийом голімумабу в дозах 50 і 100 мг п/ш кожні 4 тиж упродовж 5 років зумовлює достовірне стійке клінічне покращення, сповільнення рентген-прогресування та має задовільний профіль безпеки.
Результати дослідження GO-VIBRANT щодо ефективності та безпеки внутрішньовенної (в/в) форми голімумабу в лікуванні ПсА були представлені на конгресі EULAR (2017) у м. Мадрид, Іспанія (A. Kavanaugh, M.E. Husni, D.D. Harrison et al., 2017). 480 пацієнтів, які не отримували попередньо біологічну терапію, були включені в дослідження та приймали голімумаб у дозі 2 мг/кг в/в або плацебо на 0-му, 4-му тижні й надалі кожні 8 тиж усього впродовж 24 тиж.
Первинною кінцевою точкою була відповідь ACR20 на 14-й тиждень. ACR20 отримано в 75,1% пацієнтів групи голімумабу проти 21,8% – групи плацебо. На 14-му тижні лікування відповідь ACR50 мали 43,6% пацієнтів, які отримували голімумаб, порівняно з 6,3% пацієнтів групи плацебо, відповідь ACR70 – 24,5 проти 2,1%, а відповідь PASI75 – 59,2 проти 13,6% (для всіх р<0,001).
Також на 14-й тиждень відзначено покращення за шкалою HAQ-DI (-0,60 у групі голімумабу проти -0,12 у групі плацебо; р<0,001). На 24-му тижні відповідь ACR50 у групі голімумабу була досягнута в більшої кількості пацієнтів порівняно з плацебо (53,5 проти 6,3%). У дослідженні отримано достовірне покращення при лікуванні голімумабом ентезитів, дактилітів та ураження шкіри. Індекс PASI75 в основній групі виявився достовірно вищим порівняно з групою плацебо (59,2 проти 13,6% хворих відповідно).
На 24-му тижні лікування відзначено достовірне сповільнення рентген-прогресування: утворення ерозій, деструкції суглобів і звуження суглобової щілини порівняно з плацебо; за ПсА-модифікованою шкалою Sharp / van der Heijde рентгенологічні зміни становили -0,4 у групі голімумабу та 2,0 у групі плацебо (р<0,001).
У ході дослідження серед серйозних небажаних побічних ефектів зареєстрували 2 раптові смерті, 2 злоякісні новоутворення, 1 демієлінізуюче захворювання. Більш як 1 небажане явище мали 40,6% пацієнтів групи плацебо та 46,3% – групи голімумабу, інфекційні ускладнення реєстрували найчастіше.
Нижче наводимо клінічний випадок лікування ПсА з використанням голімумабу, котрий спостерігали в нашій клініці.
Клінічний випадок
Пацієнт М., 43 роки, надійшов до І ревматологічного відділення Олександрівської клінічної лікарні м. Києва в жовтні 2017 року. Мав скарги на ранкову скутість, обмеження рухів у поперековому та шийному відділах хребта, біль і набряк у правому променево-зап’ястковому суглобі, колінних суглобах, суглобах стопи. Крім цього, хворого турбували свербіж, сухість шкіри та лущення в місцях висипання.
Анамнез захворювання. Псоріаз із 1995 року. Біль у спині та суглобах турбує з 2005 року. З 2015-го пацієнт спостерігається в нашій клініці. З лютого 2015 року призначено метотрексат у дозі 15 мг на тиждень, проте з огляду на високу активність захворювання пацієнт був вимушений постійно приймати нестероїдні протизапальні препарати (НПЗП) і глюкокортикоїди (ГК) у дозі від 15 до 5 мг за преднізолоном.
Анамнез життя. Травм, операцій, переломів не було. Хронічні захворювання заперечує. Не палить, алкоголь не вживає. Професійні шкідливості відсутні. Сімейний анамнез не ускладнений.
Об’єктивний статус. Будова тіла нормостенічна, зріст – 181 см, вага – 78 кг, індекс маси тіла – 23,8. Псоріаз шкіри мав генералізований характер. Індекс PASI – 29,2. Постава кіфотична, посилений грудний кіфоз, поперековий лордоз згладжений. Тест Шобера – 16 см, люмбальна флексія – 3,5 см. Пальпаторно наявність болю на передній верхній клубовій ості з обох боків, остистих відростках Тh11, L4-L5 та місці прикріплення ахіллового сухожилка справа. Тести Кушелевського та симптом Патрика слабко позитивні справа. Сила м’язів задовільна.
Помірний набряк, біль та обмеження рухів у колінних суглобах, правому променево-запястковому суглобі, дактиліт IV пальця лівої стопи, ІІ пальця правої стопи. Периферичні лімфатичні вузли не збільшені. У легенях дихання везикулярне, хрипів немає. Тони серця звучні, ритмічні, патологічні шуми відсутні. Живіт м’який, під час пальпації безболісний. Нижня межа печінки – по краю реберної дуги. Селезінка не пальпується. Периферичних набряків немає, випорожнення в нормі, діурез достатній.
Результати лабораторних досліджень. Загальний аналіз крові: гемоглобін – 141 г/л; еритроцити – 4,2×1012/л; лейкоцити – 8,7×109/л; швидкість осідання еритроцитів (ШОЕ) – 87 мм/год; тромбоцити – 299×109/л; гематокрит – 38,9%; п – 5%; с – 65%; л – 20%; м – 7%; е – 3%. Біохімічний аналіз крові: холестерин – 5,1 ммоль/л; білірубін – 19,4 мкмоль/л; креатинін – 79 ммоль/л; загальний білок – 76,1 г/л; АЛТ – 36,0 МО/л; АСТ – 34,7 МО/л; ГГТП – 29,0 ОД/л; сечова кислота – 360 ммоль/л; сечовина – 7,2 ммоль/л; глюкоза – 5,5 ммоль/л; С-реактивний білок (СРБ) – 48 мг/л. Загальний аналіз сечі – без клінічно значущих змін.
Результати інструментальних досліджень. Електрокардіографія, ехокардіографія, ультразвукова діагностика органів черевної порожнини – без клінічно значущих відхилень. Магнітно-резонансна томографія сакроілеальних з’єднань – ознаки правобічного сакроіліїту.
На підставі вищенаведених даних встановлено клінічний діагноз: ПсА, спондилоартритичний варіант, активність 3 ступеня, з ураженням шийного та поперекового відділів хребта, правобічний сакроіліїт, ураження колінних суглобів, правого променево-зап’ясткового суглоба, суглобів стоп, кистей, дактиліти; рентген-стадія – ІІ, ФНС – ІІ. Псоріаз шкіри поширений, генералізована форма, стаціонарна стадія.
Зважаючи на високу активність захворювання, відсутність достатнього ефекту від тривалого прийому метотрексату, необхідність постійного застосування ГК і НПЗП, погодженість хворого із запропонованим лікуванням, було вирішено призначити біологічну терапію, інгібітор ФНП-α, голімумаб. До початку прийому препарату, згідно з протоколом призначення біологічних агентів, пацієнт був обстежений на гепатити В та С, виконано рентгенографію органів грудної клітки, туберкуліновий тест, пацієнта оглянув фтизіатр.
Протипоказань до призначення інгібітора ФНП-α не виявлено. Отже, лікування хворого включало: голімумаб (Сімпоні) 1 раз на місяць 50 мг / 0,5 мл п/ш; метотрексат 15 мг на тиждень; фолієва кислота 10 мг на тиждень; метилпреднізолон 12 мг на добу з поступовим зменшенням; мелоксикам 15 мг на добу за потребою; лікувальна фізкультура.
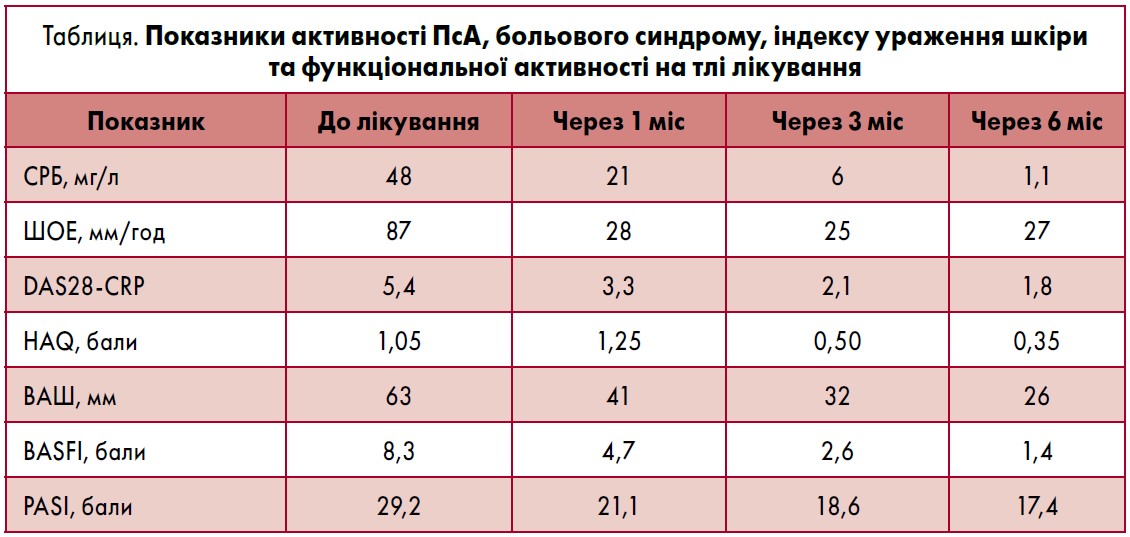
Надалі заплановано огляд через місяць і наступні кожні 3 міс для моніторингу ефективності та безпеки терапії. З метою визначення активності захворювання визначали СРБ, ШОЕ, DAS28-CRP; з метою оцінювання вираженості больового синдрому використовували візуальну аналогову шкалу (ВАШ), функціонального статусу хворого – BASFI та НАQ, площі ураження та тяжкості псоріазу – індекс PASI. Результати спостереження представлено в таблиці.
За результатами спостереження відзначено значне покращення стану хворого на тлі прийому голімумабу. Впродовж 6 міс лікування спостерігали зменшення гострофазових показників (СРБ, ШОЕ), інтенсивності больового синдрому за ВАШ, інтегрального показника активності захворювання DAS28-CRP, покращення функціональної здатності пацієнта за опитувальником BASFI та якості життя хворого за анкетою НАQ.
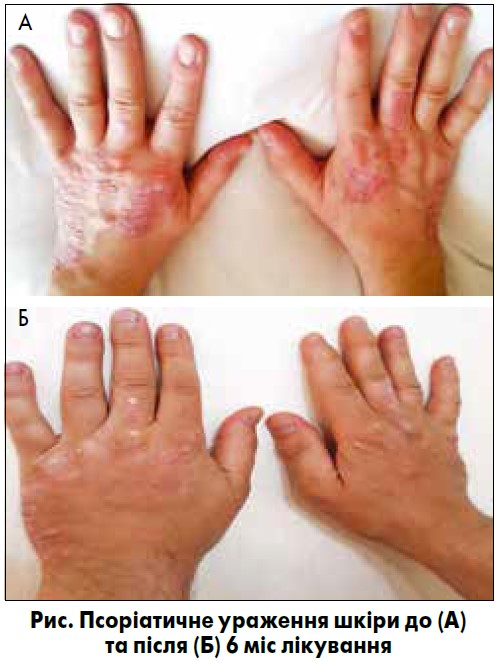 Також реєстрували зменшення площі та ступеня шкірних проявів псоріазу за індексом PASI. Ураження шкіри та їх динаміка представлені на рисунку.
Також реєстрували зменшення площі та ступеня шкірних проявів псоріазу за індексом PASI. Ураження шкіри та їх динаміка представлені на рисунку.
Важливим досягненням призначеного лікування виявилась і повна відміна ГК уже через 3 міс після призначення голімумабу. Через 6 міс пацієнт мав стійку клініко-лабораторну ремісію.
Хворий продовжує лікування: метотрексат у дозі 15 мг на тиждень, фолієва кислота 10 мг на тиждень і голімумаб 50 мг п/ш 1 раз на місяць. Спостереження триває.
Висновки
Імунобіологічна терапія кардинально змінила якість життя багатьох хворих, покращила прогноз цілої низки захворювань. Понад 1 млн людей у світі застосовують біологічні агенти для лікування ревматологічних захворювань, злоякісних новоутворень, захворювань бронхолегеневої системи тощо. Велика кількість досліджень у всьому світі з новими класами біологічних препаратів триває, акумулюються й аналізуються дані, показання та режими застосування, можливі побічні ефекти, в тому числі в разі тривалого використання.
Економічна доцільність застосування імунобіологічної терапії визнана багатьма дослідженнями та підтримується на державному рівні в деяких країнах. На жаль, для української популяції ревматологічних хворих, біологічні агенти застосовують не так широко, як цього інколи потребують пацієнти в разі недостатньої ефективності чи відсутності ефекту від синтетичних ХМПРП, однак певний власний досвід її застосування все ж накопичується.
Значна прихильність пацієнтів до застосування голімумабу зумовлена насамперед режимом його застосування (1 раз на місяць), оптимальною для хворого п/ш формою введення, що можна проводити амбулаторно чи в домашніх умовах у разі повторного застосування, вираженою навіть після першого введення ефективністю та задовільним профілем безпеки.
Література
- Національний підручник із ревматології / За ред. В.М. Коваленка, Н.М. Шуби. – К., 2013.
- Яременко О.Б. Псоріатичний артрит: клініко-лабораторна діагностика та фармакотерапія: методичні рекомендації / О.Б. Яременко, Д.Л. Федьков, О.І. Івашківський [та ін.]. – К., 2015.
- Gossec L., Smolen J.S., Ramiro S., et al. European League Against Rheumatism (EULAR) recommendations for the management of psoriatic arthritis with pharmacological therapies: 2015 update. Ann. Rheum. Dis. 2016; 75: 499-510.
- Kavanaugh A., Husni M.E., Harrison D.D., et al. Safety and Efficacy of Intravenous Golimumab in Patients With Active Psoriatic Arthritis: Results Through Week Twenty-Four of the GO-VIBRANT Study. Arthritis Rheumatol. 2017; 69 (11): 2151-2161.
- Kavanaugh A., McInnes I.B., Mease P., еt al. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long-term extension of a randomised, placebo-controlled trial (the GO-REVEAL study). Ann. Rheum. Dis. 2014; 73 (9): 1689-94.
- Mease P.J., Coates L.C. Considerations for the definition of remission criteria in psoriatic arthritis. Semin. Arthritis Rheum. 2018; 47 (6): 786-796.
- Mease P.J., Gladman D.D., et al. Prevalence of rheumatologist-diagnosed psoriatic arthritis in patients with psoriasis in European/North American dermatology clinics. J. Am. Acad. Dermatol. 2013; 69: 729-735.
- Schwartzman S., Li Y., et al. Economic impact of biologic utilization patterns in patients with psoriatic arthritis. Clin. Rheumatol. 2017; 36 (7): 1579-1588.
- Villani A.P., Rouzaud M., Sevrain M., et al. Prevalence of undiagnosed psoriatic arthritis among psoriasis patients: systematic review and meta-analysis. J. Am. Acad. Dermatol. 2015; 73: 242-248.
- Wilson F.C., Cynthia M.I., et al. Time trends in epidemiology and characteristics of psoriatic arthritis over 3 decades: a population-based study. J. Rheumatol. 2009; 36 (2): 361-367.
PHUA/BIO/0618/0001
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (58) червень 2018 р.