3 грудня, 2018
Біліарний сладж та жовчнокам’яна хвороба: актуальні науково-практичні аспекти
 Лікарі різних спеціальностей у своїй практичній діяльності часто стикаються з такими патологічними станами, які за певних умов можуть трансформуватись у серйозні захворювання. До них належить біліарний сладж, який слід розглядати як ранній прояв жовчнокам’яної хвороби (ЖКХ). Метаболічні порушення, зміни фізико-хімічних властивостей жовчі, підвищення її літогенності та зниження скорочувальної функції жовчного міхура передують літогенезу. Тому терапевтичний вплив на ці патогенетичні механізми дозволяє запобігти розвитку ЖКХ. Це вкрай важливо, адже стандартом лікування захворювання є холецистектомія – оперативне втручання, яке за частотою виконання поступається лише апендектомії.
Лікарі різних спеціальностей у своїй практичній діяльності часто стикаються з такими патологічними станами, які за певних умов можуть трансформуватись у серйозні захворювання. До них належить біліарний сладж, який слід розглядати як ранній прояв жовчнокам’яної хвороби (ЖКХ). Метаболічні порушення, зміни фізико-хімічних властивостей жовчі, підвищення її літогенності та зниження скорочувальної функції жовчного міхура передують літогенезу. Тому терапевтичний вплив на ці патогенетичні механізми дозволяє запобігти розвитку ЖКХ. Це вкрай важливо, адже стандартом лікування захворювання є холецистектомія – оперативне втручання, яке за частотою виконання поступається лише апендектомії.
Основною причиною підвищення літогенності жовчі є зміна співвідношення її компонентів: холестерину, жовчних кислот та фосфоліпідів. Надмірна концентрація холестерину в жовчі призводить до її згущення, внаслідок чого утворюються кристали моногідрату холестерину. Осідаючи на стінках жовчного міхура, вони створюють умови для виникнення біліарного сладжу. Відомо, що застій жовчі у жовчному міхурі за принципом зворотного зв’язку пригнічує холерез, для якого характерне зниження синтезу розчинників жовчі (лецитину, жовчних кислот та їх кон’югатів). Це супроводжується підвищенням літогенності жовчі – і, як наслідок, гіпомоторний жовчний міхур не може видалити густий вміст. Тому між індексом літогенності жовчі та гіпокінетичною дисфункцією жовчного міхура існує тісний кореляційний зв’язок. У подальшому до застою жовчі долучається запальний компонент, це призводить до того, що патологічний процес переходить у початкову стадію ЖКХ – біліарний сладж (з англ. «sludge» – бруд, каламуть). Незважаючи на очевидний патогенетичний зв’язок біліарного сладжу та ЖКХ, така трансформація відбувається тільки у 8-23% пацієнтів. Після усунення етіологічного фактора (наприклад, у жінок після пологів) можливий спонтанний регрес біліарного сладжу. Проте це не означає, що такі пацієнти взагалі не потребують медикаментозного лікування. Якщо під час ультразвукового дослідження (УЗД) у пацієнта візуалізуються ознаки біліарного сладжу, своєчасне проведення профілактичних заходів дає змогу запобігти розвитку ускладнень.
У рамках науково-практичної конференції з міжнародною участю «Х Український гастроентерологічний тиждень», яка відбулася 27-28 вересня в м. Дніпро, про науково-практичні аспекти лікування біліарного сладжу і ЖКХ та методи їх корекції в актуальному інтерв’ю нашому кореспонденту докладно розповів доцент кафедри внутрішньої медицини № 1 Національного медичного університету імені О.О. Богомольця Володимир Володимирович Чернявський.
? Чим зумовлена актуальність проблеми ЖКХ? Яке значення має біліарний сладж у патогенезі цього захворювання?
– ЖКХ – це захворювання, з яким у своїй практичній діяльності стикаються не тільки гастроентерологи, а й терапевти, сімейні лікарі, хірурги. Сьогодні існують вичерпні рекомендації Європейської асоціації з вивчення печінки (EASL, 2016) щодо ведення пацієнтів із ЖКХ. Проте важливою умовою ефективності лікування є співпраця лікаря та хворого. Тому до вибору лікувальної тактики необхідно підходити аргументовано, обов’язково враховуючи індивідуальні особливості пацієнта.
Біліарний сладж – це осад, який складається з мікроскопічних преципітатів холестерину і білірубінату кальцію та слизу. В окремих клінічних ситуаціях сладж може бути початковою стадією ЖКХ. Проте таку трансформацію розглядають як певною мірою дієтозалежний феномен, який може зникати спонтанно завдяки скороченням жовчного міхура (за умови нормальної моторики органа). Якщо цього не відбувається, в осаді можуть утворюватись холестеринові мікроліти. У загальній популяції у пацієнтів без ЖКХ біліарний сладж виявляють у 1,7-4% осіб. Серед пацієнтів із порушеннями функції шлунково-кишкового тракту ця проблема зустрічається у 7,5% випадків. У хворих із біліарною диспепсією осад у жовчному міхурі виявляють у 24-55% випадків.
? Чи супроводжується біліарний сладж характерними клінічними проявами? Чи може ця патологія спричинити розвиток ускладнень?
– Пасаж сладжу з жовчного міхура до міхурової протоки може мати симптоми, ідентичні тим, появу яких спричиняють жовчні камені. Цей феномен асоціюється з жовчною колікою, панкреатитом, холангітом і холециститом. Біліарний сладж також виявляють у значної частини пацієнтів з ідіопатичним панкреатитом. Що стосується ускладнень, пов’язаних із біліарним сладжем, сьогодні існують дані про схильність таких хворих до розвитку біліарного панкреатиту (33-75%), дисфункції сфінктера Одді (50-93%), утворення каменів (8-20%), рідше – ниркової коліки. Персистенція біліарного сладжу з періодичними епізодами його зникнення та повторної появи, яка зустрічається у 30-60% випадків, потребує від лікаря прийняття рішення про вибір оптимального підходу до лікування пацієнта, яке, крім медикаментозної терапії, має включати рекомендації щодо дієти та модифікації способу життя.
? Чи могли б Ви навести цікавий клінічний випадок пацієнта із підозрою на ЖКХ?
– Пацієнтка, 18 років, ІМТ – 27,2 кг/м2, звернулась за консультацією гастроентеролога зі скаргами на ниючий біль у правій підреберній ділянці, здуття живота, несформовані випорожнення. Симптоми з’явилися близько 7 днів тому. Пацієнтка 2 тижні тому лікувалась із приводу гострого бронхіту (з її слів, приймала антибіотики, амброксол, вітаміни). Під час УЗД виявлено біліарний сладж та конкремент розміром до 15 мм у діаметрі у жовчному міхурі, ознаки метеоризму. Пацієнтці призначено урсодеоксихолеву кислоту (УДХК, Холудексан) у дозі 900 мг 1 р/добу та мебеверин 400 мг 1 р/ добу. Через 7 днів лікування дискомфорт у правому підребер’ї зник. Через 1 місяць пацієнтка звернулась за альтернативною консультацією зі скаргами на метеоризм та несформовані випорожнення до 3 разів на добу, які продовжували її турбувати. За результатами повторного УЗД порівняно з попередніми знімками відзначено позитивну динаміку (конкременти відсутні, жовч однорідна).
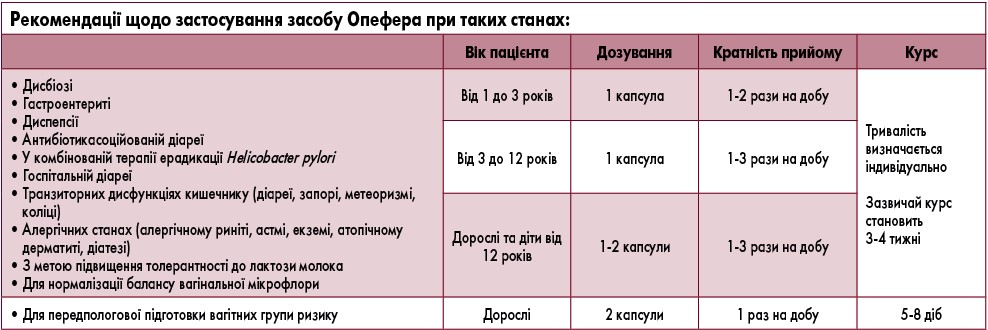
Згідно з даними амбулаторної карти пацієнтки, з приводу гострого бронхіту вона отримувала цефтріаксон 2 г 1 р/добу протягом 7 днів. Тому єдиною проблемою даної пацієнтки залишалася антибіотикасоційована діарея, і було прийнято рішення про її лікування метронідазолом 1000 мг 1 р/добу (курс – 7 днів) у комбінації з пробіотиком Опефера – 2 капсули на добу (курс – 14 днів). Використання цієї терапевтичної тактики забезпечило хороші результати.
? Чим можна пояснити таке фантастичне виліковування ЖКХ за 1 місяць?
– Перш за все потрібно зазначити, що у пацієнтки була не ЖКХ. В інструкції для медичного застосування препарату цефтріаксон вказано, що за наявності тіней на сонограмі слід враховувати можливість утворення преципітатів кальцієвої солі цефтріаксону. Частота затінень на сонограмі жовчного міхура, які вважались жовчними каменями, збільшувалася при застосуванні цефтріаксону в дозі 1 г на добу і вище. Частіше це зустрічається у дітей. Зазвичай такі преципітати зникають після завершення антибіотикотерапії. У рідкісних випадках утворення преципітатів кальцієвої солі супроводжується появою характерних симптомів. У таких клінічних ситуаціях хворий потребує призначення консервативного лікування, і лікар повинен прийняти рішення про дострокове припинення антибіотикотерапії на підставі оцінки співвідношення користь/ризик для конкретного пацієнта.
? Чому у цій клінічній ситуації для корекції антибіотикасоційованої діареї Ви обрали пробіотичний засіб Опефера?
– Головним завданням у випадку ліквідації антибіотикасоційованої діареї є оптимізація бактеріального складу кишечнику. З цією метою у практичній медицині застосовують пребіотики, пробіотики та синбіотики. Проте дедалі більшу увагу лікарів-клініцистів привертають синбіотики, які поєднують властивості пре- і пробіотика в одному засобі та мають значно більш широкий спектр терапевтичних ефектів стосовно нормалізації складу мікрофлори кишечнику, підвищення її захисних функцій, у тому числі імунітету, знешкодження патогенних мікроорганізмів (K.R. Randey, 2015).
При виборі оптимального пробіотика ми керувались критеріями не тільки збалансованого бактеріального складу засобу, а й наявності інших компонентів, які б сприяли більш ефективному відновленню мікрофлори кишечнику. За цими критеріями ми обрали про- та пребіотичний комплекс із протизапальною дією Опефера (компанія World Medicine), який містить у своєму складі живі ліофілізовані бактерії 1,94×109 КУО (Lactobacillus rhamnosus – 0,5×109 КУО, Lactobacillus plantarum – 0,2×109 КУО, Streptococcus thermophiles – 0,5×109 КУО, Lactobacillus acidophilus – 0,5×109 КУО, Bifidobacterium spp. (Bifidobacterium bifidum, Bifidobacterium longum, Bifidobacterium infantis) – 0,24×109 КУО), Saccharomyces boulardii – 65 мг, сухий екстракт ромашки аптечної (Matricaria chamomilla L.) – 50 мг, інулін – 200 мг. Лакто- та біфідобактерії у складі комбінованого пробіотика мають високу антагоністичну активність відносно широкого спектра патогенних та умовно-патогенних мікроорганізмів, пригнічують життєдіяльність стафілококів, шигел, ротавірусів, протея, ентеропатогенної кишкової палички, деяких дріжджоподібних грибів. Це сприяє розмноженню корисних бактерій у кишечнику, а також підтримці фізіологічної рівноваги мікробіому, підвищенню неспецифічної резистентності організму. Компоненти засобу Опефера чинять імуностимулюючу дію, активуючи синтез деяких амінокислот, вітамінів, всмоктування заліза, кальцію.
! Що стосується ЖКХ, слід зазначити, що лакто- та біфідобактерії, які містить пробітик Опефера, покращують пристінкове травлення у кишечнику, беруть участь у ферментативному розщепленні білків, жирів, вуглеводів та процесах метаболізму жовчних кислот і холестерину.
S. boulardii чинять біологічну захисну дію відносно нормальної кишкової мікрофлори. Наявність у складі засобу Опефера екстракту квіток ромашки аптечної розширює спектр терапевтичних ефектів пробіотика за рахунок протизапального, спазмолітичного, антимікробного, в’яжучого, потогінного, жовчогінного та седативного ефектів.
! Серед компонентів, які містить у своєму складі пробіотик Опефера, слід виокремити ІНУЛІН – рослинний полісахарид, який є полімером D-фруктози. Позитивна дія інуліну на організм включає: підвищення імунітету та активацію захисних механізмів, гепатопротекцію, елімінацію з організму важких металів та радіонуклідів, стимуляцію росту та активності лактобактерій, прискорення процесів травлення, зменшення інтоксикації, зниження ризику розвитку онкологічних захворювань, покращення всмоктування кальцію та магнію, а також імуностимулювальний, гіпохолестеринемічний, гіпоглікемічний ефекти.
? Яка тактика медикаментозної корекції біліарного сладжу?
– Лікування біліарного сладжу включає корекцію харчування та фізичної активності пацієнта, а також призначення препаратів УДХК у дозі 10-15 мг/кг маси тіла одноразово на ніч. Ефективність урсотерапії, тривалість якої має становити не менше 3 місяці, сягає 85-95%. За необхідності терапію продовжують до повної елімінації сладжу з жовчного міхура (як правило, до 6 місяців). Таким пацієнтам із періодичністю 1 раз у 3 місяці слід проводити УЗД та лабораторне дослідження крові (рівень загального холестерину, аланінамінотрансферази, аспартатамінотрансферази, лужної фосфатази, гаммаглютамілтранспептидази).
? Чи маєте Ви досвід застосування препаратів УДХК у лікуванні біліарного сладжу? Який із представлених на фармацевтичному ринку України препаратів УДХК Ви рекомендували б для використання у пацієнтів із біліарним сладжем?
– Ми провели дослідження за участю 32 пацієнтів (10 чоловіків та 22 жінок) із біліарним сладжем. За результатами УЗД, окрім сонографічних ознак осаду в жовчному міхурі, звертає на себе увагу висока частота супутніх УЗ-ознак дифузних змін підшлункової залози (56,3%) і стеатозу печінки (40,6%). Пацієнтам призначено препарат Холудексан (компанія World Medicine) у дозі 10-15 мг/кг одноразово на ніч. Позитивна УЗ-динаміка та покращення біохімічних показників крові спостерігалися вже через 1, 2 та 3 місяці.
! Холудексан володіє кількома механізмами дії, які дозволяють досягти максимального терапевтичного ефекту. У випадку біліарного сладжу УДХК у складі препарату Холудексан сприяє зниженню літогенності жовчі – патогенетичного механізму, що ініціює утворення конкрементів у жовчному міхурі. Крім запобігання літогенезу, УДХК сприяє розчиненню уже наявних холестеринових каменів.
Дані численних наукових досліджень підтверджують важливу роль у розвитку ЖКХ порушення ліпідного обміну на різних його рівнях. УДХК нівелює ці розлади за рахунок вираженого гіпохолестеринемічного ефекту, а саме – зниження всмоктування холестерину в кишечнику, його синтезу в кишечнику та екскреції в жовч. Антихолестатичний ефект препарату Холудексан реалізується завдяки інгібуванню секреції токсичних жовчних кислот і стимуляції екзоцитозу в гепатоцитах шляхом активації Са2+-залежної α-протеїнкінази, що супроводжується зниженням концентрації гідрофобних жовчних кислот. Не менш важливим є холеретичний ефект УДХК. Індукція бікарбонатного холерезу активує виділення гідрофобних жовчних кислот у кишечник.
Серед інших позитивний ефектів лікарського засобу Холудексан слід виділити: цитопротективний (УДХК вбудовується у фосфоліпідний шар мембрани, стабілізує її та підвищує стійкість клітин до дії ушкоджувальних факторів), диференційний вплив на регенерацію гепатоцитів (активація мітозу після резекції печінки, що підтверджено в експериментах на тваринах, і гальмування проліферації клітин гепатоми у людини), модуляцію апоптозу (завдяки зниженню концентрації Са2+ у клітині та збереженню цитохрому С у мітохондріях, гальмуванню апоптозу гепатоцитів при холестатичних захворюваннях печінки, доведеному антиапоптичному ефекті відносно структур центральної нервової системи та апоптичному – щодо слизової оболонки кишечнику), імуномодулювальний (зниження експресії молекули HLA 1-го класу гепатоцитів та HLA 2-го класу холангіоцитів, інгібування синтезу прозапальних цитокінів), протизапальний (зниження рівня еозинофілів і простагландину Е2 у хворих із первинним біліарним цирозом, зниження активності фосфоліпази А2 у пацієнтів із ЖКХ, гальмування вивільнення медіаторів запалення при запальних захворюваннях кишечнику). Існують дані щодо антитоксичного ефекту УДХК у відношенні центральної нервової системи та печінки та протипухлинної дії (запобігання виникненню специфічних для раку кишечнику мутацій гена Ras, блокування активації «диких» типів Ras, гальмування експресії циклооксигенази‑2 у ракових клітинах, стимуляція апоптозу у слизовій оболонці товстого кишечнику).
! Результати багатьох клінічних досліджень підтверджують, що застосування комбінації статинів та УДХК є найбільш ефективним для досягнення цільового рівня показників ліпідного обміну при дисліпідемії. На фоні застосування УДХК також покращуються показники глікемічного контролю та підвищується чутливість рецепторів до інсуліну.
Ефективність застосування лікарського засобу Холудексан підтверджено у низці клінічних випробувань. Зокрема, доведений позитивний вплив УДХК на ліпідний обмін у хворих із постхолецистектомічним синдромом. У пацієнтів з ЖКХ після видалення жовчного міхура, крім порушень функцій позапечінкових жовчних проток і сфінктера Одді, які формують постхолецистектомічний синдром, має місце дисліпідемія з підвищенням у сироватці крові вмісту загального холестерину, холестерину ліпопротеїнів низької і дуже низької щільності, тригліцеридів і зниженням концентрації холестерину ліпопротеїнів високої щільності.
! Призначення персоніфікованого дієтичного лікування та препарату УДХК Холудексан сприяє зменшенню сонографічних ознак стеатозу печінки, діаметра холедоха, зниженню у сироватці крові вмісту атерогенних ліпідів і підвищенню рівня холестерину ліпопротеїнів високої щільності (Г.А. Анохина, В.В. Харченко, 2016).
? Яке місце посідають препарати УДХК у лікуванні та профілактиці ЖКХ?
– Згідно із чинними рекомендаціями з лікування ЖКХ (EASL, 2016), літоліз із застосуванням препаратів УДХК не рекомендований за наявності конкрементів у жовчному міхурі. Це пояснюється низькою ефективністю цієї терапії, яка становить тільки 63% (за даними хірургічної періодики – 27%). Розчиненню піддаються лише некальцифіковані конкременти за умови збереження нормальної функції жовчного міхура. Курс лікування у таких випадках має становити не менше 6 місяців. Проте існує високий ризик рецидиву захворювання: через 5 років – 25-64%, через 10 років – 49-80%. Тому методом вибору лікування симптомних конкрементів жовчного міхура є лапароскопічна холецистектомія.
Проте у рекомендаціях EASL (2016) вказано, що урсопрофілактика у дозі ≥500 мг 1 р/добу рекомендована при швидкому схудненні (>1,5 кг у тиждень) та після баріатричних втручань, які у 70% випадків призводять до розвитку ЖКХ. Часто трапляються ситуації, коли пацієнт не дає згоду на лапароскопічну холецистектомію та наполягає на медикаментозному лікуванні. Тому хворому слід навести переконливі аргументи, що такий вибір не завжди є виправданим, адже кількість пацієнтів, яких можна вилікувати УДХК, становить 6-30%. Проте випадки успішного лікування ЖКХ за допомогою УДХК не є поодинокими, і такі клінічні ситуації зустрічались у моїй практиці.
Наприклад, пацієнтка, 31 рік, ІМТ – 22,4 кг/м2, звернулась за консультацією у зв’язку з виявленим за допомогою УЗД конкрементом у жовчному міхурі розміром до 12 мм у діаметрі. Хворій рекомендована лапароскопічна холецистектомія, на яку вона не погодилась. Згідно із висновком УЗД, проведеного за півроку до ідентифікації конкременту, виявлено пристінковий осад у жовчному міхурі. Відомо, що протягом 3 міс до появи симптомів пацієнтка отримувала комбіновані оральні контрацептиви, які їй призначив гінеколог. Хвору поінформовано про можливі ускладнення ЖКХ на будь-якому етапі лікування. Пацієнтці призначено препарат Холудексан у дозі 900 мг 1 р/добу. Через 3 місяці лікування констатовано відсутність УЗ-динаміки, проте уже після 6 місяців лікування сонографія жовчного міхура показала однорідний вміст та відсутність конкрементів. Через 7 років: УЗД – стінка жовчного міхура 3 мм, вміст однорідний.
? Які профілактичні заходи дозволяють запобігти розвитку ЖКХ?
– Профілактика літогенезу та запобігання появі симптомів на тлі наявних конкрементів у жовчному міхурі включає здоровий спосіб життя, раціональне харчування, фізичну активність та підтримання оптимальної маси тіла. Цей комплекс профілактичних заходів рекомендований також у пацієнтів із серцево-судинними захворюваннями, ожирінням, цукровим діабетом 2 типу, неалкогольною жировою хворобою печінки та ін.
У розвитку ЖКХ важливу роль відіграє порушення мікробіому кишечнику. Сьогодні існують дані про достовірну різницю складу кишкової мікрофлори у пацієнтів із ЖКХ і без неї. Тому підтримання нормального складу мікробіому кишечнику – це один із шляхів запобігання розвитку ЖКХ. Серед профілактичних заходів при ЖКХ, які включають, зокрема, дієтотерапію та нормалізацію складу жовчі, важливе місце займає нутритивна підтримка за допомогою про- та пребіотичних засобів.
Для лікування біліарного сладжу та розчинення холестеринових конкрементів у жовчному міхурі широко застосовують препарати УДХК. У багатьох клінічних ситуаціях УДХК не може замінити холецистектомію. Проте використання УДХК є привабливою та реальною альтернативою у лікуванні окремих пацієнтів із ЖКХ, а також можливе як доповнення до хірургічного лікування або ударно-хвильової літотрипсії жовчних конкрементів. Важливе місце серед представлених на вітчизняному фармацевтичному ринку засобів УДХК належить препарату Холудексан, який відрізняється оптимальним співвідношенням ціни та якості.
Підготувала Ілона Цюпа
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (49), жовтень 2018 р.