21 грудня, 2018
Эффективность, безопасность и перспективы рационального подхода в клиническом применении фитопрепаратов
Продолжение. Начало в № 15-16.
 Среди ПР, ассоциированных с назначением препаратов на основе ЛР, преобладают проявления различных аллергических реакций (64,6% случаев), вторую позицию занимают осложнения в ЖКТ (10% случаев), сердечно-сосудистые нарушения и ПР со стороны центральной и периферической нервной системы составили 3 и 2% случаев соответственно. Также обращает на себя внимание то, что 7,6% из них относились к серьезным ожидаемым ПР, возникавшим преимущественно на фоне применения препаратов отечественного производства. Однако после отмены препарата в 100% случаев эти нежелательные явления проходили без последствий.
Среди ПР, ассоциированных с назначением препаратов на основе ЛР, преобладают проявления различных аллергических реакций (64,6% случаев), вторую позицию занимают осложнения в ЖКТ (10% случаев), сердечно-сосудистые нарушения и ПР со стороны центральной и периферической нервной системы составили 3 и 2% случаев соответственно. Также обращает на себя внимание то, что 7,6% из них относились к серьезным ожидаемым ПР, возникавшим преимущественно на фоне применения препаратов отечественного производства. Однако после отмены препарата в 100% случаев эти нежелательные явления проходили без последствий.
В структуре системных ПР не наблюдалось значимой разницы между фитопрепаратами и синтетическими ЛС (как показывает статистика, в Украине с 1996 года при медицинском применении ЛС любого происхождения доминирует лекарственная аллергия и осложнения со стороны ЖКТ). Это говорит о том, что, с одной стороны, нет абсолютно безопасных ЛС (независимо от того, растительного они или синтетического происхождения), а с другой – что необходим постоянный контроль возможных ПР вследствие приема фитопрепаратов со стороны врачей разных специальностей и более продуманный подход к безрецептурному отпуску указанных ЛС. Необходимо также обратить внимание еще на одно обстоятельство: в 2,7% случаев ПР относились к непредвиденным, т. е. информация об этих ПР отсутствовала в инструкции по применению препарата.
Таким образом, даже, казалось бы, хорошо изученные в ходе научных исследований фитопрепараты, имеющие вдобавок клинически доказательную базу, могут преподнести неприятные «сюрпризы».
В качестве примера приведем клинико-фармакологическую характеристику успешно применяемого препарата, содержащего основное БАВ расторопши пятнистой – силимарин, который представляет собой комплекс 4 изомеров: силибинин, изо-силибинин, силидианин, силикристин (Соколов С. Я., 2000). Во второй половине ХХ ст. на фармацевтическом рынке появились лекарственные препараты на основе этого ЛР, включенного к тому времени в фармакопеи большинства стран мира, в т. ч. и европейскую (Савустьяненко А. В., 2009).
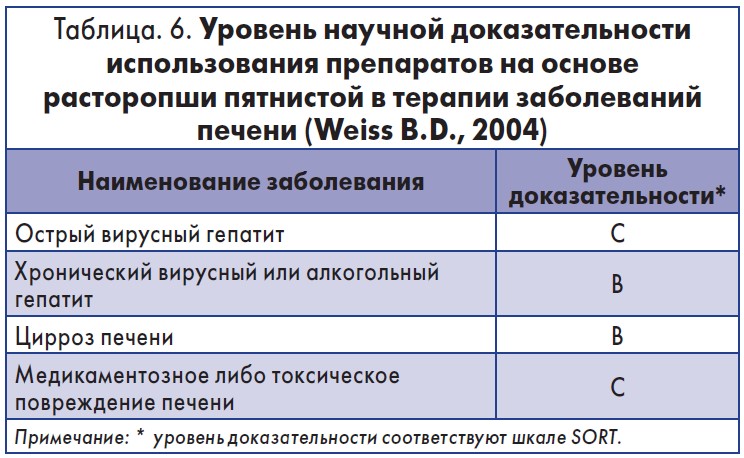
Фармакологические свойства силимарина разнообразны (Соколов С. Я., 2000): антиоксидантное, антитоксическое, гемостатическое, гепатопротекторное, дезинтоксикационное, желчегонное, противовоспалительное, тонизирующее организм, улучшающее пищеварение, холеретическое, холекинетическое. Эксперты Всемирной организации здравоохранения (ВОЗ) считают, что основные эффекты силимарина – антиоксидантный, антигепатотоксический, противовоспалительный и противоаллергический имеют убедительную доказательную базу (WHO, 2002). В нашей стране в медицинской практике нашли широкое применение более 10 препаратов на основе семян расторопши как отечественного, так и зарубежного производства, применяемых при различных заболеваниях гепатобилиарной системы (Савустьяненко А. В., 2009) (табл. 6).
Управление пострегистрационного мониторинга ГП «Государственный фармакологический центр» МЗ Украины за период 1996-2009 гг. зарегистрировало 26 случаев ПР при медицинском применении препаратов силимарина отечественного (38,4%) и зарубежного (61,6%) производства. В 88,4% всех случаев это были ожидаемые несерьезные ПР, которые проходили без последствий для здоровья пациентов; в 19,2% – ни коррекция дозового режима, ни отмена препарата не потребовались; в 38,4% – препарат отменили, в 38,4% – не только был отменен препарат, но и назначена дополнительная фармакотерапия, а у 3,8% пациентов одновременно с отменой силимарина отменялся прием сопутствующих ЛС и осуществлялись фармакотерапевтические мероприятия «прикрытия» ПР. Значимые возрастные различия у взрослой части пациентов отсутствовали (мужчин было 46,1%, женщин – 44,4%, детей – 9,5%).
В перечне всех системных нарушений, вызванных медицинским применением силимарина, лидирующие позиции занимали аллергические реакции (69,1%), проявлявшиеся преимущественно изменениями со стороны кожи и ее придатков (61,5%); расстройства функции ЖКТ (тошнота, рвота, боли в эпигастральной области, диарея, извращение вкусовых ощущений) – 26,8%; слуховые и вестибулярные расстройства – 3,8%. Следует отметить, что аллергический анамнез был отягощен только у 5,5% пациентов с аллергическими реакциями.
Как уже отмечалось, последствия взаимодействия ЛС между собой при одновременном применении или с пищей неоднозначны: они могут либо усиливать благоприятный терапевтический эффект, либо быть источником возникновения и развития ПР (Викторов А. П. и соавт., 2007). Например, при одновременном приеме силимарина и пероральных контрацептивных средств и препаратов, применяемых при эстрогензаместительном лечении, возможно снижение эффективности последних. В то же время силимарин может активизировать действие таких ЛС, как диазепам, алпрозолам, кетоконазол, ловастатин, винбластин, благодаря своему ингибирующему воздействию на систему цитохрома Р450, что требует внимания со стороны врача и осознанного самоконтроля самого пациента, особенно полиморбидного.
Вместе с тем необходимо отметить, что при сопоставлении, согласно критериям ВОЗ, объемов продаж и, соответственно, назначений с числом зарегистрированных случаев ПР, препараты силимарина, разрешенные для медицинского применения в Украине, эффективны и достаточно безопасны. Однако бесконтрольный их прием может принести вред пациенту.
Длительный прием препаратов на основе ЛР может привести к привыканию, поэтому рекомендуется периодически менять травы и сборы из них (Кукес В. Г. и соавт., 1999; Соколов С. Я., 2000). В среднем схему траволечения советуют обновлять каждые 3-4 нед. Более того, многие ЛР непригодны для приема их длительными курсами – накапливаясь в организме, они начинают оказывать на него выраженное отрицательное воздействие.
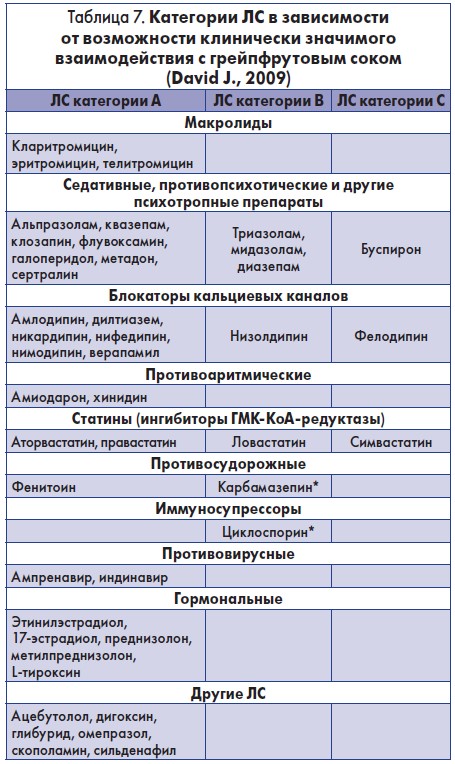
Нельзя также не учитывать возможное негативное взаимодействие препаратов ЛР с пищей (Викторов А. П. и соавт., 2007). В этом плане нельзя не упомянуть о горячей дискуссии, разгоревшейся и в прессе, и в медицинских кругах в начале нынешнего столетия, по поводу негативных последствий взаимодействия грейпфрутового сока с представителями различных фармакологических ЛС. В последние годы приводимые тогда аргументы получили несколько иную трактовку. Спектр ЛС, метаболизм которых может нарушаться под воздействием грейпфрутового сока, на самом деле не так уж широк. В таблице 7 они дифференцированы на 3 категории (А, В и С) в зависимости от выраженности ингибирующего эффекта при употреблении 1 стакана грейпфрутового сока (200-250 мл сока получают из 1 целого плода) обычной концентрации.
 Рекомендации относительно употребления грейпфрутового сока на фоне приема различных ЛС (David J., 2009):
Рекомендации относительно употребления грейпфрутового сока на фоне приема различных ЛС (David J., 2009):
- категория А – вероятность клинически значимого взаимодействия низкая или крайне малая. Пациенты, принимающие ЛС этой категории, могут пить грейпфрутовый сок без опасений относительно их взаимодействия;
- категория В – взаимодействие указанных ЛС с грейпфрутовым соком вероятно: пациенты, принимающие ЛС категории В, не должны избегать употребления грейпфрутового сока, но они и их лечащий врач обязаны знать, что эффекты препаратов могут усиливаться;
- категория С – значительная вероятность клинически значимого взаимодействия, поэтому следует избегать употребления грейпфрутового сока или заменить ЛС, имеющим более низкую вероятность взаимодействия с этим соком.
Нередки случаи негативных последствий для здоровья из-за взаимодействия БАВ, содержащихся в ЛР, и некоторых продуктов питания (Викторов А. П. и соавт., 2007). Например, на фоне приема ингибиторов фермента моноаминокасидазы (МАО) недопустимо употребление продуктов с высоким содержанием тирамина (зрелые сыры, мясные копчености, копченая, маринованная и вяленая рыба, вина, пиво и др.), так как это может спровоцировать развитие АГ и наступление сосудистых катастроф.
Рост популярности траволечения ассоциируется с повышением частоты случаев фитогепатопатии, причем эта тенденция прослеживается во многих странах (Gunawan B., Kaplowitz N., 2004). Особой гепатотоксичностью обладают растения, содержащие пирролизидиновые алкалоиды (окопник лекарственный, крестовник плосколистный, растения рода Кроталярия, дубровник, гелиотропы). Известны случаи массового заболевания гелиотропным гепатитом вследствие употребления в пищу хлеба, приготовленного из зерна с примесью семян сорняка гелиотропа опущенноплодного. Токсическое действие растительных пирролизидинов может проявляться даже развитием веноокклюзионной болезни печени (Whiting P. W. et al., 2002). На патогенез индуцированных ЛС повреждений печени влияют и некоторые компоненты растения, в процессе метаболизма преобразующиеся в гепатотоксические агенты. Так, был зарегистрирован целый ряд случаев фитогепатита после употреблении микстуры, в составе которой были валериана и шлемник, в связи с чем продажи этой микстуры были запрещены в США еще в 2001 г. Отмечено проявление гепатотоксических реакции даже на гомеопатические препараты (Бабак О. Я., 2008).
Чтобы предотвратить возникновение ПР на фоне приема фитопрепаратов, необходимо учитывать многие факторы: состояние сердечно-сосудистой системы (уровень АД, частота сердечных сокращений и др.); ЖКТ (характер стула, показатели рН и др.); исходное состояние центральной нервной системы (чувство подавленности, возбудимость и пр.); наличие онкологических патологий; возраст и пол; беременность; период грудного вскармливания (например, шишки хмеля обыкновенного, листья шалфея лекарственного подавляют лактацию, а плоды аниса обыкновенного, трава клевера лугового, ядра грецких орехов и др. – усиливают ее). Практикующему врачу необходимо всегда помнить, что рациональная фитотерапия основана на соблюдении определенных принципов относительно профилактики и лечения ПР (табл. 8).
У авторов данной статьи не было цели дискредитировать фитопрепараты (а также их разработчиков и производителей), применяемые в моно- или комбинированных схемах лечения, или фитотерапию в целом. Право на активное использование, эффективное и безопасное применение этих ЛС давно уже не оспаривается. Каждый из них имеет свой известный «фармакотерапевтический коридор» с вполне удовлетворительным клиническим результатом. Речь идет о том, чтобы привлечь внимание к необходимости рационального назначения этих ЛС с учетом всего комплекса возможных проблем, связанных с взаимодействием между собой как в экстракорпоральных, так и в интракорпоральных условиях – между собой и организмом пациента, особенно при длительном применении, прежде всего у полиморбидных больных.
При этом особое значение приобретает способность БАВ ЛР оказывать влияние на фармакодинамику и фармакокинетику синтетических ЛС при взаимодействии с ними. Так, зверобой, индуцирующий CYPЗА4 и CYP2Е1, снижает концентрацию в крови не только производных кумарина, но и дигоксина, теофиллина, циклоспорина, ингибиторов протеазы амитриптилина и пероральных контрацептивов. Причем данный эффект более выражен у женщин, чем у мужчин. Имеются данные, когда женьшень провоцировал маниакальные эпизоды, а йохимбин повышал риск развития АГ у пациентов, принимающих антидепрессанты.
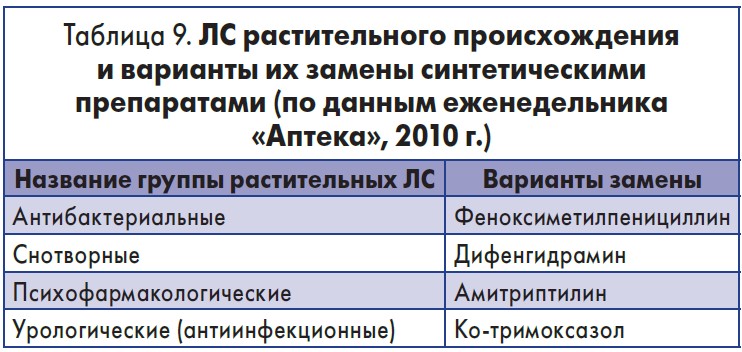
Отдельно следует остановиться на концепции «ответственного самолечения» и «самопрофилактики», сформировавшейся в начале 80-х гг. прошлого столетия. Ее внедрение предполагало использование препаратов группы ОТС (оver the counter – безрецептурное лекарство), в т. ч. и на основе ЛР. Принадлежность к этой группе в первую очередь определялось известностью и изученностью фармакологических свойств ЛС, доказательным хорошим профилем безопасности и относительно редкими несерьезными ПР. Кроме того, предполагалось, что такой подход будет сочетаться с экономической доступностью и удобством (приемлемостью) для пациента. И если добавить к этим факторам высокий уровень санитарной и общей культуры населения, а также добросовестную рекламу производителей ОТС-препаратов – это способствовало бы уменьшению нагрузки на врачей и лечебные учреждения, а медицинскому персоналу дало бы возможность сосредоточиться на больных, требующих неотложной или специализированной помощи. К сожалению, в мировой медицинской практике эта инициатива к особым успехам не привела. Более того, в последние годы в странах Евросоюза (в связи со снижением объемов продаж) наблюдается тенденция к замене некоторых растительных препаратов с сомнительной эффективностью на ЛС синтетического или иного происхождения (табл. 9).
Безусловно, каждое из имеющихся на фармацевтическом рынке ЛС имеет свою лечебную ценность, но отношение к ним должно быть рациональным, без «мифологизации». Лечащие врачи и пациенты не должны заблуждаться, думая, что фитопрепараты во всех случаях абсолютно безопасны. Такими же сомнительными следует признать и такие аргументы, как высокая стоимость (и, как следствие, недоступность) синтетических ЛС, возможность приобрести фитопрепарат без рецепта, уверенность в позитивном многовековом опыте использования лекарственных трав и тому подобные заблуждения.
Скорее всего, люди по-прежнему будут заниматься самолечением в силу разного рода обстоятельств и причин. Но чтобы самолечение не нанесло ущерба ни больному, ни государству, оно должно находиться под постоянным компетентным врачебным контролем и ответственным самоконтролем со стороны самого больного. Ответственность перед конкретным пациентом и перед обществом в целом, желание выбрать наиболее эффективную терапевтическую стратегию, способную избавить больного от страданий, выдвигает ряд задач, которые могут быть решены только совместными усилиями врачей, фармацевтов, разработчиков и производителей ЛС.
Медична газета «Здоров’я України 21 сторіччя» № 18 (439), вересень 2018 р.