6 січня, 2019
RePer: многоцентровое ретроспективное обсервационное исследование по оценке терапии первой линии на основе пертузумаба, трастузумаба и таксанов у пациенток с распространенным HER2-положительным раком грудной железы
Повышенная экспрессия рецептора человеческого эпидермального фактора роста 2 типа (HER2) и амплификация его гена имеют место примерно в 15-20% случаев рака грудной железы (РГЖ) и ассоциированы с повышенной агрессивностью опухоли, неблагоприятным прогнозом и сокращением выживаемости пациенток [1]. Показано, что при распространенном злокачественном РГЖ комбинация химиотерапии (в частности, таксанов) и трастузумаба (моноклонального антитела, направленного против мембранного HER2) способна обеспечивать высокую частоту ответа и увеличение выживаемости больных [2, 3]. Однако, поскольку применение антрациклина в комбинации с трастузумабом характеризуется повышенным риском кардиотоксичности [1, 4], было предложено использовать альтернативные комбинации на основе трастузумаба (например, с винорелбином, капецитабином, гемцитабином, летрозолом или анастрозолом), которые показали определенную эффективность при распространенном РГЖ [5-10]. При этом тройные комбинации на основе трастузумаба (т.е. трастузумаб + 2 химиотерапевтических средства) не продемонстрировали преимущества в сравнении с двойными комбинациями (трастузумаб + 1 химиотерапевтический препарат) [11, 12], поэтому стандартным лечением 1-й линии оставалась комбинация таксана и трастузумаба. Но недавно в рандомизированном клиническом исследовании III фазы Cleopatra было установлено, что применение в комбинации с трастузумабом и доцетакселом пертузумаба (инновационного препарата на основе гуманизированных моноклональных антител, мишенью для которых является HER2) обеспечивает четкое преимущество как в плане выживаемости без прогрессирования (ВБП) заболевания, так и общей выживаемости (ОВ) по сравнению со стандартной терапией трастузумабом и доцетакселом [13-15]. Полученные результаты стали основой для одобрения этого режима в качестве терапии 1-й линии при распространенном HER2-положительном РГЖ. В последующем результаты исследования II фазы подтвердили эффективность и безопасность применения комбинации пертузумаба, трастузумаба и паклитаксела (вводимого 1 раз в неделю) в качестве терапии 1-й и 2-й линии при распространенном РГЖ [16].
В настоящее время комбинация трастузумаб/пертузумаб и таксан рассматривается как золотой стандарт терапии 1-й линии при HER2-положительном распространенном РГЖ. Незначительное количество предварительных отчетов у больных, получавших такое лечение вне рамок клинических исследований, подтверждают его эффективность и переносимость [17, 18]. С учетом того, что больные, получавшие лечение в рамках проспективных рандомизированных исследований, обычно отбираются для участия в них на основании строгих критериев включения/исключения, а их популяция необязательно отражает характеристики реальной популяции пациенток, нами было выполнено крупное ретроспективное обсервационное исследование с участием пациенток с распространенным HER2-положительным РГЖ, получавших терапию 1-й линии с использованием комбинации пертузумаба, трастузумаба и таксана, на базе нескольких онкологических центров Италии.
Результаты
В целом была выполнена ретроспективная оценка данных 264 пациенток с HER2-положительным распространенным РГЖ (доцетаксел – 205 женщин, паклитаксел – 59 женщин), которые получали лечение с сентября 2012 г. по август 2017 г. в 22 итальянских онкоцентрах.
Основные характеристики включенных в исследование пациенток и диагностированных у них злокачественных опухолей грудной железы представлены в таблице 1.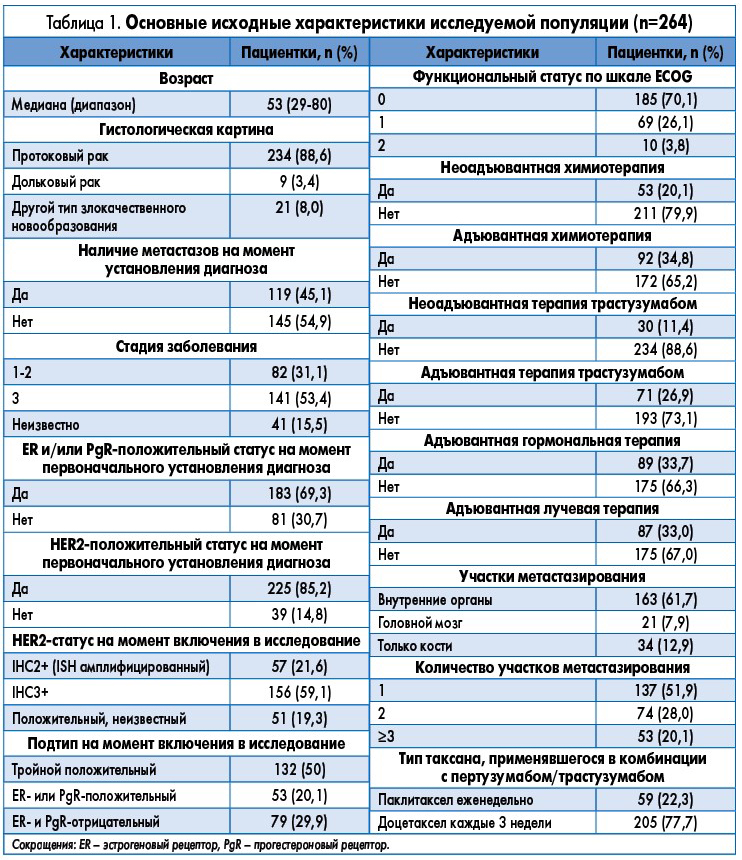
Как видно из данных таблицы, медиана возраста пациенток в исследовании составляла 53 года, медиана показателя оценки общего функционального состояния (ФС) по шкале Восточной объединенной онкологической группы (ECOG) – 0 баллов. 97 пациенток (36,7%) исходно находились в периоде пременопаузы, а 167 (63,3%) – в постеменопаузе.
79 пациенток имели опухоли с негативным результатом анализа на наличие обоих типов гормональных рецепторов, 53 пациентки имели опухоли, экспрессирующие один гормональный рецептор, а 132 пациентки – «трижды положительные» (ER-, PgR-, HER2-положительные) опухоли.
145 пациенток получали предшествующие режимы неоадъювантной (53 женщины) или адъювантной (92 женщины) химиотерапии, включавшие трастузумаб у 30 из 53 и у 71 из 92 пациенток соответственно. 10 пациенток не получали предшествующую терапию трастузумабом на ранней стадии. 13 пациенток получали эндокринную терапию без химиотерапии, но в комбинации с трастузумабом в качестве адъювантного лечения.
Из 264 включенных в исследование пациенток 145 (54,9%) имели рецидив заболевания со значением медианы длительности безрецидивного интервала, равным 53 мес (диапазон – 7-342), тогда как 119 пациенток (45,1%) – метастатическое заболевание de novo. На момент начала лечения у 61,7% пациенток были выявлены висцеральные метастазы, у 12,9% – только костные поражения, у 7,9% – асимптомные метастазы в головной мозг, а у 48,1% – множественные участки метастазирования.
Назначенное лечение
Все пациентки получали режимы лечения на основе пертузумаба в качестве химиотерапии 1-й линии по поводу HER2-положительного распространенного РГЖ, и у них могла быть проведена оценка его эффективности. Медиана длительности периода последующего наблюдения составила 21 мес (диапазон – 3-59). Медиана длительности лечения пертузумабом/трастузумабом и химиотерапии составила 4 мес (диапазон – 1-16), медиана количества циклов химиотерапии равна 6 (диапазон – 1-9). Медиана числа циклов терапии доцетакселом составляла 6 (диапазон – 1-20), а медиана количества еженедельных введений паклитаксела – 16 (диапазон – 2-33). Прекращение применения таксанов наиболее часто было обусловлено кумулятивной гематологической токсичностью.
После прекращения химиотерапии 234 пациентки (88,6%) получали поддерживающую терапию пертузумабом/трастузумабом, при этом медиана ее длительности составляла 15 мес (диапазон – 2-43). Примечательно, что 46% пациенток получали такое лечение на протяжении более чем 12 мес в условиях отсутствия прогрессирования заболевания.
Наряду с применением пертузумаба/трастузумаба 103 пациенткам (39%) была назначена эндокринная поддерживающая терапия. Облучение головного мозга было назначено 30 пациенткам на фоне поддерживающей терапии пертузумабом и трастузумабом, в то время как 10 пациенток уже получали лучевую терапию по поводу метастазов в головной мозг до начала применения терапии 1-й линии. В течение периода последующего наблюдения поддерживающее лечение пертузумабом/трастузумабом было прекращено у 144 пациенток (54,6%). Наиболее частыми причинами прекращения терапии являлись прогрессирование заболевания (109 пациенток), токсичность (10 пациенток), решение самой пациентки (8 пациенток) или врачебное решение (17 пациенток).
Эффективность
В целом было зарегистрировано 40 случаев (15,2%) достижения полного ответа (ПО) и 169 случаев (64%) частичного ответа (ЧО) на лечение, при этом общая частота ответа (ОЧО) составила 77,3% (95% доверительный интервал – ДИ – 72,2-82,3) (табл. 2).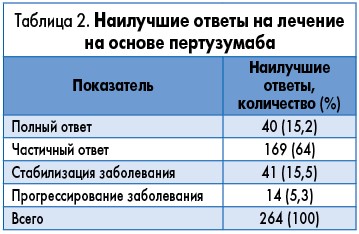
Стабилизация заболевания (СЗ) была зафиксирована у 15,5% пациенток. Клиническая польза (КП), определяемая как ответ на лечение или стабильное течение заболевания на протяжении как минимум 6 мес, была констатирована у 247 (93,6%) пациенток (95% ДИ 90,6‑96,5). Как показано в таблице 3, при выполнении анализа объективных ответов в зависимости от ER/PgR-статуса наблюдались различия, не достигшие статистической значимости (p=0,06).
Среди тех пациенток, у которых на момент установления диагноза уже имелись метастазы (119 женщин), было зафиксировано 18 случаев достижения ПО (15,1%) и 81 ЧО (68,1%), при этом показатель ОЧО составил 83,2% (95% ДИ 76,5-89,9), а частота получения КП – 95,8% (95% ДИ 92,2-99,4). У 75 пациенток, получавших предшествующую неоадъювантную/адъювантную терапию трастузумабом, наблюдалось 12 ПО (16%) и 46 ЧО (61,3%) со значением показателя ОЧО 77,3% (95% ДИ 67,8‑86,8). СЗ была зафиксирована у 15 пациенток (20%), а о КП сообщалось у 72 пациенток (96%; 95% ДИ 91,6-100).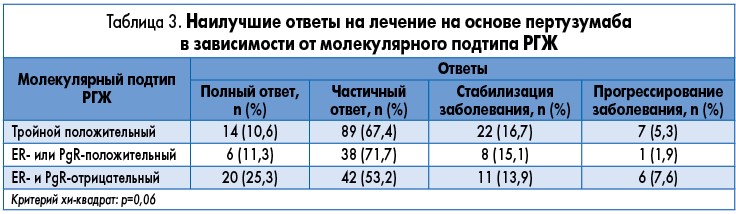
При проведении сравнения между пациентками, ранее не получавшими трастузумаб, и больными, которые уже получали предшествующую терапию этим препаратом, было установлено отсутствие различий в ОЧО (p=0,64).
ОЧО была несколько выше у пациенток с висцеральными метастазами (83,4%) по сравнению с больными с другими участками метастазирования (74,6%) или с вовлечением в метастатический процесс только костной ткани (67,6%), хотя эти различия не достигали статистически достоверной значимости (p=0,07). У пациенток с исходным наличием метастазов в головном мозге (21 пациентка) ОЧО составляла 52,4%, тогда как в подгруппе пациенток без данной локализации метастатического процесса – 81,5% (p=0,002).
В нашей серии клинических случаев значимое различие в частоте ответа наблюдалось в зависимости от вида таксана, назначавшегося в комбинации с пертузумабом/трастузумабом. Так, ОЧО составила 82,9% на фоне применения доцетаксела и 66,1% при применении паклитаксела (p=0,005).
Все пациентки за исключением 30 (27 – ввиду прогрессирования заболевания, 1 – ввиду кардиотоксичности, 2 – ввиду выбытия из последующего наблюдения) после прекращения химиотерапии получали трастузумаб/пертузумаб в качестве поддерживающей терапии. В целом у 37 из 234 пациенток (15,8%) в дальнейшем было констатировано улучшение показателей ответа.
Из 169 пациенток с ER- и/или PgR-положительными опухолями, получавших поддерживающую терапию пертузумабом/трастузумабом, 103 пациентки (60,9%) получали в дополнение эндокринную поддерживающую терапию. Из них у 18 пациенток (17,5%) было продемонстрировано дальнейшее улучшение ответа. Напротив, у 66 пациенток, получавших только пертузумаб/трастузумаб, без гормонального лечения, ЧО в дальнейшем увеличилась лишь в 8 случаях – 12,1% (p=0,39). В этой подгруппе пациенток медиана длительности поддерживающей терапии трастузумабом/пертузумабом составила 8 мес (диапазон – 1-37), а медиана длительности поддерживающей эндокринной терапии – 11 мес (диапазон – 1-55 мес). Центральная нервная система как место дальнейшего прогрессирования заболевания вовлекалась в процесс у 33 пациенток без предшествующих метастазов в головной мозг (13,6%) и у 12 пациенток (57,1%) с исходным наличием метастазов в головном мозге.
Долгосрочные исходы
В целом у включенных в исследование 264 пациенток медиана ВБП составила 21 мес (95% ДИ 17-25), тогда как медиана ОВ не была достигнута (рис. 1).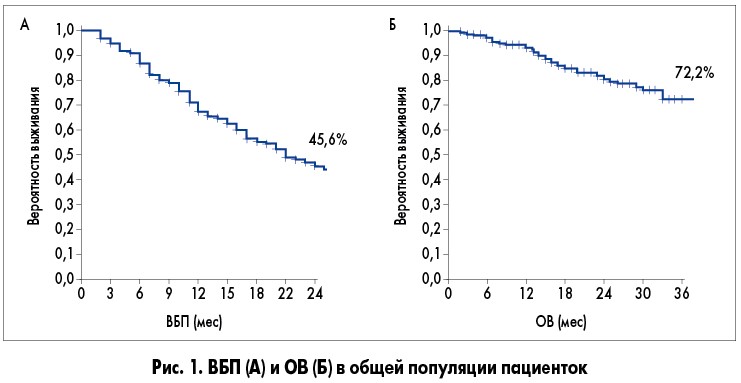
Показатели частоты 1-летней ВБП и 2-летней ОВ приведены в таблице 4.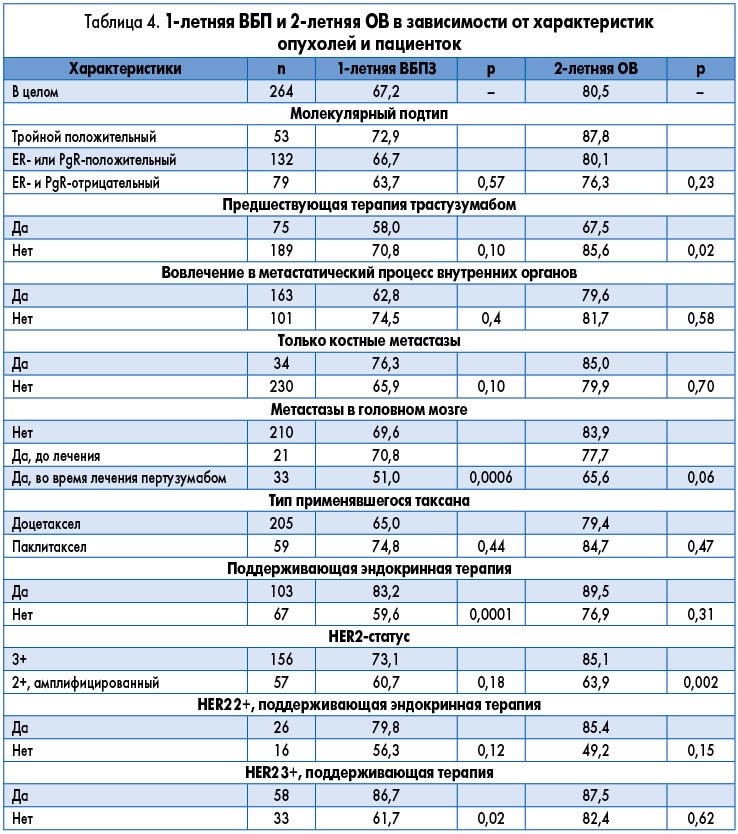
При проведении анализа ВБП и ОВ не наблюдалось каких-либо статистических различий в зависимости от экспрессии гормональных рецепторов или ее отсутствия (p=0,57 и p=0,23 соответственно). Сопоставимые значения медианы ВБП были достигнуты при сравнении подгрупп в зависимости от предшествующего лечения трастузумабом: 13 мес у пациенток, ранее получавших такую терапию, и 23 мес у ранее не получавших ее больных (р=0,10). Напротив, более длительная ОВ была зафиксирована у пациенток, ранее не получавших трастузумаб (р=0,02). Вовлечение в метастатический процесс внутренних органов или наличие только костных метастазов не оказывало какого-либо влияния на ВБП (p=0,40 и p=0,10 соответственно) или ОВ (p=0,58 и p=0,70 соответственно).
У пациенток без исходного наличия метастазов в головном мозге отмечалось большее значение медианы ВБП (26 мес; 95% ДИ 22-30) в сравнении с пациентками с установленным наличием метастазов в головной мозг (20 мес; 95% ДИ 13‑27) или с теми пациентками, у которых метастазы в головной мозг развились во время лечения на основе пертузумаба (13 мес; 95% ДИ 9-17; p=0,0006). Соответственно, частота 2-летней ОВ составила 83,9% у пациенток без исходного наличия метастазов в головном мозге, 77,7% – у пациенток с документально зафиксированным наличием метастазов в головном мозге и 65,6% у тех пациенток, у которых развитие метастазов в головном мозге было констатировано в процессе лечения.
Тип таксана, назначаемого в комбинации с пертузумабом/трастузумабом, не оказывал значимого влияния на долгосрочные исходы – показатели ВБП и ОВ были аналогичными (p=0,44 и p=0,47 соответственно). Поддерживающая эндокринная терапия, назначенная в дополнение к поддерживающему лечению пертузумабом и трастузумабом, была ассоциирована с более длительной ВБП (рис. 2А, 2Б) – она составляла 28 мес (95% ДИ 26-31) в сравнении с 17 мес (95% ДИ 13-21) у пациенток, не получавших поддерживающей эндокринной терапии соответственно (p=0,0001).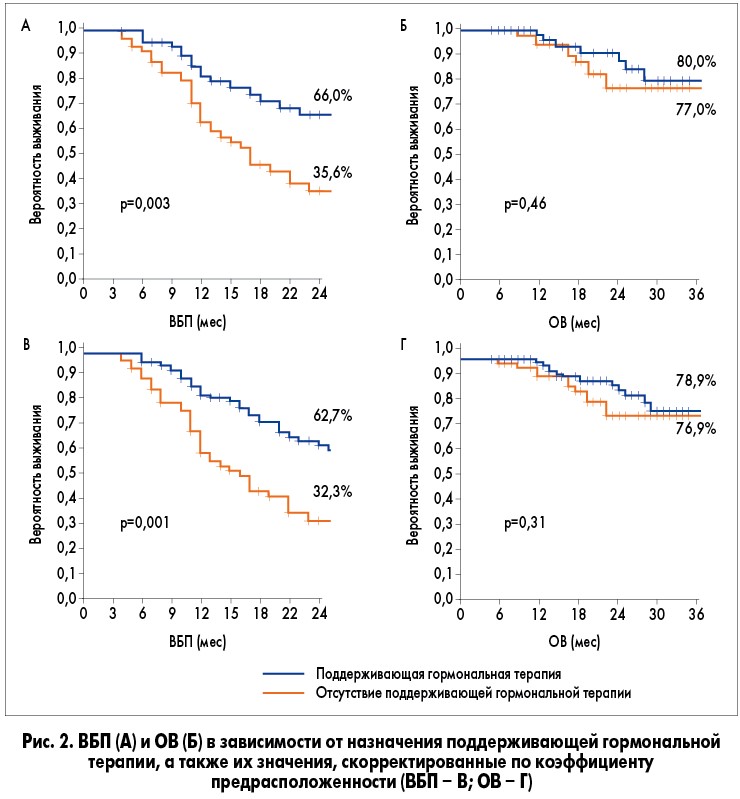
Напротив, каких-либо различий в ОВ в зависимости от поддерживающей эндокринной терапии к настоящему времени не наблюдалось (p=0,31). Результаты были подтверждены при коррекции по коэффициенту предрасположенности – с медианой ВБП 17 мес (95% ДИ 12-22) у пациенток, которые не получали гормональную терапию, и 29 мес (95% ДИ 25-33) у пациенток, которым она назначалась (p=0,003). Каких-либо различий в ОВ в зависимости от проведения поддерживающей эндокринной терапии не наблюдалось и в поле коррекции данных с учетом коэффициентов предрасположенности (p=0,46) (рис. 2В, 2Г).
Не отмечалось значимых различий в медиане ВБП в зависимости от гиперэкспрессии HER2/амплификации гена (p=0,18). Напротив, HER2-статус влиял на ОВ. При этом частота 2-летней ОВ составила 63,9% у пациенток с опухолями с HER2 2+ / амплификацией гена и 85,1% – у пациенток с HER2 3+ опухолями. У пациенток с опухолями с HER2 2+ / амплификацией гена не наблюдалось различий в медиане ВБП в зависимости от двойной поддерживающей терапии (р=0,12). Напротив, в подгруппе пациенток с HER2 3+ опухолями поддерживающая эндокринная терапия, назначенная в дополнение к двойной блокаде HER2, обеспечила достижение более длительной ВБП (p=0,02). Что же касается ОВ, то по данному показателю не наблюдалось каких-либо статистических различий, даже несмотря на то, что у пациенток с опухолями с HER2 2+ / амплификацией, которые получали поддерживающую эндокринную терапию, было продемонстрировано недостоверно большее значение ОВ (p=0,15). У пациенток с HER2 3+ опухолями эндокринная поддерживающая терапия также не оказывала влияния на срок ОВ (p=0,62) (табл. 4).
При проведении многофакторного анализа (табл. 5) преимущество в плане ВБП было ассоциировано с меньшим значением ФС (p=0,07), наличием метастазов на момент установления диагноза (p=0,006) и наличием единственного участка метастазирования (p<0,0001).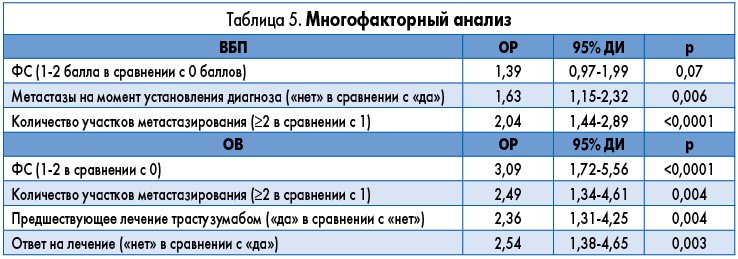
Параметрами, связанными с преимуществом в плане ОВ, являлись меньшее значение оценки ФС (p<0,0001), наличие единственного участка метастазирования (p=0,004), отсутствие предшествующего лечения трастузумабом (p=0,004) и клинический ответ на лечение на основе пертузумаба (p=0,003).
В целом в ходе данного исследования не было идентифицировано новых проблем с безопасностью. Наиболее частыми нежелательными явлениями были диарея, сыпь, воспаление слизистых оболочек и зуд. О возникновении эпизодов фебрильной нейтропении не сообщалось. После прекращения терапии таксанами частота всех нежелательных явлений существенно снизилась.
Что же касается кардиотоксичности, все включенные в исследование пациентки имели исходное значение фракции выброса левого желудочка >50%. В целом у 25 пациенток (9,4%) возникли проявления кардиотоксичности той или иной степени. Кардиотоксичность привела к полной отмене лечения у 9 пациенток (3,4%).
Обсуждение
Данный анализ подтверждает эффективность терапии 1-й линии, включающей пертузумаб, трастузумаб и доцетаксел/паклитаксел, в реальной популяции пациенток с HER2-положительным распространенным РГЖ; при этом частота достижения ответа составила 77,3%, КП – 93,6%, а медиана ВБП – 21 мес. Эти результаты согласуются с результатами, полученными в исследовании Cleopatra [14].
Следует отметить, что существуют некоторые различия между популяцией пациенток в данном исследовании и больными, которые были включены в исследование Cleopatra. Что касается пациенток, получавших предшествующую терапию трастузумабом на ранней стадии заболевания, то в данном исследовании их количество составляло 75 (28,4%), тогда как в опорном исследовании – 47 (11,7%). Более того, в исследуемой популяции пациенток было меньше больных с висцеральными поражениями (61,7% в сравнении с 78,1% в опорном исследовании) и больше пациенток с гормон-рецептор-положительными опухолями (70,1% в сравнении с 47,0%). Кроме того, 103 (39%) пациентки получали поддерживающую эндокринную терапию, которая не допускалась в исследовании Cleopatra. Пациентки с исходным наличием метастазов в головном мозге были включены в наш анализ, в то время как из регистрационного исследования их исключали. В нашей популяции пациенток использование доцетаксела было ассоциировано с более высокой ОЧО в сравнении с применением паклитаксела: 82,9% против 66,1% (p=0,005).
В целом поддерживающая эндокринная терапия была дополнительно назначена к поддерживающей терапии пертузумабом/трастузумабом у 103 пациенток. Как и ожидалось, в подгруппе пациенток, получавших оба типа поддерживающего лечения, отмечался наиболее благоприятный долгосрочный исход: медиана ВБП составила 28 мес, а 2-летняя ОВ – 89,5%.
Мы сообщили о сопоставимой эффективности исследуемого режима терапии в подгруппах, различающихся в зависимости от предшествующего лечения трастузумабом. При этом медиана ВБП составила 17 мес у получавших предварительную терапию трастузумабом пациенток в сравнении с 23 мес у ранее не получавших ее больных (p=0,10). У ранее не получавших трастузумаб пациенток наблюдалась высокая частота 2-летней ОВ (85,6% в сравнении с 67,5%).
Данные, касающиеся эффективности терапии 1-й линии на основе трастузумаба у пациенток с рецидивом после нео-/адъювантной терапии трастузумабом, все еще остаются противоречивыми, даже несмотря меньшее преимущество у пациенток с рецидивом после адъювантной/неоадъювантной терапии трастузумабом [20, 21]. Комбинация пертузумаба и трастузумаба, по-видимому, превосходит использование только одного препарата, оказывающего целенаправленное воздействие на HER2 [13, 14, 22]. Фактически считается, что пертузумаб потенцирует эффект трастузумаба посредством предотвращения димеризации HER2, стимулирования антителозависимой клеточноопосредованной цитотоксичности и ввиду использования различных эпитопов HER2 в качестве участков связывания пертузумаб, как предполагается, проявляет синергичное с трастузумабом действие, обеспечивая более полную блокаду сигнальных путей HER2 [23, 24]. В исследовании II фазы по оценке применения пертузумаба и трастузумаба без химиотерапии у 66 ранее получавших лечение пациенток, у которых развилось прогрессирование заболевания на фоне терапии трастузумабом, были продемонстрированы значения ОЧО и КП, равные 24,2% и 50%, а медиана ВБП составила 5,5 мес. Эти результаты подтверждают эффективность добавления пертузумаба к трастузумабу даже у получавших интенсивное предшествующее лечение пациенток с прогрессированием заболевания в условиях применения режима на основе трастузумаба [25]. В исследовании Cleopatra небольшая подгруппа пациенток, ранее получавших трастузумаб на ранней стадии (т.е. 88 пациенток), имели существенно более благоприятный исход в отношении ВБП (ОР – относительный риск – 0,62), чем пациентки, ранее не получавшие трастузумаб (ОР 0,60) [13], что указывает на преимущество добавления пертузумаба даже в тех случаях, когда у пациенток оказались неэффективны ранние режимы терапии на основе трастузумаба. Более того, в регистрационном исследовании отмечалось преимущество в плане ОВ в группе пертузумаба даже у пациенток, ранее получавших предшествующую терапию трастузумабом (ОР 0,68) [14].
В нашей популяции пациенток имелась подгруппа больных с ранним рецидивом (во время или до истечения 12 мес с момента завершения адъювантной терапии трастузумабом, n=14; 5,3%), тогда как в исследовании Cleopatra имел место 12-месячный интервал между окончанием применения трастузумаба и включением пациенток в исследование. Несмотря на указанные различия, даже в этой подгруппе пациенток лечение не продемонстрировало меньшей эффективности. К сожалению, мы не располагаем данными о последующих линиях терапии, которые могли повлиять на результаты в отношении ОВ.
Другим ключевым моментом является длительность химиотерапии на основе таксанов, ассоциированная с применением пертузумаба/трастузумаба. В нашем исследовании медиана длительности терапии доцетакселом была меньше, чем в исследовании Cleopatra (6 циклов в сравнении с 8 циклами соответственно), при этом были получены аналогичные результаты в плане эффективности. В регистрационном исследовании рекомендовалось проведение как минимум 6 циклов терапии доцетакселом (13). В этой ситуации использование не является предметом для дискуссий. Однако решения в отношении количества циклов терапии доцетакселом должны приниматься индивидуально у каждой конкретной пациентки – с учетом ее ФС, бремени болезни и токсичности препарата. Более того, поддерживающая терапия пертузумабом и трастузумабом повышает эффективность лечения, не сопровождаясь при этом увеличением частоты значимых нежелательных явлений. Полученные в ходе нашего исследования данные также показывают, что при HER2+/ER+ опухолях добавление эндокринной поддерживающей терапии к пертузумабу/трастузумабу улучшает долгосрочные исходы и представляет собой оптимальный вариант для тех пациенток, которые не переносят химиотерапию.
В ходе ретроспективного исследования недавно были оценены данные 155 пациенток, получавших лечение трастузумабом/пертузумабом и таксаном в качестве лечения 1-й линии на базе 8 итальянских центров; его результаты сравнивались с таковыми в исследовании Cleopatra [17]. Пациентки, включенные в это обсервационное исследование, чаще имели гормон-рецептор-положительные опухоли и меньшее количество висцеральных метастазов; при этом большее количество больных получали адъювантную терапию трастузумабом. Медиана количества циклов терапии доцетакселом составляла 7, а медиана ВБП – 27,8 мес без каких-либо значимых различий в плане эффективности между анализируемыми подгруппами.
В ходе другого ретроспективного обсервационного исследования изучался исход у пациенток с HER2-положительным распространенным РГЖ, получавших лечение в условиях реальной клинической практики с использованием пертузумаба в качестве терапии 1-й линии [18]. В рамках этого исследования 249 пациенток получали трастузумаб, пертузумаб и таксан в качестве режима 1-й линии по поводу распространенного РГЖ. Из них 61% ранее получали неоадъювантную/адъювантную терапию трастузумабом, 60% этих пациенток имели гормон-рецептор-положительные опухоли. Медиана количества циклов терапии пертузумабом составляла 11 (диапазон – 1-41), медиана ее длительности – 7,3 мес (диапазон – 0,7-29). 226 пациенток получали доцетаксел, 21 – паклитаксел, 2 – наб-паклитаксел. Медиана количества циклов терапии доцетакселом составляла 6 (диапазон – 1-27). В последующем около 25% пациенток с гормон-рецептор-положительными опухолями получали эндокринную терапию. Медиана ВБП составляла 16,9 мес, а оцененная частота ВБП в течение 1 года – 62%.
В недавнем метаанализе оценивалась эффективность и безопасность лечения на основе пертузумаба у пациенток с распространенным HER2-положительным РГЖ. В него было включено 5 рандомизированных клинических исследований, участие в которых приняли 3742 пациентки. В целом режим терапии пертузумабом/трастузумабом/доцетакселом был ассоциирован со значимым снижением частоты смертельных исходов (ОР 0,67; 95% ДИ 0,57-0,78), а также с увеличением ОВ (ОР 0,66; 95% ДИ 0,35-0,67) и ВБП (ОР 0,64; 95% ДИ 0,58-0,71) без достоверного усиления кардиотоксичности [26].
Наше исследование предоставляет доказательства в поддержку применения трастузумаба, пертузумаба и таксана в качестве режима терапии 1-й линии у пациенток с HER2-положительным распространенным РГЖ в повседневной клинической практике. К настоящему времени оно представляет собой исследование с наибольшим количеством пациенток и наличием доступных данных об эффективности комбинации двойной блокады HER2 и гормональной терапии в качестве стратегии поддерживающего лечения. Полученные результаты убедительно свидетельствуют в пользу применения всех видов лечения, имеющихся сегодня в распоряжении клиницистов и положительно влияющих на исходы заболевания в этой подгруппе пациенток.
Список литературы находится в редакции.
Статья печатается в сокращении.
A multicenter retrospective observational study of first-line treatment with pertuzumab, trastuzumab and taxanes for advanced HER2 positive breast cancer patients.
RePer Study, Cancer Biology & Therapy, DOI: 10.1080/15384047.2018.1523095
Перевела с англ. Елена Терещенко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (56), грудень 2018 р


