5 лютого, 2019
Кардіоваскулярна профілактика в практиці сімейного лікаря
 Профілактика серцево-судинних захворювань (ССЗ) – одна з ключових складових сучасної медицини і, зокрема, сімейної медицини, оскільки ССЗ займають провідне місце в структурі захворюваності та смертності населення світу. В Україні частка серцево-судинної (СС) смертності становить близько 68,0% у структурі загальної летальності, при цьому 32% – серед осіб працездатного віку.
Профілактика серцево-судинних захворювань (ССЗ) – одна з ключових складових сучасної медицини і, зокрема, сімейної медицини, оскільки ССЗ займають провідне місце в структурі захворюваності та смертності населення світу. В Україні частка серцево-судинної (СС) смертності становить близько 68,0% у структурі загальної летальності, при цьому 32% – серед осіб працездатного віку.
Нині ССЗ зумовлюють значну інвалідизацію населення та залишаються провідною причиною втрати працездатності.
Стратегії кардіоваскулярної профілактики
За пропозицією Джеффрі Роуза, декілька десятиліть тому було визначено два підходи щодо профілактики ССЗ:
- популяційна стратегія, спрямована на зниження поширеності ССЗ на популяційному рівні через зміну способу життя і покращення екології (наприклад, заборона куріння в громадських місцях, зниження техногенного забруднення довкілля, зменшення споживання солі тощо);
- стратегія високого ризику – профілактичні заходи, спрямовані на зниження рівня факторів ризику (ФР) СС‑подій (артеріальної гіпертензії (АГ), гіперліпідемії, куріння, цукрового діабету (ЦД), ожиріння, гіподинамії та ін.) в групі дуже високого ризику, до якої належать особи без ССЗ або зі встановленими ССЗ.
При роботі сімейного лікаря з окремими індивідами доцільно розрізняти три стратегії:
- первинну профілактику для осіб низького ризику (з метою запобігання виникнення ФР ССЗ);
- первинну профілактику для осіб високого ризику (з метою впливу на ФР та запобігання виникнення ССЗ);
- вторинну профілактику для осіб із ССЗ і їх еквівалентами (з метою попередження ускладнень ССЗ).
Вважається, що максимальний профілактичний ефект досягається у випадку одночасного використання популяційної й індивідуальної стратегій.
Сучасна кардіоваскулярна профілактика – це сукупність дій на суспільному й індивідуальному рівні, спрямована на усунення або мінімізацію кількості ССЗ і їх ускладнень. Вона включає чотири послідовні етапи:
- І етап – оцінка індивідуального сукупного СС‑ризику;
- ІІ етап – визначення ключових індивідуальних цілей СС‑профілактики;
- ІІІ етап – вибір методів немедикаментозних і фармакологічних втручань та складання плану заходів зі зниження СС‑ризику для конкретного пацієнта;
- IV етап – моніторинг результатів і, в разі необхідності, корекція заходів профілактичних втручань.
І етап: оцінка індивідуального сукупного СС‑ризику
Першочерговим завданням лікаря первинної ланки охорони здоров’я є своєчасне виявлення людей з високим кардіоваскулярним ризиком для розробки та здійснення індивідуальних профілактичних втручань. Поняття «кардіоваскулярний ризик» означає ймовірність розвитку в людини фатальних і нефатальних СС‑подій, патогенетичним підґрунттям яких є атеросклероз, за певний період часу. Згідно з позицією ESC це ризик фатальної СС‑події впродовж 10 років.
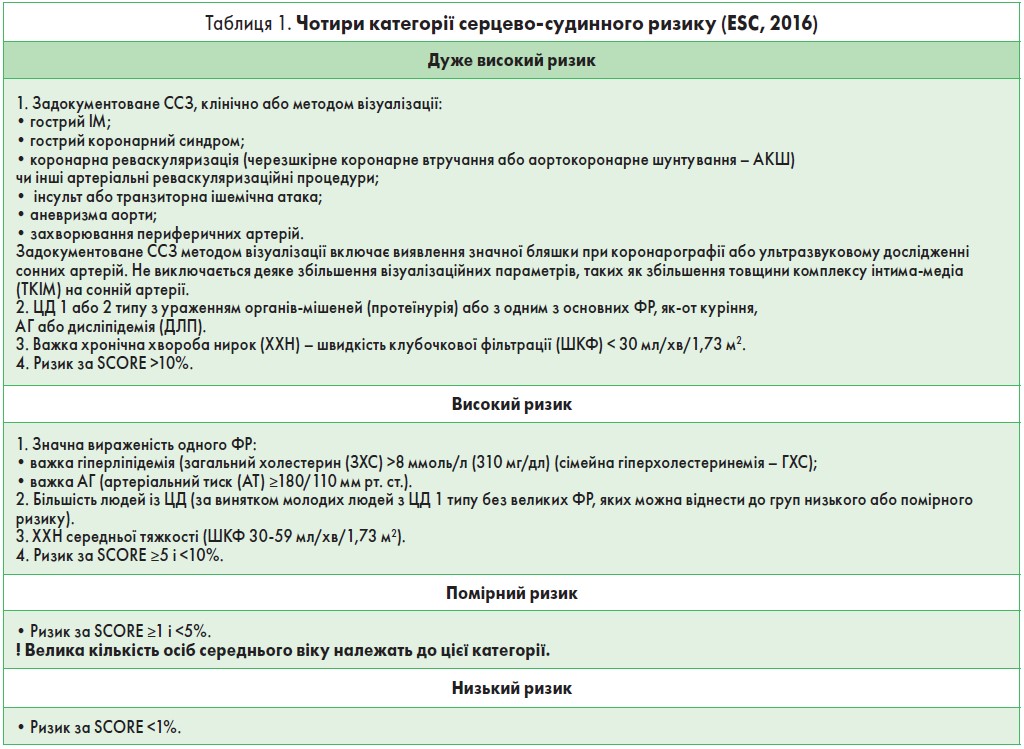
Виокремлюють чотири рівні (категорії) ризику ССЗ (ESC, 2016): дуже високий, високий, помірний, низький. Дуже високий і високий ризик передусім мають пацієнти з верифікованим симптомним чи асимптомним ССЗ на ґрунті атеросклерозу. Оцінку ризику для осіб з відсутністю явної/прихованої СС‑патології, але з множинними ФР пропонується виконувати за допомогою системи SCORE (Systematic COronary Risk Estimation). Вона дозволяє оцінити ризик фатальної атеросклеротичної події (інфаркт міокарда (ІМ), інсульт, розрив або розшарування аневризми аорти тощо), тобто смерті від ССЗ, у проміжку часу в найближчі 10 років (табл. 1).
Практичні рекомендації щодо використання шкали SCORE для оцінки СС‑ризику
- Карта SCORE (або її онлайн-версія HeartScore) використовується тільки в рамках первинної профілактики для осіб віком ≥40 років. Рекомендується проводити скринінг ФР, в тому числі визначення ліпідного профілю в дорослих чоловіків, починаючи із 40 років, і в жінок з 50 років або в постменопаузальному періоді.
- Карта SCORE не повинна застосовуватися щодо осіб з верифікованими ССЗ атеросклеротичної природи, оскільки останні автоматично належать до категорії осіб високого або дуже високого ризику.
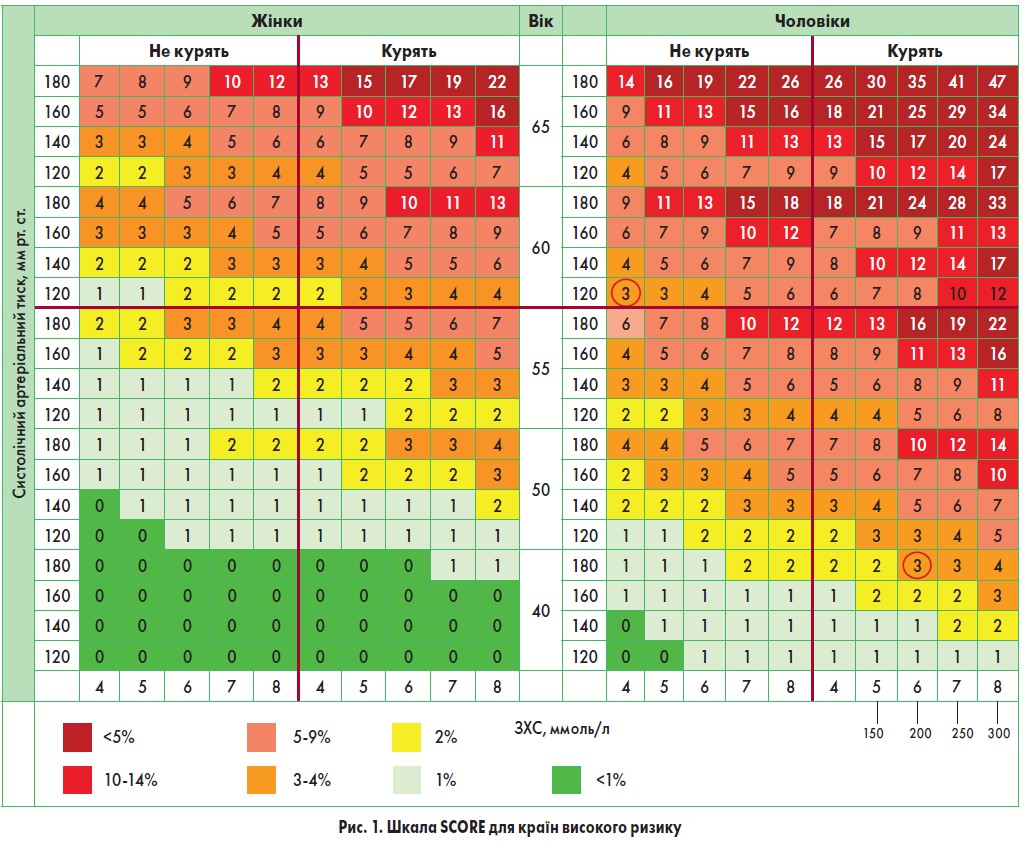
- Залежно від епідеміологічної ситуації в окремих європейських країнах розроблено дві шкали SCORE: для країн з низьким і високим СС‑ризиком. Україна належить до країн з дуже високим ризиком. Такий же ризик мають Вірменія, Азербайджан, Білорусь, Болгарія, Грузія, Казахстан, Киргизстан, Латвія, Литва, Македонія, Молдова, Росія та Узбекистан (рис. 1).
- Сукупний СС‑ризик розраховують за шкалою SCORE так. За необхідними 5 параметрами (стать, вік, статус куріння (так/ні), АТ, ЗХС – ммоль/л) необхідно знайти клітинку, найближчу до віку пацієнта, рівня холестерину і систолічного АТ.
- Критерієм високого ризику вважається ймовірність смерті від ССЗ ≥5%, дуже високого ризику – ≥10%.
Утім, використання зазначеного критерію для оцінки СС‑ризику експерти вважають недостатнім, оскільки слід враховувати ризик усіх СС‑подій (і фатальних, і нефатальних). Підраховано, що при 5% ризику смерті ризик усіх (фатальних і нефатальних) СС‑подій приблизно вдвічі більший і складає близько 10% (тобто ризик розвитку ІМ, інсульту або смерті оцінюється в 10%), при цьому він найбільший у чоловіків молодого віку (близько 15%) і трохи нижчий у жінок і літніх людей.
- Слід пам’ятати, що СС‑ризик, визначений за шкалою SCORE (для відповідних за віком осіб, особливо в Україні) переважно недооцінений. У країнах дуже високого ризику (Україна) СС‑ризик є вищим, ніж за шкалою SCORE, оскільки остання не враховує інші потужні незалежні ФР ССЗ (ЦД, малорухливий спосіб життя, ожиріння, спадкову схильність тощо).
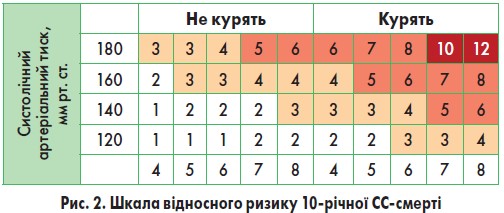
- Для молодих людей з високим рівнем ФР низький абсолютний ризик може приховувати дуже високий відносний ризик. Щоб мотивувати молодих людей змінити нездоровий спосіб життя, оцінюють відносний ризик, який на тлі перегляду щоденних звичок може знизитися (рис. 2).
Нові маркери оцінки СС‑ризику в осіб без симптомів ССЗ
 Сьогодні активно впроваджуються нові способи ідентифікації пацієнтів з високим СС‑ризиком серед безсимптомних осіб із можливими субклінічними ознаками атеросклерозу, у яких на шкалою SCORE ризик також недооцінений: ультразвукове дослідження (УЗД) сонних артерій для визначення ТКІМ, розрахунок кісточково-плечового індексу (КПІ) тощо. Маркери асимптомного атеросклерозу – це додаткові критерії високого СС‑ризику, які рекомендовано визначати в пацієнтів з нетиповим або помірним профілем ризику ССЗ (за SCORE). Більш детальний перелік маркерів субклінічного атеросклерозу представлений в оновлених європейських клінічних настановах з лікування АГ (ESH/ESC, 2018). У переліку ознак ураження органів-мішеней при АГ переважну більшість становлять маркери ураження артерій (або субклінічного атеросклерозу): пульсовий тиск, ТКІМ або атеросклеротична бляшка, КПІ, артеріальна жорсткість (швидкість поширення пульсової хвилі), мікроальбумінурія (МАУ) (табл. 2).
Сьогодні активно впроваджуються нові способи ідентифікації пацієнтів з високим СС‑ризиком серед безсимптомних осіб із можливими субклінічними ознаками атеросклерозу, у яких на шкалою SCORE ризик також недооцінений: ультразвукове дослідження (УЗД) сонних артерій для визначення ТКІМ, розрахунок кісточково-плечового індексу (КПІ) тощо. Маркери асимптомного атеросклерозу – це додаткові критерії високого СС‑ризику, які рекомендовано визначати в пацієнтів з нетиповим або помірним профілем ризику ССЗ (за SCORE). Більш детальний перелік маркерів субклінічного атеросклерозу представлений в оновлених європейських клінічних настановах з лікування АГ (ESH/ESC, 2018). У переліку ознак ураження органів-мішеней при АГ переважну більшість становлять маркери ураження артерій (або субклінічного атеросклерозу): пульсовий тиск, ТКІМ або атеросклеротична бляшка, КПІ, артеріальна жорсткість (швидкість поширення пульсової хвилі), мікроальбумінурія (МАУ) (табл. 2).
Активне виявлення субклінічного ураження артерій – це сучасна стратегія ранньої верифікації високого СС‑ризику в безсимптомних осіб як з ГХС, так і з АГ. Комплексну оцінку стану артерій у пацієнтів з АГ бажано проводити на рівні роботи лікаря загальної практики і обов’язково – на рівні лікаря-консультанта (спеціаліста). Найдоступнішими щодо рутинного використання в звичайній лікарській практиці є:
- визначення МАУ як маркера стану ендотелію та проведення офтальмоскопії з візуалізацією судин очного дна, що надають інформацію про ураження дрібних артерій при АГ і стан мікроциркуляції;
- УЗД судин шиї з метою виявлення атеросклеротичних бляшок та обчислення ТКІМ (>0,9 мм або візуалізація хоча б однієї атеросклеротичної бляшки), що свідчать про вираженість субклінічного атеросклерозу в артеріях середнього калібру (каротидних, коронарних, церебральних);
- визначення КПІ АТ (<0,9), що дозволяє встановити вираженість субклінічного або клінічно маніфестованого периферичного атеросклерозу – маркера системного атеросклеротичного ураження.
! Верифікація хоча б одного з вищезазначених маркерів субклінічного ураження артерій свідчить про високий СС‑ризик в обстежуваного навіть за відсутності в нього симптомів ССЗ і в разі низького чи помірного ризику за SCORE.
Прогностичне значення маркерів субклінічного атеросклерозу
- Поява МАУ при АГ будь-якого ступеня тяжкості вказує на більш ніж 2-кратне збільшення ризику розвитку ішемічної хвороби серця (ІХС) та її ускладнень.
- МАУ або підвищення співвідношення креатинін/альбумін сечі понад 20 мг/г при АГ є незалежним предиктором виникнення тяжких судинних подій: відносний ризик СС‑смерті в гіпертензивних осіб упродовж року зростає більш ніж у 4,5 раза, виникнення ІХС – у 3,3 раза.
- Збільшення ТКІМ загальної сонної артерії на кожні 0,10 мм також супроводжується зростанням ризику ІМ на 15%, інсульту – на 18%.
- Зниження КПІ <0,9 супроводжується збільшенням ризику розвитку ІХС у 2-3 рази, порушень мозкового кровообігу – у 4-5 разів, смерті – більш ніж удвічі (дослідження ARIC).
! Згідно з оновленими європейськими рекомендаціями з профілактики ССЗ вимірювання КПІ, а також ТКІМ та/або скринінг атеросклеротичних бляшок у сонних артеріях слід проводити в усіх асимптомних дорослих помірного кардіоваскулярного ризику (рекомендація ІІа, В), насамперед з АГ, з метою ранньої верифікації високого ризику.
Безсимптомним пацієнтам з помірним рівнем ризику рекомендується проводити комп’ютерну томографію для визначення рівня коронарного кальцію (індекс Агатстона), що є незалежним маркером розвитку ІХС та прогнозу захворювання. Дослідження The Rotterdam calcification study показало, що верхній діапазон значень індексу свідчить про 12-кратне підвищення ризику розвитку ІМ незалежно від класичних ФР навіть у людей старечого віку.
Пацієнти, які потребують оцінки сукупного СС‑ризику за шкалою SCORE:
- чоловіки віком ≥40 років і жінки віком ≥50 років (або після настання менопаузи) незалежно від наявності/відсутності симптомів і ФР;
- особи з ≥1 ФР (АГ, ДЛП, куріння тощо);
- особи, які висловили бажання оцінити свій СС‑ризик;
- особи зі спадковою схильністю щодо раннього розвитку ССЗ або спадковою гіперліпідемією;
- особи з підозрою на ССЗ;
- особи з нічним апное й еректильною дисфункцією;
- представники соціально незахищених верств населення незалежно від інших ФР (вважається, що вони перебувають в групі підвищеного СС‑ризику).
На індивідуальному рівні стратифікація СС‑ризику в осіб без симптомів ССЗ дозволяє сімейному лікарю і пацієнту:
- встановити індивідуальний СС‑ризик, ґрунтуючись на концепції «ризик – вік» (наприклад, 40-літній чоловік-курець з ФР може мати такий же СС‑ризик, як 60-літній чоловік без ФР);
- сформувати мотивацію пацієнта і його відповідальність щодо збереження власного здоров’я;
- визначити індивідуальний план зниження СС‑ризику, чіткі цілі і терміни профілактичних втручань.
ІІ етап: ключові цілі профілактики ССЗ
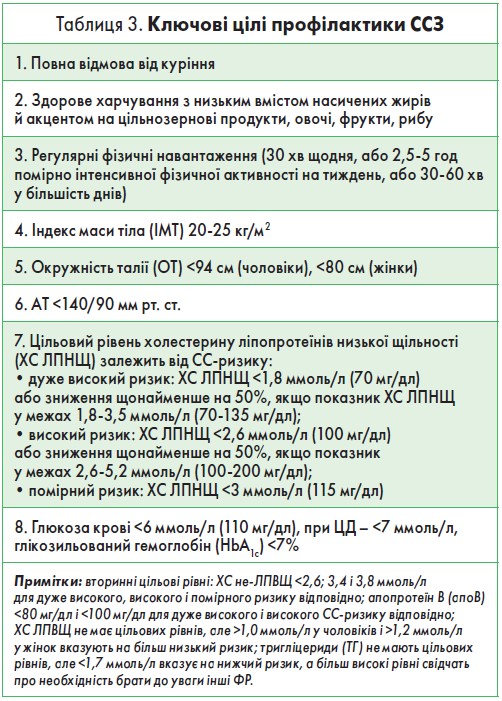 Наступним кроком після встановлення ступеня СС‑ризику є визначення індивідуальних цілей активного й ефективного профілактичного втручання. Основна вимога – персоніфікація рекомендацій щодо корекції кожного наявного у пацієнта ФР. Заходи із СС‑профілактики, насамперед, показані хворим на ССЗ та іншим категоріям осіб високого / дуже високого ризику розвитку кардіоваскулярної патології. У таблиці 3 представлені узагальнені ключові цілі СС‑профілактики.
Наступним кроком після встановлення ступеня СС‑ризику є визначення індивідуальних цілей активного й ефективного профілактичного втручання. Основна вимога – персоніфікація рекомендацій щодо корекції кожного наявного у пацієнта ФР. Заходи із СС‑профілактики, насамперед, показані хворим на ССЗ та іншим категоріям осіб високого / дуже високого ризику розвитку кардіоваскулярної патології. У таблиці 3 представлені узагальнені ключові цілі СС‑профілактики.
Сімейний лікар разом з пацієнтом на основі результатів індивідуальної стратифікації СС‑ризику та визначених цілей профілактики складають відповідний план зниження СС‑ризику. Європейськими рекомендаціями з профілактики ССЗ (ESC, 2016) наголошується на необхідності ефективної взаємодії лікаря і пацієнта на шляху до оптимізації процесу оздоровлення способу життя. Для цього пропонують 10 стратегічних кроків:
1) створити лікувальний союз на основі взаємної симпатії між лікарем і пацієнтом;
2) консультувати всіх пацієнтів і членів їхніх сімей з ФР або ССЗ;
3) допомогти пацієнту усвідомити тісний взаємозв’язок між способом життя і станом здоров’я;
4) з’ясувати існування бар’єрів чи моделей
поведінки, здатних вплинути на зміну способу життя;
5) досягти самостійного вибору пацієнтом розуміння необхідності модифікації способу життя;
6) залучити пацієнта до активного самовиявлення ФР ССЗ;
7) використовувати комбінацію різних впливів на стимулювання зміни способу життя;
8) скласти індивідуальний план для досягнення цілей зміни способу життя:
9) за необхідності залучати інших спеціалістів та медичний персонал (психотерапевта, дієтолога, медсестер тощо);
10) моніторувати процес зміни способу життя на постійній основі.
ІІІ етап: вибір методів немедикаментозних і фармакологічних втручань
Третій крок – складання комплексу немедикаментозних і медикаментозних втручань згідно з індивідуальним набором ФР, встановленою категорією ризику і визначеними цілями. Найважливішою складовою первинної і вторинної профілактики атеросклерозу та його ускладнень є модифікація способу життя, яка включає відмову від куріння, боротьбу з надлишковою масою тіла (особливо при центральному ожирінні), достатню фізичну активність, раціональне харчування. Однак особлива увага надається фармакологічному контролю АГ та ГХС. Модифікація цих ФР переконливо продемонструвала зниження захворюваності і смертності в осіб як з недіагностованими, так і з діагностованими ССЗ. Зокрема, ефективне зниження рівня систолічного АТ в популяції на 10% у поєднанні зі зниженням ЗХС на 10% сприяє зменшенню кардіоваскулярної захворюваності та смертності майже наполовину.
IV етап: моніторинг результатів реалізації заходів профілактики
Моніторинг і, за потреби, корекція заходів профілактичних втручань є найдовшим етапом ведення пацієнта високого кардіоваскулярного ризику, що включає оцінку динаміки ефективності лікування (досягнення поставлених цілей), контроль можливих побічних ефектів фармакотерапії, корекцію доз лікарських засобів, навчання пацієнта з метою підвищення його прихильності до тривалої терапії тощо.
Сучасні рекомендації щодо модифікації способу життя і фармакотерапії з метою зниження СС‑ризику
Рекомендації щодо куріння
Будь-який вид куріння (активне чи пасивне) є сильним і незалежним ФР ССЗ, тому всі курці мають отримати рекомендації щодо припинення куріння. За необхідності їм слід запропонувати допомогу, в тому числі фармакологічну (нікотинзамісна терапія (НЗТ), варениклін або бупропіон). НЗТ, варениклін та бупропіон зазвичай призначаються в рамках програми лікування абстинентного синдрому. НЗТ у формі жувальної гумки, трансдермальних нікотинових пластирів, назального спрею, інгаляторів і сублінгвальних таблеток широко застосовується для допомоги в найважчі перші тижні відмови. Описано успішний досвід при відсутності побічних ефектів застосування нікотинового пластиру в пацієнтів з ІХС. Антидепресант нортриптилін та антигіпертензивний засіб клонідин також допомагають кинути курити, але через наявність побічних ефектів є препаратами другої лінії.
Слід уникати пасивного куріння, оскільки воно також збільшує ризик ССЗ. Необхідно формувати в дітей, підлітків і молоді розуміння шкоди куріння. Особливу увагу слід приділяти особам, які нещодавно кинули курити, з метою запобігання збільшення маси тіла.
Рекомендації щодо харчування
Відомо, що характер харчування пов’язаний з ризиком виникнення ССЗ як за рахунок впливу на рівень ЗХС, АТ, масу тіла та розвиток ЦД, так і через інші механізми. У таблиці 4 представлені основні складові здорового харчування і принципи дієтотерапії в рамках СС‑профілактики відповідно до європейських рекомендацій.
У пацієнтів із підвищеним рівнем ЗХС і його проатерогенних фракцій, а також в осіб з ризиком їх підвищення оптимізацію харчування слід доповнити такими рекомендаціями:
- не вживати більше 3 яєчних жовтків на тиждень, включно з жовтками, використовуваними для приготування їжі;
- обмежити споживання субпродуктів (печінки, нирок), ікри, креветок; усіх видів ковбас, вершкового масла, жирних сортів молочних продуктів;
- смаження їжі на тваринних жирах слід замінити відварюванням, тушкуванням, приготуванням на пару, в духовці; перед приготуванням необхідно зрізати жир зі шматків м’яса та шкіру з птиці;
- віддавати перевагу рибним стравам, овочам і фруктам;
- готувати на рослинних оліях.
Рекомендації щодо контролю маси тіла
Надмірна вага й ожиріння асоціюються з підвищеним ризиком смерті при ССЗ. З іншого боку, існує J‑подібна залежність між значенням ІМТ і смертністю від усіх причин. Загальна смертність найнижча в осіб з ІМТ 20-25 кг/м2. Надмірна вага визначається як ІМТ ≥25-30 кг/м2, ожиріння – як ІМТ ≥30 кг/м2. Абдомінальне ожиріння можна легко виявити шляхом вимірювання ОТ; це слід виконувати в усіх осіб з надлишковою вагою, наявністю ДЛП або підвищеним ризиком виникнення кардіоваскулярних подій. Рекомендується контролювати два показники маси тіла:
- при ІМТ >25 кг/м2 (особливо >30 кг/м2) показано знижувати вагу, оскільки це асоціюється з позитивними ефектами щодо контролю АТ і ДЛП і зменшує ризик ССЗ;
- при ОТ 80-88 см у жінок і 94-102 см у чоловіків подальше збільшення маси тіла заборонене. Рекомендовано знижувати масу тіла при ОТ >88 см у жінок і >102 см у чоловіків.
! Зниження маси тіла можна досягти за рахунок зменшення споживання висококалорійних продуктів, що зумовлює дефіцит калорій (до 300-500 ккал/день).
Рекомендації щодо фізичної активності
Будь-яка фізична активність асоціюється зі зниженням ризику ССЗ.
- Здорові дорослі повинні займатися 2,5-5 год на тиждень аеробною фізичною активністю середньої інтенсивності, або 30-60 хв у більшість днів, або 1-2,5 год на тиждень.
- Осіб, які ведуть малорухливий спосіб життя, необхідно заохочувати розпочинати тренувальні програми легкої інтенсивності.
- Аеробна фізична активність має проводитися декількома сеансами тривалістю ≥10 хв упродовж тижня (4-5 днів/тиж).
- Пацієнти, які перенесли ІМ, АКШ, стентування, хворі на стабільну стенокардією або серцеву недостатність, після консультації з лікарем повинні виконувати аеробні динамічні (нестатичні) фізичні навантаження помірної або значної інтенсивності з тривалістю сеансу 30 хв щонайменше тричі на тиждень. Пацієнтам, які ведуть малорухливий спосіб життя, тренувальну програму рекомендовано розпочати з легких фізичних вправ після оцінки можливих ризиків.
Рекомендації з корекції психосоціальних факторів
Рекомендована мультимодальна поведінкова стратегія, що включає освітні програми, фізичне тренування, психологічну терапію для усунення впливу психосоціальних факторів ризику. За наявності клінічно значущої депресії, тривоги, ворожості можна розглянути психо- та/або відповідну фармакотерапію для корекції афективних симптомів і поліпшення якості життя. Такий підхід може покращити настрій та підвищити якість життя.
Фармакотерапія як обов’язковий компонент первинної і вторинної серцево-судинної профілактики
Немедикаментозна профілактика ССЗ є базовим етапом будь-яких профілактичних заходів. З метою зниження ризику розвитку ССЗ та їх ускладнень у хворих високого СС‑ризику з АГ, ДЛП, ЦД, ожирінням, іншими ФР та їх поєднанням необхідним компонентом первинної профілактики є фармакотерапія: гіпотензивна (переважно на основі інгібіторів ренін-ангіотензин-альдостеронової системи – РААС), гіполіпідемічна (насамперед, статини, рідше – інші лікарські засоби), гіпоглікемічна (при ЦД).
Вторинна СС‑профілактика передбачає використання фармакотерапії, спрямованої на покращення прогнозу пацієнтів: зниження ризику СС‑ускладнень і смерті та збільшення тривалості життя. У рамках цього підходу застосовуються три групи медикаментів, яким притаманна здатність знижувати ризик розвитку СС‑ускладнень у хворих з діагностованими ССЗ атеросклеротичного ґенезу приблизно на 20-25%: інгібітори РААС (ІАПФ або антагоністи рецепторів ангіотензину); статини; антитромбоцитарні препарати (переважно ацетилсаліцилова кислота).
Медична газета «Здоров’я України 21 сторіччя» № 1 (446), січень 2019 р.