27 лютого, 2019
Вітамін D та патофізіологія запальних захворювань шкіри
Шкіра людини – місце, де синтезується вітамін D і діє біологічно активна форма цього вітаміну. У шкірі вітамін D бере участь у низці процесів: від проліферації, диференціації й апоптозу кератиноцитів до підтримки бар’єрної функції та імунорегуляції [1], – у зв’язку з чим використовується в лікуванні багатьох хвороб шкіри [2].
У цьому огляді представлено некласичні функції вітаміну D у шкірі та описано його роль при запальних дерматологічних захворюваннях на прикладі атопічного дерматиту (АД) та псоріазу.
Головні структурні та функціональні молекули шкіри
Шкіра є першою лінією захисту від інфекційних агентів. Вона складається з 3 шарів: епідермісу, дерми і гіподерми, а також може мати різноманітні придатки на кшталт волосяних фолікулів, потових, сальних та апокринних залоз. Епідерміс, своєю чергою, складається з кератиноцитів (95%), меланоцитів, клітин Лангерганса (спеціалізований підряд мієлоїдних дендритних клітин – ДК) і клітин Меркеля. Розрізняють 4 шари епідермісу, кожен з яких містить кератиноцити на різних стадіях диференціації [1]: базальний шар, де присутні проліферуючі кератиноцити; остистий шар, у якому розпочинається диференціація цих клітин; зернистий шар, що характеризується багатими на кератогіалінові гранули кератиноцитами, які містять маркери пізньої диференціації (профілагрин, лорикрин), а також на наповнені ліпідами ламелярні тільця; роговий шар (РШ), утворений остаточно диференційованими мертвими клітинами (корнеоцитами). Плазматична мембрана корнеоцитів заміщена нерозчинним білковим шаром, що має назву «зроговілий конверт» (ЗК) та складається з інволюкрину, лорикрину, філагрину та малих білків, багатих на пролін і сполучених за допомогою трансглутамінази.
Вітамін D: синтез і функції
Вітамін D є жиророзчинним, він зустрічається у двох основних формах: ергокальциферол (вітамін D2), що виробляється рослинами, та холекальциферол (вітамін D3), який ми отримуємо з продуктів тваринного походження. Провідним джерелом вітаміну D у людей є синтез у шкірі під дією сонячного світла. Дія ультрафіолетового (УФ) випромінювання з довжиною хвилі 290-315 нм на 7-дегідроксихолестерин (7-ДГХ) має наслідком утворення превітаміну D, який підлягає термічній ізомеризації до більш стабільного вітаміну D – холекальциферолу. Останній надалі проходить 2 реакції гідроксильного окиснення. У ході першої з них, яка відбувається у печінці, під дією 25-гідроксилази вітаміну D формується молекула 25-гідроксивітаміну (25(OH)D – кальцидіол), а в ході другої (у нирках) вплив 1α-гідроксилази забезпечує утворення активного метаболіту вітаміну – 1,25-дигідроксивітаміну D (1,25(OH)2D – кальцитріолу) [5]. Рівень вітаміну D у сироватці регулюється станом метаболізму кальцію та фосфору, а також впливами паратиреоїдного гормону та фактора росту фібробластів [6, 7]. Насиченість організму вітаміном D оцінюється за допомогою визначення сироваткового рівня 25(OH)D – головної циркулюючої форми. Відповідно до рекомендацій Американського ендокринологічного товариства, дефіцит вітаміну D має місце в разі сироваткової концентрації 25(OH)D <20 нг/мл (50 нмоль/л), а недостатність – 21-29 нг/мл (52,5-72,5 нмоль/л) [8].
Упродовж тривалого часу функцією вітаміну D вважалася підтримка нормальної архітектури скелета шляхом контролю гомеостазу кальцію та фосфору, проте в останні кілька десятиліть було виявлено позаскелетні ефекти цього вітаміну, в тому числі його роль у регуляції проліферації клітин, їх диференціації, апоптозу, а також в імунних процесах [9, 10]. Зазначена активність опосередкована власним рецептором вітаміну D (РВД), який після активації взаємодіє з ретиноїдним рецептором X, формуючи гетеродимерний комплекс. Останній бере участь у регуляції експресії генів-мішеней, яку називають геномною дією вітаміну D.
Роль вітаміну D у фізіології шкіри
У шкірі вітамін D відіграє життєво важливу роль: кератиноцити є не лише джерелом цього вітаміну, а й мішенню дії його активної форми [1]. Лише ці клітини здатні синтезувати вітамін з його попередника 7-ДГХ. Кератиноцитам також властива експресія РВД, отже, вони відповідають на дію активної форми вітаміну. Шлях метаболізму та функціонування вітаміну D3 у шкірі людини показаний на рисунку.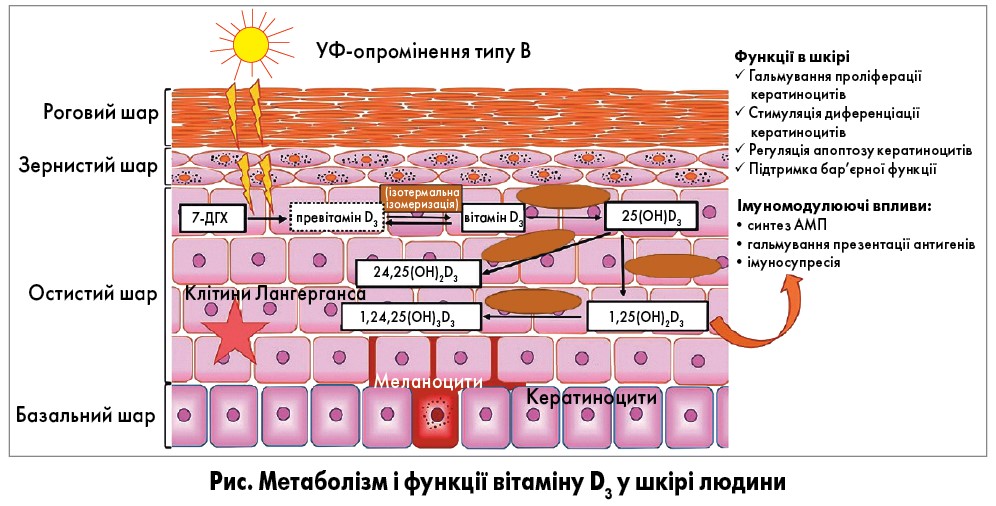
Вітамін D і диференціація та проліферація епідермісу
Вітамін D дозозалежно впливає на проліферацію та диференціацію клітин шкіри безпосередньо та у взаємодії з кальцієм, що було підтверджено багатьма дослідженнями in vitro. У низькій концентрації (≤10-9 M) 1,25(OH)2D3 посилює проліферацію кератиноцитів, натомість у високій концентрації (>10-8 M) – гальмує, стимулюючи диференціацію [11, 12]. Останній процес відбувається шляхом посилення синтезу структурних компонентів ЗК [14, 15], частково опосередкованим зростанням внутрішньоклітинного рівня кальцію, посиленим утворенням керамідів і безпосередньо стимуляцією РВД [15-18].
Вітамін D і бар’єрна функція шкіри
Іншим аспектом проліферації та диференціації кератиноцитів є підтримка епідермального бар’єра. Дослідження показали, що місцеве нанесення кальцитріолу відновлює цілісність шкірного бар’єра, порушену внаслідок нанесення кортикостероїда чи натрію лаурилсульфату [21, 22]. Вітамін D зміцнює епідермальний бар’єр шляхом посилення синтезу структурних білків ЗК, а також стимуляції утворення довголанцюгових глікозилкерамідів, необхідних для утворення ліпідного бар’єрного шару.
Вітамін D та апоптоз кератиноцитів
Вплив вітаміну D на апоптоз кератиноцитів, як і дія на проліферацію, є дозозалежним. У фізіологічних концентраціях вітамін D запобігає апоптозу, зумовленому такими проапоптотичними стимулами, як кераміди, УФ‑випромінювання, фактор некрозу пухлин (ФНП) тощо; водночас у високих концентраціях він здатен спричиняти апоптоз кератиноцитів [24]. Показано, що антиапоптотичні та цитопротекторні ефекти вітаміну D опосередковуються сфінозин‑1-фосфатом та активацією кількох сигнальних шляхів [25].
Вітамін D й імунні функції шкіри
Вроджений імунітет шкірних покривів включає структури фізичного бар’єра шкіри (РШ), імунні клітини (нейтрофіли, моноцити, макрофаги, ДК, природні кілери тощо) й антимікробні пептиди (АМП). Синтез останніх є первинним механізмом захисту від шкідливих факторів довкілля та мікробної інвазії [26, 27]. У шкірі виявляють понад 20 білків з антибактеріальними функціями, однак головними групами є β-дефензини та кателіцидини [26]. Ці білки опосередковують антимікробну активність, безпосередньо руйнуючи мембрану бактеріальної клітини й оболонку вірусу, а також запускаючи різноманітні сигнальні шляхи з метою ініціації імунної відповіді організму-господаря. Крім того, ці групи АМП стимулюють проліферацію кератиноцитів та їх міграцію, що необхідно для загоєння дефектів шкіри [28].
В інтактній шкірі рівень АМП є низьким, утім, при порушенні цілісності шкіри чи розвитку інфекції він зростає. Одночасно відбувається посилення місцевого синтезу вітаміну D. У багатьох дослідженнях було показано, що після лікування 1,25(OH)2D експресія дефензину в кератиноцитах і себоцитах зростає [30-33]. Повідомлялося, що вітамін D також регулює синтез АМП кількома непрямими шляхами, в тому числі регулюючи активність серинових протеаз, що руйнують ці білки [36].
Окрім регуляції синтезу АМП у шкірі, 1,25(OH)2D3 та кальципотріол (аналог вітаміну D) опосередковують місцеву імуносупресію шляхом гальмування презентації антигенів, впливаючи безпосередньо на клітини Лангерганса або непрямо модулюючи продукцію цитокінів кератиноцитами [37, 38]. Нещодавні дослідження показали, що кальципотріол опосередковує місцеву імуносупресію в шкірі шляхом індукції CD4+CD25+ T‑регуляторних клітин, що запобігає подальшій антигенспецифічній проліферації CD8+ T‑лімфоцитів і продукції інтерферону (ІФН) γ [39, 40].
Роль вітаміну D при певних запальних захворюваннях шкіри
Псоріаз
Псоріаз є хронічною багатофакторною патологією, в разі якої провідну роль відіграє дисрегуляція імунної системи, в тому числі інфільтрація шкіри клітинами-ефекторами вродженого імунітету (плазмацитоїдними ДК (пДК), мієлоїдними ДК (мДК), нейтрофілами, природними кілерами тощо), аномально високі рівні АМП і непереносимість власної ДНК [47]. Відомо, що пДК виробляють ІФН‑α, який запускає запальний каскад, стимулюючи дозрівання мДК й активуючи аутоімунні Т‑клітини [48]. Під час їх активації зростає рівень ФНП і підвищується активність синтази оксиду азоту, внаслідок чого розширюються судини та розвивається запалення [49]. Інший підклас мДК продукує інтерлейкін (ІЛ) 20, що посилює проліферацію кератиноцитів, та ІЛ‑23 і ІЛ‑12, які активують Т‑клітини [50]. Нейтрофіли і природні кілери, присутні у вогнищах псоріазу, беруть участь у секреції АМП та прозапальних цитокінів [51, 52].
Вогнища псоріазу також характеризуються посиленою інфільтрацією Т‑клітинами, передусім CD4+ T‑хелперами 1 типу (Th1) та CD8+ цитотоксичними T‑клітинами, які секретують цитокіни на кшталт ФНП та ІФН‑γ. Крім того, в цих ділянках наявна велика кількість ІЛ‑17-продукуючих Т‑лімфоцитів і природних кілерів.
ІЛ‑23, що виробляється мДК й іншими лейкоцитами, сприяє диференціації Т‑лімфоцитів у Т‑хелпери 17 типу та цитотоксичні Т‑лімфоцити 17 типу. Обидва ці типи Т‑клітин секретують ІЛ‑17, ІЛ‑17F та ІЛ‑22 [53]. Ці цитокіни разом з ІФН‑γ та ФНП зумовлюють активацію та проліферацію кератиноцитів. Таким чином, у відповідь на цитокіни, вивільнені ДК та Т‑лімфоцитами, кератиноцити секретують АМП, прозапальні цитокіни (ІЛ‑1, ІЛ‑6 і ФНП), різні хемокіни та білки [55]. Ці розчинні медіатори діють як хемоатрактанти для нейтрофілів й інших імунних клітин. Надмірне функціонування Т‑лімфоцитів за умов псоріазу та зниження їх супресивної функції призводять до стійкого неконтрольованого запального процесу [56-58].
Роль вітаміну D при псоріазі
Вітамін D відіграє важливу роль у патогенезі псоріазу, що було доведено в багатьох дослідженнях, які виявили дефіцит або низький рівень цієї речовини в пацієнтів із зазначеною хворобою [59-61]. Кілька досліджень типу «випадок – контроль» повідомили про зворотний зв’язок між сироватковим рівнем 25(OH)D та тяжкістю псоріазу [62-66]. Однак у популяційному дослідженні Wilson [67] було виявлено відсутність відмінностей у сироватковому рівні 25(OH)D в осіб з псоріазом і без нього. Слід зазначити, що концентрація 25(OH)D залежить від расової приналежності, харчування, контакту з УФ‑променями, тому результати досліджень із цього питання потребують ретельної інтерпретації.
Лікування вітаміном D може ефективно зменшувати вираженість симптомів псоріазу, що було підтверджено багатьма клінічними дослідженнями. Finamor і співавт. [68] показали, що в пацієнтів із псоріазом, які отримували 35000 МО вітаміну D3 1 р/добу впродовж 6 міс, спостерігалося достовірне покращення за індексом площі і тяжкості псоріазу (Psoriasis area severity index score, PASI) одночасно з вираженим зростанням сироваткового рівня 25(OH)D. Деякі дослідження продемонстрували відмінну ефективність і безпеку аналогів вітаміну D (кальципотріолу, такальцитолу, максакальцитолу) в лікуванні псоріазу [69-71].
Ефект вузькосмугової фототерапії УФ‑променями типу А та В, яка широко застосовується в лікуванні псоріазу, частково опосередкований підвищенням сироваткового рівня 25(OH)D [72-74]. Клінічне дослідження, що порівнювало дієвість і безпеку різних методів лікування псоріазу, виявило, що сполучення кальципотріолу та вузькосмугової фототерапії двічі на тиждень найшвидше знижувало оцінку за шкалою PASI [75]. Також повідомлено, що поєднання вітаміну D чи його аналогів з кортикостероїдами є ефективнішим за будь-яку монотерапію, оскільки цим речовинам властиві взаємодоповнюючі впливи: вітамін D може протидіяти стероїд-індукованій атрофії шкіри шляхом відновлення епідермального бар’єра, натомість глюкокортикоїди знижують вираженість подразнення шкіри навколо вогнища псоріазу, спричиненого аналогами вітаміну D [76-78].
Вітамін D протидіє псоріазу багатьма шляхами: зокрема, зменшує здатність пДК індукувати проліферацію Т‑лімфоцитів і секрецію ІФН‑γ [79]; знижує інфільтрацію псоріатичних вогнищ T‑лімфоцитами 17 типу [80, 81]; гальмує впливи запальних цитокінів (ІЛ‑12, ІЛ‑23, ІЛ‑1α, ІЛ‑1β, ФНП), які в надмірній кількості наявні в ураженій псоріазом шкірі [82, 83]; пригнічує дію псоріазину та коебнеризину – хемоатрактантів, які посилюють псоріатичне запалення [84].
Крім протидії запальним явищам, вітамін D відновлює функції ураженого псоріазом епідермісу, впливаючи на експресію генів ЗК LCE3B і LCE3C – спадкових факторів ризику псоріазу [86]; зміцнюючи щільні з’єднання між епідерміоцитами [87]; нормалізуючи експресію та топографію інтегринів [88].
Атопічний дерматит
АД є хронічним або рецидивуючим захворюванням шкіри, яке спричиняється складними взаємодіями між генетичними й імунологічними факторами, а також чинниками довкілля. Ця хвороба характеризується хронічним запаленням, порушенням епітеліального бар’єра, імунологічними розладами та підвищеним сироватковим IgE.
Дефекти бар’єрної функції шкіри при АД
В епідермісі пацієнтів з АД визначаються значні порушення бар’єрної функції та зростання трансепідермальних втрат води, що робить уражену АД шкіру чутливою до проникнення алергенів, бактерій, грибів і вірусів. Механізмами цих порушень є нестача або дефекти молекул структурних білків (філагрину, інволюкрину, лорикрину, кератинів K5 та K16 тощо), епідермальних протеаз та їх інгібіторів; зміни рН РШ; зниження вмісту керамідів, що підтримують цілісність ліпідного бар’єра й утримують воду [99, 100].
Імунні порушення при АД
Імунні розлади за умов АД є двофазними: у гострій стадії домінує Th2-опосередковане запалення, а при хронічному процесі – Th0 та Th1. Отже, при гострому ураженні відзначається зростання рівнів ІЛ‑4, ІЛ‑5 та ІЛ‑13 (цитокіни Th2-лімфоцитів), а за умов хронічного – ІФН‑γ та ІЛ‑12 [99]. У 80% випадків АД також присутнє підвищення сироваткового рівня IgE зі зростанням специфічних антитіл до харчових алергенів чи аероалергенів [103]. Крім дефектів набутого імунітету, в пацієнтів з АД фіксується дисфункція різноманітних компонентів вродженого імунітету (порушення шкірного бар’єра, погіршення функції природних кілерів, пДК, нейтрофілів, знижена секреція АМП) [113, 114].
Роль вітаміну D при АД
Вплив вітаміну D на частоту виникнення та тяжкість АД добре вивчений. У великих популяційних дослідженнях було показано, що дефіцит або нестача вітаміну D супроводжується підвищенням ризику розвитку АД [117, 118]. Обсерваційні дослідження виявили, що в дорослих і дітей з АД рівень вітаміну D нижчий у порівнянні з групою контролю [119-121]. Продемонстровано також, що тяжкість АД зворотно корелює з рівнем вітаміну D [120-123]. Однак є й деякі суперечливі результати [124, 125].
Багато клінічних досліджень показали, що прийом харчових добавок вітаміну D сприяє зменшенню тяжкості АД за шкалою SCORAD та індексом площі і тяжкості екземи (EASI) [121, 135-138]. Механізмами цього впливу вважаються нормалізація рівнів цитокінів (ІЛ‑2, ІЛ‑4, ІЛ‑6, ІФН‑γ), гальмування продукції IgE та протидія активації мастоцитів, відновлення епідермального бар’єра, активація синтезу АМП [138, 140, 144]. Сприятливий ефект УФ‑опромінення, що широко використовується при АД, також частково опосередкований корекцією дефіциту вітаміну D [72].
Пацієнти з АД схильні до колонізації шкіри золотистим стафілококом, що погіршує перебіг хвороби внаслідок продукції екзотоксинів. Gilaberte і співавт. [145] виявили асоціацію між низьким рівнем вітаміну D та вірулентністю Staphylococcus aureus. Це було підтверджено в клінічному дослідженні, в якому призначення вітаміну D 2000 МО/день протягом 4 тиж супроводжувалося зниженням колонізації стафілококом і зменшенням вираженості клінічних симптомів АД [146]. Лікування вітаміном D також має сприятливий ефект за умов герпетичної екземи, яка часто розвивається в пацієнтів з АД [147, 143].
Висновки
Окрім загальновідомого впливу на обмін кальцію та фосфору, роль вітаміну D у забезпеченні функції деяких тканин/органів, особливо шкіри, є сферою особливого інтересу дослідників. Це пояснюється тим, що зазначений вітамін чинить низку плейотропних ефектів у шкірі, серед яких – продиференціаційний, антиапоптотичний, імуномоделюючий. З вітаміном D також тісно пов’язані патогенетичні механізми багатьох хвороб шкіри, він здатен позитивно впливати на наслідки деяких дерматопатологій. На сьогодні доведена сприятлива дія терапевтичних втручань (топічних і системних) з використанням вітаміну D при таких захворюваннях, як псоріаз та атопічний дерматит.
Umar M., Sastry K. S., Al Ali F. et al. Vitamin D and the Pathophysiology of Inflammatory Skin Diseases. Skin Pharmacol Physiol 2018; 31: 74-86. DOI: 10.1159/000485132.
Переклала з англ. Лариса Стрільчук
ДОВІДКА «ЗУ»
Нутрицевтик Д‑кап (ТОВ «Омніфарма Київ») містить 50 мкг (2000 МО) холекальциферолу в 1 капсулі. Оскільки дефіцит вітаміну D3 зазвичай зумовлений проживанням у північних і помірних широтах з недостатнім УФ‑опроміненням; надмірним перебуванням у закритих приміщеннях і носінням закритого одягу; масовим використанням сонцезахисних кремів, що перешкоджають природній інсоляції; суттєвим зменшенням рухової активності (насамперед у мешканців міст); уживанням великої кількості рафінованих продуктів, населення України перебуває в групі ризику цього стану, особливо в осінньо-зимовий період. Вітамін D3 синтезується у клітинах шкіри організму під дією УФ-променів, тому додаткове надходження вітаміну D3 особливо актуальне навесні та в осінньо-зимовий період. Крім того, контроль рівня вітаміну D3 важливий в осіб з цукровим діабетом, метаболічним синдромом, ожирінням, остеопорозом, аутоімунними (в тому числі ревматоїдним артритом) та дерматологічними захворюваннями (в тому числі АД). Уживання Д‑кап по 1 капсулі 2 р/добу слугує додатковим джерелом вітаміну D3 з метою підтримки його оптимального рівня в організмі.
Медична газета «Здоров’я України 21 сторіччя» № 2 (447), січень 2019 р.


