25 березня, 2019
Периоперационное применение кеторолака при редукционной маммопластике: существует ли риск формирования гематомы?
В случае обострения опиоидного кризиса хирурги все чаще сосредотачивают усилия на минимизации использования наркотических аналгетиков. Кеторолак обладает доказанной эффективностью в купировании постоперационного болевого синдрома, однако его использование ограничено из-за опасений возникновения послеоперационного кровотечения и образования гематомы.
Во всем мире вызывают тревогу статистические данные, касающиеся злоупотребления наркотическими препаратами. В настоящее время свыше 2 млн американцев испытывают зависимость от опиоидов, предписанных по лечебным показаниям, а число случаев смерти вследствие передозировки этих препаратов с 2000 года увеличилось почти в четыре раза. Поскольку хирургические методы лечения напрямую связаны с применением опиоидов, очевидна важная роль хирургов и анестезиологов в разрешении данной проблемы. Кроме того, известно, что молодой возраст является фактором риска злоупотребления наркотиками, что определяет значимость снижения частоты периоперационной опиоидной аналгезии при лечении подростков и молодых лиц.
Кеторолака трометамин является нестероидным противовоспалительным препаратом (НПВП) с выраженным обезболивающим и противовоспалительным эффектом. На фармацевтическом рынке доступны лекарственные формы кеторолака как для перорального, так и для парентерального применения. Этот препарат часто используется в сочетании с опиоидами для купирования болевого синдрома в послеоперационном периоде, при этом документально подтверждена возможность снижения дозы последних у взрослых, детей и подростков. Известно также, что кеторолак ингибирует агрегацию тромбоцитов, поэтому при его использовании возникают опасения относительно развития послеоперационного кровотечения и формирования гематомы.
С учетом вышеизложенного учеными Harvard Medical School было проведено исследование, в котором изучалась связь между назначением кеторолака и образованием гематомы у девочек-подростков и молодых женщин, подвергшихся редукционной маммопластике. Кроме того, одной из целей исследования была оценка влияния периоперационного применения кеторолака на потребность в опиоидной аналгезии.
Пациенты и методы
В ходе исследования были проанализированы данные медицинских карт пациенток (n=500), перенесших билатеральную редукционную маммопластику. Во всех случаях операции были выполнены одним хирургом по методу Wise (формирование нижней питающей «ножки»).
Перед операцией пациентки должны были воздерживаться от курения в течение по меньшей мере 3 месяцев и прекратить прием НПВП и других антиагрегантных препаратов в течение как минимум 14 дней. В послеоперационном периоде наблюдения контрольные посещения назначались через 1 неделю, 1 месяц, 6 месяцев и 1 год.
В каждом случае, при условии отсутствия противопоказаний, хирург информировал о разрешении использовать кеторолак анестезиолога и ассистента, и препарат назначался на их усмотрение. Хирург не был осведомлен о предписанной аналгезии. Интраоперационно кеторолак, как правило, вводили в течение 20 минут после ушивания раны для достижения максимальной послеоперационной аналгезии. Редукционная маммопластика проводилась без применения тумесцентного раствора, однако местная анестезия эпинефринсодержащими препаратами осуществлялась в начале и в конце операции.
Анализ проводился с учетом демографических и антропометрических характеристик пациенток, данных о наличии сопутствующих заболеваний, в том числе геморрагических диатезов, почечной недостаточности и аллергии на кеторолак или другие НПВП. Пациентки были распределены по категориям в зависимости от величины индекса массы тела (ИМТ), который рассчитывали отдельно для пациенток в возрасте до 20 лет и старше 20 лет с использованием соответственно калькулятора ИМТ ребенка/подростка и калькулятора ИМТ взрослого Центров по контролю и профилактике заболеваний США.
Информация относительно оперативного вмешательства включала сведения о введении лекарственных средств (особенно дозы опиоидных и неопиоидных аналгетиков), о массе резецированной ткани молочной железы и о развитии послеоперационной гематомы. Гематома определялась как клинически идентифицируемый отек мягких тканей, вторичный по отношению к локализованному накоплению крови, что требовало проведения вмешательства (дренаж под местной анестезией или хирургическая эвакуация).
Результаты
Характеристики пациентов
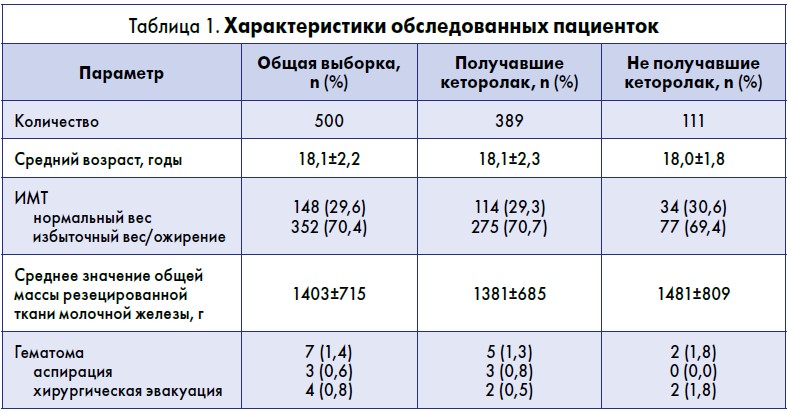
В исследование было включено 500 женщин. Средний возраст на момент операции составил 18,1±2,2 года, в среднем общая масса резецированной ткани молочной железы составила 1403±715 г. Большинство участниц исследования (70,4%) имели избыточный вес или ожирение. Одна пациентка в общей выборке страдала болезнью Виллебранда; каких-либо других заболеваний из группы геморрагических диатезов у остальных участниц диагностировано не было. Также не зарегистрировано случаев почечной недостаточности, гиперчувствительности к кеторолаку или другим НПВП.
В общей сложности 389 участниц (77,8%) получали внутривенно кеторолак в течение периоперационного периода, из них 356 (71,2%) пациенткам по меньшей мере одна доза вводилась во время операции, а 170 (34,0%) – после операции; 137 лиц получали кеторолак как интра-, так и постоперационно. Медиана общей интраоперационной дозы составила 30 мг (межквартильный диапазон – 0 мг), послеоперационной – 90 мг (межквартильный диапазон – 30 мг). Пациентки, получавшие кеторолак, статистически значимо не отличались от остальных по возрасту, ИМТ или общей массе резецированной молочной железы (табл. 1).
Образование гематомы
В 1,4% случаев в течение 24 ч после операции сформировались гематомы. У 7 пациенток наблюдалась односторонняя гематома, из них троим проведена аспирация крови под местной анестезией, а четырем – оперативная эвакуация под общей анестезией. Ни в одном случае регидратация или трансфузия не потребовалась. Каких-либо осложнений или рецидивов гематом после вмешательства не зарегистрировано. Следует отметить, что формирование гематомы не зависело от возраста, ИМТ или массы резецированной ткани молочной железы, а также не было связано с введением кеторолака. Не было различий средних доз кеторолака у пациенток с гематомой и без таковой (р>0,20).
Периоперационная аналгезия без применения кеторолака
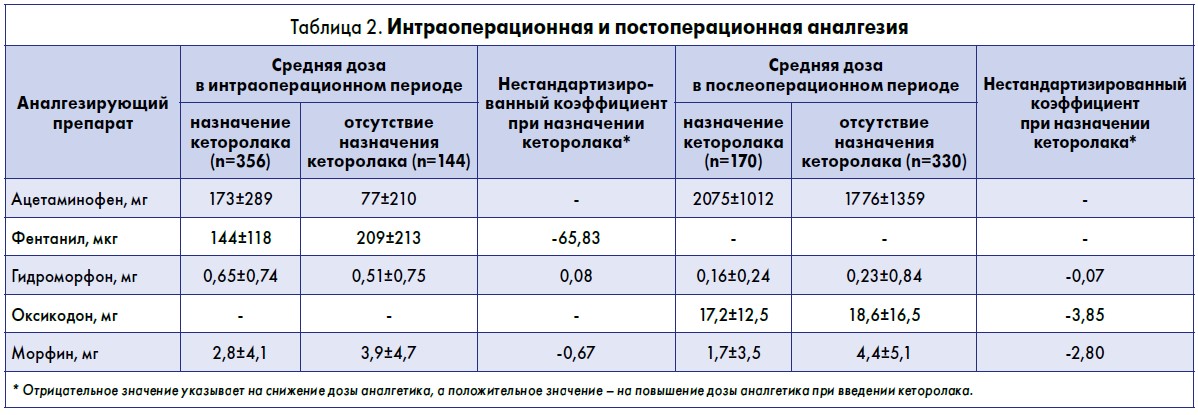
В ходе исследования пациентки получали аналгезирующие препараты помимо кеторолака (табл. 2). Во время операции вводились такие лекарственные средства: ацетаминофен внутривенно, фентанил, гидроморфон и морфин. После операции применяли: ацетаминофен и оксикодон перорально, гидроморфон и морфин внутривенно. НПВП, кроме кеторолака, не использовали; кроме того, до операции не назначали ацетаминофен или габапентин.
Пациенткам, получавшим кеторолак, назначали значительно более высокую среднюю дозу ацетаминофена как во время, так и после операции. Поэтому доза ацетаминофена использовалась в качестве ковариаты в линейном регрессионном анализе при изучении влияния введения кеторолака на среднее значение общей дозы опиоидов.
Пациенткам, которым вводили кеторолак интраоперационно, назначали значительно меньшую дозу фентанила и морфина (р<0,001), но большую гидроморфона (р<0,001). На фоне применения кеторолака в послеоперационном периоде пациенткам значительно реже требовалось введение оксикодона и морфина (р<0,001).
Обсуждение
В ходе ретроспективного анализа данных девочек-подростков и молодых женщин (n=500), прошедших редукционную маммопластику, выполненную во всех случаях одним хирургом, не было обнаружено связи между внутривенным введением кеторолака и образованием послеоперационной гематомы. Вместе с тем использование кеторолака ассоциировалось со снижением дозы некоторых опиоидных аналгетиков (фентанил и морфин интраоперационно, оксикодон и морфин после операции). С другой стороны, применение кеторолака во время вмешательства было связано с более высокой дозой гидроморфона.
Кеторолак является НПВП с выраженным аналгезирующим эффектом, конкурентным неселективным ингибитором циклооксигеназы (ЦОГ). Ингибиторы ЦОГ блокируют выработку метаболитов арахидоновой кислоты, в частности тромбоксана А2, важного медиатора агрегации тромбоцитов. Известно, что кеторолак временно ингибирует функцию тромбоцитов у здоровых лиц (что способствует увеличению времени кровотечения), не оказывая существенного влияния на процессы коагуляции или фибринолиза. Вместе с тем есть основания полагать, что функция тромбоцитов ускоряется вследствие воздействия физиологических факторов стресса, вызванного хирургическим вмешательством.
В литературных источниках отсутствуют данные, подтверждающие усиление кровотечения после операций на фоне применения кеторолака. Существующие на этот счет опасения основаны главным образом на результатах когортного исследования (Strom et al., 1996) и описаниях клинических случаев. Авторы упомянутого исследования сообщили о значительном повышении частоты послеоперационных кровотечений у пациентов в возрасте старше 75 лет, получавших кеторолак в высоких дозах на протяжении более 5 дней. При этом следует учитывать, что исследователями пятна крови на повязке трактовались как послеоперационное кровотечение. По сути, клинически значимое кровотечение развивалось с частотой один случай на каждую тысячу пациентов, получавших кеторолак.
В исследовании, описанном в данной статье, участвовали значительно более молодые (средний возраст – 18,1 года) и более здоровые пациенты, в основном не имевшие сопутствующих заболеваний (кроме избыточного веса/ожирения). Кроме того, участники получали кеторолак в относительно низких дозах в течение не более 3 дней. Согласно результатам метаанализа (Gobble RM, Orgill DP., 2015) 27 двойных слепых рандомизированных контролируемых исследований, не выявлено значительного повышения частоты послеоперационного кровотечения при использовании кеторолака.
В отношении применения кеторолака при редукционной маммопластике представляют интерес два исследования. В ретроспективном анализе (Cawthorn T.R. et al., 2012) было установлено, что однократное внутривенное введение кеторолака в периоперационном периоде ассоциировалось с повышением вероятности хирургической эвакуации гематомы в более чем три раза (относительный риск – 3,6). Помимо того что относительный риск не может быть рассчитан в ретроспективном анализе, в это исследование также были включены пациенты из двух учреждений, следовательно, операции выполнялись разными хирургами, каждый из которых использовал свою собственную технику редукционной маммопластики; при этом авторами не было предпринято попыток коррекции этих переменных. Во втором ретроспективном анализе историй болезни пациенток с макромастией (n=293) обнаружено, что при введении кеторолака во время операции повышалась частота интраоперационного и послеоперационного кровотечения. Однако лишь пять пациенток получали кеторолак интраоперационно, и опять же, контроль переменных, обусловленных техникой операции, не проводился.
Для сравнения: преимуществом представленного исследования является участие одного хирурга и единая техника редукционной маммопластики. Следует акцентировать внимание на том, что в настоящее исследование были включены лица значительно более молодые, чем участники двух вышеупомянутых исследований. Это важно по двум причинам. Во-первых, возраст может быть фактором, снижающим частоту периоперационных кровотечений при редукционной маммопластике. Во-вторых, молодые пациенты подвержены большему риску постоянного употребления опиоидов после операции, а это означает, что незначительное повышение риска кровотечений может быть компенсировано за счет предотвращения вреда от назначения опиоидов. Кроме того, образование гематомы является легко поддающимся лечению осложнением; в описанной выборке пациентов не наблюдалось рецидивов или отдаленных последствий.
В исследовании продемонстрировано, что применение кеторолака способствует значительному снижению доз наркотических аналгетиков, назначаемых интраоперационно и послеоперационно. Данные о необходимости введения во время операции более высоких доз гидроморфона пациенткам, получавшим кеторолак, следует рассматривать с учетом того, что эти же пациентки получали более низкие дозы фентанила и морфина. В то же время использование тактики назначения кеторолака не повышает частоту образования послеоперационной гематомы. Кроме того, специалисты в области хирургии молочной железы, безусловно, должны рассматривать применение кеторолака внутривенно не только как часть мер по влиянию на опиоидный кризис, но и как вариант минимизации риска побочных эффектов, связанных с опиоидами, включая тошноту, рвоту, угнетение дыхания, седацию и длительное пребывание в стационаре.
Следует отметить и ограничения описанного исследования. Поскольку был проведен ретроспективный анализ, авторы не имели возможности проспективно собрать данные о степени контроля боли, а также о генезе и частоте побочных эффектов. Кроме того, дизайн исследования не позволил отследить амбулаторное употребление и злоупотребление опиоидами. Тот факт, что в исследовании представлен опыт одного хирурга, ограничивает внешнюю валидность результатов. Потому важно проведение мультицентровых исследований с включением пациентов, прооперированных с использованием разных методик.
Таким образом, кеторолак является безопасным аналгетическим средством при проведении редукционной маммопластики у подростков и молодых женщин. Его применение не повышает риск образования послеоперационной гематомы.
Эти результаты крайне значимы для обеспечения хирургической помощи, поскольку хирурги и анестезиологи заинтересованы в оптимизации лечения болевого синдрома без повышения риска потенциального злоупотребления опиоидами среди своих пациентов.
Подготовила Виктория Лисица
По материалам J.M. Firriolo, L.C. Nuzzi, L.C. Schmidtberg, B.I. Labow.
Perioperative Ketorolac Use and Postoperative Hematoma Formation in Reduction Mammaplasty: A Single-Surgeon Experience of 500 Consecutive Cases. Plast. Reconstr. Surg. 142: 632e, 2018.