31 травня, 2019
Ефективність декслансопразолу у лікуванні пацієнтів з ерозивним езофагітом
Гастроезофагеальний рефлюкс – це патологічний процес, який може виникати у здорових немовлят, дітей та дорослих без відчутних наслідків [1]. Гастроезофагеальна рефлюксна хвороба (ГЕРХ) характеризується закиданням у стравохід шлункового вмісту, що зумовлює стійкі симптоми, такі як печія, кашель, біль в епігастрії, блювання і регургітація. Прояви ГЕРХ прийнято розділяти на п’ять варіантів: функціональна печія, гіперчутливість стравоходу, неерозивна ГЕРХ, ерозивний езофагіт (EE) та стравохід Барретта. Ці фенотипи радше клінічно відрізняються, ніж пов’язані між собою, незважаючи на наявність подібних симптомів [3]. Більше того, симптоми ГЕРХ не можуть достовірно свідчити про наявність ЕЕ, а тяжкість симптомів не корелює зі ступенем ураження слизової оболонки. Оскільки симптоми ГЕРХ не завжди супроводжуються ендоскопічними змінами, діагноз ЕЕ потребує візуальних доказів пошкодження слизової оболонки над гастроезофагеальним з’єднанням [4, 5].
Сьогодні спостерігається тенденція до підвищення частоти печії у дітей і підлітків з ГЕРХ, що деякою мірою пояснює значну поширеність ЕЕ з віком. Незважаючи на те що кількість доказів невелика, в одному дослідженні було виявлено, що частота наявності ендоскопічно підтверджених ознак ЕЕ становила 10,5% у дітей 12 років з ГЕРХ і 19,5% у дітей 17-річного віку. Поширеність печії у загальній педіатричній популяції дорівнює 1,8% дітей від 3 до 9 років, 3,5% дітей від 10 до 17 років і 22% дітей старше 18 років [6], тимчасом як серед 615 опитаних дітей віком від 10 до 17 років печія була відмічена щонайменше у 5-8% [7, 8].
Поширеність ЕЕ вища у пацієнтів педіатричного профілю з наявними в анамнезі неврологічними розладами чи оперативними втручаннями з приводу атрезії стравоходу. Таким чином, діти зі стійкими симптомами ГЕРХ, а також зі станами, які провокують ГЕРХ, є претендентами на емпіричне лікування інгібіторами протонної помпи (ІПП) [1, 2].
Отримано вагомі докази того, що короткі курси (наприклад, 8 тижнів) лікування ІПП, такими як омепразол, езомепразол, лансопразол, рабепразол і пантопразол, є ефективними для загоєння дефектів при ЕЕ та зменшення симптомів у дітей віком від 1 до 17 років [9-15]. У міжнародних клінічних настановах рекомендують у дітей застосовувати ІПП як терапію першої лінії протягом 3 міс для повного загоєння виразок при ЕЕ (на основі експертної оцінки) [1]. Однак рекомендації щодо підтримувальної терапії ІПП у педіатричних пацієнтів з лікованим ЕЕ змінилися, оскільки частота рецидивів після загоєння варіює від 2,2 до 25% [1, 16, 17]. Вища частота рецидивування спостерігалася у значної частини пацієнтів з тяжчими проявами езофагіту або тих, що мають супутні захворювання, які провокують ГЕРХ [1, 17]. Отже, підтримувальна терапія ІПП може бути більш необхідною для пацієнтів з тяжчими проявами ЕЕ та/або наявністю супутніх захворювань [1, 17].
! У 2009 р. було схвалене застосування у дорослих ІПП декслансопразолу (Дексілант®, Takeda) у капсулах у добовій дозі 30 мг для підтримання загоєння дефектів слизової оболонки стравоходу, усунення печії (до 6 міс), в тому числі пов’язаної з симптоматичною неерозивною ГЕРХ (4 тижні). Декслансопразол у добовій дозі 60 мг протягом 8 тижнів був схвалений для лікування хворих на ЕЕ [18]. У 2016 р. декслансопразол було схвалено для застосування у пацієнтів віком 12-17 років з ГЕРХ.
Деклансопразол є енантіомером лансопразолу з унікальною подвійною формулою, яка забезпечує сповільнене вивільнення діючої речовини, що подовжує тривалість дії лікарського засобу, внаслідок чого зменшується виділення шлункового соку [18, 19]. Після прийому всередину частина гранул вивільняє 25% дози препарату при рН ≥5,5, що відбувається у проксимальній частині дванадцятипалої кишки. Наступна частина гранул вивільняє 75% дози декслансопразолу далі вздовж шлунково-кишкового тракту при рН ≥6,75 [19, 20].
! В одному дослідженні у дорослих пацієнтів швидкість загоєння ерозій при ЕЕ у разі застосування добової дози декслансопразолу 60 мг була вищою порівняно з такою при введенні лансопразолу у добовій дозі 30 мг (85,3 проти 79,0%; P=0,05).
Проте в іншому дослідженні не виявлено різниці у загоєнні дефектів слизової оболонки (на тлі прийому декслансопразолу у дозі 60 мг його частота становила 86,9%, на фоні застосування лансопразолу 30 мг – 84,6%) [21]. Після загоєння дефектів слизової оболонки стравоходу декслансопразол у дозах 30 і 60 мг також показав ефективність у підтриманні загоєння ерозій аж до 6 міс, а також у контролі печії протягом більше ніж 90% днів терапії [22]. Порівнянний фармакокінетичний профіль спостерігався у підлітків, які приймали декслансопразол 1 раз на день [23].
У цьому дослідженні ми вивчали безпечність застосування, переносимість та ефективність декслансопразолу у лікуванні та підтримувальній терапії при ЕЕ у підлітків з підтвердженим діагнозом ЕЕ. Висновки мають практичне застосування для лікування ГЕРХ у дітей і підлітків.
Зважаючи на те що симптоми ГЕРХ, а також пов’язані з ГЕРХ пошкодження слизової оболонки стравоходу можуть проявлятися і в майбутньому [24], зусилля з контролю чи запобігання подальшому пошкодженню стравоходу, а також поліпшення якості життя є особливо важливими для цих молодих пацієнтів.
Методи
У статті представлені результати багатоцентрового (включено пацієнтів з 18 міст) 36-тижневого дослідження, метою якого була оцінка безпечності та ефективності декслансопразолу у лікуванні підлітків (віком 12-17 років) з ЕЕ.
Учасники дослідження
З 237 учасників із симптомами ГЕРХ у дослідження включено 62 пацієнти з ендоскопічно підтвердженим ЕЕ з різним перебігом захворювання (за Лос-Анджелеською класифікацією рефлюкс-езофагіту).
Дизайн дослідження
Дослідження складалося з трьох етапів: скринінг (до 21 дня), лікування (8 тижнів + 16 тижнів підтримувальної терапії) та спостереження. Підлітки з підтвердженим діагнозом ЕЕ приймали декслансопразол у дозі 60 мг (n=62) протягом 8 тижнів. Далі у групі, де було відмічено загоєння дефектів слизової оболонки, прийом лікарського засобу припинено. У групі, в якій не було відмічено загоєння дефектів слизової оболонки, прийняте рішення про перехід на таку схему лікування: 30 мг декслансопразолу (n=25) та плацебо (n=26) тривалістю 16 тижнів. З 24-го тижня лікування було відмінено та почалась фаза спостереження пацієнтів.
Результати
Характеристика пацієнтів
На початку дослідження у більшості пацієнтів діагностовано EE ступеня A або B, у 2 пацієнтів – ступеня C або D.
Найчастіше в анамнезі пацієнтів відзначали закрепи (4,8%) та пневмонію (4,8%), крім того, у 4,8% хворих раніше виконували езофагогастродуоденоскопію.
При біопсії шлунка не виявлено патологічних змін у 64,5% хворих, найбільш частою патологічною знахідкою був хронічний гастрит за відсутності H. pylori (33,9% усіх пацієнтів).
Печія і біль в епігастрії були найчастішими симптомами, що спостерігались у 76 і 73% пацієнтів відповідно.
Фазу спостереження завершили 24 пацієнти. Середні показники дотримання прихильності до лікування становили 95 і 96%, вони були зафіксовані під час відкритої фази загоєння та подвійної сліпої фази спостереження відповідно.
Безпечність
Під час відкритої фази загоєння 38 (61,3%) пацієнтів повідомили загалом про 79 побічних ефектів, жоден з них не вважався пов’язаним із лікуванням. Про головний біль у фазі загоєння повідомляли найчастіше – 12,9% пацієнтів, про орофарингеальний біль – 8,1%, діарею – 6,5% і назофарингіт – 6,5% пацієнтів.
Під час фази підтримувального лікування 18 (72,0%) пацієнтів, які отримували декслансопразол, і 16 (61,5%) пацієнтів, які отримували плацебо, повідомили відповідно про 45 і 46 побічних ефектів.
Як і у фазі загоєння, у фазі підтримувальної терапії головний біль був найбільш частим симптомом в обох групах: у 6 (24,0%) пацієнтів, які приймали декслансопразол, і в 4 (15,4%) пацієнтів, які приймали плацебо.
Дванадцять (67%) і 5 (36%) пацієнтів, які відповідно отримували декслансопразол або плацебо у підтримувальній фазі, відмітили побічні ефекти після курсу лікування.
Не було відзначено клінічно значущих наслідків за результатами клінічних аналізів, вітальними показниками, даними електрокардіографії або фізикального обстеження.
Середнє підвищення рівня гастрину в сироватці крові становило 64,1 пг/мл після 4 тижнів відкритої фази загоєння, ці результати залишалися стабільними протягом наступних 4 тижнів цієї фази.
Ефективність
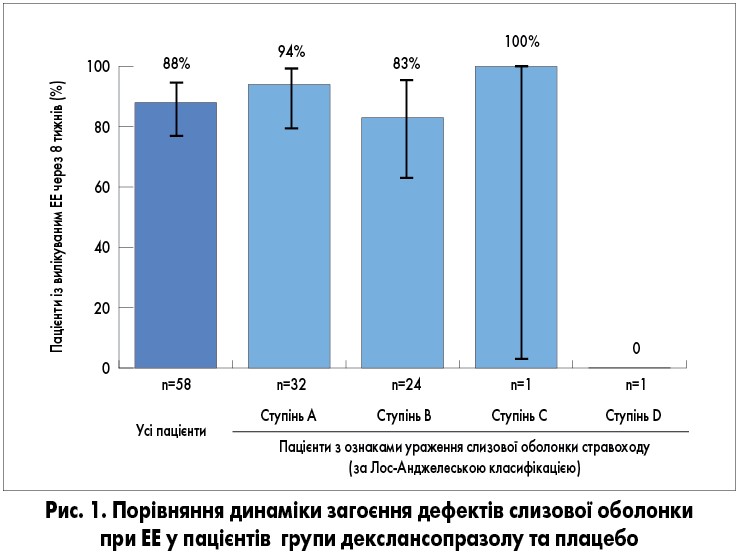
Фаза загоєння дефектів слизової оболонки стравоходу. Після 8 тижнів лікування декслансопразолом у дозі 60 мг у 88% пацієнтів з ЕЕ під час відкритої фази було відмічено загоєння дефектів слизової оболонки (95% довірчий інтервал – ДІ – 76,7; 95,0). У 82% осіб, які протягом 8-тижневої відкритої фази приймали декслансопразол, було виявлено загоєння ерозій (95% ДІ 70,5; 90,8). У 3 із 7 пацієнтів, у яких дефекти слизової оболонки залишилися, ступінь ЕЕ не змінився, в інших 3 пацієнтів була зафіксована позитивна динаміка (зі ступеня В до А у 2 хворих і зі ступеня D до B в 1 хворого), в 1 пацієнта динаміка була негативна (ЕЕ ступеня B трансформувався у ступінь C). Загальне дотримання прихильності до лікування серед цих пацієнтів становило 85-100%. Загоєння було досягнуто у 94% пацієнтів з ЕЕ ступеня А та у 83% пацієнтів з ЕЕ ступеня В (рис. 1).
Під час відкритої фази загоєння печія частіше виникала удень, ніж уночі; печія була відсутня в середньому протягом 73,9% днів і 85,4% ночей. Протягом 8 тижнів відкритої фази загоєння в середньому упродовж 65,8% діб печію у денний чи нічний час не фіксували. У середньому пацієнти не використовували препарат для усунення печії протягом 96,6% днів.
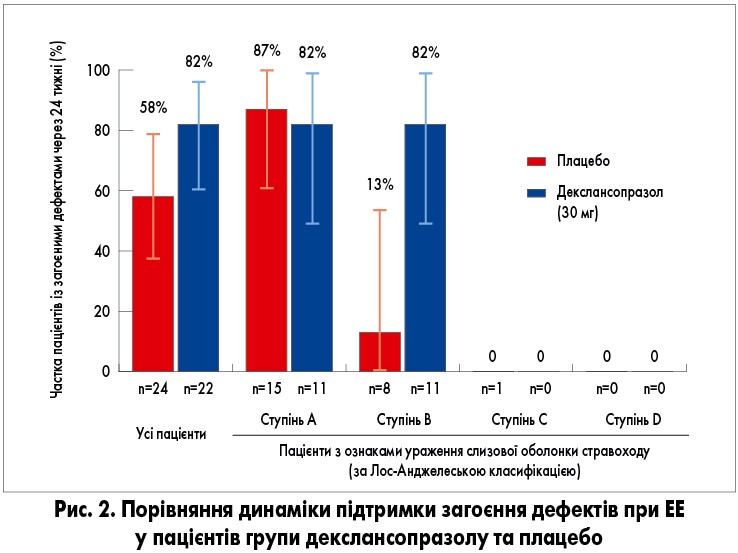
Фаза підтримувальної терапії загоєних дефектів слизової оболонки стравоходу. Після загоєння дефектів слизової оболонки стравоходу в кінці 16-тижневої подвійної сліпої фази оцінювали дані 22 і 24 пацієнтів, що приймали декслансопразол у дозі 30 мг і плацебо відповідно. Утримання загоєння слизової оболонки в кінці 16-тижневої подвійної сліпої фази було досягнуто у 82% (18 з 22) пацієнтів (95% ДI 59,7; 94,8; р порівняно з плацебо 0,114) і 58% (14 з 24) хворих (95% ДІ 36,6; 77,9), які приймали декслансопразол у дозі 30 мг 1 раз на день (n=22) і плацебо (n=24) відповідно (рис. 2). При аналізі всіх від самого початку включених у дослідження пацієнтів утримання загоєння дефектів слизової оболонки спостерігалося у 72% (95% ДI 50,6; 87,9; р порівняно з плацебо 0,249) і 54% (95% ДI 33,4; 73,4) пацієнтів, рандомізованих для застосування декслансопразолу 30 мг 1 раз на день і плацебо відповідно. У 4 хворих констатовано рецидив на тлі прийому декслансопразолу у дозі 30 мг 1 раз на день: у 3 пацієнтів ступінь ЕЕ став початковим, а в 1 пацієнта змінився зі ступеня В до ступеня А.
У 10 пацієнтів, які приймали плацебо, виявили рецидив ЕЕ: у 4 із них ступінь тяжкості ЕЕ повернувся до ступеня В, а у 2 – до ступеня А. У 4 пацієнтів ЕЕ рецидивував до менш тяжкого ступеня ніж той, яким був на початку: у 3 пацієнтів з ЕЕ ступеня В на початковому етапі виник рецидив ЕЕ ступеня А, в 1 пацієнта з ЕЕ ступеня С на початковому етапі – ступеня В.
Серед пацієнтів з ЕЕ ступеня А на початковому етапі спостерігалися аналогічні показники збереження стадії загоєння як у разі прийому декслансопразолу (82%), так і плацебо (87%; рис. 2). Більша різниця показників збереження загоєння слизової оболонки спостерігалася у пацієнтів з ЕЕ ступеня В: у 82% осіб, що приймали декслансопразол, і 13% – плацебо. В 1 пацієнта з ЕЕ ступеня С на початку дослідження, який отримував плацебо, загоєння не утрималося.
Частота виникнення печії вдень переважала під час відкритої фази лікування, тимчасом як уночі – у фазі підтримувальної терапії. У середньому частка днів без печії удень у пацієнтів, які приймали декслансопразол, склала 89,7%, плацебо – 82,7%. Частка днів без печії уночі становила 95,6% у хворих, які приймали декслансопразол, і 90,3% – плацебо. Печія (удень або уночі) була відсутня в середньому протягом 86,6 і 68,1% діб у групі декслансопразолу і плацебо відповідно. Відмінності між групами декслансопразолу та плацебо були статистично незначущими.
Фаза спостереження (без лікування). Пацієнти з загоєними дефектами слизової оболонки стравоходу в кінці підтримувальної фази припинили прийом препарату перед початком фази спостереження. Протягом 3 міс спостереження пацієнти, які раніше отримували декслансопразол або плацебо, не відзначали печію удень або вночі в середньому протягом 86,3 і 83,6% діб. У жодного з пацієнтів під час періоду спостереження не виник рецидив симптомів, які потребували лікування ІПП або блокаторами H2‑каналів. Однак в 1 пацієнта було повідомлено про повторне виникнення ГЕРХ як побічну дію, пов’язану з застосуванням лікарського засобу, що досліджувався під час фази підтримувальної терапії. Цьому пацієнту у подальшому був призначений омепразол.
Пацієнти груп декслансопразолу та плацебо під час подвійної сліпої фази не використовували препарати для усунення печії в середньому протягом 99,1 і 97,7% днів відповідно. Під час фази спостереження необхідність у застосуванні препаратів для купірування печії залишилася незначною. У середньому частка днів, у які не було потреби приймати препарат, становила 96,9 і 100,0% у групах декслансопразолу і плацебо відповідно.
Обговорення
Поширеність ЕЕ з віком збільшується. В осіб молодого віку з тривалим анамнезом рефлюксної хвороби розвиваються ураження слизової оболонки стравоходу, подібні до таких у дорослих [8, 13, 29]. У педіатричних хворих симптомами рефлюксу є регургітація, кашель, біль в епігастрії та печія [2]. У підлітків печія та регургітація – первинні симптоми, що вказують на наявність ГЕРХ, у дорослих ці симптоми переважають [1, 30]. Наразі ІПП є препаратами вибору для усунення симптомів ГЕРХ і загоєння ерозій слизової оболонки стравоходу у дорослих [30], а також рекомендуються як терапія першої лінії у дітей з ЕЕ [1]. Наше дослідження продемонструвало, що профілі безпечності та переносимості декслансопразолу у підлітків відповідали таким у дорослих [31]. Більшість зафіксованих побічних ефектів, пов’язаних із прийомом декслансопразолу, були легкими. Протягом дослідження лише 1 пацієнт повинен був припинити лікування у зв’язку з побічними ефектами, які, із великою ймовірністю, були пов’язані з неадекватною реакцією організму на прийом декслансопразолу.
! У нашому дослідженні застосування декслансопразолу сприяло загоєнню дефектів слизової оболонки стравоходу у 88% підлітків, що можна порівняти із загоєнням у дослідженнях дорослих (85 і 87%) [21].
Спостерігалась відчутна різниця результатів у підлітків і дорослих у підтриманні загоєння дефектів слизової оболонки: у значної частини підлітків (82%) загоєння ерозій відбувалося протягом 16 тижнів підтримувальної терапії декслансопразолом, тимчасом як у дорослих (66%) утримали заживлення на 24 тижні лікування. Важливо відзначити, що у дорослих пацієнтів перебіг ЕЕ був тяжчим (приблизно 30% хворих мали ЕЕ ступенів С і D), ніж у підлітків у нашому дослідженні. Хоча тривалість досліджень була різною, Boccia та співавт. показали, що підліткам з неускладненим ГЕРХ не обов’язково проводити підтримувальну терапію після загоєння дефектів слизової оболонки [16]. Виходячи з цього, а також наміру мінімізувати період прийому плацебо, в дослідженні була застосована коротша, ніж у дорослих, фаза підтримувальної терапії. Різниця частоти загоєння дефектів слизової оболонки у разі застосування декслансопразолу та плацебо була відмічена, але не досягла статистичної значущості.
У нашому дослідженні у 58% підлітків підтримувалося загоєння дефектів слизової оболонки на фоні прийому плацебо, а в дорослих цей показник становив лише 14% [22]. Підтримання загоєння дефектів слизової оболонки стравоходу після застосування плацебо у педіатричних пацієнтів, на відміну від дорослих, можна пояснити віковими відмінностями. У літературі пропонується думка про те, що ЕЕ у підлітковому віці може бути початковою стадією захворювання дорослих [6-8, 32]. Отже, у підлітків, що одужали, ризик розвитку рецидиву нижчий, ніж у дорослих, у яких спостерігався тяжчий перебіг ЕЕ (за Лос-Анджелеською шкалою).
Підгруповий аналіз у підлітків підтверджує гіпотезу про те, що ефективність плацебо у підтриманні загоєння дефектів слизової оболонки зумовлена менш тяжким перебігом захворювання.
Таким чином, це дослідження показує доцільність застосування декслансопразолу як одного з варіантів лікування пацієнтів з ЕЕ. Прийом декслансопразолу загалом є безпечним і забезпечує більшу частку підтримання загоєння дефектів слизової оболонки порівняно з плацебо. В цілому, у підлітків з легкою формою ЕЕ (ступінь А) ймовірність підтримання загоєння дефектів слизової оболонки стравоходу більша, ніж у тих, що мають ЕЕ інших ступенів тяжкості (В, С, D). Декслансопразол також продемонстрував вищу ефективність у підтриманні загоєння дефектів слизової оболонки, ніж плацебо, у пацієнтів з тяжчим перебігом захворювання.
Переклала з англ. Ольга Мигалатюк
UA/ (PPIF)/0519/0026
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (52), травень 2019 р.