20 грудня, 2016
Европейская панкреатология: что нового?

По материалам 48-й встречи Европейского клуба панкреатологов
6-9 июля в г. Ливерпуле (Великобритания) состоялась очередная встреча Европейского клуба панкреатологов. В рамках этого мероприятия было представлено более 400 устных и постерных докладов.
Наше внимание привлек целый ряд сообщений. Начнем с анатомии: М.A. Suarez-Munoz и соавт. (Испания) «Волюметрия (измерение объема) поджелудочной железы поджелудочной железы». Этот метод состоит в специальной обработке данных компьютерной томографии (КТ) в аксиальной, корональной и сагиттальной проекциях, при этом исключается объем кровеносных и лимфатических сосудов поджелудочной железы (ПЖ). Исследование провели 50 пациентам, которым КТ выполнялась по поводу патологии, не связанной с ПЖ и другими органами пищеварения. Средний объем ПЖ составил 86,82±24,13 мл. Различий объема ПЖ в зависимости от пола обследованных найдено не было. У пациентов младше 70 лет объем ПЖ составлял >80 мл, а у более старших пациентов, как правило, <70 мл.
Несколько сообщений были посвящены патогенезу хронического панкреатита (ХП). Особое внимание уделялось генетической предрасположенности к ХП. Так, в докладе J. Rosendahl (Германия) подробно проанализированы различные мутации, которые приводят к внутриорганной активации трипсиногена: мутации катионического трипсиногена (PRSS1), ингибитора Казаля (SPINK1), химотрипсина C (CTRC), карбоксипептидазы А1 и др. В ряде случаев эти мутации являются основным механизмом развития заболевания, а в других случаях – способствующим фоном. В любом случае мутации играют роль «спички», к которой нужно поднести «огонь», то есть некий разрешающий фактор (алкоголь, курение и др.). Тогда начнется активация трипсиногена, которая из-за генетического дефекта ингибирования трипсина не останавливается в должной мере, и развивается панкреатит. Таков принцип патогенеза большинства генетически обусловленных панкреатитов.
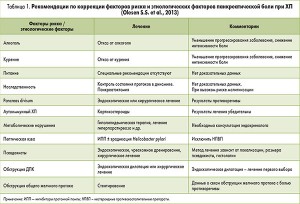
Подробную лекцию о патофизиологии и лечении боли при ХП прочитал A. Drewes (Дания). К основным механизмам боли относятся следующие:
– местные причины: воспалительный фокус (масса) в ПЖ, псевдокиста и др.;
– обструкция протоков;
– экстрапанкреатические осложнения (пептическая язва и др.);
– воспаление (провоспалительные цитокины);
– внутритканевая гипертензия;
– осложнения хирургического или эндоскопического вмешательства;
– лекарственно-индуцированная дисфункция кишечника (парез при применении опиоидов);
– повышенная продукция холецистокинина;
– дефицит гастроинтестинальных гормонов, нарушения кишечной перистальтики, синдром избыточного бактериального роста в тонкой кишке;
– периферическая сенситизация, психосоматика, нейропатия;
– другие причины (изменения со стороны энтеральной нервной системы, повышение симпатического тонуса, мезентериальная ишемия, сопутствующая патология, опиоидиндуцированная гипералгезия).
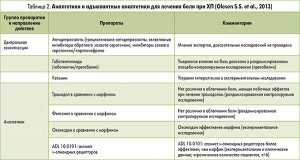
Кроме того, A. Drewes привел доказательные исследования, касающиеся купирования боли при ХП (табл. 1, 2). Докладчик также опирался на обзорную статью S.S. Olesen и соавт. о патогенезе и лечении абдоминальной боли при ХП. (Полный текст этой статьи можно посмотреть по ссылке: http://www.pancreapedia.org/sites/ www.pancreapedia.org /files/DOI%20Pathogenis%20and% 20Treatment%20of%20Pain%20in%20CP.pdf.)
Профессор D. Whitcomb (США) выступил с программной лекцией о готовящихся международных рекомендациях по диагностике и лечению ХП. По мнению экспертов, ХП необходимо рассматривать в соответствии со следующим определением: «ХП – это патологический фибровоспалительный синдром у индивидов с генетическими, внешними и/или другими факторами риска, которые приводят к развитию персистирующего патологического ответа на повреждение паренхимы или стресс». Общие признаки при установленном диагнозе ХП и на его поздних стадиях включают атрофию и фиброз паренхимы ПЖ, абдоминальную боль, неравномерность протоков и их стеноз, кальцификацию, нарушение внешне- и внутрисекреторной функции ПЖ, дисплазию. Рекомендации находятся в процессе разработки и пока не опубликованы.
Целый ряд докладов был посвящен диагностике заболеваний ПЖ и, в частности, ХП. A.R.G. Sheel (Великобритания) рассказал о роли эндосонографии в диагностике ранних стадий ХП. Эндосонография – революционная инновация в панкреатологии, она все шире применяется для визуализации ПЖ. Эндосонография для выявления образований <2 см более информативна, чем КТ, позволяет визуализировать и паренхиму, и протоки ПЖ, а также выполнить биопсию и лечебные манипуляции.
Лектор привел результаты обследования 805 больных с диагнозом ХП в панкреатологическом центре Ливерпуля за период 2003-2016 гг. При тщательном обследовании у 116 (14,4%) больных диагноз ХП был снят, из них в 31% случаев был установлен диагноз синдрома хронической абдоминальной боли. У этих пациентов при тщательном инструментальном обследовании изменений со стороны ПЖ выявлено не было. В 24% случаев у пациентов были обнаружены минимальные изменения ПЖ, которые нельзя было квалифицировать как ХП. В 8% случаев диагноз ХП изменен на диагноз рецидивирующего острого панкреатита (ОП), а в 20% случаев изменения ПЖ были связаны с перенесенным ОП. У 4% пациентов с ошибочным диагнозом ХП выявлена внутрипротоковая муцинозная неоплазия. У 13% диагноз ХП был снят по другим причинам (диагностирован рак ПЖ, стеатоз ПЖ и др.). Интересно, что для установления правильного диагноза пациентам было проведено в целом 252 радиологических исследования, в том числе 170 КТ, 61 эндосонография, 20 магнитно-резонансных холангиопанкреатографий (2 из них с введением секретина) и 1 эндоскопическая ретроградная холангиопанкреатография.
J. Iglesias-Garcia (Испания) доложил о результатах проспективного перекрестного корреляционного исследования. 43 больным были выполнены эндосонография ПЖ с эластографией и эндоскопический секретиновый тест с оценкой продукции бикарбонатов. Получена сильная корреляция между результатами эластографии, позволяющей оценить степень фиброза ПЖ, и продукцией бикарбонатов. Это свидетельствует об информативности эластографии для определения выраженности фиброзирования ПЖ.
Серия докладов была посвящена различным аспектам трофологической недостаточности при ХП с внешнесекреторной недостаточностью ПЖ (ВНПЖ). В частности, в докладе S. Stigliano (Италия) речь шла об остеопатии при ХП. Остеопатия приводит к повышению риска переломов, снижению качества жизни пациентов даже при отсутствии переломов. Очень важно, что остеопатия относится к осложнениям ХП, которые можно предотвратить.
Снижение минеральной плотности костной ткани развивается при ряде заболеваний органов пищеварения:
• целиакия – риск переломов повышен на 40%;
• гастрэктомия – остеопатия в 37-42% случаев;
• болезнь Крона – остеопения в 22-55% случаев, остеопороз в 3-6% случаев;
• язвенный колит – остеопения в 32-67% случаев, остеопороз в 4-50% случаев;
• ортотопическая трансплантация печени / первичный билиарный цирроз – в 46% случаев (17% – в первый год);
• ХП – остеопороз в 23% случаев, любая остеопатия – в 65% случаев.
По результатам мультицентрового перекрестного европейского исследования, включавшего 135 больных ХП, которым выполнялась двойная энергетическая рентгеновская абсорбциометрия, остеопения диагностирована в 40,7% случаев, остеопороз – в 23,7% случаев. Нормальная минеральная плотность костной ткани имела место в 35,6% случаев. Патологические изменения локализовались в шейке бедра в 37% случаев, в поясничном отделе позвоночника – в 22% случаев, обе локализации отмечались в 41% случаев. По результатам статистического анализа, независимыми факторами риска развития остеопатии являются старший возраст и женский пол. Снижают риск развития остеопатии повышенный индекс массы тела и, возможно, сахарный диабет. Не выявлено корреляции между минеральной плотностью кости, фекальной эластазой и уровнем витамина D в крови.
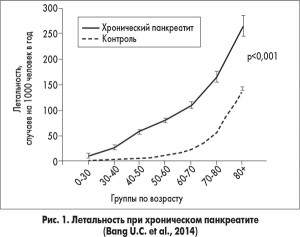
Особое внимание привлек доклад N. Vallejo-Senra (Иcпания) о кардиоваскулярном риске при ВНПЖ у больных с ХП. Докладчик привел результаты проведенного в Дании национального ретроспективного когортного исследования, демонстрирующие достоверное увеличение смертности больных ХП по сравнению с общей популяцией (рис. 1). Вклад в летальность при ХП вносит и кардиоваскулярная патология.
Патофизиология кардиоваскулярных событий при ХП:
• алкоголь и курение;
• сахарный диабет;
• трофологическая недостаточность (ВНПЖ):
• дефицит липопротеинов высокой плотности, аполипопротеина А‑1, липопротеина А;
• дефицит витамина D;
• дефицит микронутриентов;
• воспалительный синдром, ассоциированный с мальнутрицией.
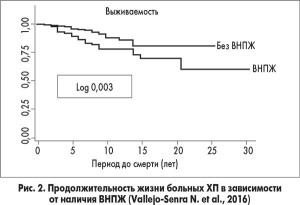
По данным исследования N. Vallejo-Senra, продолжительность жизни больных ХП без ВНПЖ достоверно больше, чем с ВНПЖ (рис. 2).
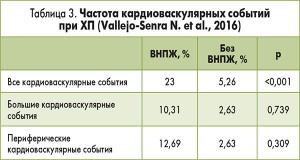
В рамках проспективного когортного исследования автор обследовал 430 пациентов. Диагноз ХП устанавливали на основе данных эндосонографии, при необходимости выполняли магнитно-резонансную томографию, магнитно-резонансную холангиопанкреатографию с секретином. Диагноз ВНПЖ основывался на результатах триглицеридного дыхательного теста. Оценивали нутритивный статус (гемоглобин, магний, альбумин, преальбумин, ретинолсвязывающий белок, гликозилированный гемоглобин). К большим кардиоваскулярным событиям относили инфаркт миокарда, инсульт, а к периферическим – артериальный тромбоз, перемежающуюся хромоту и др. Результаты исследования представлены в таблице 3. Риск кардиоваскулярных событий при ВНПЖ составил 2,46, без ВНПЖ – 0,67 (р<0,001). Выводы: более 10% больных ХП в течение 8 лет наблюдения имели кардиоваскулярные события; кардиоваскулярные события ассоциируются с ВНПЖ, артериальной гипертензией и злоупотреблением алкоголем, курением; в перспективе необходимо изучить влияние заместительной ферментной терапии на частоту кардиоваскулярных событий при ХП.
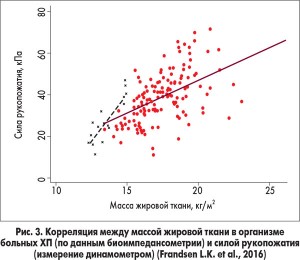
L.K. Frandsen и соавт. (Дания) обследовали 166 больных ХП и показали, что при ВНПЖ снижается сила скелетных мышц. Так, эти авторы обнаружили корреляцию между массой жировой ткани в организме пациента по данным биоимпедансометрии и силой скелетных мышц, например силой рукопожатия (измерялась динамометром) (рис. 3). Следовательно, при ВНПЖ появляется и постепенно нарастает астения.
M. Moneo (Испания) обследовал 42 больных ХП при первом визите к врачу. У пациентов с ВНПЖ со следующей частотой был выявлен дефицит:
• витамина А – 34,6%;
• витамина Е – 15,4%;
• витамина D – 80,7%;
• ретинолсвязывающего белка – 38,5%;
• магния – 7,7%;
• преальбумина – 42,3%.
Интересно, что при отсутствии ВНПЖ дефицит витамина D определялся в 75,1% случаев, то есть этот гиповитаминоз не зависит от ВНПЖ. При ВНПЖ избыточная масса тела имела место в 46,2% случаев, ожирение – в 3,8% случаев, только 3,8% пациентов имели сниженную массу тела.
Профессор M. Lerch (Германия) прочитал лекцию «Хронический панкреатит: показания и оптимизация заместительной ферментной терапии».
Основные симптомы ХП – боль, стеаторея, похудение:
– боль – рецидивирующая опоясывающая, часто сочетается с болью в пояснице;
– стеаторея – экскреция более 7 г жира в сутки как результат мальабсорбции;
– похудение – потеря более 20% массы тела.
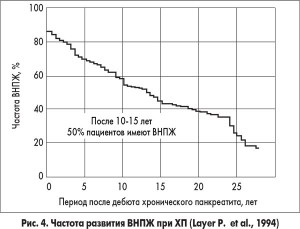
Частота развития ВНПЖ при ХП представлена на рисунке 4.
Характеристика ВНПЖ:
– мальдигестия жиров, белков и углеводов;
– стеаторея, флатуленция, абдоминальная боль;
– снижение массы тела;
– задержка развития у детей;
– дефицит жирорастворимых витаминов;
– снижение минеральной плотности костей;
– дефицит минералов (цинк, магний и др.);
– повышение заболеваемости и смертности.
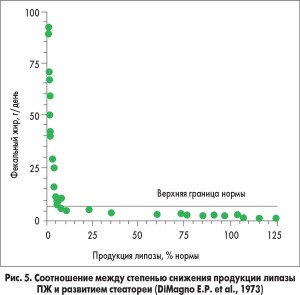
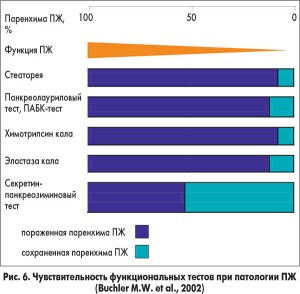
Секретин-панкреозиминовый тест, который является золотым стандартом прямого зондового теста для диагностики ВНПЖ, в настоящее время на практике не применяется как из-за сложности методики выполнения, так и из-за высокой стоимости стимуляторов. Информативным методом диагностики ВНПЖ, но также редко применяющимся на практике является количественное определение жира в кале. Возможность выполнения теста определяется необходимостью сбора кала за 72 ч. Кроме того, стеаторея развивается только в тех случаях, когда сохранено 10% и менее функционирующей паренхимы ПЖ с соответствующим снижением продукции липазы (рис. 5, 6). К рисунку 6 следует добавить, что триглицеридный дыхательный тест позволяет диагностировать ВНПЖ при сохранении >60% паренхимы ПЖ, то есть по информативности приближается к секретин-панкреозиминовому тесту.
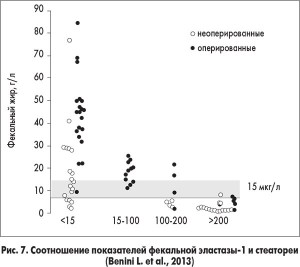
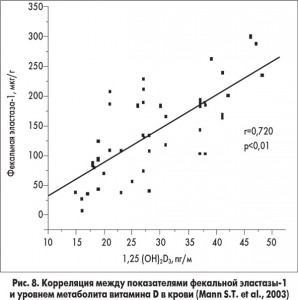
Для диагностики ВНПЖ широко применяется фекальный эластазный тест. Показатели фекальной эластазы‑1 коррелируют со стеатореей, то есть эти показатели ниже при стеаторее (рис. 7). Кроме того, найдена корреляция с уровнем витамина D в крови (рис. 8). Это свидетельствует об отражении показателями фекальной эластазы‑1 снижения экзокринной функции ПЖ и выраженности мальабсорбции.
Преимущества фекального эластазного теста:
– неинвазивный беззондовый метод;
– эластаза‑1 – панкреатоспецифический фермент;
– минимальные изменения активности эластазы при кишечном транзите;
– стабильность фермента;
– простое измерение в техническом отношении;
– нет необходимости в отмене ферментных препаратов;
– относительно невысокая стоимость.
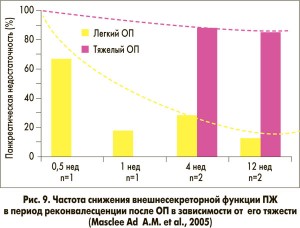
ВНПЖ развивается не только при ХП, но и при других заболеваниях ПЖ, например после перенесенного ОП (рис. 9).
Особенно часто развивается ВНПЖ, в том числе тяжелая ВНПЖ со стеатореей, у пациентов, перенесших тяжелый ОП, который потребовал выполнения некрэктомии. Так, после некрэктомии стеаторея развивается в 25% случаев, ВНПЖ без стеатореи – в 33% случаев, тогда как внешняя секреция ПЖ остается нормальной в 42% случаев. У пациентов, перенесших ОП, но без выполнения некрэктомии, функция ПЖ сохранена в 87% случаев, ВНПЖ формируется в 13% случаев, а стеаторея вообще не регистрируется.
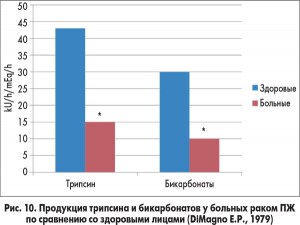
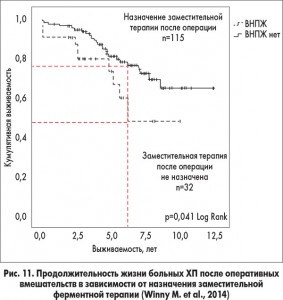
ВНПЖ развивается у значительной части больных раком ПЖ (рис. 10), часто диагностируется при сахарном диабете, особенно 1 типа. ВНПЖ формируется и является основанием для назначения ферментных препаратов после хирургических вмешательств по поводу ХП (резекций ПЖ и др.; рис. 11).
Во избежание стеатореи необходимо наличие 30 тыс. ЕД FIP липазы в дуоденальном просвете в постпрандиальном периоде (10% от нормы), но с учетом опасностей для липазы, принимаемой per os (действие кислоты и пепсина в желудке, возможный асинхронизм пассажа панкреатина и химуса в случае приема таблетированного препарата), нужно назначать больше – 40-50 тыс. ЕД FIP на основной прием пищи и 20-25 тыс. ЕД FIP на перекус.
Показания к ферментной заместительной терапии:
– препараты панкреатина показаны при доказанной или предполагаемой стеаторее;
– поскольку количественное определение жира в кале проводится редко, ферментные препараты показаны при патологических результатах функциональных тестов и клинических проявлениях мальабсорбции (снижение массы тела, абдоминальная боль, выраженный метеоризм, диспепсия, диарея);
– ферментные препараты показаны ex juvantibus при нечетких симптомах.
В готовящихся к публикации унифицированных Европейских рекомендациях по диагностике и лечению ХП (HaPanEu) представлены следующие положения, касающиеся заместительной ферментной терапии.
– Каковы показания к заместительной ферментной терапии при ХП?
• Заместительная терапия показана при ХП с ВНПЖ при наличии клинических симптомов или лабораторных признаков мальабсорбции. Рекомендуется соответствующее исследование нутритивного статуса для выявления признаков мальабсорбции (уровень 1A, сильное согласие).
– Каковы ферментные препараты выбора?
• Покрытые кишечнорастворимой оболочкой микросферы или минимикросферы размером <2 мм являются препаратами выбора при ВНПЖ. Микро- или минитаблетки размером 2,2-2,5 мм могут быть также эффективны, но научные доказательства их эффективности при ХП ограничены. Сравнительные клинические исследования различных ферментных препаратов отсутствуют (уровень 1B, сильное согласие).
Комментарий. Эффективность панкреатических ферментных препаратов зависит от нескольких факторов:
• степень смешивания с пищей и сопровождение каждой порции принятой пищи ферментами;
• синхронность эвакуации из желудка с пищей;
• смешивание с дуоденальным химусом и желчными кислотами;
• быстрое высвобождение ферментов в двенадцатиперстной кишке.
– Как должны назначаться ферментные препараты?
• Пероральные ферментные препараты должны быть распределены между основными приемами пищи и перекусами (уровень 1A, сильное согласие).
– Какова оптимальная доза ферментных препаратов при ВНПЖ вследствие ХП?
• Минимальная доза липазы 40-50 тыс. ЕД FIP на основной прием пищи и половинная доза на перекус (уровень 1A, сильное согласие).
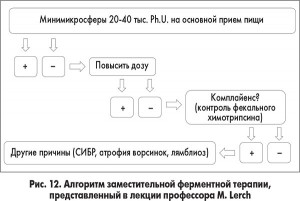
Профессор M. Lerch представил алгоритм заместительной ферментной терапии (рис. 12).
Использование форм ферментных препаратов (в частности, минимикросфер), обеспечивающих максимально возможную площадь контакта пищи и фермента, является предпочтительным, поскольку способствует повышению эффективности гидролиза липидов. Даже незначительное уменьшение размера частиц – с 1,8-2 мм до 1,0-1,2 мм – приводит к почти четырехкратному увеличению скорости работы ферментов и повышению эффективности пищеварения и, следовательно, к улучшению коррекции нутритивного статуса на 25%.
Инновацией в заместительной ферментной терапии является создание препаратов на основе микробной липазы, например липротамазы. Профессор M. Lerch рассказал о доказательных исследованиях и перспективах применения таких препаратов (результаты одного из таких исследований представлены ниже). Микробные ферменты имеют ряд положительных качеств: широкая субстратная специфичность, сохранение активности в широких рамках рН и др.
В лекции было подчеркнуто, что при недостаточной эффективности ферментных препаратов их необходимо сочетать с ингибиторами протонной помпы для коррекции рН в дуоденальном просвете. Ферментные препараты важно назначать в начале приема пищи, что создает лучшие условия для реализации их эффекта.
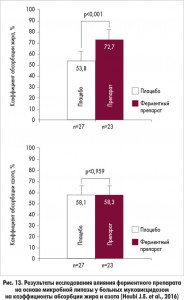
В продолжение лекции профессор M. Lerch рассказал о результатах двойного слепого рандомизированного плацебо-контролируемого исследования эффективности и безопасности нового ферментного препарата на основе микробной липазы при муковисцидозе (Heubi J.E., Германия; рис. 13). Следует отметить, что этот препарат выпускается в жидкой форме (для питья), это позволяет назначать его маленьким детям и при необходимости вводить через зонд.
Мониторинг эффективности лечения ВНПЖ:
– позитивная динамика клинических симптомов (увеличение массы тела, нормализация витаминного статуса, исчезновение абдоминальных симптомов);
– при отсутствии положительной динамики клинических проявлений необходимо провести функциональные тесты (триглицеридный дыхательный тест), оценить экскрецию жира с калом.
Интересные результаты получены при проведении экспериментального исследования A. Mosseler (Германия) «Таурин при ВНПЖ для улучшения усвоения жира». Таурин – сульфокислота, основная функция которой состоит в образовании конъюгатов с желчными кислотами. При ВНПЖ повышена потеря таурина из-за нарушения энтерогепатической циркуляции желчных кислот. Имеет значение и то, что синдром избыточного бактериального роста в тонкой кишке приводит к деконъюгации желчных кислот. В рамках испытания были обследованы две группы животных с ВНПЖ (перевязка панкреатического протока), которых лечили только ферментным препаратом или ферментным препаратом в сочетании с таурином. Было выявлено, что таурин позитивно влияет на абсорбцию жиров у экспериментальных животных.
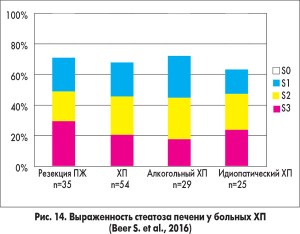
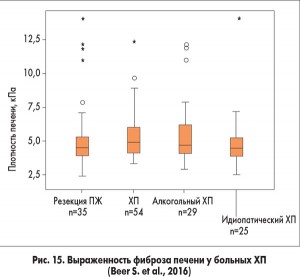
Несколько докладов были посвящены ХП, стеатозу ПЖ и их сочетанию со стеатозом печени. S. Beer и соавт. (Германия) обследовали 35 больных после резекции ПЖ по поводу ХП, 54 больных с ХП, не подвергавшихся хирургическому лечению. Стеатоз и фиброз печени оценивали с помощью фибротеста и фиброскана. Проводили фекальный эластазный тест. Результаты представлены на рисунках 14 и 15. Авторы сделали вывод о том, что у больных ХП высока частота стеатоза (особенно после резекции ПЖ) и фиброза печени, но эти изменения со стороны печени не ассоциировались со злоупотреблением алкоголем, степенью снижения внешне- и внутрисекреторной функции ПЖ. Во всех случаях фиброз печени ассоциировался с ее стеатозом.
P.O. Coe (Великобритания) использовал магнитно-резонансную томографию со спектроскопией для выявления жира в ПЖ. Исследовали ткань ПЖ 12 больных, перенесших резекцию железы, а также анализировали результаты томографии 15 добровольцев. Автору удалось разработать метод количественной неинвазивной оценки содержания жира в ПЖ. Это важно, поскольку эксперимент показал, что накопление жира в ПЖ предрасполагает к развитию аденокарциномы.
G. Zsori и соавт. (Венгрия) проводили лечение неалкогольной жировой болезни печени и ПЖ метформином. Были обследованы 14 больных. Степень накопления жира в печени и ПЖ оценивали по шкале Хаунсфильда (КТ). Назначали метформин в средних терапевтических дозах на 4 мес. Если степень накопления жира в печени за период лечения достоверно уменьшилась, то существенного снижения выраженности стеатоза ПЖ не произошло. Таким образом, ни данное, ни более ранние исследования не дали отчетливого результата в отношении лечения стеатоза ПЖ.
Профессор H. Friess выступил с лекцией о хирургическом лечении ХП.
Показания к оперативному лечению ХП:
– некупируемая боль;
– дуоденальный стеноз;
– стеноз холедоха;
– стеноз панкреатического протока;
– компрессия портальной вены;
– подозрение на рак ПЖ.
Основной вывод лекции: раннее хирургическое вмешательство (<3 лет от начала абдоминальной боли) приводит к значительно лучшим показателям.
Результаты интересного ретроспективного исследования «В выходные и праздничные дни в стационар поступают больные с более тяжелым ОП» представил S. Fernandes (Португалия). Действительно, при ретроспективном анализе историй болезни 524 больных оказалось, что в выходные и праздничные дни тяжелый ОП (по классификации Атланта) диагностировали в 68,9% случаев поступлений в стационар, а в будние дни – в 56% (p=0,02). Достоверной разницы в летальности не было.
S. Beer (Германия) изучал вопрос о связи рака ПЖ с повышенным поступлением кадмия в сигаретном дыме в организм пациентов. Исследованы 16 образцов ткани рака ПЖ и окружающая неопухолевая ткань (операционный материал). Кадмий в ткани определяли методом графитовой атомной абсорбции. В опухолевой ткани содержание кадмия составило 13,58±3,99 мкг/г, а в окружающей опухоль ткани – 5,60±1,36 мкг/г (p<0,05). Автор сформулировал гипотезу о том, что курение вызывает рак ПЖ вследствие высокой концентрации кадмия в сигаретном дыме.
В Ливерпуле были доложены результаты еще ряда интересных и перспективных исследований, но все их невозможно изложить в рамках статьи.
Участники встречи в Ливерпуле вернулись домой с новой информацией и позитивными впечатлениями.
Литература
1. 48th European Pancreatic Club (EPC) meeting // Pancreatology. – 2016. – Vol. 16, No 3S1. – P. S1-S130.
2. Cardiovascular risk (CVR) associated with pancreatic exocrine insufficiency (PEI) in patients with chronic pancreatitis (CP) / N. Vallejo-Senra, D. De la Inglesia-Garcia, A. Lopez-Lopez et al. / 48th European Pancreatic Club (EPC) meeting // Pancreatology. – 2016. – Vol. 16, No 3S1. – P. S80.
3. Chronic pancreatitis: novel concepts in biology and therapy / Ed. M.W. Buchler et al. – Berlin; Wien: Wissenschafts-Verlag; A Blackwell Publishing Company, 2002. – 614 р.
4. The different courses of early- and late-onset idiopathic and alcoholic chronic pancreatitis / P. Layer, H. Yamamoto, L. Kalthoff et al. // Gastroenterology. – 1994. – Vol. 107, No 5. – P. 1481-1487.
5. DiMagno E.P. Pancreatic cancer: a continuing diagnostic dilemma / E.P. DiMagno // Ann. Intern. Med. – 1979. – Vol. 90, No 5. – P. 847-848.
6. DiMagno E.P. Relations between pancreatic enzyme outputs and malabsorption in severe pancreatic insufficiency / E.P. DiMagno, V.L. Go, W.H. Summerskill // N. Engl. J. Med. –1973. – Vol. 288, No 16. – P. 813-815.
7. Effect of tramadol and morphine on pain and gastrointestinal motor function in patients with chronic pancreatitis / C.H. Wilder-Smith, L. Hill, W. Osler, S. O’Keefe // Dig. Dis. Sci. – 1999. – Vol. 44. – P. 1107-1116.
8. Etemad B. Chronic pancreatitis: diagnosis, classification, and new genetic developments / B. Etemad, D.C. Whitcomb // Gastroenterology. – 2001. – Vol. 120. – P. 682-707.
9. Fecal elastase‑1 is useful in the detection of steatorrhea in patients with pancreatic diseases but not after pancreatic resection / L. Benini, A. Amodio, P. Campagnola et al. // Pancreatology. – 2013. – Vol. 13, No 1. – P. 38-42.
10. Fioravanti B. The ORL‑1 receptor system: are there opportunities for antagonists in pain therapy? / B. Fioravanti, T.W. Vanderah // Curr. Top. Med. Chem. – 2008. – Vol. 8. – P. 1442-1451.
11. Groger G. Exocrine pancreatic function in diabetes mellitus / G. Groger, P. Layer // Eur. J. Gastroenterol. Hepatol. – 1995. – Vol. 7, No 8. – P. 740-746.
12. High prevalence of fatty liver disease in patients with chronic pancreatitis / S. Beer, T. Karlas, J. Wiegand et al. / 48th European Pancreatic Club (EPC) meeting // Pancreatology. – 2016. – Vol. 16, No 3S1. – P. S71-S72.
13. Inhibition of neuronal Ca(2+) influx by gabapentin and pregabalin in the human neocortex / K. Fink, D.J. Dooley, W.P. Meder et al. // Neuropharmacology. – 2002. – Vol. 42. – P. 229-236.
14. Insulin dependence and pancreatic enzyme replacement therapy are independent prognostic factors for long-term survival after operation for chronic pancreatitis / M. Winny, V. Paroglou, H. Bektas et al. // Surgery. – 2014. – Vol. 155, No 2. – P. 271-279.
15. Keller J. Human pancreatic exocrine response to nutrients in health and disease / J. Keller, P. Layer // Gut. – 2005. – Vol. 54, Suppl. 6. – P. 1-28.
16. Lieb J.G. Review article: pain and chronic pancreatitis / J.G. Lieb, P.E. Forsmark // Aliment. Pharmacol. Ther. – 2009. – Vol. 29, No 7. – P. 706-719.
17. Malnutrition is a common complication in chronic pancreatitis out-patients and significantly associates with impaired muscle function / L.K. Frandsen, S.S. Olesen, J.L. Poulsen et al. / 48th European Pancreatic Club (EPC) meeting // Pancreatology. – 2016. – Vol. 16, No 3S1. – P. S46.
18. Masclee Ad A.M. Pancreatic exocrine insufficiency after acute pancreatitis / A.M. Masclee Ad, T. Symersky // Asian Pacific digestive disease week 2005. Proceedings of a Solvay satellite symposium. – Seoul (Korea), 2005. – P. 9-12.
19. Mortality, cancer, and comorbidities associated with chronic pancreatitis: a Danish nationwide matched-cohort study / U.C. Bang, T. Benfield, L. Hyldstrup et al. // Gastroenterology. – 2014. – Vol. 146, No 4. – P. 989-994.
20. Obesity and fatty pancreatic infiltration are risk factors for pancreatic precancerous lesions (PanIN) / V. Rebours, S. Gaujoux, G. d’Assignies et al. // Clin. Cancer Res. – 2015. – Vol. 21, No 15. – P. 3522-3528.
21. Opioid-induced bowel dysfunction: pathophysiology and management / C. Brock, S.S. Olesen, A.E. Olesen et al. // Drugs. – 2012. – Vol. 72. – P. 1847-1865.
22. Pancreatic function after severe acute biliary pancreatitis: the role of necrosectomy / L. Sabater, E. Pareja, L. Aparisi et al. // Pancreas. – 2004. – Vol. 28, No 1. – P. 65-68.
23. Pathogenesis and treatment of pain in chronic pancreatitis / S.S. Olesen, E. Tieftrunk, G.O. Ceyhan, A.M. Drewes // http://www.pancreapedia.org /sites/www.pancreapedia.org/files /DOI%20Pathogenis%20and%20Treatment %20of%20Pain%20in%20CP.pdf
24. Pharmacological pain management in chronic pancreatitis / S.S. Olesen, J. Juel, C. Graversen et al. // World J. Gastroenterol. – 2013. – Vol. 19, No 42. – P. 7292-7301.
25. A randomized, controlled clinical trial of a novel microbial lipase (NM-BL) in patients with exocrine pancreatic insufficiency due to cystic fibrosis / J. Heubi, D. Schaeffer, R. Ahrens et al. / 48th European Pancreatic Club (EPC) meeting // Pancreatology. – 2016. – Vol. 16, No 3S1. – P. S108.
26. Vitamin D3 in patients with various grades of chronic pancreatitis, according to morphological and functional criteria of the pancreas / S.T. Mann, H. Stracke, U. Lange et al. // Dig. Dis. Sci. – 2003. – Vol. 48, No 3. – P. 533-538.