20 грудня, 2016
Ессенціальні фосфоліпіди при неалкогольній жировій хворобі печінки: оновлений огляд доказової бази
Неалкогольна жирова хвороба печінки (НАЖХП) і алкогольна хвороба печінки (АХП) є однією жировою хворобою печінки (ЖХП), яку спричиняють різні фактори (ожиріння, алкогольна залежність, цукровий діабет (ЦД) тощо) і яка лишається важливою проблемою охорони здоров’я. ЖХП прогресує від простого стеатозу до стеатогепатиту і потенційно цирозу з розвитком гепатоцелюлярної карциноми. Лікування НАЖХП передусім спрямоване на корекцію компонентів метаболічного синдрому. Усім пацієнтам рекомендуються дієта і фізичні навантаження. Деякі фармакологічні агенти продемонстрували обнадійливі результати, хоча дані останніх досліджень не дозволяють дійти чітких висновків. З АХП склалась аналогічна ситуація. Протягом багатьох років нетоксичні ессенціальні фосфоліпіди (ЕФЛ) широко і з успіхом застосовуються при різноманітних хворобах печінки. Проте останній клінічний огляд наявних результатів конкретно щодо ЖХП датується ще 1988 роком, тому метою цієї роботи було оцінити клінічні ефективність і безпеку ЕФЛ у пацієнтів із цими розповсюдженими хворобами.
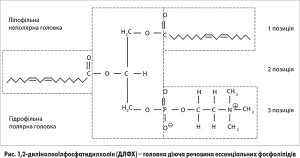
ЕФЛ містять полієнілфосфатидилхолін (також відомий як полієновий фосфатидилхолін) і являють собою високоочищений екстракт насіння соєвих бобів зі стандартизованим умістом 72-96% холіну. Молекулою, яка домінує кількісно і якісно в ЕФЛ, є 1,2-дилінолеоїлфосфатидилхолін (ДЛФХ) (рис.). Високий рівень ДЛФХ є головною відмінністю між ЕФЛ і типовими фосфоліпідами, які надходять з їжею або синтезуються в організмі. Завдяки призначенню ЕФЛ у печінці значно підвищується кількість ДЛФХ.
Фосфоліпіди формують подвійний шар на клітинних і внутрішньоклітинних мембранах, забезпечуючи їхню плинність і біологічну активність. Ефективність ЕФЛ у лікуванні хвороб печінки забезпечується не лише здатністю ДЛФХ вбудовуватись у пошкоджені ділянки мембран, що покращує регенерацію печінки і заміщує ендогенні, менш ненасичені молекули фосфатидилхоліну, а й покращенням функціонування мембран. В експериментах in vitro та in vivo було продемонстровано, що ЕФЛ впливають на мембранозалежні функції клітин і здійснюють антиоксидантні, протизапальні, антифібротичні, апоптозмодулюючі, регенеративні, мембранорепаративні, мембранозахисні, клітинно-сигнальні, рецептормодулюючі і ліпідорегулюючі ефекти.
Матеріали і методи
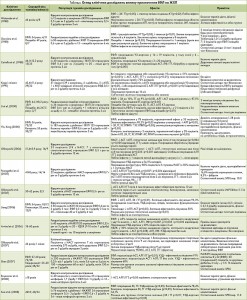
По базах даних Medline, Embase, Cochrane Library, в національних журналах і літературних посиланнях було проведено пошук відповідних гепатогастроентерологічних статей, опублікованих у 1988-2014 рр. На першому етапі пошук відбувався за комбінацією ключових слів «NADLF» (НАЖХП), «ALD» (АХП), «Essetiale», «EPLs» (ЕФЛ), «polyenylphosphatidylcholine», «polyene phosphatidylcholine», «dilinoleoylphosphatidylcholine», «phosphatidylcholine» і «therapy» (лікування). На другому етапі відбирали роботи, у яких було зазначено мінімальний уміст фосфатидилхоліну в екстракті соєвих бобів 72% (оскільки цей рівень є необхідним для лікування пацієнтів і забезпечує достатню кількість ДЛФХ як ключового компонента ЕФЛ) або вивчався оригінальний препарат ЕФЛ Essentiale®/Ессенціале®. Дослідження менш очищеного фосфатидилхоліну, отриманого із соєвих бобів або інших джерел, з аналізу виключали. Усі неангломовні статті перекладали англійською. Із 83 клінічних досліджень було відібрано 25 робіт, репрезентативних щодо ЖХП, дизайну і досліджуваних показників, у тому числі 1 аналіз клінічних випадків і 7 подвійних сліпих досліджень (табл.).
Результати
53 клінічні дослідження щодо ЕФЛ і НАЖХП було опубліковано після 1988 р., з яких 45 – після 2000 р. 23 дослідження (переважно рандомізовані) були відкритими контрольованими, 3 – подвійними сліпими. Дози і тривалість лікування становили 1,05-1,8 г/добу і від 4 тижнів до >12 міс відповідно; у більшості досліджень використовували дозу 1,8 г/добу впродовж 3-6 міс. В деяких дослідженнях лікування починали з парентерального введення 500-1000 мг ЕФЛ від 10 днів до 4 тижнів з подальшим переходом на пероральний прийом. В 1 дослідженні ЕФЛ призначали лише внутрішньовенно в дозі 500 мг/добу протягом 30 днів. Причинами НАЖХП і її більш тяжкої форми, а саме неалкогольного стеатогепатиту (НАСГ), переважно були ожиріння і ЦД 2 типу, проте НАЖХП/НАСГ також частково асоціювалися з гіперліпідемією, артеріальною гіпертензією, ішемічною хворобою серця / атеросклеротичним кардіосклерозом, хронічним вірусним гепатитом, холециститом / жовчнокам’яною хворобою, гіпотиреозом і вагітністю. Наявні дослідження дозволяли проаналізувати суб’єктивні симптоми, а також клінічні, біохімічні, візуалізаційні та гістологічні дані.
У першому клінічному дослідженні, проведеному в Японії, 6 пацієнтів із ЖХП, спричиненою ожирінням, були успішно проліковані низькокалорійною дієтою, фізичними навантаженнями і ЕФЛ 1,5 г/добу протягом 8 тижнів порівняно із 6 пацієнтами, що на додаток до дієти і фізичних навантажень отримували попередник нікотинової кислоти (Watanabe et al., 1988). За даними комп’ютерної томографії, у групі ЕФЛ відбулося значне зменшення акумуляції жиру в печінці (до лікування 27±18 HU; після лікування 54±8 HU, що свідчить про зниження інтенсивності стеатозу).
Cairella і співавт. (1989) з Італії вивчали ефективність ЕФЛ при лікуванні гепатобіліарної дисфункції, призначаючи препарат у дозі 1,8 г/добу протягом 3 міс. До кожної із груп (ЕФЛ і контрольна) увійшло 20 пацієнтів з індексом маси тіла (ІМТ) 35,34±4,89 кг/м2. Екскреторні параметри, загальний білірубін, лужна фосфатаза і гамма-глутамілтрансфераза (ГГТ) нормалізувались у всіх пацієнтів групи ЕФЛ, проте залишились підвищеними у 15-35% хворих контрольної групи. У групі ЕФЛ ультрасонографічна картина значно покращилась у 14 і нормалізувалась у 6 випадках, тоді як у контрольній групі лише незначно змінилась у 3 пацієнтів. Koga і співавт. (1991) спостерігали довготривалі ЕФЛ-індуковані покращення або нормалізацію ультрасонографічної картини у 39 пацієнтів із ЖХП, обумовленою ожирінням.
У 2000 р. у рандомізованому подвійному сліпому дослідженні було встановлено позитивний вплив ЕФЛ 1,8 г/добу на загальний холестерин (ЗХ), тригліцериди (ТГ) і трансамінази, що супроводжувався значним покращенням КТ-сканограм печінки (Li et al., 2000).
Досвід застосування ЕФЛ у пацієнтів з пізнім ЦД і ЖХП починається з рандомізованого плацебо-контрольованого подвійного сліпого дослідження (Gonciarz et al., 1988). 30 пацієнтів дотримувалися дієти зі зниженою калорійністю (1200 ккал/добу) і вмістом білка 1 г/кг. 5 хворих групи плацебо і 7 пацієнтів групи ЕФЛ отримували толбутамід 1,0-1,5 г/добу. Половина пацієнтів додатково отримували ЕФЛ 1,8 г/добу, решта – плацебо. Протягом 6-місячного періоду лікування розмір печінки майже не змінився в групі плацебо і значно зменшився в групі ЕФЛ. Гістологічне дослідження біоптатів печінки мало відповідний результат: значне покращення у 4 пацієнтів, які отримували ЕФЛ, і лише в 1 хворого групи плацебо (пізніше в нього все одно з’явились ознаки прогресування до цирозу). Через 1, 3 і 6 міс лікування рівень ГГТ значно знизився в групі ЕФЛ, при цьому в контрольній групі зміни були статистично несуттєвими. Трансамінази і білірубін упродовж дослідження залишались у нормальному діапазоні.
Після цього подвійного сліпого дослідження в 7 інших клінічних дослідженнях було підтверджено ефективність ЕФЛ при діабет-індукованій ЖХП. Yin і Kong (2000) лікували 185 пацієнтів стандартною дієтою, пероральними протидіабетичними засобами і фізичними навантаженнями; 125 пацієнтів додатково отримували ЕФЛ 1,8 г/добу протягом 3 міс. Аланінамінотрансфераза (АЛТ), ЗХ і тригліцериди сироватки, холестерин ліпопротеїнів низької (ХС ЛПНП) і високої щільності (ХС ЛПВП) значно покращились у 90,2% пацієнтів групи ЕФЛ і лише в 51% хворих контрольної групи, і ця різниця була статистично суттєвою (р<0,05). Рівні глюкози натще покращилися в обох групах.
У дослідженні Poongothai і співавт. (2005) 22 пацієнти, крім стандартної дієти, отримували протидіабетичні засоби залежно від тяжкості глікемії: 22,7% – метформін, 22,7% – похідні сульфонілсечовини, 45,5% – комбінацію цих препаратів і 9% – інсулін. Додатково всім пацієнтам призначили ЕФЛ 2,1 г/добу перорально протягом 6 міс. Ехотекстура печінки покращилась у 80% пацієнтів з початково тяжкими змінами паренхіми і в 50% осіб з помірними змінами, що супроводжувалося покращенням рівнів ГГТ і трансаміназ.
Ohbayashi і співавт. (2007) лікували пацієнтку з НАСГ натеглінідом (секретагог інсуліну) протягом 7 міс, а потім призначали ЕФЛ 1,5 г/добу; загальна тривалість терапії становила 2 роки. Після лікування було констатовано нормалізацію індексу інсулінорезистентності НОМА, гепаторенального ехоконтрасту, трансаміназ, ГТТ і феритину. Результати біопсії, яку оцінювали за критеріями Брунта, показали зниження стадії з 2 до 0 вже після 9 міс лікуваня ЕФЛ; зменшилися стеатоз, балонування, інтраацинарне запалення; повністю зникло запалення портального тракту.
Протягом останніх 8 років у 3 дослідженнях вивчали комбіноване лікування метформіном і ЕФЛ у пацієнтів із ЦД; автори спостерігали подібні позитивні ефекти щодо аспартатамінотрансферази (АСТ), ГГТ, ліпідів крові і ультрасонографічної картини (Buyeverov et al., 2008; Sun et al., 2008; Sas et al., 2013). Також в останньому дослідженні в групі ЕФЛ печінковий фіброгенез значно сповільнювався порівняно з контролем (р=0,02).
Ohbayashi (2004) і Ohbayashi і співавт. (2006) підтвердили, що в пацієнтів із НАСГ при довготривалому призначенні ЕФЛ спостерігається покращення функцій печінки навіть після завершення лікування. Протягом перших 4 тижнів було зафіксоване значне зниження рівнів трансаміназ, яке тривало впродовж наступних 12 міс терапії. Порівняння біоптатів печінки, отриманих до і після 6 міс лікування, показало значне зменшення стеатозу, балонування, запалення часточок і перипортальної зони.
Упродовж останніх років ЕФЛ порівнювали з іншими сполуками, потенційно ефективними щодо НАЖХП. У відкритих рандомізованих контрольованих дослідженнях порівнювали ЕФЛ з гіпенозидами Gynostemma pentaphyllum, екстрактом червоних рисових дріжджів і діамонію гліциризинатом (Liang, 2006; Fan et al., 2010; Guo et al., 2012; Shen, 2007).
Порівняно з гіпенозидами G. pentaphyllum ЕФЛ продемонстрували більш значне покращення клінічних симптомів, ЗХ і ТГ сироватки, ультразвукової картини і печінкової функції. Виражений ефект ЕФЛ спостерігався у 93,3% випадків (Liang, 2006). У дослідженні Guo і співавт. (2012) ЕФЛ порівняно з діамонію гліциризинатом ефективніше знижували рівні атерогенних ліпідів крові і тяжкість стеатозу печінки. Аналіз ультрасонограм щодо кількості пацієнтів зі значним покращенням показав достовірну перевагу ЕФЛ (Shen, 2007).
У рандомізованому подвійному сліпому контрольованому дослідженні порівняли ЕФЛ 1,05 г/добу та урсодезоксихолеву кислоту (УДХК) 7-10 мг/кг упродовж 3 міс (Arvind et al., 2006). Крім НАЖХП, учасники також страждали на ЦД або ожиріння (ІМТ >30 кг/м2). Пацієнти з кардіоваскулярними захворюваннями, іншими хворобами печінки, ускладненнями діабету (у т. ч. кетоацидозом), жінки в період вагітності або лактації і пацієнти з алкогольною залежністю в анамнезі з дослідження виключалися. Протягом скринінгового періоду пацієнти припиняли прийом усіх лікарських препаратів. Згідно з отриманими даними, ЕФЛ є значно ефективнішими за УДХК. У групі ЕФЛ 45% пацієнтів були задоволеними результатами терапії щодо значного зменшення симптомів (нудоти, загального нездужання, здуття живота) порівняно із 30% хворих грипи УДХК. Після 4 тижнів лікування суттєвих змін ультрасонографічної картини не спостерігалося, проте після 12 тижнів у 20% пацієнтів групи ЕФЛ і в 10% хворих групи УДХК було зафіксоване покращення. У групі ЕФЛ значно знизилися рівні АЛТ, АСТ і ЛФ, при цьому в групі УДХК суттєвого зниження зазнала лише АЛТ. За відповіддю на лікування пацієнти із ЦД та ожирінням статистично не відрізнялися.
Далі буде.
Підготував Олексій Терещенко