4 жовтня, 2016
Функціональна диспепсія у призмі Римських критеріїв ІV
Функціональні розлади шлунково-кишкового тракту (ШКТ) є однією з найбільш актуальних проблем сучасної гастроентерології. Як свідчить світова статистика, функціональна диспепсія (ФД) є четвертим за частотою діагнозом, який установлюють сімейні лікарі, терапевти за результатами первинного огляду пацієнтів.
У країнах Західної Європи частота синдрому диспепсії серед дорослого населення коливається від 25-28% до 43-52% (Данія, Швеція, Норвегія, Велика Британія). Результати популяційних досліджень указують на те, що симптоми диспепсії частіше визначаються у жінок (55-60%), ніж у чоловіків (40-45%). При цьому тільки в 33-40% випадків диспептичні прояви пов’язані з хронічними захворюваннями ШКТ («органічна диспепсія»), а в 60-67% виставляється діагноз ФД. Незважаючи на таку поширеність у популяції, не повністю розкриті етіопатогенетичні механізми ФД, до цього часу існують труднощі у верифікації діагнозу, що лежить в основі недостатньої ефективності проведеної терапії [1, 2, 4].
Сучасна концепція про синдром диспепсії та його варіанти особливо активно почала розроблятися протягом останніх 30 років. У 1988 р. в Римі під час Всесвітнього конгресу гастроентерологів з ініціативи його учасників був створений постійно діючий Робочий комітет (Working Team Committee) із вивчення функціональних захворювань ШКТ, який очолив професор D.A. Drossman (США), а в рамках цього комітету сформована Міжнародна робоча група з удосконалення діагностичних критеріїв функціональних розладів ШКТ (голова – професор N.J. Talley, Австралія). У Римських критеріях I (1988), II (1999) і III (2006) послідовно переглядалися й уточнювалися поняття ФД і її симптомів, а також діагностичні критерії та лікування на основі результатів сучасної доказової медицини [2].
У травні 2016 р. в Сан-Дієго проходив черговий Американський гастроентерологічний тиждень. Однією з головних подій цього великого наукового форуму стало представлення нових Римських критеріїв IV (2016) функціональних розладів ШКТ, які тепер рекомендовано називати розладами взаємодії між головним мозком і ШКТ (disorders of gut-brain interaction).
Відповідно до Римських критеріїв IV (2016) розрізняють два варіанти диспепсії [6, 7]:
– вторинну диспепсію (при виразковій хворобі, пухлинах шлунка тощо);
– функціональну диспепсію.
У Римських критеріях ІІІ виділяли також 2 види диспепсії: «органічну» та «функціональну».
Визначення ФД (Римські критерії IV): скарги, що входять у поняття ФД, мають тривати останні 3 міс при загальній тривалості 6 міс і «спричиняти занепокоєння» (bothersome) у пацієнта. Обов’язковою умовою постановки діагнозу ФД має бути відсутність органічних захворювань.
Симптоми, що входять у поняття ФД (Римські критерії IV):
– відчуття переповнення в надчеревній ділянці;
– раннє насичення;
– біль і відчуття печії в епігастрії.
Якщо в Римських критеріях IІІ «спричиняють занепокоєння» відносилося лише до «відчуття переповнення», то тепер, відповідно до нових критеріїв, відноситься до всіх симптомів ФД.
Основні клінічні варіанти ФД (Римські критерії IV):
– постпрандіальний дистрес-синдром (ПДС);
– синдром епігастрального болю (CЕБ).
Постпрандіальний дистрес-синдром характеризується наявністю таких скарг, як відчуття переповнення в надчеревній ділянці і раннє насичення, що відмічаються «більше 3 разів на тиждень» і завжди виникають після прийому їжі.
У Римських критеріях IІІ для постановки діагнозу ПДС симптоми мали з’являтися «декілька разів на тиждень».
Синдром епігастрального болю характеризується наявністю таких симптомів, як біль і відчуття печії в епігастрії, що спостерігаються «принаймні 1 раз на тиждень» і можуть виникати після прийому їжі, зникати після прийому їжі або відзначатися натщесерце.
У Римських критеріях IV підкреслено, що такі ознаки, як персистуюче блювання, зникнення клінічних симптомів після випорожнення кишечнику, біль у правому підребер’ї, не характерні для ФД.
Суттєвим слід вважати і доповнення про те, що у хворих на ФД часто спостерігаються такі симптоми, як печія, відрижка, нудота, відчуття здуття в епігастрії.
Раніше, відповідно до Римських критеріїв III, при виявленні, наприклад, у хворого з ПДС нудоти і відрижки потрібно було виставити такий діагноз: «Синдром функціональної диспепсії: постпрандіальний дистрес-синдром. Синдром неспецифічної надмірної відрижки. Синдром хронічної ідіопатичної нудоти».
Зараз, відповідно до нових Римських критеріїв ІV, лікар може розглядати нудоту і відрижку як «можливі додаткові ознаки» (possible adjunctive features) ФД.
У Римських критеріях ІV також указано на те, що різні варіанти ФД (ПДС і СЕБ) можуть поєднуватися між собою, а також із гастроезофагеальною рефлюксною хворобою (ГЕРХ) і синдромом подразненого кишечнику (СПК).
Патогенез ФД, як підкреслюється в нових Римських критеріях IV, є комплексним і включає низку патофізіологічних факторів. До них насамперед відносяться [5]:
1) порушення евакуаторної функції шлунка (сповільнене випорожнення у 25-35% хворих і прискорене менш ніж у 5% пацієнтів із ФД). Виражене сповільнення, що супроводжується блюванням і втратою апетиту, є характерним уже для гастропарезу;
2) розлади акомодації шлунка (здатність фундального відділу розслаблятися після прийому їжі) спостерігаються приблизно у 1/3 пацієнтів із ФД (частіше за постінфекційного перебігу ФД);
3) у хворих на ФД часто виявляється гіперчутливість шлунка і дванадцятипалої кишки (ДПК) до розтягнення, а також до соляної кислоти і ліпідів;
4) у Римських критеріях IV наводиться і низка нових патофізіологічних факторів, які були відсутні в попередніх критеріях:
а) перенесені інфекції. Постінфекційна ФД виникає у 10-20% хворих, які перенесли інфекцію ШКТ. Її розвиткові сприяють генетичні фактори й особливості самого інфекційного агента. При цьому підкреслюється, що на відміну від постінфекційного варіанту СПК постінфекційна ФД може мати короткотривалий перебіг;
б) запалення слизової оболонки ДПК низького ступеня активності;
в) підвищення проникності слизової оболонки ДПК;
г) збільшення вмісту еозинофілів у слизовій оболонці ДПК (дуоденальна еозинофілія).
У рамках Американського гастроентерологічного тижня велику увагу приділяли дуоденальній еозинофілії, назвавши її «новим захворюванням», з якою пов’язано 40% випадків ПДС, а також підвищення ризику подальшого приєднання ГЕРХ (N.J. Talley, Австралія). При цьому інгібітори протонної помпи (ІПП) мають здатність знижувати вміст еозинофілів у слизовій оболонці ДПК;
5) роль Helicobacter pylori в розвитку ФД оцінюється в нових Римських критеріях ІV дещо суперечливо.
З одного боку, у розділі, присвяченому патофізіології ФД, ця інфекція розглядається як можлива причина ФД, якщо успішна ерадикація веде до стійкого зникнення диспептичних скарг. З іншого боку, у розділі, де обговорюються принципи лікування ФД, вказується, що подібні випадки слід розглядати відповідно до положень Кіотського консенсусу [3], згідно з якими в разі стійкого зникнення диспептичних скарг після ерадикації такі хворі мають виключатися з групи ФД і розцінюватися як пацієнти, що страждають на диспепсію, асоційовану з H. pylori;
6) важлива роль у розвитку ФД відводиться психосоціальним факторам. До них відносяться депресія і підвищена тривожність, невротичні реакції, фізичний і емоційний вплив у дитячому віці, труднощі подолання стресових ситуацій у житті.
Діагностика
Як і в попередніх Римських критеріях, діагноз ФД виставляється на основі оцінки:
– скарг;
– анамнезу;
– відсутності «симптомів тривоги» або «червоних прапорців»: зменшення маси тіла, персистуюче блювання, гастроінтестинальна втрата крові, анемія, прогресуюча дисфагія, нічна діарея, нічний біль, незрозуміле підвищення температури тіла, вік старше 40 років, лімфаденопатія, утворення в животі, що пальпується. Симптоми тривоги мають низьку чутливість і не є ранніми ознаками серйозного захворювання: при їх появі, як правило, захворювання вже має прогресуючий характер;
– відсутності ятрогенних факторів (наприклад, прийом нестероїдних протизапальних препаратів – НПЗП);
– результатів тестування на H. pylori і проведення ерадикаційної терапії, особливо в країнах із високою частотою виявлення серед населення цієї інфекції (стратегія «test and treat»).
Після цього має бути розглянуто можливість проведення емпіричного лікування хворих.
Фіброезофагогастродуоденоскопію (ФЕГДС) рекомендовано проводити всім пацієнтам, у яких виявляються «симптоми тривоги».
Проте діагноз ФД вважається діагнозом виключення, який може бути поставлений тільки після ретельного обстеження хворого!
Лікування ФД
Лікування ФД включає передусім проведення загальних заходів, таких як освіта (education) і переконання (reassurance) хворих, нормалізація способу життя, дієтичні рекомендації (часте, дрібне харчування з обмеженням вмісту жирів), відмова від кави, куріння, алкоголю та прийому НПЗП. У нових Римських критеріях ІV відзначається доцільність цих заходів, але вказується на відсутність систематичних досліджень їх доказовості.
Проведення медикаментозної терапії визначається варіантом перебігу ФД. При СЕБ як препарати першої лінії пропонуються ІПП і Н2-блокатори, які, за результатами контрольованих досліджень, виявляються на 10-15% ефективнішими, ніж плацебо. При цьому підкреслюється, що застосування ІПП не є ефективним при ПДС, лікування якого рекомендується починати з призначення прокінетиків.
Можливості використання психотропних засобів, які часто призначаються при лікуванні ФД як препарати другої лінії, оцінюються в нових Римських критеріях ІV досить стримано. Незважаючи на їх більш високу ефективність порівняно з плацебо, відзначається, що більшість досліджень включали малу кількість пацієнтів і були не дуже високої якості. Нещодавно опубліковані результати великого багатоцентрового дослідження, у якому брали участь відомі фахівці з лікування ФД, показали, що амітриптилін у невеликих дозах дещо ефективніший при лікуванні СЕБ, ніж плацебо, тоді як інгібітор зворотного захоплення серотоніну есциталопрам не впливає на випорожнення шлунка і не дає ефекту ні при ПДС, ні при СЕБ.
Психотерапевтичні методи, що стосуються зазвичай хворих, резистентних до інших методів лікування, хоча і виявилися результативними в контрольованих дослідженнях, також не були доказовими через малу кількість досліджуваної групи.
Відзначається також, що виявлені у низки хворих на ФД запальні зміни слизової оболонки ДПК з підвищеним вмістом в ній еозинофілів визначають доцільність вивчення можливості використання у цієї категорії пацієнтів препарату монтелукаст (антагоніст cysLT-рецепторів, які стабілізують мембрани еозинофілів).
Отже, як і в попередніх рекомендаціях, призначення ІПП і прокінетиків є основою медикаментозної терапії хворих на ФД. У призмі перерахованих вище фактів призначення комплексного препарату Лімзер (представлений на ринку України компанією Мега Лайфсайенсіз) має бути ефективним засобом для одночасного нівелювання різноманітних проявів ФД. Одна капсула препарату містить 20 мг омепразолу в кишковорозчинних гранулах і 30 мг домперидону в особливій формі випуску – гранулах із пролонгованим вивільненням (SR-форма). За рахунок використання SR-форми забезпечується достатня терапевтична концентрація домперидону протягом тривалого періоду. Така інноваційна технологія виготовлення дозволяє ефективно використовувати Лімзер 1 раз на добу (за 10-15 хв до прийому їжі).
Мета дослідження: вивчити клінічну ефективність препарату Лімзер у лікуванні хворих на функціональну диспепсію.
Матеріали і методи
На базі кафедри пропедевтики внутрішніх хвороб медичного факультету ДВНЗ «УжНУ» (Закарпатська обласна клінічна лікарня ім. А. Новака) обстежено та проліковано 24 хворих на ФД.
Усі дослідження були виконані за згодою пацієнтів, а методика їх проведення відповідала Гельсінській декларації 1975 р. та її редакції 1983 р. Серед обстежених хворих жінок було 18 (75%), чоловіків – 6 (25%). Середній вік становив 34,5±3,7 року.
Діагноз ФД встановлювався на підставі аналізу симптомів, анамнезу захворювання, результатів фізикального обстеження хворих, а також даних лабораторно-інструментальних обстежень (загальний аналіз крові та сечі, біохімічний аналіз крові, ультразвукове обстеження органів черевної порожнини, ФЕГДС). Отже, діагноз ФД виставили після виключення органічних захворювань, за яких виникають симптоми диспепсії (виключення «вторинної диспепсії»), а також негативних тестів на визначення Н. pylori.
При постановці діагнозу ФД ураховували характер симптомів, частоту їх виникнення, тривалість, а також зв’язок із прийомом їжі.
Усім пацієнтам із ФД на фоні модифікації способу життя (відмова від шкідливих звичок, дієтичні рекомендації) проводилося медикаментозне лікування препаратом Лімзер (Мега Лайфсайенсіз) по 1 капсулі 1 раз на добу зранку за 15 хв до прийому їжі протягом 14 днів. Динаміку клінічної симптоматики оцінювали після проведеного лікування (через 14 днів).
Результати та їх обговорення
При опитуванні обстежених хворих встановили, що клінічна картина, окрім скарг гастроентерологічного характеру, включала і загальні неврастенічні прояви, а саме: порушення сну, дратівливість, поганий настрій, періодичний головний біль.
Для виявлення диспептичних скарг проводили ретельне опитування обстежених хворих. При цьому пацієнти відзначали відчуття раннього насичення, необґрунтоване відчуття переїдання, важкості, переповнення в надчеревній ділянці, здуття в епігастрії, відчуття дискомфорту після їжі, нудоту, зниження апетиту.
Інтенсивність, частота і час появи симптомів диспепсії були різноманітні. Скарги могли виникати натщесерце, після прийому їжі, або навпаки – зменшувалися після прийому їжі. При цьому значна частина хворих настільки звикли до свого стану, що часто не звертали на це увагу. Певні труднощі виникли і при спробі встановити точні терміни початку захворювання, оскільки найчастіше хворі не могли точно пригадати час появи багатьох диспептичних розладів, частоту їх виникнення (навіть інтенсивних симптомів). Часто це було пов’язано з тим, що хворі для «полегшення» свого стану самостійно вживали цілу низку препаратів (антациди, ферменти, Н2-гістаміноблокатори), які приймалися спорадично і стихійно, без консультації лікаря.
Поряд з цим після ретельного аналізу результатів опитування встановили, що вище перераховані скарги виникали принаймні один раз на тиждень, а деякі – більше трьох разів на тиждень, що реєструвалися останні 3 міс при загальній тривалості 6 міс.
Отже, на основі проведених діагностичних заходів і після виключення органічних патологій ШКТ встановлено діагноз ФД у всіх 24 обстежених хворих. При цьому в більшості хворих це поєднаний варіант ФД, а саме проявів ПДС і СЕБ.
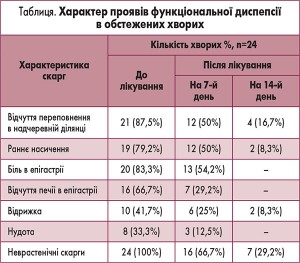
Розподіл скарг в обстежених хворих відповідно до Римських критеріїв IV до та після лікування подано в таблиці.
Проведена медикаментозна терапія з використанням комплексного препарату Лімзер виявилася ефективною в обстежених хворих на ФД. Уже наприкінці першого тижня лікування в них на 37,5% зменшилося відчуття переповнення в надчеревній ділянці, на 29,2% – раннє насичення та біль в епігастрії, на 20,8% – нудота, на 16,7% – печія в епігастрії.
Після проведеного курсу терапії у хворих на ФД зникли такі симптоми, як біль в епігастрії, відчуття печії в епігастрії та нудота. Слід підкреслити, що без призначення специфічного лікування наприкінці 2-го тижня спостереження скарги неврастенічного характеру мали лише 29,2% обстежених пацієнтів із ФД. Отже, зникнення/зменшення проявів ФД приводить до зменшення скарг неврастенічного характеру і, відповідно, поліпшення якості життя цих пацієнтів.
Таким чином, комплексний механізм дії препарату Лімзер дає змогу безпосередньо впливати на симптоми ФД. Домперидон підвищує тонус нижнього стравохідного сфінктера (при цьому усувається такий симптом, як відрижка), нормалізує перистальтику шлунка, прискорює евакуацію шлункового вмісту до ДПК (знімає відчуття болю, важкості, переповнення, нудоти). Омепразол знижує секрецію соляної кислоти, що приводить до усунення печії та відрижки кислим.
Домперидон майже не проникає через гематоенцефалічний бар’єр і не викликає побічних явищ з боку центральної нервової системи. Такі побічні ефекти, як головний біль і загальна слабкість, виникають рідко, а екстрапірамідні порушення й ендокринні ефекти – лише в поодиноких випадках, що дозволяє застосовувати його досить довго. Домперидон блокує периферичні дофамінові рецептори, усуває інгібуючий вплив дофаміну на моторну функцію травного тракту і підвищує евакуаторну та рухову активність шлунка. Не зважаючи на селективність, також має невеликий терапевтичний ефект при порушеннях моторики тонкого і товстого кишечнику.
Омепразол належить до противиразкових засобів, які пригнічують базальну та стимульовану секрецію соляної кислоти в парієтальних клітинах шлунка внаслідок специфічної дії на H+-K+-АТФ-азу (протонна помпа). Антисекреторний ефект після прийому омепразолу розвивається дуже швидко (протягом першої години) та зберігається протягом доби. Омепразол завдяки своїй високій ліпофільності легко проникає в парієтальні клітини шлунка, концентрується в них і чинить цитопротекторну дію.
Таким чином, завдяки комплексній дії препарату Лімзер ефективно усуваються такі симптоми диспепсії, як відчуття болю та печії в епігастрії, переповнення, важкості, раннього насичення в надчеревній ділянці, нудоти та відрижки, що найбільшою мірою погіршують якість життя пацієнтів із ФД. Отже, комбінований препарат Лімзер – поєднання домперидону в особливій формі випуску (гранули з пролонгованим вивільненням – SR-форма) та омепразолу – є ефективним засобом для лікування ФД змішаного характеру, а саме як проявів постпрандіального дистрес-синдрому, так і синдрому епігастрального болю.
Висновки
1. Лімзер є ефективним і безпечним засобом для лікування хворих із функціональною диспепсією.
2. Лімзер може використовуватися для лікування поєднаного варіанту функціональної диспепсії, а саме постпрандіального дистрес-синдрому та синдрому епігастрального болю.
Література
1. Бельмер С.В. Современное понимание функциональной диспепсии / С.В. Бельмер // Лечащий врач. – М., 2011. – № 6. – С. 22-28.
2. Ивашкин В.Т. Функциональная диспепсия: краткое практическое руководство / В.Т. Ивашкин, А.А. Шептулин, В.А. Киприанис. – М.: МЕДпресс-информ, 2011. – 112 с.
3. Киотский глобальный консенсус по Helicobacter pylori-ассоциированному гастриту / K. Sugano, J. Tack, E.J. Kuipers [et al.] // РМЖ. – 2015. – № 28. – С. 1673-1681.
4. Палій І.Г. Функціональна диспепсія: сучасні уявлення про механізми виникнення й тактику ведення пацієнтів / І.Г. Палій // Практикуючий лікар. – 2013. – № 3. – С. 25-30.
5. Age, gender and women’s health and patient / L.A. Houghton, M. Heitkemper, M.D. Crowell [et al.] // Gastroenterology. – 2016. – № 150 (6). – Р. 1332-1343.
6. Drossman D.A. Rome IV – Functional GI disorders: disorders of gut-brain interaction / D.A. Drossman, W.L. Hasler // Gastroenterology. – 2016. – № 150 (6). – Р. 1257-1261.
7. Gastroduodenal disorders / V. Stanghellini, F.C.L. Chan, W.L. Hasler [et al.] // Gastroenterology. – 2016. – 150 (6). – Р. 1380-1392.