4 жовтня, 2016
Харчові фактори ризику раку підшлункової залози
Серед причин летальності, зумовленої онкологічною патологією, рак підшлункової залози (РПЗ) посідає 4-те місце [29]. Прогноз за даної патології несприятливий: показник 1-річної виживаності становить 25%, а 5-річної – менше 5% [12]. Хірургічне втручання залишається єдиним способом лікування, але, на жаль, на момент встановлення діагнозу більш ніж у 80% пацієнтів виявляють віддалені метастази [6]. Оскільки не існує жодного ефективного способу скринінгу на РПЗ, кращим заходом щодо зниження захворюваності і смертності від РПЗ є ефективна первинна профілактика, а саме – корекція модифікованих факторів, зокрема харчування.
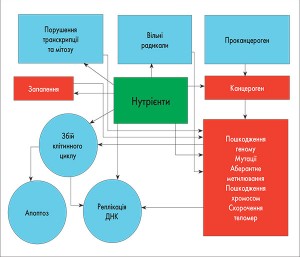
Можливі механізми впливу нутрієнтів, що підвищують ризик виникнення раку, наведено на рисунку.
Фрукти та овочі
Результати великих популяційних досліджень дають підстави вважати, що споживання фруктів і овочів зворотньо-пропорційно ризику розвитку РПЗ [4]. Це було підтверджено й дослідженнями «випадок – контроль» [8], які виявили користь від вживання в їжу цитрусових, дині, ягід, темно-зелених овочів, томатів, квасолі, гороху, жовтих овочів, харчових волокон та продуктів з цільного зерна. Вплив фруктів, особливо цитрусових, обумовлений вмістом у них флавоноїдів, таких як гесперідін, рутин і діосмін, які своєю чергою мають протипухлинні, антипроліферативні та проапоптотичні властивості [2]. Крім того, цитрусові також містять каротиноїди, такі як бета-каротин і лютеїн: сполуки, що потенційно також можуть знижувати ризик розвитку раку [14]. Цитрусові лимоноїди, такі як лимонин і номілін, мають антиоксидантні та протипухлинні властивості [26].
Таким чином, збагачення раціону за рахунок цитрусових може знизити ризик розвитку РПЗ.
Цільнозернові продукти
Метааналіз чотирьох досліджень підтвердив наявність зворотного зв’язку між кількістю продуктів з цільного зерна в раціоні й ризиком розвитку РПЗ [11]. У деяких країнах спостерігалася додаткова користь від включення в раціон продуктів з цільного зерна, збагачених фолієвою кислотою. Можливо, протипухлинні властивості вівса зумовлені вмістом у ньому ксантохумолу, що було підтверджено результатами експериментальних досліджень.
Таким чином, включення до раціону продуктів з цільного зерна зменшує ризик розвитку РПЗ, а збагачення цих продуктів фолієвою кислотою може забезпечувати додатковий превентивний вплив.
М’ясо
Відомо, що споживання червоного м’яса позитивно пов’язано з ризиком розвитку РПЗ у чоловіків [22]. Це можна було б пояснити тим, що чоловіки споживають більше смаженого, приготовленого на грилі або барбекю м’яса, ніж жінки [21], або цей взаємозв’язок може бути вторинним відносно того, що в чоловіків спостерігаються більш високі концентрації заліза, ніж у жінок [30]. Проте автори проекту EPIC виявили й позитивний асоціативний зв’язок між споживанням червоного м’яса та ризиком розвитку РПЗ у жінок. Підвищений ризик був пов’язаний зі споживанням баранини, телятини та м’яса диких тварин [8].
У ході недавнього метааналізу було встановлено, що вживання кожних 50 г обробленого м’яса щоденно пов’язано зі збільшенням ризику РПЗ на 19% [30].
Таким чином, з метою зменшення ризику РПЗ слід обмежувати включення до раціону обробленого червоного м’яса та м’яса, приготованого при дуже високих температурах, тобто у фритюрі, при обсмажуванні або на барбекю.
Риба
Можливим фактором зниження ризику розвитку РПЗ є надходження до організму омега‑3 поліненасичених жирних кислот з довгим ланцюгом (w‑3 ПНЖК), основним джерелом яких є риба. Вони здатні запобігати розвитку злоякісних новоутворень підшлункової залози через свої протизапальні властивості з огляду на той факт, що хронічне запалення може відігравати певну роль у її канцерогенезі. У ході недавнього метааналізу, який включав 9 проспективних когортних досліджень і 10 досліджень «випадок – контроль», установити зворотний зв’язок між споживанням риби або w‑3 ПНЖК та ризиком виникнення РПЗ не вдалося [27], і такий результат відповідав іншим опублікованим дослідженням [13].
Спосіб приготування риби може впливати на ризик розвитку РПЗ, оскільки внаслідок її обробки може змінюватися ліпідний профіль або створюються нові хімічні речовини. У рибі, приготовленій у фритюрі, зменшується кількість w‑3 ПНЖК і створюється кілька хімічних речовин, які можуть сприяти канцерогенезу і збільшують ризик розвитку РПЗ. За даними метааналізу, зворотний кореляційний зв’язок спостерігався лише для несмаженої риби [27]. Результати проспективного когортного дослідження визначили можливу користь від збагачення раціону w‑3 ПНЖК як первинної профілактики РПЗ [20]. Крім того, було встановлено зв’язок між більш високим споживанням несмаженої риби чи молюсків і низькою частотою розвитку РПЗ [20]. Однак є певні застереження щодо збагачення раціону молюсками, оскільки вони потенційно можуть містити хімічні речовини, які є канцерогенними [3]. А результати одного дослідження «випадок – контроль» визначили слабкий позитивний зв’язок між споживанням молюсків і захворюваністю на РПЗ [8], що було підтверджено й іншими дослідженнями [20].
Таким чином, споживання несмаженої риби може сприяти зниженню ризику розвитку РПЗ.
Жир
Надходження жиру у дванадцятипалу кишку сприяє вивільненню холецистокініну, який індукує секрецію панкреатичних ферментів, що при тривалому перебігу може призвести до ацинарної гіпертрофії та гіперплазії підшлункової залози і, отже, непластичних процесів. Інші механізми, які можуть спричинити розвиток РПЗ, включають у себе секрецію жовчних кислот і розвиток інсулінорезистентності.
У більшості досліджень «випадок – контроль» визначено позитивний асоціативний зв’язок споживання насичених [9], мононенасичених [3] жирних кислот і ПНЖК [17] з РПЗ. Кілька когортних досліджень показали позитивний зв’язок між ризиком РПЗ і загальною кількістю споживання жирів [25], насичених жирних кислот, таких як масло й вершки [31], і мононенасичених жирних кислот [32]. Проте інші проспективні дослідження, у тому числі Nurses’ Health cohort Study (NHS) [23], наявність такого зв’язку не підтвердили.
Таким чином, споживання жирів, а також насичених і ненасичених жирних кислот може бути пов’язано з ризиком розвитку РПЗ.
Рафінований цукор
Вважається, що споживання підсолоджених безалкогольних напоїв підвищує ризик розвитку РПЗ [24], проте в інших дослідженнях були отримані протилежні результати [7], за якими цей взаємозв’язок простежується лише серед жінок [28]. Об’єднаний аналіз 14 когортних досліджень визначив наявність слабкого позитивного асоціативного зв’язку між ризиком розвитку РПЗ та споживанням газованих солодких безалкогольних напоїв [19].
Таким чином, прямий зв’язок між споживанням цукру-рафінаду й РПЗ відсутній, проте синдроми гіперінсулінемії, ожиріння, метаболічний синдром і цукровий діабет позитивно пов’язані з ризиком розвитку РПЗ.
Алкоголь
Встановлено, що алкоголь може бути незалежним чинником ризику розвитку РПЗ, але деякі дослідження свідчать, що це стосується лише надмірного його споживання [33]. Проте дослідження когорти EPIC не виявило зв’язку між споживанням алкоголю й ризиком розвитку РПЗ [15]. Більшість досліджень основну тригерну роль відводять курінню.
Таким чином, вживання алкоголю пов’язане з невеликою часткою всіх видів раку підшлункової залози (як правило, у людей, які споживають значну кількість етанолу), та обумовлює розвиток у цієї групи алкогольного панкреатиту. Куріння є сильним додатковим фактором, що впливає на ризик розвитку РПЗ.
Кава
Автори дослідження, проведеного на початку 1980-х, керуючись припущенням про існування зв’язку між споживанням кави й ризиком розвитку РПЗ, виявили зворотний зв’язок між споживанням кави (як натуральної, так і кави без кофеїну [1]) і ризиком розвитку РПЗ [5].
Таким чином, можна зробити висновок, що вживання кави в будь-якій кількості не підвищує ризик розвитку РПЗ.
Зелений чай
Зелений чай багатий на флавоноїди, такі як катехін і епікатехін, що мають антипроліферативні властивості й індукують апоптоз у ракових клітинах ПЗ. Аналіз 14 когортних досліджень не визначив зв’язку між споживанням чаю й ризиком розвитку РПЗ [19], а також типами чаю (зеленого порівняно з чорним). Отримані дані були підтверджені результатами дослідження EPIC, які також не виявили зв’язку між споживанням чаю й ризиком розвитку РПЗ [1]. Загальне споживання чаю є безпечним у помірних кількостях. Результати сучасних досліджень не виявили будь-якої захисної ролі чаю щодо РПЗ. Проте протилежні результати були отримані в іншому дослідженні, проведеному в Китаї, яке продемонструвало, що регулярне вживання зеленого чаю пов’язано зі зниженням ризику розвитку РПЗ на 32%. Збільшення споживання й тривале чаювання знижують ризик розвитку РПЗ у жінок, низька температура чаю асоційована зі зниженням ризику розвитку РПЗ у чоловіків і жінок, незалежно від кількості та тривалості чаювання [16].
Куркумін
Цей поліфенол є представником куркуміноїдів, що містяться у спеції куркумі, і має антиоксидантні, протизапальні та протипухлинні властивості. Клінічні випробування показали відсутність токсичності куркуміну за умови його споживання в дозі до 10 г/добу. Біодоступність куркуміну, що міститься в харчових продуктах, збільшується, якщо ці продукти проварити або споживати з олією. У ході недавнього дослідження вивчався комбінаторний ефект гарцинолу та куркуміну на клітини РПЗ людини й було виявлено синергічний ефект.
За наявними даними, слід підвищувати споживання куркуміну, проте необхідні подальші дослідження для з’ясування механізмів, що лежать в основі впливу куркуміну на рак підшлункової залози.
Таким чином, куркумін виявив протипухлинні властивості і його використання може знижувати ризик розвитку РПЗ.
Мікроелементи
Антиоксиданти можуть мати проективні властивості щодо процесів канцерогенезу, оскільки відомо, що вони сприяють зменшенню окисного пошкодження ДНК й генетичних мутацій. Результати дослідження VITAL не виявили зв’язку між деякими відомими антиоксидантними агентами (β-каротин, лютеїн у комплексі із зеаксантином, лікопін, вітамін С, вітамін Е та цинк) з ризиком розвитку РПЗ, проте був підтверджений зворотний зв’язок із селеном [10]. Можливо, це зумовлено важливими властивостями селену, який є основою ферментної антиоксидантної системи організму, має імуномодулювальні властивості, стимулює механізми синтезу й транскрипції ДНК, має протизапальну дію, впливає на метаболізм пухлинних клітин (пригнічення) та стимулює апоптоз ракових клітин. В експериментальних роботах було продемонстровано, що дефіцит селену асоційований з уповільненням проліферації тканини підшлункової залози, інфільтрацією ацинарної тканини макрофагами й фібробластами, формуванням атрофічних змін, зменшенням кількості функціонально активних мітохондрій в ацинарних клітинах.
Результати дослідження EPIC також свідчать про те, що високе споживання селену обумовлювало зниження ризику розвитку РПЗ [18], і ці висновки були підтверджені ще двома дослідженнями, які описали зворотний зв’язок між концентраціями селену й ризиком розвитку РПЗ.
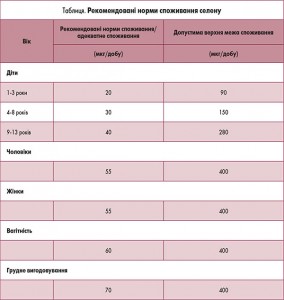
Таким чином, адекватна кількість селену в раціоні (табл.) може сприяти зниженню ризику розвитку РПЗ.
У разі ж якщо через низку причин не вдається ввести адекватну кількість селену в раціон за рахунок продуктів харчування, до терапії слід додавати препарати, що містять даний мікроелемент. Наразі на фармацевтичному ринку України представлений єдиний лікарський препарат Цефасель, що містить селен у вигляді неорганічної солі – селеніту натрію. Біодоступність селеніту натрію становить 60-70% і є набагато вищою, ніж органічних сполук селену, що дозволяє, приймаючи одну таблетку на добу, отримувати добову норму селену.
Таким чином, завершуючи цей огляд, можна зробити висновок, що корекція модифікованих факторів ризику РПЗ є одним з найбільш обнадійливих методів первинної профілактики процесів канцерогенезу та розвитку патологічних змін. Важливим є включення до раціону адекватних кількостей як макро-, так і мікроелементів, зокрема селену. Перспективи подальших досліджень повинні включати визначення механізмів впливу мікроелементів і продуктів харчування на процеси канцерогенезу в тканинах підшлункової залози та проведення контрольованих досліджень щодо впливу окремих продуктів на ризик розвитку онкологічної патології підшлункової залози.
Література
1. Bhoo-Pathy N., Uiterwaal C.S., Dik V.K. et al. Intake of coffee, decaffeinated coffee, or tea does not affect risk for pancreatic cancer: results from the European Prospective Investigation into Nutrition and Cancer Study // Clin Gastroenterol Hepatol. – 2013. – 11. – С: 1486-1492.
2. Buer C.S., Imin N., Djordjevic M.A. Flavonoids: new roles for old molecules // J Integr Plant Biol. – 2010. – 52. – С: 98-111.
3. Chan J.M., Wang F., Holly E.A. Pancreatic cancer, animal protein and dietary fat in a population-based study, San Francisco Bay Area, California // Cancer Causes Control. – 2007. – 18. – С: 1153-1167.
4. Chan J.M., Wang F., Holly E.A. Vegetable and fruit intake and pancreatic cancer in a population-based case-control study in the San Francisco bay area // Cancer Epidemiol Biomarkers Prev. – 2005. – 14. – С: 2093-2097.
5. Dong J., Zou J., Yu X.F. Coffee drinking and pancreatic cancer risk: a meta-analysis of cohort studies // World J Gastroenterol. – 2011. – 17. – С: 1204-1210.
6. Freitas D., Fernandes Gdos S., Hoff P.M. et al. Medical management of pancreatic adenocarcinoma // Pancreatology. – 2009. – 9. – С: 223-232.
7. Gallus S., Turati F., Tavani A. et al. Soft drinks, sweetened beverages and risk of pancreatic cancer // Cancer Causes Control. – 2011. – 22. – С: 33-39.
8. Ghadirian P., Nkondjock A. Consumption of food groups and the risk of pancreatic cancer: a case-control study // J Gastrointest Cancer. – 2010. – 41. – С: 121-129.
9. Gong Z., Holly E.A., Wang F. et al. Intake of fatty acids and antioxidants and pancreatic cancer in a large population-based case-control study in the San Francisco Bay Area // Int J Cancer. – 2010. – 127. – С: 1893-1904.
10. Han X., Li J., Brasky T.M. et al. Antioxidant intake and pancreatic cancer risk: the Vitamins and Lifestyle (VITAL) Study // Cancer. – 2013. – 119. – С: 1314-1320.
11. Jansen R.J., Robinson D.P., Stolzenberg-Solomon R.Z. et al. Fruit and vegetable consumption is inversely associated with having pancreatic cancer // Cancer Causes Control. – 2011. – 22. – С: 1613-1625.
12. Klapman J., Malafa M.P. Early detection of pancreatic cancer: why, who, and how to screen // Cancer Control. – 2008. – 15. – С: 280-287.
13. Larsson S.C., Hakanson N., Permert J. et al. Meat, fish, poultry and egg consumption in relation to risk of pancreatic cancer: a prospective study // Int J Cancer. – 2006. – 118. – С: 2866-2870.
14. Marti N., Mena P., Canovas J.A. et al. Vitamin C and the role of citrus juices as functional food // Nat Prod Commun. – 2009. – 4. – С: 677-700.
15. Rohrmann S., Linseisen J., Vrieling A. et al. Ethanol intake and the risk of pancreatic cancer in the European Prospective Investigation into Cancer and Nutrition (EPIC) // Cancer Causes Control. – 2009. – 20. – С: 785-794.
16. Wang J., Zhang W., Sun L. et al. Green tea drinking and risk of pancreatic cancer: a large-scale, population-based case-control study in urban Shanghai // Cancer Epidemiol. – 2012. – 36. – С: e354-358.
17. Zhang J., Dhakal I.B., Gross M.D. et al. Physical activity, diet, and pancreatic cancer: a population-based, case-control study in Minnesota // Nutr Cancer. – 2009. – 61. – С: 457-465.
18. Banim P.J., Luben R., McTaggart A. et al. Dietary antioxidants and the aetiology of pancreatic cancer: a cohort study using data from food diaries and biomarkers // Gut. – 2013. – 62. – С: 1489-1496.
19. Genkinger J.M., Li R., Spiegelman D. et al. Coffee, Tea, and Sugar-Sweetened Carbonated Soft Drink Intake and Pancreatic Cancer Risk: A Pooled Analysis of 14 Cohort Studies // Cancer Epidemiology Biomarkers & Prevention. – 2012. – 21. – С: 305-318.
20. He K., Xun P., Brasky T.M. et al. Types of Fish Consumed and Fish Preparation Methods in Relation to Pancreatic Cancer Incidence: The VITAL Cohort Study // American Journal of Epidemiology. – 2013. – 177. – С: 152-160.
21. Inoue-Choi M., Flood A., Robien K. et al. Nutrients, Food Groups, Dietary Patterns, and Risk of Pancreatic Cancer in Postmenopausal Women // Cancer Epidemiology Biomarkers & Prevention. – 2011. – 20. – С: 711-714.
22. Larsson S., Wolk A. Red and processed meat consumption and risk of pancreatic cancer: meta-analysis of prospective studies // British journal of cancer. – 2012. – 106. – С: 603-607.
23. Michaud D.S., Giovannucci E., Willett W.C. et al. Dietary Meat, Dairy Products, Fat, and Cholesterol and Pancreatic Cancer Risk in a Prospective Study // American Journal of Epidemiology. – 2003. – 157. – С: 1115-1125.
24. Mueller N.T., Odegaard A., Anderson K. et al. Soft Drink and Juice Consumption and Risk of Pancreatic Cancer: The Singapore Chinese Health Study // Cancer Epidemiology Biomarkers & Prevention. – 2010. – 19. – С: 447-455.
25. No..thlings U., Wilkens L.R., Murphy S.P. et al. Meat and Fat Intake as Risk Factors for Pancreatic Cancer: The Multiethnic Cohort Study // Journal of the National Cancer Institute. – 2005. – 97. – С: 1458-1465.
26. Patil J.R., Jayaprakasha G., Murthy K.C. et al. Characterization of Citrus aurantifolia bioactive compounds and their inhibition of human pancreatic cancer cells through apoptosis // Microchemical Journal. – 2010. – 94. – С: 108-117.
27. Qin B., Xun P., He K. Fish or Long-Chain (n‑3) PUFA Intake Is Not Associated with Pancreatic Cancer Risk in a Meta-Analysis and Systematic Review // The Journal of Nutrition. – 2012. – 142. – С: 1067-1073.
28. Schernhammer E.S., Hu F.B., Giovannucci E. et al. Sugar-Sweetened Soft Drink Consumption and Risk of Pancreatic Cancer in Two Prospective Cohorts // Cancer Epidemiology Biomarkers & Prevention. – 2005. – 14. – С: 2098-2105.
29. Siegel R., Naishadham D., Jemal A. Cancer statistics, 2012 // CA: A Cancer Journal for Clinicians. – 2012. – 62. – С: 10-29.
30. Stolzenberg-Solomon R.Z., Cross A.J., Silverman D.T. et al. Meat and Meat-Mutagen Intake and Pancreatic Cancer Risk in the NIH-AARP Cohort // Cancer Epidemiology Biomarkers & Prevention. – 2007. – 16. – С: 2664-2675.
31. Stolzenberg-Solomon R.Z., Pietinen P., Taylor P.R. et al. Prospective Study of Diet and Pancreatic Cancer in Male Smokers // American Journal of Epidemiology. – 2002. – 155. – С: 783-792.
32. Thi ebaut A.C.M., Jiao L., Silverman D.T. et al. Dietary Fatty Acids and Pancreatic Cancer in the NIH-AARP Diet and Health Study // Journal of the National Cancer Institute. – 2009. – 101. – С: 1001-1011.
33. Tramacere I., Scotti L., Jenab M. et al. Alcohol drinking and pancreatic cancer risk: a meta-analysis of the dose-risk relation // International journal of cancer. – 2010. – 126. – С: 1474-1486.