30 червня, 2016
Лечение микроскопического колита: обзор клинических рекомендаций

Микроскопический колит характеризуется хронической водянистой диареей неинфекционного генеза. Заболевание диагностируется на основании выявления воспаления в ткани толстой кишки при гистологическом исследовании. Микроскопический колит имеет два основных подтипа – лимфоцитарный и коллагеновый, у которых много общего. В частности, практически одинаковые клинические симптомы: водянистая диарея, отсутствие макроскопических изменений на слизистой оболочке толстой кишки. При обеих формах заболевания гистологическое исследование выявляет интраэпителиальный лимфоцитоз, увеличение воспалительных клеток в собственной пластинке слизистой оболочки, сохранение архитектоники крипт, при коллагеновом колите наблюдается утолщение подэпителиального коллагенового слоя [13].
Первые описания случаев микроскопического колита опубликованы в медицинской печати в начале 80-х годов прошлого столетия [11, 12]. В начале изучения анализу подвергались единичные спорадические случаи данного заболевания. За последние 30 лет диагностика микроскопического колита существенно улучшилась, заболевание интенсивно изучается и интерес к нему только растет.
До недавнего времени микроскопический колит считался редким заболеванием, было мало известно о его распространенности, этиологии, патогенезе. Благодаря широкому внедрению в медицинскую практику эндоскопической диагностики и морфологических исследований стало очевидно, что микроскопические колиты являются частой причиной хронической неинфекционной диареи [6]. На сегодняшний день микроскопический колит диагностируется в 4-13% случаев диарейного синдрома [8].
Количество публикаций, посвященных микроскопическому колиту, в последнее время увеличивается, и это свидетельствует о том, что данное заболевание диагностируется гораздо чаще. С одной стороны, это связано с улучшением диагностики, с другой – с истинным ростом заболеваемости. Новые эпидемиологические исследования, проведенные в этом столетии, подтвердили высокие цифры заболеваемости, показывающие, что фактическая заболеваемость и распространенность микроскопического колита выше, чем предполагалось первоначально [26]. Показатели заболеваемости и распространенности коллагенового колита в странах Западной Европы несколько выравниваются, в то время как показатели заболеваемости лимфоцитарного колита по-прежнему растут [23]. Эпидемиологические данные, полученные из различных регионов мира, преимущественно Северной Америки и стран Европейского региона, свидетельствуют о том, что заболеваемость коллагеновым колитом составляет 0,8-6,2 случаев на 100 тыс. населения, лимфоцитарным – 0,5-12,9 случаев на 100 тыс. населения [10, 25]. Обе формы микроскопического колита по темпам заболеваемости и распространенности приближаются к классическим воспалительным заболеваниям кишечника, таким как язвенный колит и болезнь Крона [22]. Последние эпидемиологические исследования показали, что микроскопический колит является заболеванием в основном пожилых людей, особенно пожилых пациентов женского пола [27].
Крайне редко микроскопический колит диагностируется в развивающихся странах Азии. Есть немногочисленные публикации, посвященные описанию отдельных случаев микроскопического колита в странах Восточного региона, в частности Индии [14], Турции [4], Бангладеш [21]. В настоящее время нет эпидемиологических данных относительно этого заболевания из стран Африки, где инфекционные заболевания являются наиболее распространенными. Единичные случаи были зарегистрированы в Нигерии [3]. В этом регионе микроскопический колит диагностируется крайне редко из-за отсутствия средств для колоноскопии, а также в результате низкого обращения за медицинской помощью в целом.
В нашей стране, даже в специализированных клиниках, где ежегодно проводится большое количество колоноскопий по поводу хронической диареи неинфекционного генеза, редко устанавливается диагноз «микроскопический колит». «Упущение» этого диагноза происходит по многим причинам, одна из которых связана с тем, что врач-эндоскопист просто не проводит забор биопсийного материала при нормальной визуальной картине слизистой оболочки толстой кишки. Однако при взятии гистологического материала микроскопическое заключение носит часто не конкретный, обтекаемый характер, как например «хронический колит», «неопределенный колит», и т.д. На основании отсутствия визуальных патологических изменений в толстой кишке и таких неопределенных гистологических заключений, как правило, устанавливается диагноз «синдром раздраженной толстой кишки».
В диагностике микроскопического колита ведущая роль, конечно, принадлежит врачу-эндоскописту и морфологу. Однако врач общей практики или гастроэнтеролог, направивший больного на колоноскопию с целью диагностики микроскопического колита, также должен правильно поставить задачу перед врачом-эндоскопистом и морфологом для максимально четкой диагностики данного заболевания.
Микроскопический колит – заболевание, которое не представляет особого риска для пациента, поскольку не связано с повышенной смертностью, не приводит к прогрессированию, развитию осложнений и инвалидизации. В отличие от других воспалительных заболеваний кишечника, не получено доказательств того, что имеющиеся гистологические изменения при микроскопическом колите могут привести к неблагоприятным последствиям, таким как колоректальный рак или необходимость хирургического вмешательства [15]. Однако клинические симптомы могут быть упорными, рецидивирующими и привести к ухудшению качества жизни пациентов [18].
Соответственно, целью медикаментозной терапии является облегчение симптомов и улучшение качества жизни пациентов с микроскопическим колитом при одновременной минимизации негативных последствий, связанных с применением лекарственных препаратов.
Лечение микроскопического колита претерпело существенные изменения за последние десять лет. Первоначально основными лекарственными средствами для лечения данного заболевания были антидиарейные и противовоспалительные препараты [2]. Клинические исследования и метаанализы последних лет установили эффективность новых препаратов для лечения микроскопического колита [7].
В 2015 г. вышли официальные рекомендации Американской гастроэнтерологической ассоциации (American Gastroenterological Association, AGA) по лечению микроскопического колита [19]. Данное руководство было разработано ведущими экспертами в области гастроэнтерологии и утверждено советом AGA. В основу документа положены руководящие принципы доказательной медицины [1, 9, 24]. Результаты клинических исследований проанализированы, оценены экспертами, и на их основе сформулированы основные рекомендации по лечению микроскопического колита.
Это руководство фокусируется на лечении микроскопического колита, а не на его диагностике. Поскольку результаты анализа эффективных методов лечения существенно не отличались между лимфоцитарным и коллагеновым колитом, в данных рекомендациях не проводится различия между подтипами микроскопического колита.

Авторы данного обзора 25 апреля 2015 г. обсудили качество доказательств (табл. 1) и рассмотрели другие факторы, имеющие значение для оценки риска и пользы рекомендаций.
Впоследствии авторы сформулировали основные положения рекомендаций. Хотя качество доказательств является наиболее важным фактором в определении прочности рекомендации, экспертами также учитывался баланс между их пользой и негативными последствиями (табл. 2).
Рекомендация № 1. У пациентов с симптоматикой микроскопического колита для индукции клинической ремиссии AGA рекомендует лечение с применением будесонида. Сильная рекомендация, среднее качество доказательств.

Метаанализ шести рандомизированных клинических исследований продемонстрировал очевидные преимущества будесонида в индукции клинической ремиссии. В пяти исследованиях также был достигнут гистологический ответ. Два исследования показали улучшение качества жизни пациентов, хотя разница не имела статистической значимости. Пациенты, получавшие 9 мг будесонида ежедневно, более чем в два раза чаще достигали клинической ремиссии в течение 7-13 дней по сравнению с группой не получавших лечение (относительный риск – ОР 2,52, 95% доверительный интервал – ДИ 1,45-4,40). При приеме будесонида риск серьезных побочных эффектов был низким. В связи с благоприятным профилем безопасности и эффективности, а также удобством приема (1 р/день) будесонид следует считать препаратом первой линии лечения микроскопического колита. Учитывая то, что будесонид является дорогостоящим препаратом, могут быть рассмотрены альтернативные методы терапии, если стоимость лечения является определяющим фактором. В большинстве случаев нет необходимости выполнять колоноскопию для оценки гистологического ответа на проводимую терапию. Тем не менее для пациентов, у которых сохраняются клинические симптомы после лечения будесонидом, рекомендуется проведение гистологического исследования. Отсутствие патологических изменений в биоптатах ободочной кишки является причиной для верификации другого диагноза – синдрома раздраженного кишечника или целиакии. Прекращение терапии будесонидом может быть рассмотрено после 8 недель терапии. У трети пациентов удается достигнуть клинической ремиссии и не требуется поддерживающей терапии.
Рекомендация № 2. У пациентов с клиническими симптомами микроскопического колита для индукции клинической ремиссии AGA отдает предпочтение лечению будесонидом по сравнению с месалазином. Сильная рекомендация, высокое качество доказательств.
Анализ большого количества высококачественных клинических испытаний при условии прямых доказательств показал преимущество будесонида над месалазином. Поэтому будесонид следует считать препаратом первой линии по сравнению с месалазином для лечения микроскопического колита. У пациентов с симптомами микроскопического колита, которых ежедневно лечили 9 мг будесонида, клиническая и гистологическая ремиссия была достигнута в 2 раза чаще, чем у пациентов, получавших месалазин 3 г ежедневно. Кроме того, не было выявлено статистически значимых различий в возникновении побочных эффектов.
Рекомендация № 3. У пациентов с симптоматикой микроскопического колита, которым противопоказана терапия будесонидом, для индукции клинической ремиссии AGA считает целесообразным применение месалазина. Условная рекомендация, среднее качество доказательств.
Согласно результатам одного рандомизированного клинического исследования терапия месалазином показала более низкую вероятность достижения клинического эффекта по сравнению с отсутствием лечения (отношение шансов 0,74; 95% ДИ 0,44-1,24), хотя результаты данного исследования не были статистически значимыми. На основании этих данных сделано заключение, что польза месалазина в достижении клинической ремиссии больных с микроскопическим колитом является неопределенной. Из-за недостаточно определенного баланса между эффективностью и потенциальными побочными эффектами месалазин рекомендуется условно, в качестве препарата второй линии, который может быть использован при некоторых обстоятельствах. Например, пробная терапия месалазином может подходить для пациентов, которые имеют противопоказания для назначения будесонида или показали плохой клинический ответ.
Рекомендация № 4. Для пациентов с симптоматикой микроскопического колита, у которых терапия будесонидом является недопустимой, AGA предлагает лечение преднизолоном с целью индукции клинической ремиссии. Условная рекомендация, очень низкое качество доказательств.
В небольшом рандомизированном клиническом исследовании эффективность преднизолона при лечении микроскопического колита достигла 22%. В связи с небольшой выборкой пациентов клинический эффект системных стероидов является неопределенным. Несмотря на нехватку доказательств, AGA считает, что системные кортикостероиды, в частности преднизолон, скорее всего уменьшают клинические симптомы. Хотя качество фактических данных об эффективности относительно безопасности также является низким. Обширный клинический опыт применения системных стероидов для других заболеваний позволяет предположить, что риск развития побочных эффектов при лечении микроскопического колита также будет значимым. AGA предложила условную рекомендацию для использования системных стероидов при лечении микроскопического колита из-за неопределенного баланса между клинической пользой и потенциальными побочными реакциями. Хотя в большинстве случаев системные кортикостероиды не следует использовать в качестве терапии первой линии, могут быть случаи, при которых лечение преднизолоном может стать целесообразным. Прежде всего претендентами для терапии системными стероидами становятся пациенты, которые не ответили на лечение будесонидом, при условии, что были исключены другие причины неинфекционной диареи, такие, например, как целиакия. С другой стороны, преднизолон значительно дешевле, чем будесонид, это может служить альтернативным выбором для пациентов с низкими материальными возможностями.
Рекомендация № 5. У пациентов с симптомами микроскопического колита, которым противопоказана терапия будесонидом, AGA предлагает лечение салицилатом висмута для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
В небольшом рандомизированном контролируемом исследовании с использованием салицилата висмута для лечения микроскопического колита все 7 пациентов показали клинический ответ, в то время как ни один из 7 пациентов контрольной группы не ответил на лечение. Пациенты, получавшие салицилат висмута, имели в 3 раза более высокую вероятность достижения гистологического ответа, хотя это не было статистически значимым. Отсутствуют данные о побочных эффектах салицилата висмута при длительной терапии микроскопического колита. По этим причинам AGA условно рекомендует салицилат висмута в качестве терапии второй линии либо как альтернативный метод лечения для отдельных лиц, которые могут иметь противопоказания к лечению стероидными гормонами или для которых стоимость лечения является определяющим фактором.
Рекомендация № 6. У пациентов с симптомами микроскопического колита AGA не рекомендует комбинированную терапию холестирамином и месалазином в сравнении с монотерапией месалазином с целью индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
Низкое качество доказательств основано на результатах одного рандомизированного клинического исследования, которое не показало увеличения клинического эффекта от добавления холестирамина к терапии месалазином. При предоставлении условной рекомендации в отношении комбинированной терапии холестирамином и месалазином AGA учитывает не только неопределенный баланс между пользой и риском, но и возможности нарушения всасывания других лекарственных препаратов при приеме холестирамина, что является особенно важным в лечении пожилых пациентов, когда полипрагмазия является обычным делом. AGA не может прокомментировать целесообразность монотерапии холестирамином, так как отсутствуют данные о клинических исследованиях, которые оценили подобное лечение у больных с микроскопическим колитом.
Рекомендация № 7. У пациентов с микроскопическим колитом AGA не рекомендует лечение Boswellia serrata для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
В одном рандомизированном контролируемом исследовании 44% из 16 пациентов с микроскопическим колитом показали клиническое улучшение в ответ на терапию Boswellia serrata, тогда как только у 27% из 15 пациентов клиническая ремиссия достигнута в группе плацебо. Не было выявлено никакой разницы в качестве жизни между двумя группами, побочные эффекты были более частыми в группе приема Boswellia serrata. Все полученные результаты не были статистически значимыми в дополнение к неопределенности баланса между пользой и риском терапии Boswellia serrata. Группа экспертов также высказала опасение относительно возможности доступа к стандартизованной формуле Boswellia serrata, учитывая многочисленные продукты, доступные для применения на фармацевтическом рынке, содержащие компоненты Boswellia serrata. По этим причинам AGA предоставила условную рекомендацию против рутинного использования Boswellia serrata для лечения микроскопического колита.
Рекомендация № 8. У пациентов с микроскопическим колитом AGA не рекомендует лечение пробиотиками для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
Основанием для данной рекомендации стали результаты небольшого рандомизированного исследования, сравнивающего пробиотические продукты (Lactobacillus acidophilus, Bifidobacterium animalis, lactis strains) с плацебо при лечении микроскопического колита. Полученные данные показали неопределенное преимущество в отношении клинической ремиссии, гистологического ответа и качества жизни пациентов с микроскопическим колитом при лечении пробиотиками. Из-за неопределенности баланса между пользой и риском побочных эффектов AGA условно не рекомендует использование пробиотиков для лечения микроскопического колита. Эксперты признают неопределенность полученных результатов в одном исследовании с применением конкретного пробиотического препарата и делают заключение о том, что полученные результаты не могут быть обобщены для всех доступных пробиотических продуктов.
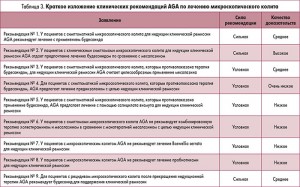
Рекомендация № 9. Для пациентов с рецидивом микроскопического колита после прекращения индукционной терапии AGA рекомендует будесонид для поддержания клинической ремиссии. Сильная рекомендация, среднее качество доказательств.
Умеренное качество доказательств получено из 2 рандомизированных клинических исследований, которые показали, что поддерживающая терапия препаратом будесонид (6 мг ежедневно в течение 6 мес) в 66% случаев приводила к снижению ОР клинического рецидива (ОР 0,34; 95% ДИ 0,19-0,60). Данный режим терапии также эффективно поддерживал гистологическую ремиссию и улучшал качество жизни пациентов с микроскопическим колитом. Прием более низких доз будесонида (чередование 3 и 6 мг в сутки) в течение 12 мес показал одинаковую эффективность в поддержании клинического ответа. Группа экспертов отмечает, что поддерживающая терапия должна быть предложена только пациентам с микроскопическим колитом, у которых развился рецидив клинических симптомов после прекращения индукционной терапии. Треть пациентов не нуждаются в проведении поддерживающей терапии, а ее прекращение может быть рассмотрено после 6-12 мес лечения.
Эти рекомендации по лечению микроскопического колита были разработаны в рамках методологии GRADE (Grading of Recommendations Assessment, Development and Evaluation) и согласованы с Институтом стандартов медицины. В результате анализа исследований можно сделать вывод о том, что для лечения микроскопического колита препаратом первой линии является будесонид – как для индукционной терапии, так и для поддержания ремиссии. Представленные прочие методы лечения могут быть использованы как альтернативные варианты лечения из-за низкого качества доказательств. Из-за отсутствия данных клинических испытаний эти рекомендации не рассматривали лечение стероидорефрактерных форм микроскопического колита [5]. Получены ограниченные данные о пользе иммунодепрессантов, таких как азатиоприн и антитела к фактору некроза опухоли, в лечении микроскопического колита [16, 17, 19, 20]. Дальнейшие клинические испытания с целью продолжения изучения новых методов позволят улучшить лечение микроскопического колита.
Литература
1. AGA Institute clinical practice guideline development process. http://www.gastro.org/guidelines/guidelines-policies.
2. Chande N., McDonald J.W., Macdonald J.K. Interventions for treating lymphocytic colitis. Cochrane Database of Systematic Reviews. 2008; (2)CD006096.
3. Ekrikpo U.E., Otegbayo J.A., Oluwasola A.O. Lymphocytic colitis presenting as difficult diarrhoea in an African woman: a case report and review of the literature. J Med Case Reports. 2010; 4: 31.
4. Erdem L., Yildirim S., Akbayir N., Yilmaz B., Yenice N., Gultekin O.S., Peker O. Prevalence of microscopic colitis in patients with diarrhea of unknown etiology in Turkey. World J Gastroenterol. 2008; 14: 4319-4323.
5. Esteve M., Mahadevan U., Sainz E. et al. Efficacy of anti-TNF therapies in refractory severe microscopic colitis. J Crohns Colitis 2011; 5: 612-618.
6. Fernandez-Ban~ares F., de Sousa M.R., Salas A. et al. Epidemiological risk factors in microscopic colitis: a prospective case-control study. Inflamm Bowel Dis. 2013; 19 (2): 411-417.
7. Gentile N.M., Abdalla A.A., Khanna S. et al. Outcomes of patients with microscopic colitis treated with corticosteroids: a population-based study. Am J Gastroenterol. 2013; 108 (2): 256-259.
8. Gentile N.M., Khanna S., Loftus E.V. Jr. et al. The epidemiology of microscopic colitis in Olmsted County from 2002 to 2010: a population-based study. ClinGastroenterolHepatol. 2014; 12 (5): 838-842.
9. Graham R., Mancher M., Wolman D.M. et al. Clinical practice guidelines we can trust. Washington, DC: Institute of Medicine; The National Academies Press, 2011.
10. Guagnozzi D., Lucendo A.J., Angueira-Lapena T., Gonzalez-Castillo S., Tenias Burillo J.M. Prevalence and incidence of microscopic colitis in patients with diarrhoea of unknown aetiology in a region in central Spain. Digestive and Liver Disease. 2012; 44 (5): 384-388.
11. Lazenby A.J., Yardley J.H., Giardiello F.M., Jessurun J., Bayless T.M. Lymphocytic (‘microscopic’) colitis: a comparative histopathologic study with particular reference to collagenous colitis. Human Pathology. 1989; 20 (1): 18-28.
12. Lindstrom C.G. ‘Collagenous colitis’ with watery diarrhoea. A new entity? Pathologia Europaea. 1976; 11 (1): 87-89.
13. Malekian V., Amirfattahi R., Sadri S., Mokhtari M., Aghaie A., Rezaeian M. Computer aided measurement of sub-epithelial collagen band in colon biopsies for collagenous colitis diagnosis. Micron. 2013; 45: 59-67.
14. Misra V., Misra S.P., Dwivedi M., Singh P.A., Agarwal V. Microscopic colitis in patients presenting with chronic diarrhea.Indian J Pathol Microbiol. 2010; 53: 15-19.
15. Munch A., Aust D., Bohr J. et al. Microscopic colitis: Current status, present and future challenges: statements of the European Microscopic Colitis Group. Journal of Crohn’s & colitis. 2012 Oct; 6 (9): 932-945.
16. Munch A., Fernandez-Banares F., Munck L.K. Azathioprine and mercaptopurine in the management of patients withchronic, active microscopic colitis. Aliment Pharmacol Ther. 2013; 37: 795-798.
17. Munch A., Ignatova S., Strom M. Adalimumab in budesonide and methotrexate refractory collagenous colitis. Scand J Gastroenterol. 2012; 47: 59-63.
18. O’Toole A., Coss A., Holleran G. et al. Microscopic colitis: clinical characteristics, treatment and outcomes in an Irish population. Int J Colorectal Dis. 2014; 29 (7): 799-803.
19. Pardi D.S., Tremaine W.J., Carrasco-Labra A. American Gastroenterological Association institute technical re-view on the medical management of microscopic colitis. Gastroenterology 2016; 150: 247-274.
20. Pola S., Fahmy M., Evans E. et al. Successful use of infliximab in the treatment of corticosteroid dependentcollagenous colitis. Am J Gastroenterol 2013; 108: 857-858.
21. Rahman M.A., Raihan A.S., Ahamed D.S. et al. Symptomatic overlap in patients with diarrhea predominant irritable bowel syndrome and microscopic colitis in a sub group of Bangladeshi population. Bangladesh Medical Research Council Bulletin. 2012; 38 (1): 33-38.
22. Sonnenberg A., Genta R.M. Geographic distributions of microscopic colitis and inflammatory bowel disease in the United States.Inflammatory Bowel Diseases. 2012; 18 (12): 2288-2293.
23. Stewart M., Andrews C.N., Urbanski S., Beck P.L., Storr M. The association of coeliac disease and microscopic colitis: a large population-based study.Alimentary Pharmacology and Therapeutics. 2011; 33 (12): 1340-1349.
24. Sultan S., Falck-Ytter Y., Inadomi J.M. The AGA Institute process for developing clinical practice guidelines part one: grading the evidence. ClinGastroenterolHepatol. 2013; 11: 329-332.
25. Tysk C., Bohr J., Nyhlin N., Wickbom A., Eriksson S. Diagnosis and management of microscopic colitis. World J Gastroenterol. 2008; 14: 7280-7288.
26. Vigren L., Olesen M., Benoni C., Sjoberg K. An epidemiological study of collagenous colitis in southern Sweden from 2001-2010. World Journal of Gastroenterology. 2012; 18 (22): 2821-2826.
27. Williams J.J., Beck P.L., Andrews C.N., Hogan D.B., Storr M.A. Microscopic colitis – a common cause of diarrhoea in older adults. Age and Ageing. 2010; 39 (2): 162-168.



