30 серпня, 2019
GOLD-2019: персоналізація лікування пацієнтів із хронічним обструктивним захворюванням легень

Хронічне обструктивне захворювання легень (ХОЗЛ) є однією з найактуальніших медичних проблем. Хоча епідеміологічні показники щодо поширеності, захворюваності та смертності від цієї патології варіюють у різних країнах, в усьому світі спостерігається тенденція до їх зростання. Це пов’язано як зі збільшенням рівня куріння, забруднення повітря різноманітними полютантами органічного й неорганічного походження, так і з подовженням середньої тривалості життя. На боротьбу з ХОЗЛ витрачаються значні економічні та наукові ресурси. Завдяки цьому щорічно вдосконалюються підходи до запобігання захворюванню, до його діагностики та лікування, що відображається в глобальних рекомендаціях GOLD [1]. У квітні в Києві відбулася VII Науково-практична конференція «Актуальні проблеми лікування хворих на хронічне обструктивне захворювання легень». Метою заходу стало освітлення найновіших тенденцій у веденні пацієнтів із ХОЗЛ на основі GOLD-2019. І це стосується не лише пульмонологів, але й сімейних лікарів, адже саме до них передусім звертається хворий.
 Основні положення ведення пацієнтів із ХОЗЛ для лікарів загальної практики – сімейної медицини представив увазі присутніх завідувач кафедри пропедевтики внутрішньої медицини Вінницького національного медичного університету ім. М.І. Пирогова, доктор медичних наук, професор Ю.М. Мостовой.
Основні положення ведення пацієнтів із ХОЗЛ для лікарів загальної практики – сімейної медицини представив увазі присутніх завідувач кафедри пропедевтики внутрішньої медицини Вінницького національного медичного університету ім. М.І. Пирогова, доктор медичних наук, професор Ю.М. Мостовой.
– Розуміння патогенезу ХОЗЛ є основою його успішного лікування, адже, лише впливаючи на кожну його складову, можна забезпечити належний контроль симптомів та запобігти прогресуванню хвороби. Патологічні зміни при ХОЗЛ включають хронічне запалення, яке прогресує, викликає структурні зміни в респіраторному тракті та альвеолах. Саме ці зміни спричинюють стійкі респіраторні симптоми та обмежують прохідність дихальних шляхів. Хронічне запалення також відіграє важливу роль у виникненні та погіршенні перебігу множинних коморбідних станів, виявлених у пацієнтів із ХОЗЛ. Таким чином, оптимальна терапія має зменшувати запалення та покращувати якість життя пацієнтів, впливаючи на вираженість симптомів.
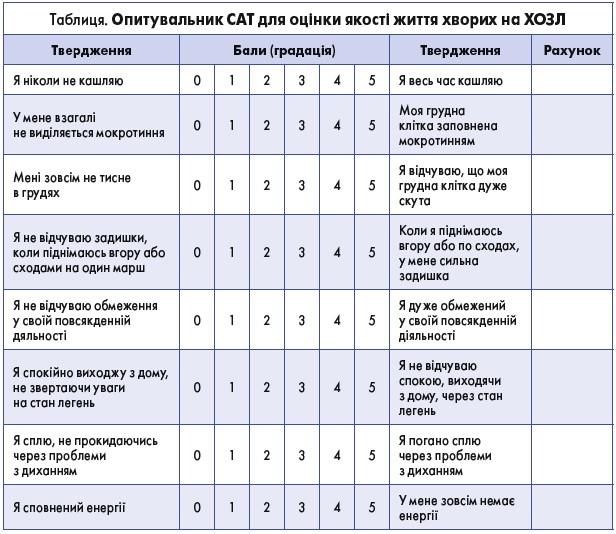
Для постановки первинного діагнозу ХОЗЛ типові скарги, оцінені за опитувальниками [тесту самоактуалізації] CAT (табл.) або [шкалою тяжкості задишки – modified Medical Research Council] mMRC, мають поєднуватися з функціональним маркером наявності ХОЗЛ: об’єм форсованого видиху за 1-шу секунду / форсована життєва ємність легень (ОФВ1/ФЖЄЛ) <0,7. Цей показник отримують, використовуючи базисну спірометрію. Крім підтвердження діагнозу ХОЗЛ це дослідження допомагає оцінити тяжкість обмеження повітряного потоку, визначити прогноз і прийняти рішення щодо корекції та зміни в підходах до лікування [1].
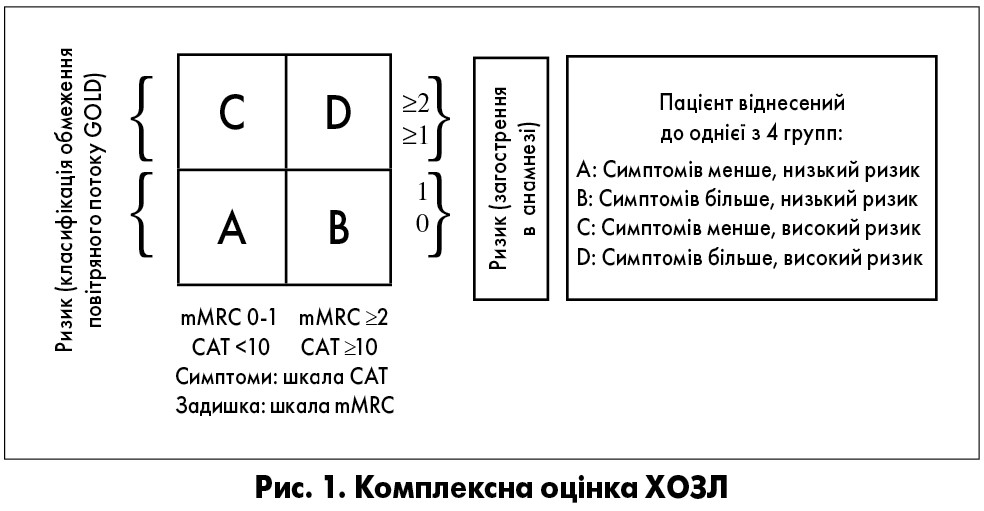
Показник спірометрії ОФВ1/ФЖЄЛ <0,7 є основою при комплексній оцінці ХОЗЛ (рис. 1). Наявність і вираженість симптомів/задишки та загострень в анамнезі дають можливість «розташувати» пацієнта в квадрат та визначити подальшу тактику лікування.
Під загостренням ХОЗЛ розуміють гостру подію, яка проявляється погіршенням респіраторних симптомів та вимагає застосування додаткових способів лікування [1], а саме:
- короткодіючих бронходилататорів при легкому загостренні;
- короткодіючих бронходилататорів, антибіотиків та/або пероральних глюкокортикоїдів (ГКК) при загостренні середньої тяжкості;
- госпіталізації та невідкладної терапії при тяжкому загостренні.
Наступним кроком після постановки діагнозу ХОЗЛ та визначення групи є призначення початкової терапії [1]:
Група А
β2-агоніст короткої дії (БАКД),
або β2-агоніст тривалої дії (БАТД),
або М-холінолітик короткої дії (МХКД),
або М-холінолітик тривалої дії (МХТД).
Група В
БАТД
або МХТД.
Група С
МХТД.
Група D
МХТД;
у разі виражених симптомів (оцінка за шкалою САТ ≥20) – МХТД / БАТД;
у разі рівня еозинофілів крові ≥300 мкл – інгаляційні кортикостероїди (ІКС) / БАТД.
Якщо відповідь на початкову терапію задовільна, лікування продовжують за тією ж схемою, але в разі недостатнього контролю симптомів чи появи загострень вносять необхідні корективи. При цьому важливо розуміти, що рекомендації щодо корекції не залежать від ABCD-групи пацієнта з ХОЗЛ. На перший план тут виступає наявність симптомів та/або загострень.
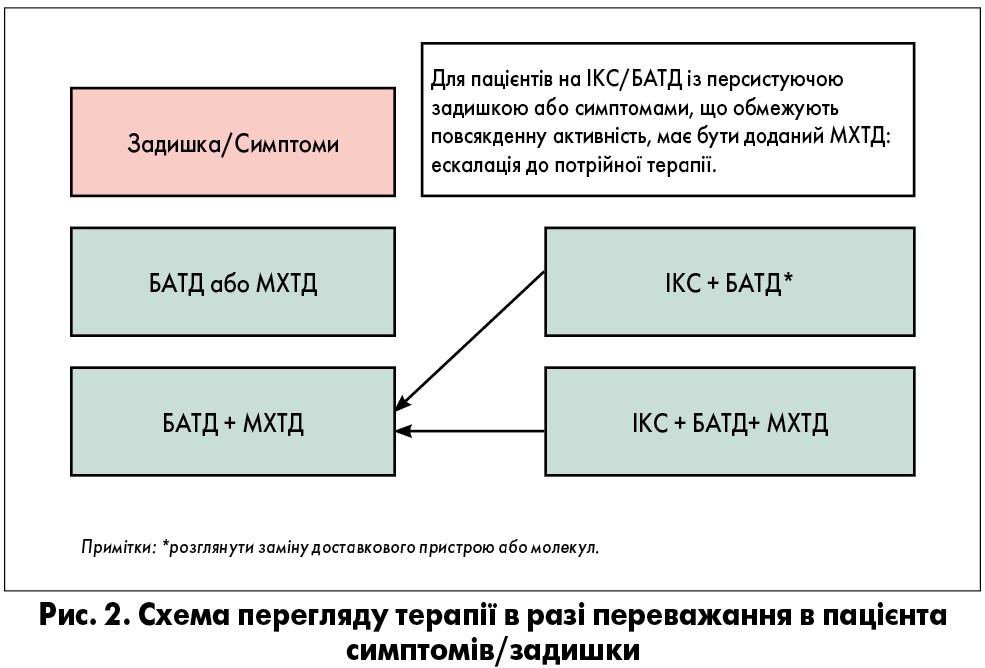
У разі переважання в клінічній картині симптомів і задишки необхідно посилити саме симптоматичну терапію, тобто додати бронходилататор (рис. 2).
Отже, якщо початкова терапія починалася з БАТД або МХТД, корекція буде полягати у використанні їх комбінації. Якщо ж стартували з комбінації ІКС/БАТД, переходять на потрійну терапію і додають МХТД. Через 2-3 міс проводиться переоцінка симптомів.
За відсутності відповіді на ІКС або в разі переведення на іншу терапію у випадку пневмонії чи при невідповідному початковому призначенні рекомендується розглянути можливість відміни ІКС [1].
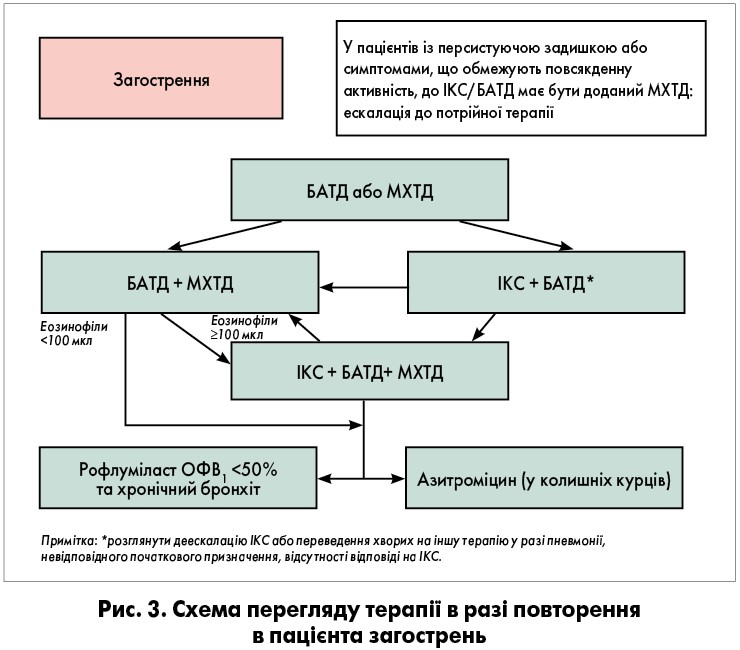
Якщо ж у пацієнта повторюються загострення, посилюють саме протизапальну терапію, тобто додають ІКС (рис. 3).
Отже, за наявності повторних загострень пацієнту з ХОЗЛ треба додати ІКС у разі, якщо:
- рівень еозинофілів ≥300 мкл + 1 загострення на рік;
- рівень еозинофілів ≥100 мкл + ≥2 легкі або помірні загострення;
- рівень еозинофілів ≥100 мкл + 1 тяжке загострення.
Кількість еозинофілів розраховують за такою формулою [2]:
Кількість еозинофілів =( 5%×7×109/л)/100% = 0,35×109/л = 350 (клітин в 1 мкл)
Якщо в пацієнтів на тлі терапії комбінацією ІКС/БАТД розвивається подальше загострення, рекомендовано перейти на потрійну терапію шляхом додавання МХТД [1].
Комбінація ІКС/БАТД більш ефективна, ніж окремі компоненти, щодо покращання функції легень, стану здоров’я і зниження частоти загострень у пацієнтів від середнього до вкрай тяжкого ХОЗЛ і з загостреннями в анамнезі (рівень доказовості А).
У 12-місячному рандомізованому подвійному сліпому плацебо-контрольованому паралельному дослідженні за участю 812 дорослих пацієнтів (середній вік 64 роки, середній ОФВ1 36% від належного) хворі отримували щодня по 2 інгаляції 2 р./день комбінації будесоніду та формотеролу в дозі 160/4,5 мкг, або будесоніду 200 мкг, або формотеролу 4,5 мкг, або плацебо. Фіксувалися тяжкі загострення та значення ОФВ1 (первинні кінцеві точки). Вторинні кінцеві точки включили пікову швидкість видиху (ПШВ), тяжкість симптомів ХОЗЛ, показник якості життя, оцінений за шкалою HRQL (Health-related quality of life), легкі загострення, частоту використання β2-агоністів та показники безпеки. Будесонід/формотерол зменшили середнє число серйозних загострень на 1 пацієнта на рік на 24% порівняно з плацебо і на 23% – з формотеролом. ОФВ1 збільшився на 15% проти плацебо і на 9% – проти будесоніду. Ранкова ПШВ у порівнянні з плацебо і будесонідом значуще покращилася вже в 1-й день; через 1 тиж, ранкова ПШВ покращилася в порівнянні з плацебо, будесонідом і формотеролом. Покращання ранкової та вечірньої ПШВ у групі комбінації будесоніду та формотеролу зберігалося протягом 12 місяців. Будесонід/формотерол значно знизив вираженість симптомів і частоту використання β2-агоністів в порівнянні з плацебо і будесонідом, а також покращив показники якості життя проти плацебо [4].
У дослідженнях, де потрійна терапія з використанням будесоніда/формотерола та тіотропія броміду порівнювалася з монотерапією тіотропієм, було показано, що комбінація препаратів на 62% знижувала частоту тяжких загострень ХОЗЛ та на 65% – частоту госпіталізацій і звернень по невідкладну медичну допомогу. Таким чином, комбінація будесоніду та формотеролу швидко й значуще знижує симптоми ХОЗЛ, покращує якість життя та зменшує кількість загострень [5].
 Завідувач кафедри фтизіатрії і пульмонології з курсом професійних хвороб ДВНЗ «Івано-Франківський національний медичний університет», доктор медичних наук, професор М.М. Островський у своїй доповіді акцентував увагу саме на ролі ІКС у зниженні ризику розвитку загострень. Згідно з GOLD-2019 загострення є ключовою подією при ХОЗЛ і основним фактором прогресування захворювання та збільшення смертності [1, 6]. Воно призводить до посилення симптомів і задишки, зниження функції легень, підвищення ризику госпіталізації, погіршення загального стану здоров’я та якості життя пацієнтів [7-9].
Завідувач кафедри фтизіатрії і пульмонології з курсом професійних хвороб ДВНЗ «Івано-Франківський національний медичний університет», доктор медичних наук, професор М.М. Островський у своїй доповіді акцентував увагу саме на ролі ІКС у зниженні ризику розвитку загострень. Згідно з GOLD-2019 загострення є ключовою подією при ХОЗЛ і основним фактором прогресування захворювання та збільшення смертності [1, 6]. Воно призводить до посилення симптомів і задишки, зниження функції легень, підвищення ризику госпіталізації, погіршення загального стану здоров’я та якості життя пацієнтів [7-9].
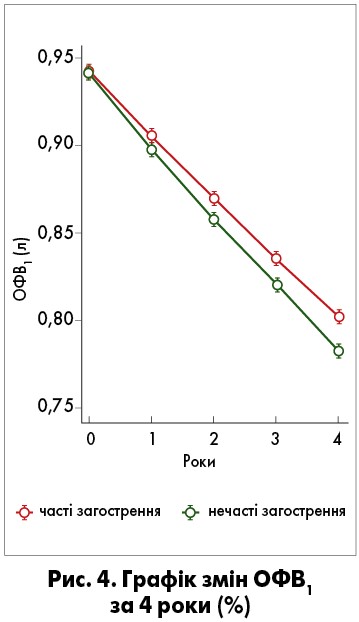
Досвід клінічної практики підтверджує прогресуюче зниження функції легень у пацієнтів із ХОЗЛ залежно від частоти загострень. У дослідженні G.C. Donaldson та співавт. було підтверджено, що в пацієнтів із більш як 1,5 загострення на рік зниження ОФВ1 було більшим (46,1 мл/рік) проти тих, у кого було менше 1,5 загострення (25,3 мл/рік) [7] (рис. 4).
Хоча й вважається, що в основі ХОЗЛ лежить виключно нейтрофільне запалення, згідно з результатами досліджень останніх років понад 35% пацієнтів із ХОЗЛ мають еозинофільний фенотип (число еозинофілів периферичної крові ≥2%). Участь еозинофілів у патогенезі викликає особливо швидке порушення структури бронхіального дерева, високу частоту загострень, що, відповідно, значно погіршує якість життя та навіть ризводить до розвитку інвалідності. В основі лежить Тh2-опосередковане запалення, яке можна якісно побороти тільки використовуючи ІКС [10-14].
У Копенгагенському популяційному дослідженні за участю 7225 пацієнтів вивчалася асоціація між кількістю еозинофілів у крові та ризиком загострень ХОЗЛ [15] (рис. 5).
Було встановлено, що в 64% хворих на ХОЗЛ і 66% пацієнтів із клінічними проявами ХОЗЛ рівень еозинофілів становив ≥2%, а підвищення рівня еозинофілів у крові понад 0,34×109/л в осіб із ХОЗЛ у загальній популяції було пов’язане з підвищенням ризику серйозних загострень у 1,76 раза.
Результати цих досліджень знайшли своє відображення в рекомендаціях GOLD-2019. У них підкреслюється, що в приблизно 1/3 пацієнтів із ХОЗЛ (GOLD ІІІ, ІV) визначається наявність еозинофільного типу запалення. Такі пацієнти демонструють більшу відповідь на лікування кортикостероїдами. Підвищення рівня еозинофілів крові від 150-200 кл/мкл пов’язане з підвищеним ризиком загострення ХОЗЛ, що частково може бути зменшено тривалим лікуванням за допомогою ІКС. Ці результати узгоджуються з патогенетичною роллю еозинофілів у загостренні ХОЗЛ і забезпечують обґрунтування терапії, яка специфічно пригнічує еозинофільне запалення.
Ключовою перевагою нових даних GOLD-2019 стала персоналізація пацієнтів. Число еозинофілів периферичної крові запропоновано в якості біомаркера для прогнозування виникнення загострення і відповіді на терапію. Це дає можливість вчасно виявляти хворих із підвищеним ризиком загострення ХОЗЛ, проводити корекцію терапії та передбачувати більшу ймовірність позитивної відповіді на лікування ІКС.
Основні цілі терапії ХОЗЛ, однакові як для лікаря, так і для пацієнта, включають:
- усунення симптомів;
- поліпшення толерантності до фізичного навантаження;
- покращання самопочуття;
- запобігання прогресуванню захворювання;
- запобігання хворобі та лікування загострень;
- зменшення смертності.
Застосування ІКС у хворих на ХОЗЛ дає можливість оптимізувати терапію та досягти зазначених цілей у найбільш проблематичних категорій пацієнтів, у тому числі хворих із загостреннями, з еозинофільним типом запалення та ознаками або анамнезом бронхіальної астми.
Серед ІКС необхідно віддавати перевагу ефективному препарату з максимально швидкою дією. Основні фармакологічні характеристики ІКС, які впливають на швидкість проникнення до дихальних шляхів, включають ліпофільність і водорозчинність. Будесонід менш ліпофільний, ніж інші ІКС, та швидше розчиняється в слизу дихальних шляхів, тому швидше всмоктується. Менш водорозчинний флутиказон, ймовірніше, затримається в просвіті дихальних шляхів і виведеться за допомогою мукоциліарного кліренсу. Комбінація будесоніду з БАТД здатна забезпечити ще більш швидкий ефект. З огляду на це, формотерол має значну перевагу над сальметеролом у швидкості настання ефекту: він починає діяти вже через 3 хвилини.
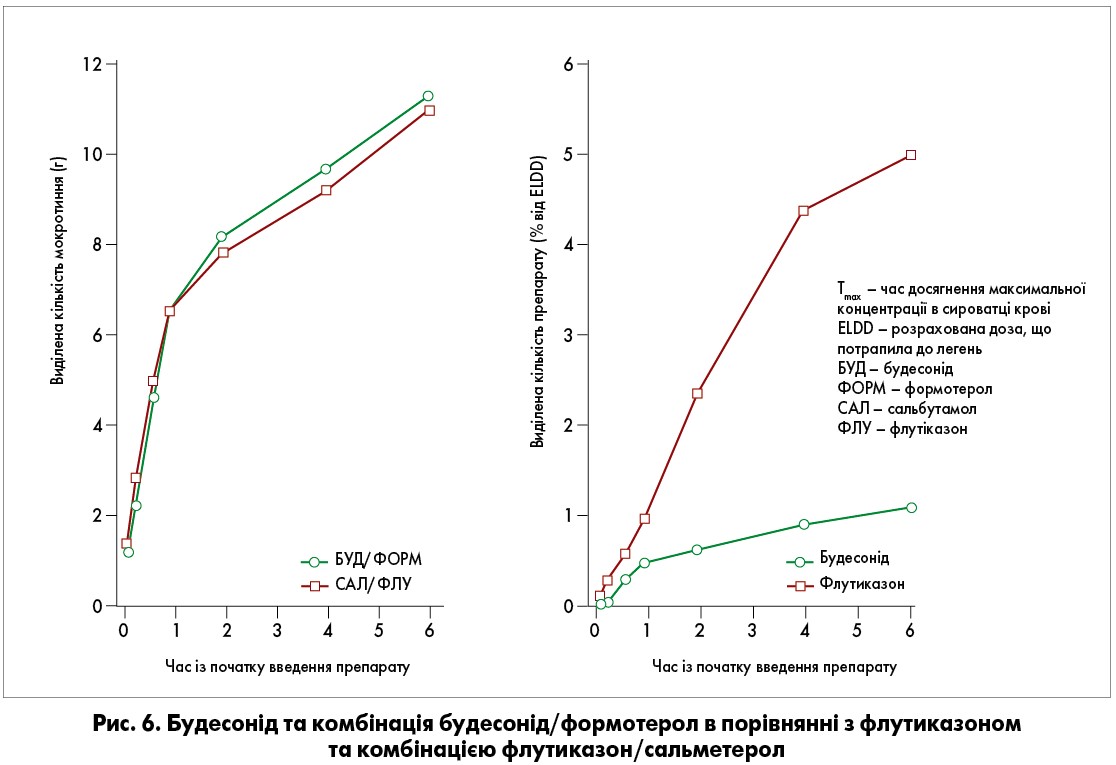
С. Dalby та співавт. у своєму дослідженні підтвердили переваги будесоніду та комбінації будесонід/формотерол у порівнянні з флутиказоном та комбінацією флутиказон/сальметерол (рис. 6).
Як можна побачити, максимальної концентрації в сироватці крові будесонід досягав через 15,5 хв, у той час як для флутиказону цей показник дорівнював 50,8 хвилини. Крім того, застосування комбінації будесонід/формотерол забезпечувало виділення більшої кількості мокротиння, ніж флутиказон/сальметерол [16].
Комбінація будесоніду та формотеролу оптимально досягає дихальних шляхів завдяки надійній системі доставки. У дослідженні INCONTROL‑1 було показано, що застосування будесоніду/формотеролу знижувало ризик загострень ХОЗЛ на 25-60% проти монотерапії формотеролом. При цьому ефективність препарату була вищою в пацієнтів, в яких визначалася більша кількість еозинофілів в крові [17].
Отже, у ході контрольованих досліджень ефективності у лікуванні ХОЗЛ комбінація будесоніду та формотеролу стабільно демонструвала більший вплив на ранкові симптоми, рівень щоденної активності, знижувала частоту загострень, у тому числі тих, які потребують госпіталізації.
Список літератури знаходиться в редакції.
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (47), 2019 р.