3 вересня, 2019
Дослідження терапевтичної ефективності, безпеки та переносимості екстракту ВN0 1030 зі вмістом кореню алтею, квітів ромашки, трави хвоща, листя волоського горіха, трави деревію, кори дуба, трави кульбаби в лікуванні гострого небактеріального тонзиліту в дітей
 Гострий тонзиліт (ГТ) (J03.0-J03.9) визначається як раптовий початок типових клінічних симптомів, включаючи біль у горлі з утрудненим ковтанням або без нього, гіперемію, збільшення мигдалин із можливою наявністю пробок, збільшення шийних лімфатичних вузлів, лихоманку, загальну слабкість. На таких пацієнтів припадає близько 5% візитів до лікаря, 50% хворих мають вік від 5 до 15 років [1]. 70-95% випадків ГТ викликані вірусними інфекціями. Бактеріальний (Streptococcal) ГТ розвивається в імунокомпетентних дітей у 15-30% випадків, у дорослих – у 5-15% випадків. Так, у більшості випадків ГТ терапія антибіотиками не показана [2, 3].
Гострий тонзиліт (ГТ) (J03.0-J03.9) визначається як раптовий початок типових клінічних симптомів, включаючи біль у горлі з утрудненим ковтанням або без нього, гіперемію, збільшення мигдалин із можливою наявністю пробок, збільшення шийних лімфатичних вузлів, лихоманку, загальну слабкість. На таких пацієнтів припадає близько 5% візитів до лікаря, 50% хворих мають вік від 5 до 15 років [1]. 70-95% випадків ГТ викликані вірусними інфекціями. Бактеріальний (Streptococcal) ГТ розвивається в імунокомпетентних дітей у 15-30% випадків, у дорослих – у 5-15% випадків. Так, у більшості випадків ГТ терапія антибіотиками не показана [2, 3].
Дотепер немає єдиного стандартного параметра для диференціальної діагностики вірусного та бактеріального тонзиліту. На основі комплексної диференціації між вірусною та бактеріальною етіологією для пацієнтів віком від 3 до 14 років було запропоновано шкалу МакАйзека, а шкалу СЕNTOR – для пацієнтів віком старше 15 років; ці шкали оцінюють наявність або відсутність декількох хронологічних даних та клінічних симптомів і виражають як загальний бал. Оцінка від -1 до 3 балів за шкалою МакАйзека та від 0 до 2 балів за шкалою СЕNTOR свідчить про високу ймовірність вірусного тонзиліту [1, 4].
У таких випадках для полегшення симптомів успішно використовують ацетамінофен або ібупрофен [1, 5, 6]. Проте зазначені симптоматичні засоби не охоплюють увесь спектр патогенетичних механізмів ГТ, що є основною причиною рецидиву, незважаючи на хороший швидкий симптоматичний ефект. Виходячи з цього, виникає потреба в лікарських засобах, що мають комплексний ефект на основні ланки патогенезу.
Основним симптомом тонзиліту є біль у горлі, що є рушійною силою як необґрунтованого призначення антибіотиків лікарями, так і готовності до застосування антибактеріальної терапії (АБТ) самими пацієнтами. Утім необґрунтована етіотропна терапія не впливає на динаміку цього симптому. Але вона є однією з основних причин глобальної проблеми резистентності до антибіотиків [2].
Завдяки цим даним використання фітопрепаратів може бути цікавим, оскільки, за даними досліджень, 28% лікарів використовують готові до застосування лікарські засоби рослинного походження в терапії тонзилофарингітів [7]. Препарати ехінацеї є найбільш вивченими з цього погляду. Проте рандомізовані дослідження не підтвердили ефективності ехінацеї в пацієнтів із ГТ [1]. Pelargonium sidoides показав ефективність у лікуванні симптомів застуди, але немає даних щодо пацієнтів із тонзилітом [8].
Брак досліджень ефективності фітотерапії, що відповідають вимогам GCP, очевидний; проте ситуація змінилася після видання відповідних рекомендацій [9]. Фітоніринговий водно-спиртовий екстракт BNO 1030, що включає сім лікарських рослин: корінь алтею (Radix althaeae), квіти ромашки (Flores chamomillae), траву хвоща (Herba equiseti), листя волоського горіха (Folia jungladis), траву деревію (Herba millefolii), кору дуба (Cortex quercus) і траву кульбаби (Herba taraxaci), відомий як Імупрет® (також відомий як Тонзилгон® N у деяких країнах). Імупрет®, на відміну від традиційних рослинних лікарських засобів, є офіційним препаратом і дозволений для продажу в аптеках Німеччини, України та ще 16 країн світу. У США цей препарат поки недоступний.
Складники лікарського засобу проявляють антивірусну, антибактеріальну, протизапальну та імуномодулюючу дію [10-16], а показання до його застосування включають: «лікування захворювань верхніх дихальних шляхів (тонзиліт, фарингіт, ларингіт) і профілактику ускладнень і рецидивів при вірусних респіраторних інфекціях». До сьогодні клінічні дослідження за участю дітей включали ефективність і профілактичні ефекти в дітей із застудою, а також лікування вірусних респіраторних інфекцій [17-20]. Проте в науковій літературі відсутні звіти про застосовні (з точки зору відповідності стандартам GCP) дослідження ефективності Імупрет® у терапії ГТ.
Метою цього дослідження була оцінка ефективності фітонірингового екстракту BNO 1030 (Імупрет®) у порівнянні з пацієнтами, які отримували стандартну симптоматичну терапію від ГТ відповідно до рекомендацій національних керівництв [21].
Матеріали та методи
Дизайн дослідження
Рандомізоване відкрите пошукове порівняльне багатоцентрове проспективне дослідження в паралельних групах проводили з червня 2017 по березень 2018 року в шістьох амбулаторних закладах України. Дослідження проводилося відповідно до стандартів GCP і Гельсінської декларації. Крім того, до включення першого пацієнта дослідження було схвалене місцевим Комітетом із питань етики та місцевими комітетами з питань етики в усіх центрах проведення дослідження. Перед включенням у дослідження батьки або законні представники кожної дитини надавали письмову інформовану згоду на участь дитини в дослідженні.
Суб’єкти
Було обрано 250 амбулаторних пацієнтів, із них 238 (після виключення з дослідження 12 осіб) із діагнозом «гострий небактеріальний тонзиліт» та віком від 6 до 18 років взяли участь у дослідженні. Пацієнти були рандомізовані на 2 групи залежно від обраної терапії: учасники групи лікування отримували BNO 1030 – стандартизований екстракт семи лікарських рослин (Імупрет®) як додаток до стандартної терапії; пацієнти з контрольної групи отримувала стандартну симптоматичну терапію. Група лікування (п=118) включала 52 (44,1%) хлопця і 66 (55,9%) дівчат (середній вік становив 8,67±3,219 року), контрольна – 62 (51,7%) хлопця і 58 (48,3%) дівчат (середній вік становив 9,66±3,296 року).
Діагностичні та диференційно-діагностичні критерії ГТ відповідають рекомендаціям DEGAM, викладеним у національних клінічних рекомендаціях [1, 21, 22]. Клінічний діагноз ГТ встановлювали на підставі наявності таких симптомів, як біль у горлі в стані спокою та при ковтанні, гіперемія та набряк мигдалин із можливими пробками на мигдалинах, шийний лімфаденіт та пірексія. Небактеріальний тонзиліт був діагностований за умови оцінки 1-3 бали за шкалою МакАйзека у пацієнтів віком 3-14 років та 0-2 бали за шкалою CENTIR у пацієнтів віком старше 15 років.
Критерії включення: суб’єкти чоловічої та жіночої статі віком від 6 до 18 років, які проходили амбулаторну терапію з діагнозом «гострий небактеріальний тонзиліт»; можливість розпочати терапію протягом 72 год із моменту появи симптомів захворювання; оцінка 1-3 бали за шкалою МакАйзека в пацієнтів віком 3-14 років, оцінка 0-2 бали за шкалою CENTOR у пацієнтів віком старше 15 років; готовність і здатність пацієнта та (або) його батьків виконати вимоги протоколу дослідження; підписана інформована згода.
Критерії виведення пацієнта з дослідження: рішення пацієнта та (або) його батьків припинити участь у дослідженні та відкликання письмової інформованої згоди; втрата контакту з пацієнтом; індивідуальна непереносимість досліджуваного лікарського засобу та стандартної схеми лікування; розвиток серйозних та/або несподіваних небажаних явищ/реакцій у пацієнта під час дослідження; значне погіршення загального стану; розвиток ускладнення основного захворювання, яке, на думку дослідника, вимагає виведення пацієнта з дослідження; порушення пацієнтом процедур, передбачених протоколом; призначення системної АБТ.
Критерії невключення: оцінка 3-5 балів за шкалою МакАйзека та 3-4 бали за шкалою CENTRO; наявність показань до негайного початку системної АБТ; підозра на інфекційний мононуклеоз (за клінічними ознаками); застосування системних антибактеріальних або протигрибкових засобів, системних глюкокортикостероїдів, цитостатиків протягом останніх 14 днів; непереносимість або індивідуальна підвищена чутливість до будь-якого складника лікарського засобу та стандартної схеми лікування.
Пацієнти обох груп були порівнянні за статтю, віком і клінічними проявами захворювання (р<0,05).
Втручання
Починаючи з рандомізації, пацієнтам двох груп призначали сувору дієту, виключення подразників (фізичних і хімічних); ацетамінофен як жарознижувальний засіб у вікових дозах (за наявності відповідних показань – біль, серйозна гіпертермія), пероральний спрей бензидаміну гідрохлориду: 0,255 мкг бензидаміну гідрохлориду – 1 натискання. Доза становить 4 натискання 3-4 рази на добу протягом 10 днів. Пацієнтам групи лікування додатково призначали BNO 1030 (Імупрет®) – пероральні краплі в таких дозах: при гострих проявах захворювання (перші 5 днів) діти віком 6-11 років отримували по 15 крапель 6 разів на добу, діти віком ≥12 років – по 25 крапель 6 разів на добу. Після полегшення проявів гострого захворювання (5-10-й дні) діти віком 6-11 років отримували по 15 крапель 3 рази на добу, а віком ≥12 років – по 25 крапель 6 разів на добу.
Пероральні краплі BNO 1030 являють собою стандартизований спиртово-водний екстракт. Діючі речовини: 100 г крапель містять 29 г спиртово-водного екстракту (екстрагент: етанол 59% (об/об), виготовлений із таких лікарських рослин:
корінь алтею (radix Althaeae) – 0,4 г;
квіти ромашки (flos Chamomillae) – 0,3 г;
трава хвоща (herba Equiseti) – 0,5 г;
листя волоського горіха (folia Juglandis) – 0,4 г;
трава деревію (herba Millefolii) – 0,4 г;
кора дуба (cortex Quercus) – 0,2 г;
трава кульбаби (herba Taraxaci) – 0,4 г;
допоміжні речовини: етанол 19% (об/об), вода очищена.
Назва та адреса виробника: Bionorica SE, Kerschensteinerstrasse, 11-15, 92318, Neumarkt, Germany.
Препарат зареєстрований в Україні і доступний без рецепта. Таким чином, його лікарська форма, виготовлення, упаковка та маркування відповідають принципам належної виробничої практики та чинним національним вимогам України. Детальний опис, який охоплює всі аспекти щодо якості та безпеки крапель BNO 1030, є частиною відповідних характеристик лікарського засобу.
В Україні затверджені показання до застосування лікарського засобу включають лікування захворювань верхніх дихальних шляхів (тонзиліт, фарингіт, ларингіт) та профілактику ускладнень і рецидивів респіраторних вірусних інфекцій.
У дослідженні брали участь практикуючі лікарі – ЛОР-спеціалісти з досвідом роботи не менше 5 років.
Критерії ефективності
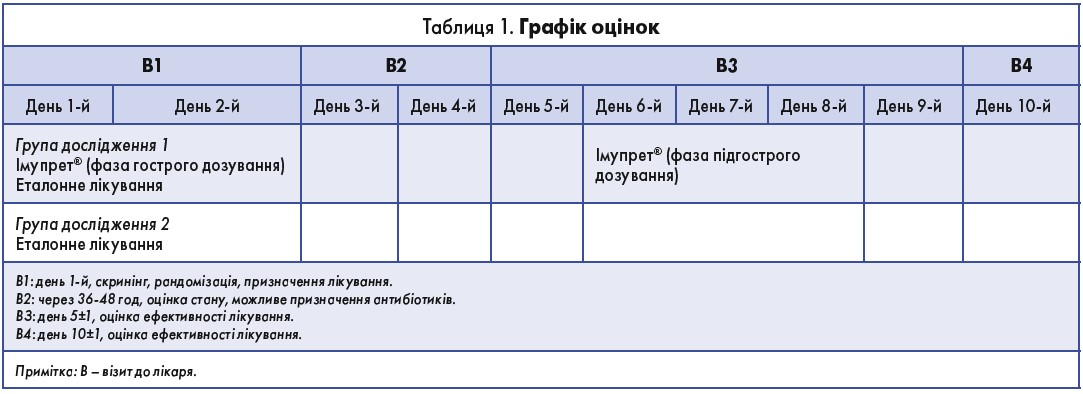
Всі дані оцінювалися лікарем на вихідному рівні та під час трьох наступних візитів протягом 10 днів (табл. 1).
Симптоми, що їх було включено до шкали місцевих проявів тонзиліту, оцінювалися при кожному візиті: гіперемія задньої стінки глотки, гіперемія, набряк і пробки на мигдалинах, біль у горлі в стані спокою і при ковтанні, подразнення горла, пов’язане з кашлем. Всі симптоми оцінювали за 4-бальною шкалою (0 – відсутній, 1 – легкий, 2 – помірний, 3 – тяжкий/виражений). Крім того, лікар оцінював загальний стан пацієнта при кожному візиті за 10-бальною візуально-аналоговою шкалою (ВАШ). Пацієнти у своїх щоденниках оцінювали свої скарги, такі як біль у горлі в стані спокою та при ковтанні, подразнення горла, кашель і загальний стан за ВАШ. Під час другого візиту (В2) лікар оцінював стан хворого і вирішував, чи потрібне призначення АБТ.
Основні критерії ефективності: зниження тяжкості симптомів захворювання, оцінюване за допомогою точкової шкали при кожному візиті у порівнянні з В1; динаміка оцінки лікарем і самооцінки пацієнтом загального стану; динаміка самооцінки пацієнтом симптомів тонзиліту. Вторинні критерії: зменшення загального балу (загальна кількість балів за кожний симптом) за бальною шкалою місцевих проявів тонзиліту при кожному візиті у порівнянні з В1; динаміка використання жарознижувальних засобів, а також оцінка «терапевтичної корисності» від застосування BNO 1030.
Обсяг вибірки
Клінічне дослідження було розроблене для отримання достовірного опису ефективності in vivo активного (додаткового) застосування BNO 1030 у порівнянні з еталонною стандартною монотерапією. Залежно від зібраних даних було проведено кілька описових і статистичних оцінок; тому біометрична оцінка розміру вибірки не потрібна. Проте для забезпечення достатнього розміру вибірки для аналізу отриманих даних було обрано розмір вибірки n=250. Пацієнтів було рандомізовано в співвідношенні 1:1.
Рандомізація
Клінічна частина рандомізованого дослідження була відкритою, без процедури засліплення. Суб’єкти – випадковим чином розподілені до однієї з двох можливих груп лікування відповідно до основного рандомізаційного списку. Рандомізацію проводили за допомогою програмного забезпечення (StatSoft – генератор випадкових чисел) для кожного пацієнта, який підписував інформовану згоду.
Статистичні методи
Для аналізу однорідності груп використовувалися описові методи статистики для опису вихідного стану групи лікування та контрольної групи (для кількісних параметрів – n, середнє арифметичне, медіана, стандартне відхилення, мінімальні та максимальні значення; для якісних параметрів – частота і частка у%). Перевірка нормальності розподілу даних у групах здійснювалася для кількісних параметрів за допомогою критерію Шапіро-Уілка. Якщо дані в групах показували нормальний розподіл за певними параметрами, групи порівнювали за цими параметрами за допомогою t-критерію Стьюдента для незалежних вибірок. В іншому випадку (якщо розподіл даних був відмінним від нормального) порівняння груп проводили згідно з критерієм Манна-Уітні. Для категоріальних параметрів групи порівнювали з використанням критерію узгодженості Пірсона (критерій хі-квадрат) або точного критерію Фішера.
Для аналізу ефективності були розраховані параметри описової статистики в кожній групі (n, середнє арифметичне, медіана, стандартне відхилення, мінімальні та максимальні значення) для всіх візитів відповідно до схеми обстеження пацієнтів.
Аналіз динаміки зазначених параметрів у кожній групі здійснювався за допомогою двостороннього дисперсійного аналізу (ANOVA) за наступною схемою: показник «Візит» фіксований (рівні: візит 1… візит n); показник «Суб’єкти» є випадковим.
Результати наступних візитів порівнювали під час В1 за допомогою контрастного аналізу з використанням простих контрастів.
Порівняння між групами в динаміці випробовуваних параметрів проводили за допомогою відмінностей dTi = (Т Візит n – Т Візит 1) оцінених параметрів із використанням критерію Манна-Уітні.
Рівень достовірності критерію Шапіро-Уілка був прийнятий рівним 0,01, а для решти критеріїв – рівним 0,05.
Аналіз проводили в програмному забезпеченні IBM SPSS 22.0.
Результати
Досліджувана вибірка
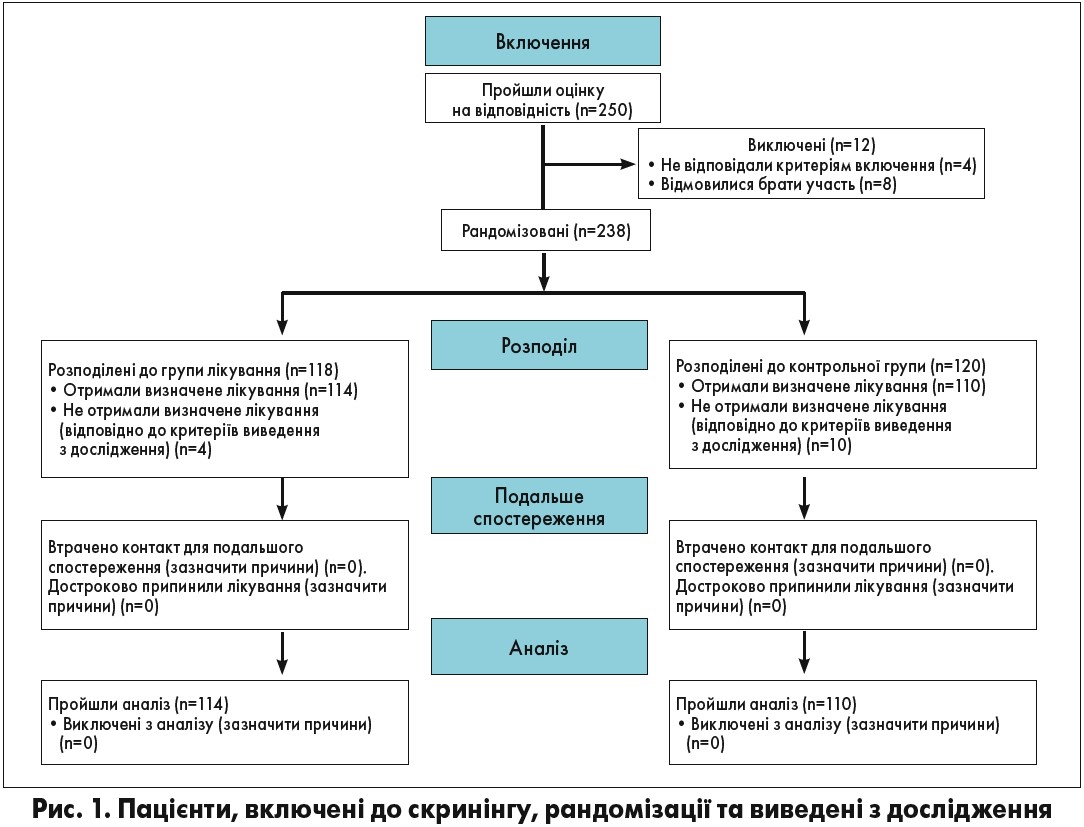
Для участі в дослідженні відібрано 250 пацієнтів віком 6-18 років (рис. 1). Дванадцять (4,8%) із них були виключені з дослідження з різних причин: через вік, що перевищував вікові критерії (n=4), і небажання пацієнта та (або) його батьків виконувати вимоги протоколу (n=8). Решта 238 пацієнтів були рандомізовані на 2 групи: контрольну (n=120) та групу лікування (n=118). Наступного дня 14 (11,7%) пацієнтів були виведені з дослідження через наявність одного з критеріїв виведення, а саме призначення системної АБТ: 10 учасників із контрольної групи та 4 пацієнти з групи лікування. Так, з червня 2017 по березень 2018 року 224 (94,1%) рандомізованих пацієнти з групи лікування та контрольної групи (114 та 110 відповідно) завершили дослідження в повному обсязі, а отримані результати були проаналізовані.
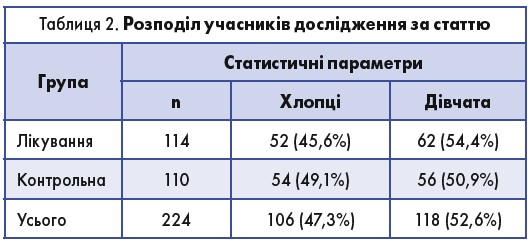 У таблиці 2 та таблиці 3 представлений розподіл учасників обох груп за статтю та віком відповідно.
У таблиці 2 та таблиці 3 представлений розподіл учасників обох груп за статтю та віком відповідно.
Середній вік пацієнтів із групи лікування та з контрольної групи становив 9,16 року: 8,67±3,219 та 9,66±3,296 відповідно.
Загалом, будь-які відмінності між вихідними (1-й день) демографічними характеристиками пацієнтів у групі лікування та контрольній групі відсутні (р>0,05).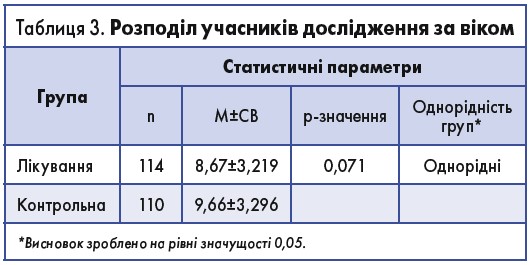
У таблиці 4 наведено порівняльні характеристики групи лікування та контрольної групи за 4-бальною оцінкою ступеня тяжкості симптомів, включених до шкали місцевих проявів тонзиліту.
У пацієнтів обох груп (р>0,05) не було виявлено значущих відмінностей у проявах тонзиліту на вихідному рівні (1-й день): гіперемія задньої стінки глотки, гіперемія, набряк і пробки на мигдалинах, біль у горлі в стані спокою та при ковтанні, подразнення горла, пов’язане з кашлем.
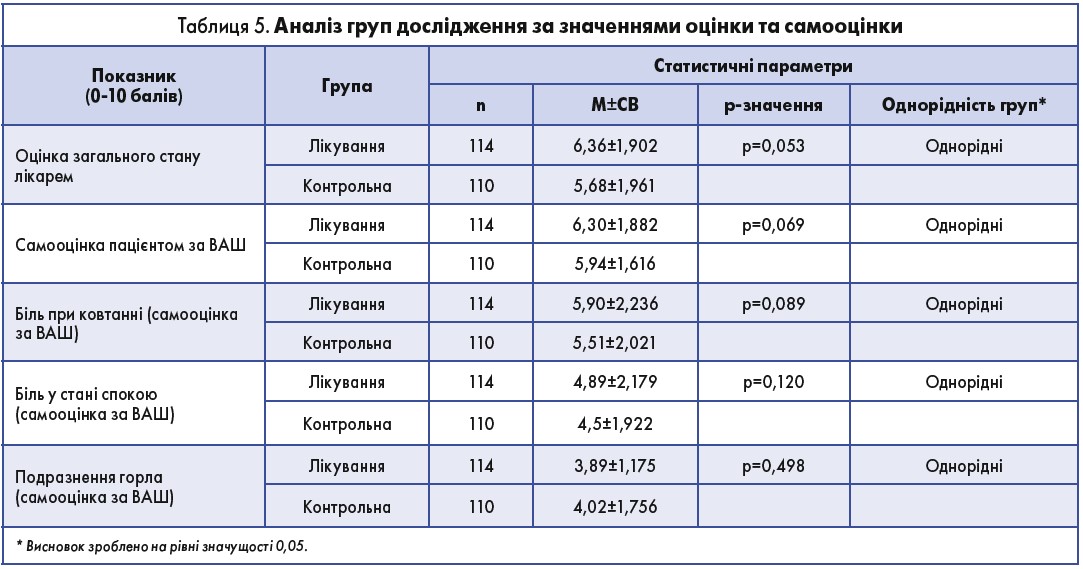
У таблиці 5 наведено порівняльні характеристики обох груп лікування за 10-бальною оцінкою лікарем та самооцінкою пацієнтом (за ВАШ) свого загального стану й тяжкості симптомів тонзиліту.
Значущих відмінностей у вихідній (1-й день) оцінці загального стану лікарем та самооцінці пацієнтом, а також самооцінці тяжкості симптомів тонзиліту пацієнтом: біль у горлі в стані спокою та при ковтанні, подразнення горла, пов’язане з кашлем, між пацієнтами обох груп не зазначалося (р>0,05).
Результати й оцінка
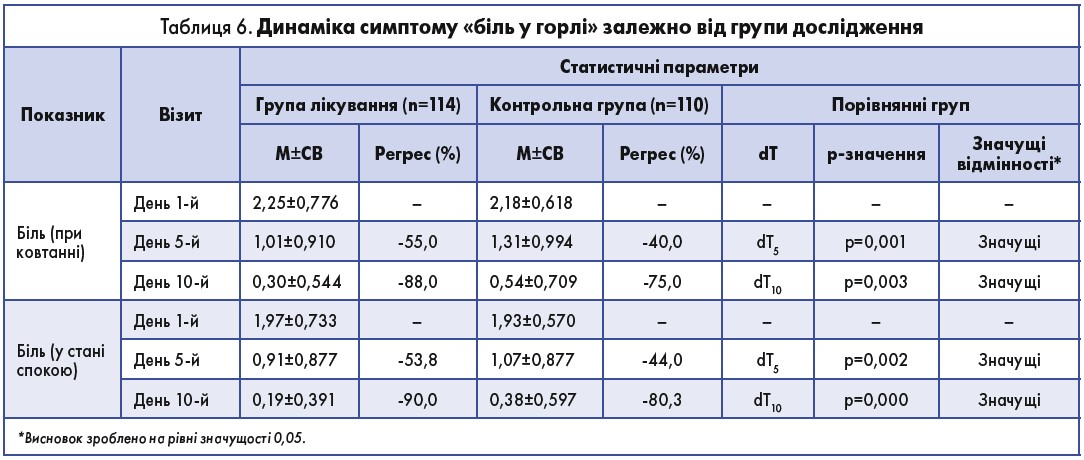
Найважливішим для пацієнта з ГТ клінічним проявом є біль у горлі. У таблиці 6 представлено оцінку динаміки симптому «біль у горлі в стані спокою та при ковтанні» у пацієнтів обох груп.
Під час терапії у хворих обох груп спостерігався регрес симптому «біль у горлі при ковтанні»: з 2,25±0,776 до 1,01±0,910 бала (-55%) на 5-й день та до 0,30±0,544 бала (-88%) на 10-й день у пацієнтів із групи лікування та з 2,18±0,618 до 1,31±0,994 бала (-40%) на 5-й день і до 0,54±0,709 бала (-75%) на 10-й день в учасників із контрольної групи. Таким чином, додаткове застосування лікарського засобу Імупрет® у стандартній терапії сприяє регресу симптому «біль у горлі при ковтанні» до 55% у порівнянні з 40% при стандартній терапії до 5-го дня. Порівняння регресійних показників симптому «болю в горлі при ковтанні» між групами показує достовірні відмінності на 5-й і 10-й день лікування (р<0,05).
При порівнянні динаміки симптому «біль у горлі в стані спокою» регрес цього симптому також спостерігався в пацієнтів обох груп: від 1,97±0,733 до 0,91±0,877 бала (-53,8%) бала на 5-й день і до 0,19±0,391 бала (-90%) на 10-й день у групі лікування. У контрольній групі він знизився з 1,93±0,570 до 1,07±0,877 бала (-44%) на 5-й день і до 0,38±0,597 бала (-80,3%) на 10-й день. Порівняння регресійних показників симптому «біль у горлі в стані спокою» між групами виявляє значущі відмінності на 5-й і 10-й дні лікування (р<0,05).
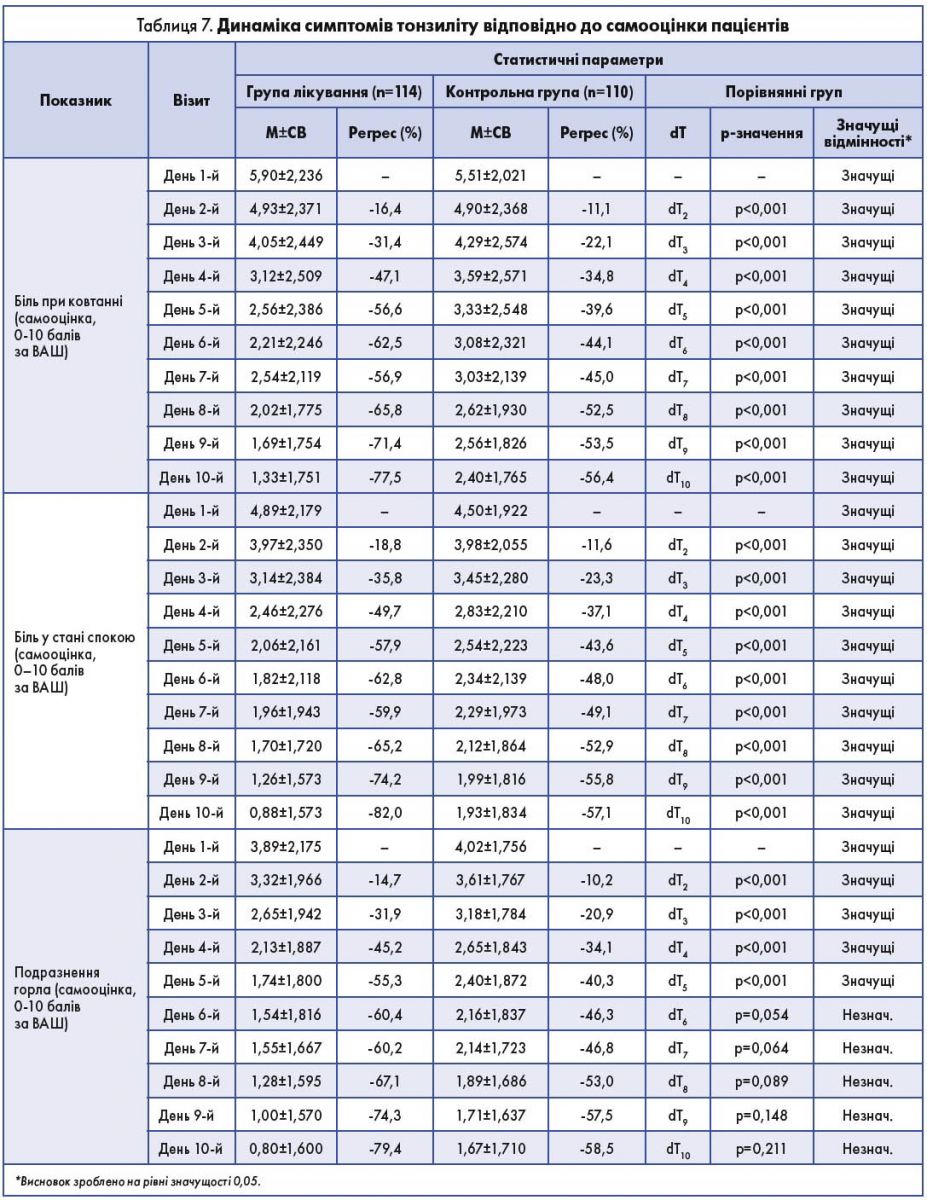
Пацієнти обох груп кожного дня заносили в щоденник оцінку своїх скарг на біль у горлі за 10-бальною ВАШ (табл. 7).
Відповідно до самооцінки в пацієнтів обох груп дослідження спостерігається регрес симптому «біль у горлі при ковтанні»: від 5,90±2,236 до 4,93±2,371 бала (-16,4%) на 2-й день і до 1,33±1,751 бала (-77,5%) на 10-й день у пацієнтів групи лікування. У пацієнтів контрольної групи він знизився з 5,51±2,021 до 4,90±2,368 бала (-1,1,1%) на 2-й і до 2,40±1,765 бала (-56,4%) на 10-й день.
Подібну динаміку самооцінки спостерігали за симптомом «біль у горлі в стані спокою». У пацієнтів групи лікування симптом знизився з 4,89±2,179 до 3,97±2,350 бала (-18,8%) на 2-й і до 0,88±1,573 бала (-82,0%) на 10-й день. Він регресував з 4,50±1,922 до 3,98±2,055 бала (-11,6%) на 2-й день і до 1,93±1,834 бала (-57,1%) на 10-й день у пацієнтів контрольної групи. Порівняння регресійних показників симптому «біль у горлі при ковтанні» відповідно до самооцінки пацієнтів між групами показує значущі відмінності з 2-го до 10-го дня лікування (р<0,05).
Добре відомо, що наявність такого симптому, як подразнення горла, пов’язане з кашлем, є однією з диференційних ознак вірусного (небактеріального) тонзиліту. Пацієнти обох груп проводили самооцінку тяжкості цього симптому під час терапії. Регрес цього симптому спостерігався в пацієнтів групи лікування з 3,89±2,175 до 3,32±1,966 бала (-14,7%) на 2-й день до 1,74±1,800 бала (-55,3%) на 5-й і до 0,80±1,600 бала (-79,4%) на 10-й день. У пацієнтів контрольної групи він знизився з 4,02±1,7756 до 3,61±1,7767 бала (-10,2%) на 2-й день, до 2,40±1,872 бала (-40,3%) на 5-й день і до 1,67±1,710 бала (–58,5%) на 10-й день. Порівняння регресійної динаміки симптому «подразнення горла, пов’язане з кашлем» у пацієнтів обох груп показує значущу різницю на 5-й день лікування (р<0,05). Починаючи з 6-го дня не спостерігалося суттєвих відмінностей у швидкості регресу цього симптому (р>0,05). Таким чином, група лікування демонструє більш швидкий регрес подразнення горла, пов’язаного з кашлем.
Гострий тонзиліт – це захворювання, завжди пов’язане з погіршенням загального стану. Ми провели оцінку динаміки цього показника за результатами оцінки лікаря та самооцінки пацієнта за 10-бальною ВАШ (табл. 8).
Як можна побачити з таблиці, оцінка загального стану лікарем у групі лікування показала поліпшення цього показника з 6,36±1,902 до 3,09±2,446 бала (-51,4%) на 5-й і до 1,04±1,554 бала (-83,6) на 10-й день. У контрольній групі – з 5,68±1,961 до 3,29±2,526 бала (-42,1%) на 5-й і до 1,52±1,724 бала (-73,2%) на 10-й день лікування. Порівняння динамічних показників поліпшення загального стану пацієнта за оцінкою лікаря показало значну різницю між групами на 5-й і 10-й день лікування (р<0,05).
Зіставні результати було виявлено при самооцінці хворого: з 6,30±1,882 бала на 1-й до 1,66±1,860 бала (-73,7%) на 10-й день у групі лікування та з 5,94±1,616 бала на 1-й день до 2,72±1,565 бала (-54,2%) на 10-й день у контрольній групі. Порівняння параметрів самооцінки показує значну різницю (р<0,05) в параметрах між групами починаючи з 2-го й до 10-го дня лікування.
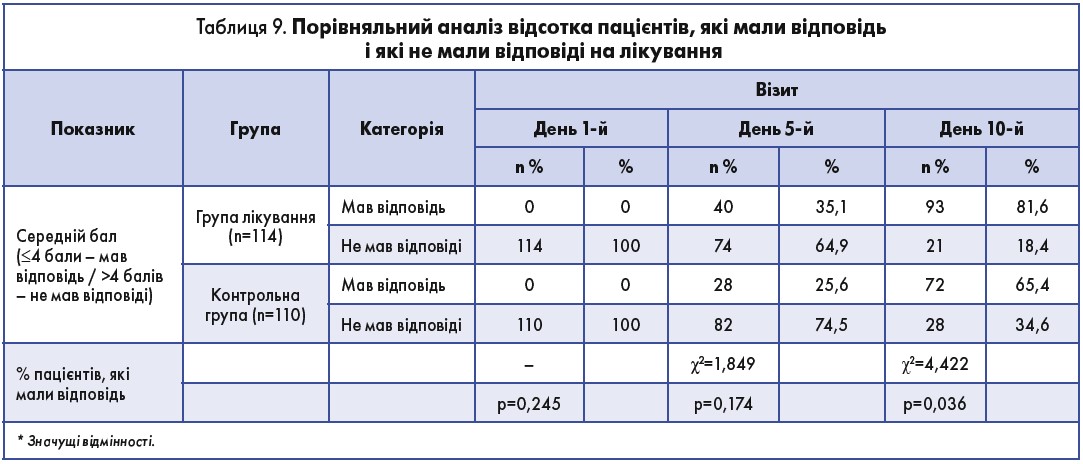
Було здійснено порівняння між групами дослідження щодо кількості пацієнтів, які мали відповідь і які не мали відповіді на лікування (зниження сумарного показника за шкалою основних проявів тонзиліту до ≤4 балів) (табл. 9).
На 10-й день 93 учасники зі 114 пацієнтів із групи лікування відповіли на терапію, а 21 хворий не відповів (81,6 проти 18,4% відповідно); зі 110 учасників із контрольної групи 72 пацієнти мали відповідь, а 38 хворих не мали відповіді (65,4 проти 34,6%).
На 10-й день параметри пацієнтів із відповіддю на терапію між групами були достовірно різними (р<0,05).
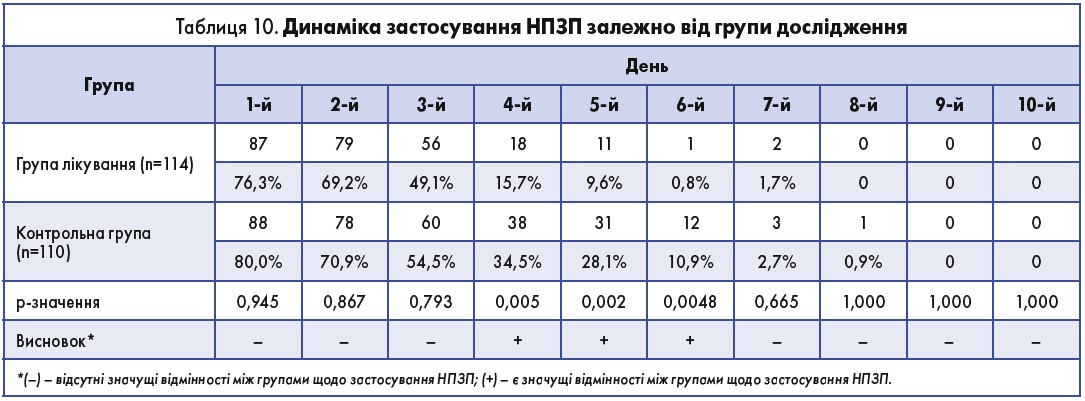
Покращання місцевих симптомів і загального стану призвело до зниження рівня застосування жарознижувальних засобів. Ми провели оцінку динаміки застосування нестероїдних протизапальних препаратів (НПЗП) (табл. 10). Ураховувався день останньої дози лікарського засобу цієї групи.
Значуща відмінність спостерігається в частоті випадків застосування жарознижувальних засобів між пацієнтами обох груп починаючи з 4-го дня лікування (р<0,05).
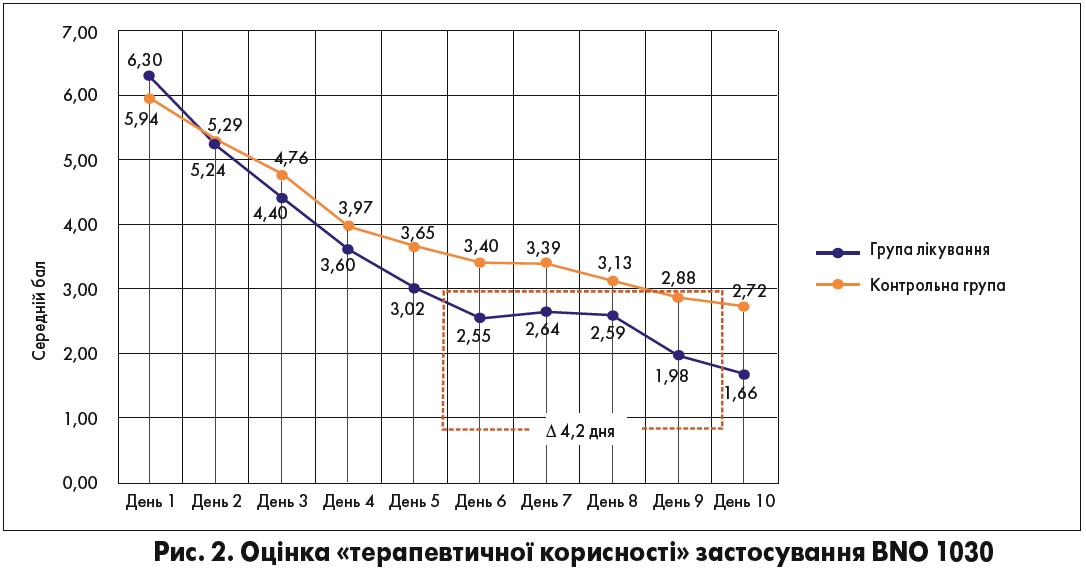
Ми провели оцінку «терапевтичної корисності» від застосування BNO 1030 у пацієнтів із ГТ. Вона базувалася на порівнянні параметрів динаміки загального стану (представлена у вигляді шкали) (рис. 2).
Як видно з рисунка, наприкінці дослідження (10-й день) пацієнти контрольної групи оцінили свій загальний стан на рівні 2,72 бала за ВАШ, що збігалося з показником самооцінки пацієнтів групи лікування до кінця 5-го дня терапії. Отже, «терапевтична корисність» у лікуванні учасників групи лікування становить 4,2 дня у порівнянні з результатами терапії пацієнтів контрольної групи.
Безпека та переносимість
Результати оцінки переносимості лікування показали, що воно переноситься добре або дуже добре у всіх випадках. У пацієнтів у процесі лікування не було зареєстровано жодних небажаних явищ.
Обговорення
Пацієнти із запальними захворюваннями мигдалин часто використовують фітотерапевтичні лікарські засоби. Проте найновіші рекомендації, що ґрунтуються на доведеній ефективності терапії ГТ, включають лише симптоматичний засіб для полегшення симптомів [1, 5, 6]. Для цього успішно застосовують системні (ацетамінофен або ібупрофен) і місцеві (бензидамін) НПЗП. У зв’язку з цим є потреба в проведенні достовірних (з погляду дотримання стандартів GСР) досліджень ефективності фітотерапевтичних лікарських засобів, зокрема BNO 1030, для лікування ГТ.
Це дослідження продемонструвало, що застосування фітотерапевтичного лікарського засобу, який містить водно-спиртовий екстракт, BNO 1030, як доповнення до стандартної симптоматичної терапії, має доведений терапевтичний ефект. У пацієнтів із групи прийому BNO 1030 було зареєстроване значуще зниження тяжкості симптомів захворювання – до ≤1 балу (оцінюваних лікарем за 4-бальною шкалою) на 5-й і 10-й дні лікування. Достовірні відмінності в динаміці самооцінки симптомів тонзиліту у хворих були зазначені з 2-го до 10-го дня лікування.
Наші результати збігаються з даними літератури [18, 20]. Результати цих досліджень показали, що BNO 1030 (Тонзилгон® N, Імупрет®) ефективний у лікуванні гострих респіраторних вірусних інфекцій і рецидивуючого тонзиліту в педіатричних пацієнтів. Наші результати також підтверджуються даними, отриманими в ході дослідження німецьких науковців, яке продемонструвало ефективність і безпеку лікарського засобу в понад 1100 дітей із рецидивуючими гострими інфекціями верхніх дихальних шляхів [19].
Гострий тонзиліт – захворювання, яке завжди супроводжується вираженим загальним розладом. Це пояснюється тим, що піднебінні мигдалини є одними з основних складових імунної системи, а їхнє запалення пов’язане з вираженими системними ефектами. Дослідження показало достовірно переважну динаміку поліпшення загального стану пацієнтів у групі лікування відповідно до оцінки лікарем і самооцінки пацієнта. Такий клінічний ефект підтверджує раніше опубліковані дані про імунологічну ефективність BNO 1030 in vitro та in vivo [26-28].
Важливим і цікавим висновком цього дослідження є те, що завдяки вираженому регресу таких симптомів, як біль у горлі та його подразнення, а також покращанню загального стану пацієнти в групі BNO 1030 застосовували в цілому менше протизапальних засобів (ацетамінофен). Багато дослідників упевнені, що біль у горлі у хворих на ГТ часто призводить як до необґрунтованого призначення антибіотиків лікарями, так і до готовності пацієнтів до застосування АБТ; на жаль, саме це чи не найголовніша причина виникнення такої глобальної проблеми світової медицини, як резистентність до антибіотиків [2, 23, 24]. Однією зі стратегій зменшення застосування антибіотиків у дорослих і дітей із неускладненими гострими респіраторними інфекціями є відстрочення призначення антибіотиків [25]. Більш швидкий регрес больового синдрому в пацієнтів, які отримують Імупрет®, продемонстрований у нашому дослідженні, є важливою причиною зниження прихильності пацієнтів і лікарів до застосування антибіотиків. У нашій роботі призначення антибіотиків було критерієм виведення пацієнта з дослідження, наприклад саме з цієї причини 14 хворих було виключено з дослідження під час В2 (10 – у контрольній групі і 4 – у групі лікування). Ці дані не є значущими, проте вони демонструють тенденцію до зниження призначення антибіотиків у групі, що застосовувала BNO 1030.
Ефективність BNO 1030 у цілому підтверджує результати попередніх досліджень за участю пацієнтів із гострими вірусними інфекціями [18-20]. Хай там як, його сильною стороною є діагноз ГТ (J03), встановлений згідно з прийнятими критеріями. Група рандомізованих пацієнтів, зіставних за діагнозом і клінічними проявами, дозволила зробити обґрунтовані висновки щодо оцінки загального результату лікування. Кількість хворих, які мали відповідь на лікування, була значно вищою в групі лікування у порівнянні з контрольною групою. «Терапевтична корисність» у лікуванні пацієнтів основної групи становить 4,2 дня, що відображає значну перевагу в кількості відповідей на лікування. Це дає можливість зменшити кількість днів відсутності дітей у школі або дошкільних установах.
Дизайн передбачав порівняльне дослідження, яке не дозволило здійснити контроль із застосуванням «плацебо». Проте порівняння проводилося проти терапії, проведеної відповідно до клінічних рекомендацій, які передбачають обов’язкове призначення симптоматичної терапії лише за допомогою системних і місцевих НПЗП [1, 21]. Завдяки цьому всі відмінності в результатах лікування можна пояснити клінічними ефектами BNO 1030.
Висновок
Додаткове застосування фітонірингового лікарського засобу BNO 1030 (Імупрет®) для лікування ГТ сприяє значному зниженню клінічних симптомів тонзиліту, поліпшенню оцінки загального стану пацієнтів та якості їхнього життя, зниженню частоти застосування жарознижувальних засобів і загальної тривалості лікування без будь-яких небажаних явищ. Включення цього лікарського засобу в схему лікування може бути рекомендоване пацієнтам із гострим небактеріальним тонзилітом.
Перспективи подальших наукових пошуків полягають у дослідженні протирецидивної ефективності препарату в пацієнтів із рецидивуючим тонзилітом.
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Popovych V.I. Am J Otolaryngol, https://doi.org/10.1016/j.amjoto.2018.10.012
За підтримки ТОВ «Біонорика».
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 2 (47), 2019 р.