13 вересня, 2019
Применение комбинации левосимендана и добутамина у больной с критическими проявлениями острой декомпенсированной сердечной недостаточности
Острая декомпенсированная сердечная недостаточность (ОДСН) – это симптомокомплекс, возникающий при нарушении насосной функции сердца: снижении сердечного выброса (СВ), недостаточной перфузии тканей, повышенном давлении в легочных капиллярах, застое в тканях. Наиболее частой причиной (60-70%) ОДСН является ишемическая болезнь сердца (ИБС) [1, 2].
Особенно высока смертность при острых формах ИБС, сопровождающихся развитием ОСН. Так, в случае регистрации ОСН при остром инфаркте миокарда (ОИМ) летальность достигает 30% в течение первого года [3]. Вместе с тем развитие отека легких без ОИМ как проявление декомпенсации хронического процесса является еще более тяжелым состоянием: внутрибольничная летальность составляет 12%, а смерть в течение года регистрируется в 40% случаев [4, 5]. Около 45% пациентов, госпитализированных с ОДСН, в течение последующего года повторно поступают в стационар хотя бы один раз [6, 7]. Риск смерти или повторной госпитализации в течение 60 суток составляет, по данным различных исследователей, от 30 до 60% [8-10]. Улучшить клинический исход при ОСН можно с помощью ранней диагностики и правильно выбранной тактики лечения, ведущей к более адекватной и длительной стабилизации состояния.
Диагноз ОСН ставится на основании характерных жалоб больного, клинических симптомов и результатов дополнительных методов обследования, таких как электрокардиография (ЭКГ), рентгенография грудной клетки, эхокардиография (ЭхоКГ), определение уровня специфических биомаркеров в крови (рис. 1) [11].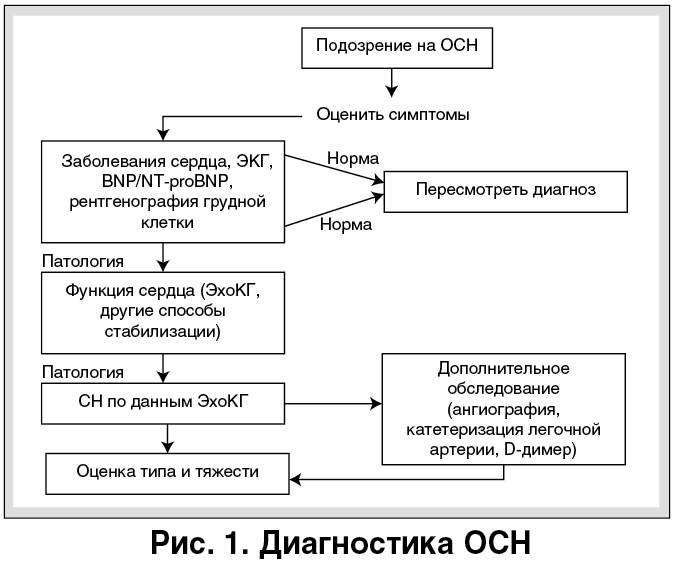
Терапевтическая тактика в лечении ОДСН направлена на уменьшение пред- и постнагрузки, улучшение транспорта кислорода, снижение давления в системе легочной артерии.
Инотропная терапия при ОДСН применяется, как правило, при неэффективности стандартных методов – ограничении возможностей наращивания дозы мочегонных и нитратов в связи с артериальной гипотензией, уменьшением диуреза. В последнее время появился ряд новых препаратов, обладающих положительным инотропным эффектом и имеющих различные механизмы действия, которые сопровождаются характерным электрофизиологическим профилем. В связи с этим было предложено несколько классификаций, среди которых стоит выделить таковую A. Varro, J. Papp [15]:
I класс – позитивная инотропия связана с усилением трансмембранного тока кальция внутри кардиомиоцитов с увеличением содержания в них циклического аденозинмонофосфата (цАМФ) в результате:
- IA – β-адренергической стимуляции, которая активирует G-протеин аденилатциклазы (добутамин);
- IB – ингибирования фосфодиэстеразы (ФДЭ), которая снижает скорость катаболизма цАМФ; достоинством ингибиторов ФДЭ является сочетание положительного инотропного эффекта с вазодилатацией, отрицательное же качество заключается в том, что они вызывают склонность к аритмиям, увеличивая летальность при длительном применении, особенно при наличии ИБС (амринон, милринон);
- IC – прямой активации аденилатциклазы; эти препараты могут удлинять продолжительность потенциала действия и увеличивать частоту сердечного ритма (форсколин);
- ID – модуляции кальциевых каналов L-типа; электрофизиологические эффекты BAY-K 8644 могут быть полностью устранены под влиянием нифедипина и других дигидропиридинов.
II класс – эти препараты различными путями усиливают внутриклеточную активность натрия:
- IIА – торможение натрий-калиевого насоса; к этой подгруппе относятся сердечные гликозиды, которые угнетают натрий-калиевую АТФазу, повышая уровень внутриклеточного натрия, и уменьшают натрий-кальциевый обмен с ростом внутриклеточного содержания кальция, одновременно уменьшается содержание внутриклеточного калия; гликозиды могут разнообразно влиять на реполяризацию (укорачивать, удлинять, не менять), что зависит от их концентрации и, соответственно, действия на различные токи ионов, участвующих в реполяризации;
- IIВ – усиление трансмембранного притока натрия через вольтаж-чувствительные натриевые каналы; известные препараты этой группы не применяются клинически в связи с высокой общей токсичностью, хотя некоторые обладают рядом благоприятных для кровообращения эффектов (включая вазодилатацию), например DPJ 201-106.
III класс – в отличие от предыдущих средств, которые усиливают инотропную функцию в результате повышения эффектов внутриклеточного кальция, препараты этого класса увеличивают чувствительность миофиламентов кардиомиоцитов к внутриклеточному кальцию – так называемый феномен сенситизации (левосимендан).
IV класс – препараты, удлиняющие реполяризацию и усиливающие сократимость (веснаринон). При этом происходит накопление кальция в миокарде. Эти препараты часто обладают комбинированным действием (включая ингибирование ФДЭ). Несмотря на подобные эффекты, веснаринон урежает сердечный ритм.
Наибольшую положительную доказательную базу среди инотропных препаратов имеют добутамин и левосимендан. При этом необходимо отметить преимущества, полученные левосименданом в сравнительных исследованиях с добутамином.
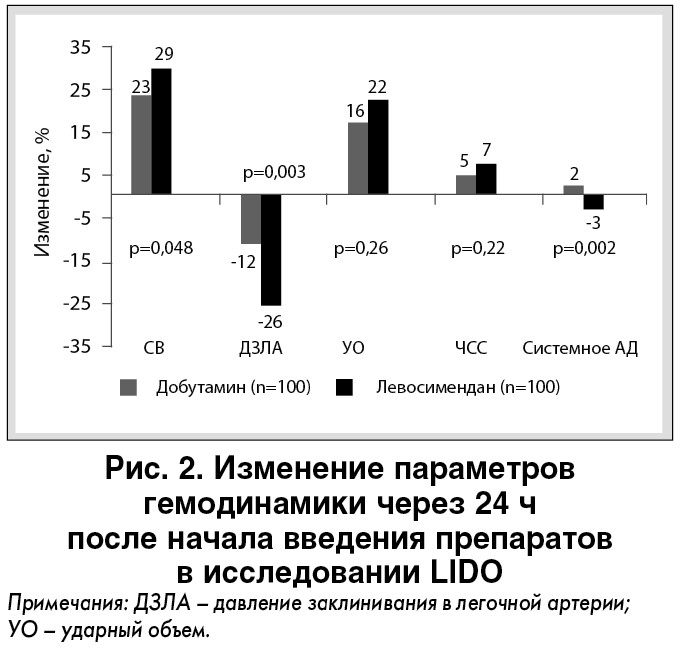 Данные многоцентровых рандомизированных исследований (LIDO, CASINO и RUSSLAN) продемонстрировали достоверное влияние на показатели внутрисердечной и системной гемодинамики как добутамина, так и левосимендана. Несмотря на более выраженное влияние левосимендана на внутрисердечную гемодинамику – повышение СВ и уменьшение давления заклинивания в легочной артерии, его использование вызывало некоторое снижение системного артериального давления – АД (в отличие от добутамина). Это было показано в испытании LIDO (рис. 2) [16].
Данные многоцентровых рандомизированных исследований (LIDO, CASINO и RUSSLAN) продемонстрировали достоверное влияние на показатели внутрисердечной и системной гемодинамики как добутамина, так и левосимендана. Несмотря на более выраженное влияние левосимендана на внутрисердечную гемодинамику – повышение СВ и уменьшение давления заклинивания в легочной артерии, его использование вызывало некоторое снижение системного артериального давления – АД (в отличие от добутамина). Это было показано в испытании LIDO (рис. 2) [16].
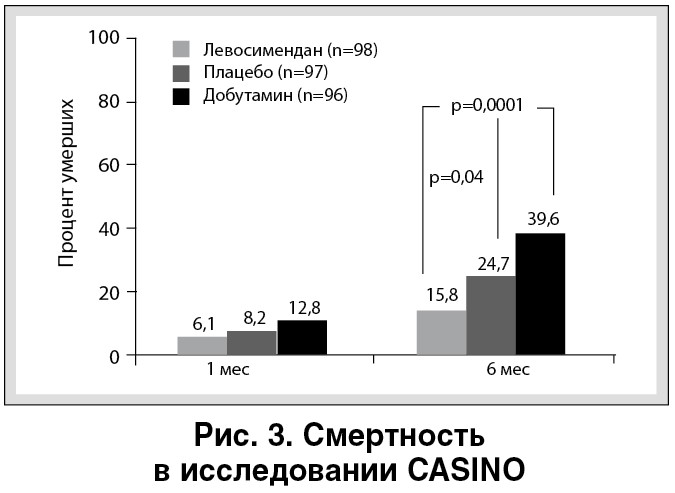
Наличие положительных гемодинамических эффектов левосимендана у больных ОДСН в дальнейших исследованиях нашло отражение в снижении риска смерти при его использовании по сравнению с плацебо (RUSSLAN, CASINO) и в сравнении с применением добутамина (LIDO, CASINO) (рис. 3) [16-18].
 Эффективность применения левосимендана в лечении ОСН доказана не только для ОДСН при хронической СН, но и при ОСН denovо – острой левожелудочковой недостаточности, возникшей вследствие развития ОИМ, по результатам многоцентровых исследований REVIVE II, SURVIVE.
Эффективность применения левосимендана в лечении ОСН доказана не только для ОДСН при хронической СН, но и при ОСН denovо – острой левожелудочковой недостаточности, возникшей вследствие развития ОИМ, по результатам многоцентровых исследований REVIVE II, SURVIVE.
Эффективность левосимендана при ОДСН в последние годы привела к его широкому использованию в странах Европы (в США он не зарегистрирован), но было определено и главное ограничение его применения – артериальная гипотензия. Эта особенность напрямую связана с механизмом действия препарата. Кроме инотропной активности, он обладает вазодилатирующим действием вследствие активации АТФ-зависимых калиевых каналов митохондрий гладкомышечных клеток сосудов. Есть такое влияние и на кардиомиоциты, что обеспечивает дополнительный кардиопротекторный эффект препарата. Подобный двойной механизм действия левосимендана позволил отнести его к группе иновазодилататоров. Поэтому с целью преодоления основного ограничения использования левосимендана у больных со сниженным АД были предприняты попытки комбинации левосимендана и прессорных аминов, в том числе добутамина.
В одном из первых исследований по изучению сочетанного применения адреномиметиков и левосимендана при резистентной к добутамину ОДСН отмечалась высокая эффективность данной комбинации [12]. В последующих исследованиях у больных тяжелой декомпенсированной СН, резистентной к терапии добутамином, перед хирургическим лечением было показано преимущество комбинированного лечения с использованием левосимендана перед совместным приемом добутамина и милринона. Эта комбинация была безопасна, эффективна, а терапевтическое действие продолжалось в течение семи дней от начала терапии. Во всех случаях данная терапия привела к устойчивому снижению давления наполнения желудочков сердца и увеличению сердечного индекса, что позволило выписать таких тяжелых больных из клиники [13, 14].
Наша клиника также располагает опытом использования левосимендана как в качестве самостоятельного агента, так и совместно с добутамином. Приводим следующий клинический случай, иллюстрирующий возможности комбинированной терапии у крайне тяжелой больной.
Пример комбинированной терапии с использованием левосимендана и добутамина
Больная Л. перенесла Q-ИМ передне-перегородочно-верхушечной локализации (13.09.09). В связи с развитием ранней постинфарктной стенокардии ей были проведены коронаровентрикулография и последующее стентирование передней межжелудочковой ветви и огибающей ветви левой коронарной артерии (08.10.09), установлено четыре стента с лекарственным покрытием. Хроническая аневризма верхушки левого желудочка. Гипертоническая болезнь 3-й степени. СН IIБ (острая левожелудочковая недостаточность: Killip III 16-20.09.09, Killip II 21-22.09.09). На фоне проводимой терапии (80 мг/сут фуросемида, 25 мг/сут верошпирона, 6,25 мг/сут карведилола, 15 мг/сут ивабрадина, 5 мг/сут изосорбида динитрата, 10 мг/сут симвастатина, 75 мг/сут клоподогреля) состояние больной стабилизировалось, и на 19-е сутки она была выписана (05.11.09). Вместе с тем на фоне назначенного лечения у пациентки прогрессировали явления СН, она была госпитализирована повторно 3.12.09 с жалобами на одышку как в покое, так и при незначительной физической нагрузке, слабость, ортопноэ, ухудшение сна из-за одышки.
Лечение до поступления: 80 мг/сут фуросемида, 25 мг/сут верошпирона, 6,25 мг/сут карведилола, 5 мг/сут изосорбида динитрата, 10 мг/сут симвастатина, 75 мг/сут клопидогреля.
При объективном осмотре кожные покровы бледно-телесного цвета, видимые слизистые без особенностей. Тоны сердечной деятельности ослабленной звучности, ритмичные, дующий систолический шум на верхушке и в точке Боткина, акцент II тона на легочной артерии. АД при поступлении – 90/60 мм рт. ст., пульс – 75 уд./мин. Частота дыхания (ЧД) – 22-25 р/мин. В легких жесткое дыхание, влажные хрипы в нижних отделах до угла лопатки, ослабление дыхания справа. Живот мягкий, увеличен в объеме за счет асцита, печень выступает на 5-7 см из-под края реберной дуги. Отеки голеней и стоп умеренной выраженности.
 На ЭхоКГ: конечно-диастолический объем – 151 мл, фракция выброса – 42%, левое предсердие – 4,7 см, дискинез верхушки, гипокинез межжелудочковой перегородки, передней и боковой стенки, диастолическая дисфункция по рестриктивному типу, легочная гипертензия до 70 мм рт. ст., выраженная недостаточность митрального и трикуспидального клапанов (3+) (рис. 4).
На ЭхоКГ: конечно-диастолический объем – 151 мл, фракция выброса – 42%, левое предсердие – 4,7 см, дискинез верхушки, гипокинез межжелудочковой перегородки, передней и боковой стенки, диастолическая дисфункция по рестриктивному типу, легочная гипертензия до 70 мм рт. ст., выраженная недостаточность митрального и трикуспидального клапанов (3+) (рис. 4).
Диагноз при поступлении: ОДСН. ИБС: стенокардия напряжения IV функционального класса. Атеросклеротический и постинфарктный (13.09.09) кардиосклероз. Стентирование 8.10.09 (передняя межжелудочковая ветвь, огибающая ветвь левой коронарной артерии, правой коронарной артерии – четыре стента). Хроническая аневризма верхушки левого желудочка. Гипертоническая болезнь 3-й степени. СН IIБ степени (IV функциональный класс по NYHA).
При поступлении в стационар у больной произведена эвакуация 1300 мл жидкости из правой плевральной полости, после постановки центрального венного катетера назначено лечение: 3,125 мг 2 р/сут карведилола, 5 мг 2 р/сут ивабрадина, 75 мг/сут клопидогреля, 70 мг 2 р/сут триметазидина MR, 12,5 мг/сут эплеренона, 20 мг торасемида внутривенно капельно.
Первые сутки: больная отмечает уменьшение одышки, однако в ночное время она усиливалась. Вес больной – 62,5 кг. Почасовый диурез за сутки составил 33 мл/ч. АД – 85/60 мм рт. ст., пульс – 68 уд./мин. Данные лабораторных анализов: калий – 4,4 ммоль/л, натрий – 145 ммоль/л, билирубин – 14 мкмоль/л, креатинин – 118 мкмоль/л (клиренс креатинина составил 42 мл/мин), АЛТ – 28 ед/л, АСТ – 24 ед/л, креатинфосфокиназа (КФК) – 67 ед/л, глюкоза – 4,6 ммоль/л, альбумины крови – 36 г/л, гемоглобин – 179 г/л. В терапии больной был отменен торасемид, добавлен фуросемид внутривенно капельно (160 мг/сут), Корвитин по 1 г/сут, коррекция кислотно-щелочного баланса.
На 2-4-е сутки: на фоне проводимой терапии субъективное состояние пациентки оставалось тяжелым, тогда как АД сохранялось на уровне 85/55 мм рт. ст., пульс – 80 уд./мин, почасовый диурез на 2-3-и сутки составил 62 мл/ч. При этом клиренс креатинина возрос и составил 60 мл/мин.
На 5-е сутки: субъективное состояние больной ухудшалось – в покое нарастала одышка (ЧД – 25-28 р/мин), ортопноэ. Объективно: АД – 80/60 мм рт. ст., пульс – 80 уд./мин, при аускультации легкого в динамике увеличилось ослабление дыхания справа и притупление в нижних отделах легких, диурез – 35 мл/ч. В лабораторных анализах отмечен рост содержания мочевой кислоты до 705 мкмоль/л. Диагностическое УЗИ грудной полости выявило наличие плевральной жидкости, в связи с чем была проведена плевральная пункция справа: извлечено 1200 мл плевральной жидкости. Принято решение об отмене карведилола и ивабрадина.
На 6-е сутки: состояние больной ухудшилось – увеличилась одышка (ЧД – 25 р/мин), сохранялась гипотензия (АД – 75/55 мм рт. ст.) при отсутствии тахикардии без использования β-блокатора и ивабрадина (пульс оставался на уровне 65 уд./мин), отсутствовал ответ на терапию фуросемидом в дозе 160-240 мг/сут (диурез <12,5 мл/ч), прогрессивно ухудшалась функция почек (креатинин – 133 ммоль/л или клиренс креатинина – 37 мл/мин). Принято решение об инотропной поддержке путем внутривенного введения добутамина. После 4-часовой инфузии добутамина 2,5-10 мкг/кг/мин АД возросло до 90/60 мм рт. ст., однако диуретический ответ отсутствовал. Поэтому к инфузии добутамина была добавлена таковая левосимендана по схеме (таблица).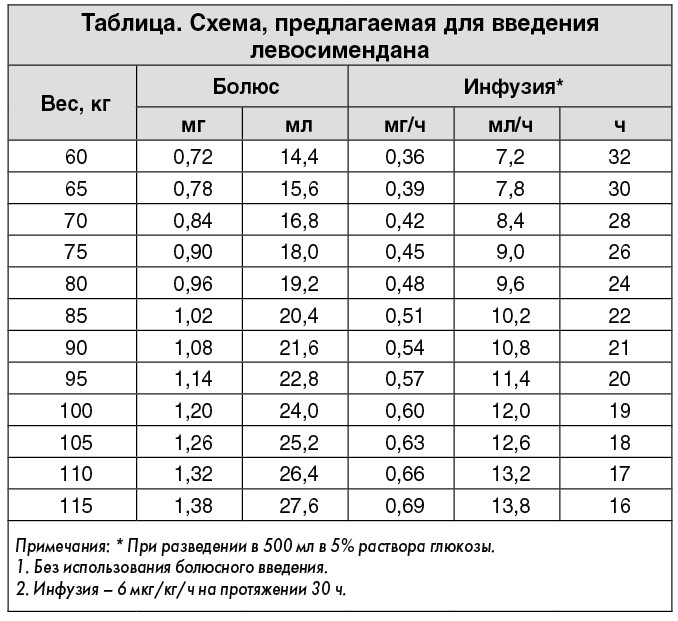
На 7-е сутки: на фоне постоянной инфузии комбинации левосимендана (0,1 мкг/кг/мин) с добутамином 2,5-10 мкг/кг/мин состояние больной остается тяжелым. АД – 90/70 мм рт. ст., пульс – 75 уд./мин, диурез – 29 мл/ч, ЧД – 25 р/мин. Лабораторные исследования: калий – 4,3 ммоль/л, натрий – 141 ммоль/л, билирубин – 13 мкмоль/л, креатинин – 140 мкмоль/л (клиренс креатинина – 35 мл/мин), мочевая кислота – 681 мкмоль/л, АЛТ – 32 ед/л, АСТ – 25 ед/л, КФК – 101 ед/л, глюкоза крови – 5,9 ммоль/л. Для стимуляции диуреза решено добавить медленную инфузию фуросемида в дозе 100 мг.
На 8-е сутки: впервые за время пребывания в стационаре у больной отмечена положительная динамика – одышка уменьшилась (ЧД – 20 р/мин), среднее дневное значение АД возросло и составило 100/70 мм рт. ст., пульс увеличился до 90 уд./мин, диурез – до 62,5 мл/ч. При этом креатинин снизился до 117 мкмоль/л (клиренс креатинина составил 42 мл/мин). К проводимой терапии решено добавить 5 мг 2 р/сут ивабрадина, 20 мг/сут валсартана, уменьшить внутривенное введение фуросемида до 60 мл/сут.
На 9-11-е сутки: пациентка отмечает устойчивое улучшение самочувствия, снижение одышки (ЧД – 17 р/мин); уменьшились отеки на ногах, почасовой диурез существенно возрос и составлял 83 мл/ч. Креатинин крови снизился до 83 мкмоль/л (клиренс креатинина увеличился до 60 мл/мин) при умеренном подъеме трансаминаз: АЛТ – до 87 ед/л, АСТ – до 55 ед/л. К лечению добавлен карведилол в дозе 3,125 мг 2 р/сут.
На 12-15-е сутки: состояние больной стабильное, одышка уменьшилась, АД – 100/70 мм рт. ст., пульс – 90 уд./мин. Диурез – 87 мл/ч. В биохимических анализах креатинин – 67 мкмоль/л (клиренс креатинина – 74 мл/мин), мочевая кислота – 551 мкмоль/л.
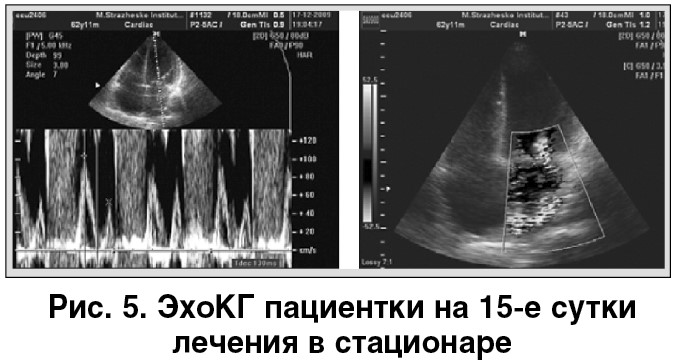 На ЭхоКГ: конечно-диастолический объем – 143 мл, фракция выброса – 41%, левое предсердие – 4,4 см, дискинез верхушки, гипокинез межжелудочковой перегородки, передней и боковой стенки, диастолическая дисфункция по рестриктивному типу, легочная гипертензия до 70 мм рт. ст., выраженная недостаточность митрального и трикуспидального клапанов (3+). Динамика показателей ЭхоКГ отсутствует (рис. 5).
На ЭхоКГ: конечно-диастолический объем – 143 мл, фракция выброса – 41%, левое предсердие – 4,4 см, дискинез верхушки, гипокинез межжелудочковой перегородки, передней и боковой стенки, диастолическая дисфункция по рестриктивному типу, легочная гипертензия до 70 мм рт. ст., выраженная недостаточность митрального и трикуспидального клапанов (3+). Динамика показателей ЭхоКГ отсутствует (рис. 5).
После стабилизации состояния больная переведена в Киевский городской центр сердца, где 28.12.2009 ей выполнено оперативное вмешательство: протезирование митрального клапана, пластика трикуспидального клапана, аортокоронарное шунтирование – четыре шунта (диагональная, огибающая ветви и передняя межжелудочковая ветвь левой коронарной артерии, а также правая коронарная артерия). Стентирована правая почечная артерия. В настоящее время пациентка находится на амбулаторном лечении по месту жительства.
Особенности приведенного клинического случая
- Комбинированное применение двух кардиотоников с различными механизмами действия.
- Использование введения левосимендана без болюсного введения препарата.
- Выраженный клинический эффект лечения при отсутствии достоверных изменений показателей кардиогемодинамики (по данным ЭхоКГ).
Таким образом, комбинированное использование двух кардиотоников (левосимендана и добутамина) помогло компенсировать ОСН и подготовить больную к оперативному вмешательству. В обычной практике сочетанное применение препаратов с кардиотоническим эффектом не практикуется, однако при неэффективности одного и/или невозможности назначения другого возможна их комбинация, особенно в случае наличия взаимоположительных свойств. Наиболее адекватным является совместное использование левосимендана и добутамина (учитывая, что левосимендан не вызывает увеличения потребности миокарда в кислороде, в отличие от добутамина). Применение левосимендана ведет к некоторому снижению АД и неэффективно при гипотензии, тогда как добутамин повышает АД, усиливая этим действие левосимендана. Оптимальность данной комбинации кардиотоников подтверждается в сравнительном исследовании S.G. De Hert, S. Lorsomradee сочетанного применения добутамина с левосименданом и милриноном [14].
Литература
- Cleland J.G., Swedberg K., Follath F. et al. The EuroHeart Failure survey programme – a survey on the quality of care among patients with heart failure in Europe. Part 1: Patient characteristics and diagnosis // Eur Heart J. – 2003. – 24 (5). – Р. 442-463.
- Fox K.F., Cowie M.R., Wood D.A. et al. Coronary artery disease as the cause of incident heart failure in the population // Eur Heart J. – 2001. – 22 (3). – Р. 228-236.
- Stevenson R., Ranjadayalan K., Wilkinson P. et al. Short and long term prognosis of acute myocardial infarction since introduction of thrombolysis // BMJ. – 1993. – 307 (6900). – Р. 349-353.
- Roguin A., Behar D., Ben Ami H. et al. Long-term prognosis of acute pulmonary oedema – an ominous outcome // Eur J Heart Fail. – 2000. – 2. – Р. 137-144.
- Fonarow G.C., Stevenson L.W., Walden J.A. et al. Impact of a comprehensive heart failure management program on hospital readmission and functional status of patients with advanced heart failure // J Am Coll Cardiol. –1997. – 30. – Р. 725-732.
- Krumhols M.H., Fonarov G.C. The treatment target in acute decompensated heart failure // Rev Cardiovasc Med. – 2001. – 2 (Suppl. 2): S7-12.
- Krumholz H.M., Chlen J., Murillo J.E. et al. Admission to hospitals with on-site cardiac cateterization facities: impact long-term costs and outcomes // Circulation. – 1998. – 98. – Р. 2010-2016.
- Cowie M.R., Wood D.A., Coats A.J. et al. Incidence and etiology of heart failure; a population-based study // Eur Heart J. – 1999. – 20. – Р. 421-428.
- McAlister F.A., Lawson F.M., Teo K.K., Armstrong A. Systematic review of randomized trials of disease management programs in heart failure // Am J Med. – 2001. – 110. – Р. 378-384.
- Rich M.V., Beckham V., Wittenberg C. A multidisciplinary intervention to prevent the readmission of elderly patients with congestive heart failure // New Engl J Med. – 1995. – 333. – Р. 1190-1195.
- Пархоменко А.Н., Иркин О.И., Брыль Ж.В. Диагностика и лечение острой сердечной недостаточности (Часть первая. Диагностика) // Медицина неотложных состояний. – 2007. – № 3 (10).
- Nanas J.N., Papazoglou P.P., Terrovitis J.V. et al. Hemodynamic effects of levosimendan added to dobutamine in patients with decompensated advanced heart failure refractory to dobutamine alone // Am J Cardiol. – 2004. – 94. – Р. 1329-1332.
- Tokuda Y., Grant P.W., Wolfenden H.D., Manganas C., Lyon W.J., Murala J.S.K. Levosimendan for patients with impaired left ventricular function undergoing cardiac surgery // Interact Cardiovasc Thorac Surg. – 2006. – 5. – Р. 322-326.
- De Hert S.G., Lorsomradee S., Cromheecke S., Van der Linden J.P. The Effects of Levosimendan in Cardiac Surgery Patients with Poor Left Ventricular Function // Anesth & Analg. – 2007. – Vol. 04 (4). – Р. 766-773.
- Терещенко С.Н. Сердечная недостаточность. – М., 2001. – Т. 2.
- Follath F., Cleland J.G.F., Just H. et al. Efficacy 1 and safety of intravenous levosimendan, a novel calcium sensitizer, in severe low output heart failure: results of a randomized, double-blind comparison with dobutamine (LIDO Study) // Lancet. – 2002. – 360. – Р. 196-202.
- Nainggolan L. CASINO results: Should docs gamble on levosimendan?
- Peck P. Levosimendan Shows Significant Survival Benefit in Decompensated Heart Failure.
Спецвипуск «Клінічні випадки та сценарії у невідкладній кардіології», вересень 2019 р


