17 квітня, 2016
Оптимізація лікування хворих на хронічний біліарний панкреатит у поєднанні з ожирінням
Хронічний панкреатит (ХП) є однією з найпоширеніших, найактуальніших проблем у сучасній гастроентерології через труднощі в ранній діагностиці та низьку ефективність лікування [1, 4, 7, 8]. Рання діагностика захворювання залишається утрудненою, особливо при легких і стертих формах ХП, коли метаболічні та патоморфологічні порушення в тканині залози компенсовані, клінічні симптоми захворювання нетипові або майже не проявляються. ХП являє собою хронічне, тривалістю понад 6 міс, прогресивне захворювання, що характеризується запально-дистрофічними і, меншою мірою, некротичними змінами в підшлунковій залозі (ПЗ), порушенням прохідності її проток, повторними загостреннями і поступовим заміщенням паренхіми органа сполучною тканиною з розвитком його екзо- й ендокринної недостатності.
Захворюваність на ХП у різних країнах Європи становить від 4 до 8 випадків на 100 тис. населення на рік, а поширеність – 200-500 хворих на 100 тис. [1]. Помітна певна залежність частоти ХП від соціально-економічного рівня країни. Найвищий рівень захворюваності спостерігається як у бідних країнах, що пов’язано з недостатнім харчуванням, так і в розвинених – через підвищене вживання алкоголю та тваринних жирів. Захворювання має тенденцію до зростання. У розвинених країнах Європи ХП значно «помолодшав» – середній вік пацієнтів із таким діагнозом знизився із 50 до 39 років, також на 30% збільшилася кількість жінок у групі хворих на ХП [6]. Частота виникнення патології постійно зростає, що пов’язано з підвищеним споживанням алкоголю і покращенням методів діагностики, у тому числі і захворювань гепатобіліарної системи [2, 3].
До числа найбільш поширених причин розвитку ХП відносяться ураження печінки і жовчовивідних шляхів (ЖВШ): функціональні розлади, хронічний холецистит, жовчнокам’яна хвороба, перенесена в анамнезі холецистектомія. Ці зміни пов’язані зі зміною колоїдної структури жовчі, підвищенням її літогенності, утворенням каменів у жовчному міхурі, дисфункцією сфінктера Одді, порушенням моторики та наявністю запального процесу у жовчних шляхах. За різними даними світової наукової літератури, у 35-60% випадків патологія ЖВШ визнана фактором, що призводить до виникнення ХП [5]. Показники поширеності захворювань ЖВШ коливаються від 26,6 до 45,5 випадків на 100 тис. населення [6]. Близько третини населення всієї планети страждає на біліарну патологію. Патологія біліарної системи характеризується істотною поширеністю, різноманітністю клінічних проявів, розвитком ускладнень. Тому своєчасна кваліфікована діагностика, раціональне лікування та профілактика мають велике значення і можуть запобігти розвитку низки ускладнень. Протягом останніх десятиліть спостерігається невпинне збільшення кількості захворювань біліарно-панкреатодуоденальної зони.
При ожирінні спостерігаються дисгормональні розлади з утворенням надмірної кількості гормонів, які мають прозапальні властивості, та зниження кількості гормонів, що мають протизапальні властивості. Це супроводжується підтриманням і наростанням хронічного запального процесу у ПЗ, також підвищується ризик виникнення ускладнень. Ожиріння знижує зовнішньосекреторну функцію ПЗ унаслідок жирового переродження ацинарних клітин, призводить до атеросклерозу судин із подальшим погіршенням трофіки ПЗ. При ожирінні спостерігається підвищений синтез та екскреція холестерину з жовчю, що супроводжується підвищенням її літогенності з утворенням біліарного сладжу та конкрементів.
Як відомо, лікування будь-якого хронічного захворювання є достатньо складним не тільки для лікаря, але й для пацієнта, оскільки потребує від хворого суворого самоконтролю та зміни способу життя.
Сьогодні перед практичним лікарем стоїть складне питання щодо вибору ефективної комбінації препаратів при лікуванні ХП для кожного пацієнта індивідуально у зв’язку з наявністю великої кількості лікарських засобів на сучасному фармацевтичному ринку. Адже вибір оптимальних лікувальних схем для цієї категорії хворих дозволить скоротити тривалість лікування, кількість госпіталізацій, попередить виникнення ускладнень і значно покращить якість життя таких пацієнтів.
Важливим у купіруванні зовнішньосекреторної недостатності та її клінічних проявів – больового, диспепсичного синдромів і наслідків мальабсорбції – є адекватно підібрана замісна (ферментна) терапія. Найпоширенішими ферментними препаратами, які застосовуються для лікування ХП, є препарати чистого панкреатину. У нашому дослідженні перевагу надали ферментному препарату Ерміталь, який містить стандартний високоактивний панкреатин у вигляді мікротаблеток. Така форма випуску забезпечує повне вивільнення резистентних до дії шлункового соку мікротаблеток із капсули у шлунку з подальшим дрібнодисперсним перемішуванням їх із кишковим вмістом та хімусом і швидким виділенням ферментів у дванадцятипалій кишці.
При лікуванні хворих на хронічний біліарний панкреатит (ХБП) в поєднанні з ожирінням доцільним є застосування препарату, що має гепатопротекторну дію, оскільки при покращенні стану печінки логічним є очікування оптимізації стану ПЗ.
Ліверія ІС – інноваційний препарат, діючою речовиною якого є метадоксин (піридоксин-L2-пірролідон-5-карбоксилат). Піридоксин є попередником піридоксаля і піридоксальфосфата, вони як коферменти беруть участь у печінковому метаболізмі вуглеводів, жовчних та амінокислот. Піролідон карбоксилат є попередником глутатіону, стимулює синтез АТФ через активацію пуринового синтезу і збільшення числа попередників гліцину і глутаміну. Метадоксин попереджує руйнування клітинної мембрани і первинну структурну дегенерацію гепатоциту, а також порушення його функцій, має гепатопротекторну та дезінтоксикаційну дію, підвищує стійкість гепатоцитів до продуктів перекисного окиснення ліпідів, індукованого впливом різних токсичних агентів; запобігає накопиченню жирів у гепатоцитах, що попереджує утворення жирової інфільтрації печінки; перешкоджає утворенню фібронектину і колагену, що гальмує процес формування цирозу печінки.
Мета дослідження – визначити ефективність включення до стандартної терапії препарату Ліверія ІС на основі вивчення клінічних синдромів, параметрів ліпідного спектру крові та структурного стану (еластичності) печінки і ПЗ у хворих на хронічний біліарний панкреатит в поєднанні з ожирінням.
Матеріали і методи
Досліджено 40 хворих на ХБП у поєднанні з ожирінням. Хворих було поділено на 2 групи. Перша група (20 осіб) отримувала загальноприйняту схему лікування. Вона включала: пантопразол 40 мг 1 р/день, Ерміталь 25 тис. (1 капс.) під час їжі, домперидон 1 таб. 3 р/день. Друга група (20 осіб) отримувала в комплексі до загальноприйнятого лікування препарат Ліверія ІС (метадоксин) по 1 таблетці (0,5 г) 2 рази на добу за 15-30 хв до їди протягом 3 міс. Вік хворих – від 30 до 71 року. Пацієнти були зіставні за віком, статтю й тривалістю захворювання на ХП, що становила 10,0±1,5 років. Оцінку ліпідограми проводили за загальноприйнятими в клініці критеріями. Структурний стан печінки та ПЗ оцінювали за їх еластичністю (жорсткістю) методом еластографії хвилі зсуву (ЕХЗ) на скануючому УЗ-апараті Ultima PA фірми «Радмир» (м. Харків, Україна) контактно датчиком лінійного формату на частотах 7-10 МГц на глибині 10-30 мм. При дослідженні печінки за допомогою цього методу проводилось по 5 вимірювань у різних ділянках кожної долі, а при обстеженні ПЗ у різних ділянках проводили 10 вимірювань.
Результати і обговорення
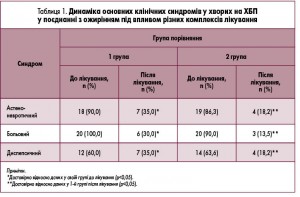
При обстеженні пацієнтів спостерігали такі клінічні синдроми: больовий, диспепсичний, астеноневротичний, які оцінювали за % хворих із проявами цих синдромів. У таблиці 1 наводимо динаміку наявності основних клінічних синдромів у хворих на ХБП в поєднанні з ожирінням під впливом вищевказаних схем лікування.
Після проведеного лікування виявлено істотне зниження кількості хворих із проявами клінічних синдромів. Включення до комплексного лікування гепатопротектора Ліверія ІС забезпечило достовірно вищу ефективність лікування за впливом на наявність досліджених клінічних синдромів.
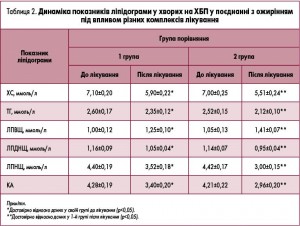
У таблиці 2 наводимо зміни показників ліпідограми під впливом вищевказаних схем лікування хворих на ХБП у поєднанні з ожирінням.
Було встановлено більш виражене зниження всіх атерогенних показників ліпідограми та підвищення захисної (антиатерогенної) фракції ліпопротеїнів високої щільності (ЛПВЩ) під впливом комплексу лікування із включенням гепатопротектора.
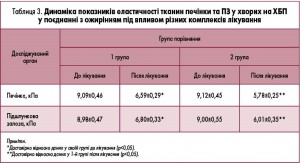
Наступним етапом дослідження стало вивчення динаміки показників еластичності тканин печінки та ПЗ при застосуванні запропонованих схем лікування.
Отримані результати після проведення лікування вказують на зниження показників жорсткості печінки та ПЗ, що свідчить про покращення їх структурного стану. Більш ефективним виявився комплекс із включенням Ліверії ІС.
Після проведеного лікування позитивна динаміка спостерігалася в обох групах (табл. 1, 2, 3). Проте у пацієнтів, котрі додатково отримували курс препарату Ліверія ІС, показники основних клінічних синдромів, ліпідограми й еластичності печінки і ПЗ були вагомішими. Показники больового, диспепсичного та астеноневротичного синдромів істотно знизилися (у 2-й групі в середньому з 80,0% до 16,6% проти показників у 1-й групі в середньому з 83,3% до 31,6%). Показник холестерину знизився на 7,0% у 2-й групі порівняно з 1-ою групою, тригліцеридів – на 9,8%, ліпопротеїнів дуже низької щільності (ЛПДНЩ) – на 9,5%, ліпопротеїнів низької щільності (ЛПНЩ) – на 14,3%, коефіцієнт атерогенності (КА) – на 13,0%, а фракція ЛПВЩ збільшилася на 11,4%. Показники жорсткості печінки та ПЗ знизилися на 12,60% і 11,60% відповідно. Дані 2-ої групи після лікування були статистично достовірними щодо таких у 1-й групі (р<0,05).
Висновок
Застосування у комплексному лікуванні ферментного препарату Ерміталь і гепатопротектора Ліверія ІС у складі комплексної терапії хворих на ХБП у поєднанні з ожирінням сприяло істотному достовірному підвищенню ефективності загальноприйнятого лікування за рівнем елімінації клінічних синдромів, оптимізації показників ліпідограми та структурного стану печінки та ПЗ (за даними ЕХЗ, р<0,05).
У перспективі доцільно дослідити вплив комплексної програми лікування із включенням ферментного препарату Ерміталь і гепатопротектора Ліверія ІС на трофологічні параметри хворих на ХБП у поєднанні з ожирінням.
Література
- Бабінець Л.С. Патогенетичні аспекти хронічного панкреатиту біліарного генезу після холецистектомії / Л.С. Бабінець, Н.В. Назарчук // Вестник клуба панкреатологов. – 2014. – № 3 (24). – С. 4-8.
- Ильченко А.А. Билиарный панкреатит / А.А. Ильченко // Русский медицинский журнал. – 2012. – № 15. – С. 803-807.
- Звягинцева Т.Д. Билиарный панкреатит / Т.Д. Звягинцева, И.И. Шаргород // Ліки України. – 2012. – № 2 (158). – С. 52-58.
- Маев И.В. Хронический панкреатит / И.В. Маев, А.Н. Казюлин, Ю.А. Кучерявый. – М.: Медицина, 2005. – 504 с.
- Степанов Ю.М. Хронічний панкреатит: біліарний механізм, чинники та перебіг / Степанов Ю.М., Заіченко Н.Г. // Запорожский медицинский журнал. – 2012. – № 1 (70). – С. 46-50.
- Щербиніна М.Б. Біліарна патологія у молодому віці: медико-соціальна характеристика пацієнтів / М.Б. Щербиніна, В.М. Гладун // Новости медицины и фармации. – 2010. – № 19. – С. 38-40.
- Nair R.J., Lawler L., Miller M.R. Chronic Pancreatitis // Am Fam Physician. – 2007. – Vol. 76. – № 11. – Р. 1679-1688.
- Convell D. Chronic pancreatitis / D. Convell, P. Banks // Curr. Opin. Gastroenterol. – 2008. – Vol. 24. – P. 586-590.