12 квітня, 2016
Сучасна лабораторна діагностика вірусних гепатитів
Як відомо, основою лабораторної діагностики вірусних гепатитів є знання про їх збудників і реплікацію, інформація про появу і зникнення маркерів інфікування, а також сучасні імунохімічні та молекулярно-біологічні методи детекції антигенів, антитіл і нуклеїнових кислот.
Лабораторна діагностика гепатиту А
Вірус гепатиту А (HAV) – це РНК-вірус, класифікований як пікорнавірус. В усіх ізолятах, зібраних у різних частинах світу, спостерігається лише один серотип HAV. Він не має зовнішньої оболонки, складається із зовнішньої білкової капсули (капсиду), що містить усередині один ланцюжок РНК, який є матрицею для синтезу вірусних білків усередині клітини-хазяїна.
Лабораторна діагностика гепатиту А (ГА) заснована на виявленні маркерів HAV: антигену HAV, антитіл (анти-HAV класів IgМ та IgG), а також РНК HAV. Остаточними доказами на користь актуальної або нещодавно перенесеної інфекції є наявність у сироватці крові (навіть в одній пробі) антитіл до HAV класу IgM (анти-HAV IgM) і наявність HAV у фекаліях. На перенесений ГА, після якого формується тривалий (найчастіше довічний) імунітет, вказує наявність антитіл до HAV класу IgG (анти-HAV IgG).
Діагноз гострого ГА підтверджується в гострій фазі процесу або ранній стадії одужання за наявності анти-HAV класу IgM, що з’являються в останні 5-10 діб інкубаційного періоду і продовжують виявлятися впродовж 6-7 міс від початку захворювання, а в 4% пацієнтів можуть персистувати до 1 року. Крім того, ці антитіла можуть спостерігатися в перші місяці в 20-30% осіб, вакцинованих інактивованою вакциною проти ГА. Утворення анти-HAV класу IgM пов’язане з первинною імунною відповіддю на потрапляння антигену, а не з інфекцією, зумовленою вакциною.
За типового перебігу ГА РНК HAV може визначатися за декілька днів до підвищення активності аланінамінотрансферази і протягом 5-59 діб захворювання, у затяжних випадках – до 95 діб.
Антиген вірусу ГА (HAV-Ag) виявляється у фекаліях хворих за 7-10 діб до появи клінічних симптомів і в перші дні захворювання, що використовується для ранньої діагностики і виявлення джерел збудника. Концентрація HAV у фекаліях є найвищою упродовж 2 тиж перед появою жовтяниці. У дорослих виділення вірусу з фекаліями зазвичай триває менше тижня після появи жовтяниці, у дітей цей період більш тривалий – кілька тижнів після клінічної маніфестації недуги. ГА не призводить до формування хронічного гепатиту та вірусоносійства. Визначення антигену HAV також знайшло застосування в санітарній вірусології при дослідженні води на наявність вірусу.
Анти-HAV класу IgG також з’являються вже на початку захворювання (з 3-4-го тижня) і зберігаються упродовж усього життя. Визначення у крові людини анти-HAV IgG (за відсутності анти-HAV IgM) свідчить про наявність імунітету до вірусу гепатиту А в результаті перенесеної в минулому інфекції або вакцинації проти цього вірусу. Анти-НAV IgG передаються від матері до плоду трансплацентарно і можуть виявлятися навіть у дітей віком понад 1 рік.
Визначення анти-HAV класу IgG використовується для вивчення імуноструктури населення, динаміки специфічного гуморального імунітету. Оцінка анти-HAV класу IgG важлива також для перед- і поствакцинального скринінгу (мінімальна протекторна концентрація анти-HAV відповідає 20 МО/л). Для визначення цього показника випускаються комерційні діагностичні препарати на основі імуноферментного аналізу (ІФА). Лабораторна діагностика заснована на виявленні маркерів HAV за допомогою специфічних імунодіагностичних методів (ІФА, радіоімунний аналіз – РІА). Зарубіжними промисловими біотехнологічними підприємствами випускаються діагностичні набори, що включають усі необхідні компоненти й реактиви для проведення тесту.
Крім твердофазних ІФА та РІА, з успіхом використовуються метод імуноелектронної мікроскопії, а також полімеразна ланцюгова реакція (ПЛР). Усі вищезгадані стратегії імунодіагностики з рівною імовірністю виявляють інапарантні, безсимптомні або клінічно маніфестні форми ГА. Особливе місце в лабораторній діагностиці ГА займають молекулярно-генетичні методи тестування РНК HAV.
Лабораторна діагностика гепатиту В
Збудник гепатиту В (ГВ) – HBV – належить до ДНК-вірусів, характеризується високою генетичною мінливістю, що зумовлює складність його імунного контролю. Сьогодні виділяють 9 підтипів вірусу, гетерогенних за поверхневим антигеном (HBsAg).
Лабораторна діагностика ГВ заснована на виявленні специфічних для нього антигенів і відповідних антитіл у крові, а також вірусних нуклеїнових кислот, основними з яких є:
• НВsAg – анти-НВs;
• анти-НВс класів IgМ та IgG;
• НВеAg – анти-НВе;
• ДНК HBV.
Найчастіше в діагностиці ГВ використовується визначення НВsAg. Цей антиген виявляється як при гострій, так і при хронічній формі захворювання (проте гостра інфекція зазвичай підтверджується наявністю високих титрів анти-НВс IgМ). У разі гострого ГВ поверхневий антиген вірусу виявляється вже через 3-5 тиж від моменту інфікування, тобто задовго до появи клінічних ознак хвороби, і в цих випадках є єдиним серологічним маркером. НВsAg постійно виявляється в переджовтяничному і жовтяничному періодах захворювання. Персистування НВsAg протягом ≥6 міс вказує на затяжний або хронічний перебіг патології та дозволяє припустити хронічне носійство вірусу.
Елімінація НВsAg і поява антитіл до нього є неодмінними умовами одужання. Необхідно враховувати, що захисні антитіла до HBsAg з’являються через 1-4 міс після зникнення HBsAg у крові і свідчать про сприятливий перебіг ГВ, припинення реплікації вірусу і фазу реконвалесценції. Цей період отримав назву «серологічне вікно», коли виявляються тільки сумарні антитіла до ядерного антигену (анти-HBc), що є єдиним серологічним маркером HBV-інфекції на даному етапі процесу.
Серологічними маркерами реплікації HBV є анти-НВс класу IgМ, НВеAg, ДНК і ДНК-полімераза, які визначаються при гострому ГВ з перших днів появи клінічних ознак і можуть бути присутніми при загостренні хронічного ГВ. Серологічні маркери реплікації HBV використовують як із метою діагностики, так і для оцінки ефективності терапії. НВсAg присутній у тканині печінки, але не в сироватці крові. Опосередковано на його наявність в організмі вказують циркулюючі антитіла – анти-НВс класів IgМ та IgG. У гострий період ГВ наявність анти-НВс класу IgМ є додатковим маркером захворювання. Проте необхідно враховувати, що близько 50% пацієнтів із хронічним ГВ також можуть мати ці антитіла в період загострення, щоправда зазвичай у низьких концентраціях.
Наявність у сироватці крові тільки анти-НВс класу IgG можлива в період між зникненням НВsAg й утворенням анти-НВs. Поєднане виявлення анти-НВс класу IgG в низькому титрі з анти-НВs вказує на перенесений гострий ГВ і наявність імунітету. Тестування НВеAg проводять у сироватках крові тільки з наявністю НВsAg. Позитивний результат цього маркера свідчить про активний процес, тобто підтверджує діагноз гострого ГВ, або свідчить про загострення хронічного ГВ. Тривалість циркуляції НВеAg має важливе прогностичне значення: виявлення НВеAg через ≥2 міс від початку захворювання вказує на можливий розвиток хронічного гепатиту. Ізольована присутність НВеAg без НВsAg у сироватці крові в більшості випадків свідчить про помилковий результат аналізу. Проте хворі, інфіковані мутантним вірусом, можуть залишатися серонегативними за НВеAg, незважаючи на наявність анти-НВе та інфекційність, що зберігається.
Наявність ДНК HBV (найбільш чутливий маркер реплікації HBV) у сироватці крові вказує на високу інфекційність цього зразка й активне розмноження вірусу в організмі. Позитивний результат вдається зареєструвати практично в усіх хворих на гострий ГВ у період розпалу недуги. Зниження концентрації ДНК HBV в процесі лікування хворих на хронічний гепатит є хорошою прогностичною ознакою, що демонструє ефективність терапії. Висока активність амінотрансфераз сироватки відображає запальне ушкодження тканини печінки, зумовлене передусім реакцією імунної системи макроорганізму у відповідь на інфікування вірусом, а не прямою цитопатичною дією вірусу на гепатоцит. Високий рівень ДНК HBV у поєднанні з низькою активністю амінотрансфераз свідчить про недостатню імунну відповідь організму. Виявлення анти-НВе за відсутності НВеAg і ДНК HBV вказує на припинення активної реплікації вірусу.
Сероконверсія НВsAg в анти-НВs, що відбувається у 90-95% хворих на гострий ГВ у стадії завершення інфекційного процесу, є показником імунітету до HBV, тобто наявність анти-НВs свідчить про перенесену інфекцію і виникнення специфічного імунітету. Особи, які мають ці антитіла в захисній концентрації (≥10 МО), не хворіють на ГВ і не потребують вакцинації.
Усі використовувані методи дослідження для визначення специфічних маркерів ГВ можна розділити на 2 групи – імунохімічні та молекулярно-біологічні. Серед імунохімічних методів основне місце належить ІФА з його високою чутливістю та специфічністю, простотою проведення і стабільністю реактивів. Молекулярно-біологічні методи (точкова і рідинна гібридизація, а також ПЛР) дозволяють виявляти ДНК HBV безпосередньо або за допомогою визначення ДНК-полімерази – ферменту, специфічного для вірусу.
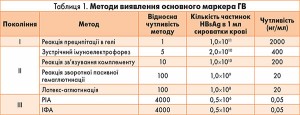
НВsAg/анти-НВs. Для виявлення основного маркера HBV розроблені різноманітні методи, що дозволяють визначити антиген у концентрації до 0,05 нг/мл та умовно поділяються на декілька поколінь (табл. 1).
Нині основним методом виявлення НВsAg є ІФА. Сучасні діагностичні препарати мають високу специфічність, але можливі й псевдопозитивні результати. Для розмежування псевдопозитивних та істинно позитивних результатів застосовується тест нейтралізації НВsAg з використанням специфічної сироватки.
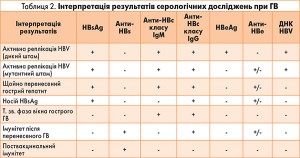
Принципово новою для системи виявлення НВsAg стала вимога до виробників діагностичних препаратів про обов’язкове включення в тест-систему слабкопозитивного контрольного зразка, що містить НВsAg у концентрації 1 нг/мл. Для визначення анти-НВsAg був випробуваний увесь спектр імунохімічних методів, основним з яких є ІФА (для якісного і кількісного аналізу) (табл. 2).
Анти-НВс класів IgМ та IgG, НВеAg – анти- НВе. Для тестування цих маркерів можуть бути використані різні варіанти твердофазного імуноаналізу: імуноферментний, радіоімунний, хемілюмінесцентний та ін.
ДНК HBV. Цей показник визначають за допомогою ПЛР. Наразі ампліфікаційні методи детекції ДНК HBV (якісна та кількісна діагностика) набули найбільшого розповсюдження.
Далі буде.