11 жовтня, 2019
Офтальмогіпертензія за умов ожиріння: чи є кортизол втраченою деталлю патофізіологічного пазла?
Нині ожиріння є глобальною загрозою громадському здоров’ю у зв’язку зі швидким зростанням розповсюдженості та асоціацією із широким спектром коморбідних патологічних станів. Безпосередній зв’язок ожиріння з підвищенням внутрішньоочного тиску (ВОТ) та наявністю глаукоми було підтверджено в більшості досліджень із цього питання [1].
Були запропоновані різні теорії виникнення цього зв’язку, в тому числі надлишок внутрішньоорбітальної жирової тканини з відповідним підвищенням епісклерального венозного тиску та порушенням відтоку водянистої вологи; підвищена в’язкість крові (зростання кількості еритроцитів, гемоглобіну, гематокриту) з відповідним збільшенням опору відтоку крові по епісклеральних венах; збільшений тиск у циліарних артеріях та ультрафільтрація водянистої вологи внаслідок цього; осмотичний зсув рідини до внутрішньоочного простору, спричинений гіперглікемією. Утім, чіткого патофізіологічного пояснення асоціації між ожирінням й офтальмогіпертензією наразі немає [1], тому метою цієї роботи було з’ясувати зазначене питання.
Стероїдіндукована офтальмогіпертензія була вперше описана McLean в 1950 р. як підвищення ВОТ після системного призначення адренокортикотропного гормона. На 4 роки пізніше про аналогічний побічний ефект місцевого призначення кортикостероїдів повідомив Francois. Сьогодні добре відомо, що офтальмогіпертензія може виникати як побічний ефект внутрішньовенної, топічної, пероральної, інгаляційної, периокулярної та внутрішньовітреальної терапії кортикостероїдами [2]. Крім того, задокументовано випадки підвищеного ВОТ та відкритокутової глаукоми внаслідок ендогенного гіперкортицизму (синдром і хвороба Кушинга) [3].
Відомо, що ВОТ у здорових осіб протягом дня коливається, досягаючи піку приблизно о 7-й ранку, а максимального зниження – рано увечері, що прямо корелює із сироватковим рівнем кортизолу. На підтвердження цієї асоціації свідчить також те, що в пацієнтів зі синдромом/хворобою Кушинга, осіб із недостатністю наднирників, які приймають кілька доз кортикостероїдів протягом доби, та хворих після адреналектомії не спостерігається добової флуктуації ВОТ [2].
Результати авторського підготовчого крос-секційного дослідження, проведеного за участю 50 осіб з ожирінням (80% жінок, 20% чоловіків, медіана віку – 44 роки, індекс маси тіла – 42,0±7,4 кг/м2, окружність талії 124,2±16,5 см), показали, що ВОТ істотно прямо корелює з ранковим сироватковим рівнем базального кортизолу (r=0,28; р=0,049). Водночас не було зафіксовано істотних кореляцій ВОТ із кількістю еритроцитів (r=0,01; р=0,966), гемоглобіном (r=0,09; р=0,550) чи гематокритом (r=0,14; р=0,329). Також не було виявлено достовірних відмінностей у ВОТ залежно від наявності цукрового діабету (за його наявності – 17,0±2,0 мм рт. ст., за відсутності – 15,9±2,0 мм рт. ст.; р=0,339) та артеріальної гіпертензії (за її наявності 16,3±1,7 мм рт. ст., за відсутності – 15,9±2,2 мм рт. ст.; р=0,470) (аналіз проведено за U‑тестом Mann-Whitney). Виявлені асоціації змусили авторів замислитися над питанням, чи є кортизол невідомою ланкою патофізіологічного зв’язку асоційованої з ожирінням офтальмогіпертензії / відкритокутової глаукоми.
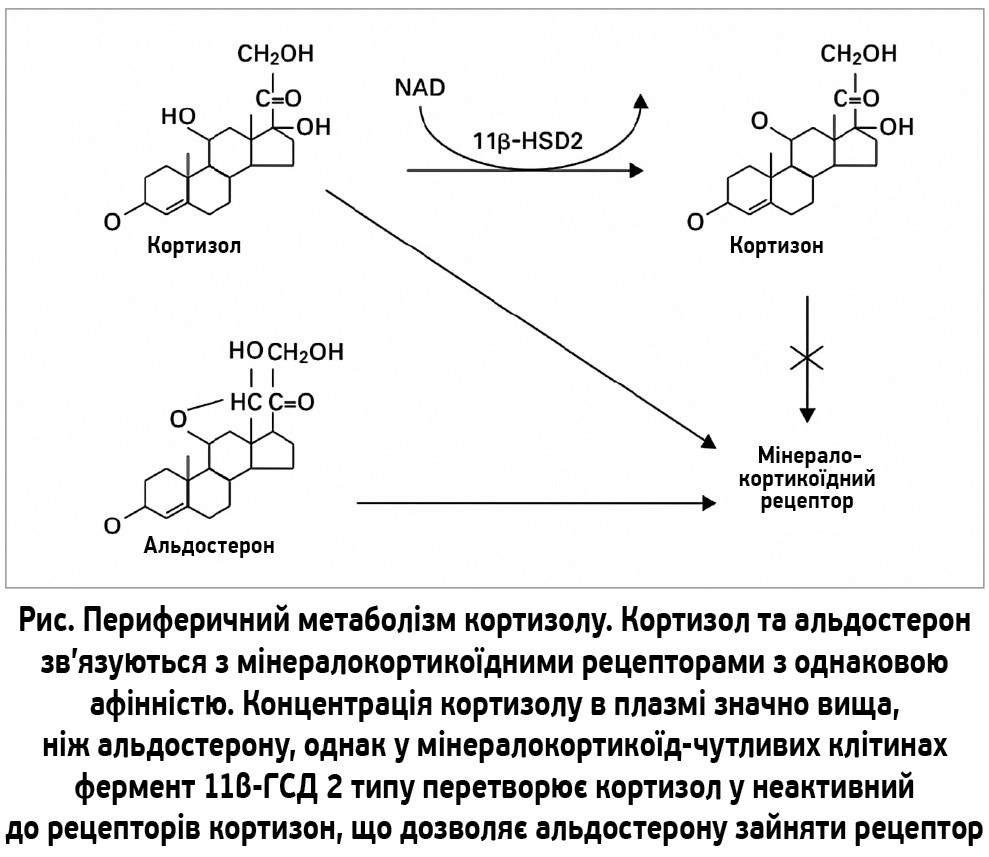
З’ясовано, що абдомінальний/вісцеральний фенотип ожиріння асоціюється з хронічною гіперактивністю гіпоталамо-гіпофізарно-наднирникової осі, що спричиняє стан так званого функціонального гіперкортицизму [4]. У жировій тканині осіб з ожирінням спостерігається надмірна експресія 11β-гідроксистероїддегідрогенази (11β-ГСД) 1 типу, рівень якої прямо корелює з вимірами загального (індекс маси тіла, відсоток жиру в організмі) та центрального (окружність талії) ожиріння, а також рівнем глюкози натще, концентрацією інсуліну та вираженістю інсулінорезистентності [5]. 11β-ГСД 1 типу є мікросомальним ферментом, що експресується переважно в жировій тканині та печінці і діє передусім як нікотинамідаденіндинуклеотидфосфат (НАДФ)-залежна редуктаза, тобто in vivo перетворює неактивний кортизон на активний кортизол, таким чином посилюючи активацію глюкокортикоїдних рецепторів (рис.). На противагу цьому інша ізоформа, а саме 11β-ГСД 2 типу, переважно експресується в тканинах, що є мішенями дії мінералокортикоїдів, й інактивує кортизол, перетворюючи його на кортизон. Подібна інактивація запобігає впливу кортизолу на неселективні мінералокортикоїдні рецептори [6].
Слід зазначити, що наявність глюкокортикоїдних та мінералокортикоїдних рецепторів, а також 11β-ГСД у тканинах ока людини й інших ссавців була продемонстрована в кількох дослідженнях [7]. Для домінування активності 11β-ГСД 1 типу співвідношення кортизол/кортизон у водянистій волозі має становити 14:1 [7]. Таким чином, можна припустити, що утворення кортизолу під дією надмірно експресованої 11β-ГСД 1 типу (кортизонредуктази) стимулює підвищення епітеліального транспорту іонів Na+ та продукцію водянистої вологи [8]. Крім того, одночасно відбувається утруднення відтоку внутрішньоочної рідини, оскільки глюкокортикоїди чинять низку впливів на клітини трабекулярної сітки, в тому числі зумовлюють зміни білків її клітин, організації цитоскелету, відкладення екстрацелюлярного матриксу, форми та функціонування клітин тощо [2, 9]. І насамкінець, пригнічення 11β-ГСД 1 типу у війчастому епітелії ока призводить до зниження ВОТ у пацієнтів з офтальмогіпертензією, що також свідчить на підтримку кортизолової теорії [8].
Слід зауважити, що кортизол також є ланкою в опублікованих раніше і згаданих вище теоріях патогенезу пов’язаної з ожирінням офтальмогіпертензії. Так, кортизол за рахунок еритропоетинового ефекту здатен дещо підвищувати в’язкість крові [10]. Кортизол також підвищує артеріальний тиск, беручи участь у кількох патофізіологічних механізмах, серед яких активація ренін-ангіотензинової системи; посилення кардіоваскулярної відповіді на вазоконстриктори (катехоламін, вазопресин, ангіотензин II); посилення чутливості β-адренергічних рецепторів до катехоламінів; пригнічення судинорозширювальних систем та агентів (NO‑синтаза, простациклін, кінін-калікреїнова система); підвищення серцевого викиду, загального периферійного опору судин та реноваскулярного опору. Крім того, кортизол демонструє власну мінералокортикоїдну активність [11]. Підвищення артеріального тиску, що виникає під дією описаних впливів, супроводжується зростанням тиску в циліарних артеріях й ультрафільтрацією водянистої вологи.
Глюкокортикоїди також посилюють розпад білків скелетних м’язів, ліполіз жирової тканини та глюконеогенез у печінці і зменшують утилізацію глюкози. Ці ефекти підвищують рівень циркулюючої глюкози крові, сприяючи інсулінорезистентності, що може спричинити осмотичне зміщення рідини до внутрішньоочного простору [12].
Загалом, на думку авторів, саме кортизол є невідомою ланкою між ожирінням та офтальмогіпертензією.
Література
- Cheung N., Wong T. Y. Obesity and eye diseases. Surv Ophthalmol. 2007; 52 (2): 180-195.
- Kersey J. P., Broadway D. C. Corticosteroid-induced glaucoma: a review of the literature. Eye (Lond) 2006; 20 (4): 407-416.
- Virevialle C., Brasnu E., Fior R., Baudouin C. Open-angle glaucoma secondary to Cushing syndrome related to an adrenal adenoma: case report. J Fr Ophtalmol. 2014; 37 (10): e169.
- Tirabassi G., Boscaro M., Arnaldi G. Harmful effects of functional hypercortisolism: a working hypothesis. Endocrine. 2014; 46 (3): 370-386.
- Lindsay R. S. et al. Subcutaneous adipose 11 beta-hydroxysteroid dehydrogenase type 1 activity and messenger ribonucleic acid levels are associated with adiposity and insulinemia in Pima Indians and Caucasians. J Clin Endocrinol Metab. 2003; 88 (6): 2738-2744.
- Stewart P. M., Krozowski Z. S. 11 beta-hydroxysteroid dehydrogenase. Vitam Horm. 1999; 57: 249-324.
- Rauz S. et al. Expression and putative role of 11 beta-hydroxysteroid dehydrogenase isozymes within the human eye. Invest Ophthalmol Vis Sci. 2001; 42 (9): 2037-2042.
- Rauz S. et al. Inhibition of 11beta-hydroxysteroid dehydrogenase type 1 lowers intraocular pressure in patients with ocular hypertension. QJM. 2003; 96 (7): 481-490.
- Genis A. The effects of glucocorticoids on trabecular meshwork and its role in glaucoma. Am J Biochem Biotechnol. 2015; 11 (4): 185-190.
- Lodish H., Flygare J., Chou S. From stem cell to erythroblast: regulation of red cell production at multiple levels by multiple hormones. IUBMB Life. 2010; 62 (7): 492-496.
- Cicala M. V., Mantero F. Hypertension in Cushing's syndrome: from pathogenesis to treatment. Neuroendocrinology. 2010; 92 (Suppl 1): 44-49.
- Geer E. B., Islam J., Buettner C. Mechanisms of glucocorticoid-induced insulin resistance: focus on adipose tissue function and lipid metabolism. Endocrinol Metab Clin North Am. 2014; 43 (1): 75-102.
- Belančić A. et al. Ocular hypertension secondary to obesity: cortisol, the missing piece of the pathophysiological puzzle? Int J Ophthalmol. 2019; 12 (6): 1050-1051.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 18 (463), вересень 2019 р.