11 квітня, 2016
Водневий дихальний тест з навантаженням харчовою лактозою у діагностиці транзиторної лактазної недостатності у дітей грудного віку

Сьогодні проблема транзиторної лактазної недостатності (ТЛН) у дітей грудного віку є дуже актуальною. Це зумовлено поширеністю та клінічними проявами ТЛН, які значно погіршують якість життя дитини та непокоять батьків (Д.В. Усенко, 2009; О.Г. Шадрін, 2012; M.B. Heyman, 2006).
За даними літератури (А.И. Хавкин, 2009; R. Arroyo, 2010; E. Sibley, 2004), лактазна недостатність (ЛН) зустрічається у 15-30% дітей грудного віку, найчастіше у перші місяці життя, і має транзиторний характер. Це пов’язано з анатомо-фізіологічною особливістю грудних дітей, насамперед недоношених, у яких спостерігається функціональна незрілість ентероцитів та низька активність лактази (А.И. Хавкин, Н.С. Жигарева, 2009; M.B. Heyman, 2006). Неврахування цих даних впливає на тривалість клінічних симптомів ТЛН: протягом тривалого часу спостерігаються зригування, метеоризм, кишкові коліки та пінисті випорожнення з кислим запахом, неспокій та ін. ТЛН сприяє розвитку дисбіозів кишечнику, алергічних реакцій тощо (В.П. Мисник, 2007; Е.А. Корниенко и соавт., 2006; А.И. Хавкин, Н.С. Жигарева, 2009; Д.В. Усенко, 2009; R. Arroyo еt al., 2010; О. Rudzeviciene, І. Narkeviciute еt al., 2004).
Лактазна недостатність – захворювання, що провокує виникнення синдрому мальабсорбції, яке зумовлене порушенням розщеплення лактози в тонкій кишці (Ю.Г. Мухіна та співавт., 2009).
Лактаза – єдиний в організмі людини фермент, який розщеплює лактозу, знаходиться на апікальній поверхні щіткової кайми ентероциту, зафіксований на його клітинній мембрані. Експериментальними дослідженнями доведено (Д.В. Усенко, А.В. Горелов, 2009), що високу активність ферменту забезпечують тільки зрілі, функціонально-активні ентероцити, а різноманітні патологічні чинники, які чинять пошкоджуючу дію на ворсини кишечнику та стан ентероцитів, слугують пусковим механізмом в розвитку ЛН.
Лактаза з’являється на 10-12 тижні гестації, а з 24 тижня починається підвищення її активності, що досягає максимуму на момент народження. З 17-го по 24-й тиждень гестації найбільша активність спостерігається у здухвинній кишці, потім вона вирівнюється у проксимальному та дистальному відділах кишечнику. З 28-го по 34-й тиждень гестації активність лактази дорівнює 30% від її рівня на 39-40 тижнях гестації (А.Г. Талалаев, 1992; M.M. Lerch et al., 1991).
За даними більшості авторів, у людини виражене зниження активності лактази відбувається до 3-5 років (Q.W. Spender et al., 1989). Зниження активності лактази починається наприкінці першого року життя дитини (до 24 міс активність лактази зворотно пропорційна віку), у шкільному віці рівень її стабільний (L.A. Heitlinger et al., 1991). Механізми ЛН дорослого типу та вродженої ЛН однакові: порушується активація ферменту і його попередники накопичуються у комплексі Гольджі (E.S. Sterch et al., 1990). На користь цієї точки зору вказує ще більш висока частота ЛН у недоношених новонароджених у разі наявності у їхніх батьків інтолерантності до лактози.
ЛН, відповідно до міжнародної класифікації, поділяється на первинну та вторинну (Ю.Г. Мухина и соавт., 2003; M.B. Heyman, 2006).
Первинна ЛН – зниження активності лактази при морфологічно незміненому ентероциті. Поділяється на вроджену, транзиторну (недоношених) та конституціональну (дорослого типу).
Вроджена ЛН – генетично детермінована, сімейна ЛН, яка успадковується за аутосомно-рецесивним типом; висока активність контролюється домінантним геном, а низька – рецисивним.
ТЛН, зумовлена функціональною незрілістю ентероцитів, зустрічається у новонароджених, особливо недоношених. Рівень активності лактази у тонкому кишечнику у новонароджених залежить від терміну гестації.
Конституціональна ЛН – дорослий тип, який характеризується індивідуальними термінами розвитку та сімейною схильністю до гіполактазії.
Коди за МКХ-10: Е73.0 – вроджена недостатність лактази, Е73.1 – вторинна недостатність лактази, Е73.8 – інші види непереносимості лактази.
Вторинна ЛН пов’язана з пошкодженням ентероцитів, що призводить до зниження активності лактази. За даними M. Pfefferkorn і співавт. (2002), ступінь зниження активності лактази безпосередньо корелює зі ступенем атрофії ворсинок та інтенсивністю запалення слизової оболонки тонкого кишечнику. Найчастіше вторинна ЛН виникає на фоні патології шлунково-кишкового тракту, при гастроінтестинальних формах алергії, дисбіозі кишечнику, а також при прийомі медикаментів, які ушкоджують слизову оболонку тонкої кишки (R. Arroyo еt al., 2010).
Виразність клінічної симптоматики при ТЛН є дуже варіабельною. Вона зумовлена:
- різним рівнем зниження активності ферменту;
- відмінністю біоценозу кишечнику;
- індивідуальними особливостями чутливості кишечнику;
- різноманітною кількістю надходження з їжею лактози.
Початок клінічних проявів ТЛН припадає на 2-4 тиждень життя, коли інтенсивно збільшується добовий об’єм спожитого дитиною молока, а грудне молоко «дозріває», і в ньому збільшується вміст лактози. У більшості немовлят поступово з’являються та посилюються зригування у зв’язку з підвищенням внутрішньочеревного тиску, починаються кишкові коліки.
Клінічна картина ТЛН складається з симптомів, що пов’язані з ферментацією лактози молочно-кислими бактеріями (метеоризм, здуття, пінисті випорожнення з кислим запахом), симптомів, зумовлених наявністю неферментованої лактози (рідкі, часті випорожнення), та в деяких випадках симптомів, пов’язаних з розмноженням патогенної флори. Клінічні прояви ТЛН негативно впливають на якість життя дитини, збільшують роздратованість, погіршують сон та апетит, уповільнюється темп фізичного та психомоторного розвитку (Е.А. Корниенко и соавт., 2006; А.И. Хавкин, Н.С. Жигарева, 2009).
У клінічній практиці на ТЛН у дітей раннього віку вказують метеоризм, кишкові коліки переважно відразу після годування дитини, порушення частоти та характеру випорожнень (рідкі, пінисті, іноді з домішками слизу), відсутність самостійних випорожнень (О.Г. Шадрін та співавт., 2011), зниження рН калу ≤5,5.
Найбільш поширений метод діагностики ТЛН у закордонній практиці – це водневий дихальний тест (ВДТ), який забезпечує визначення концентрації водню у повітрі при видиху до та після навантаження лактозою (Ю.Г. Мухина и соавт., 2003). За даними літератури, концентрація водню досягає максимальних значень через 3 год після навантаження лактозою. Це дозволяє виміряти концентрацію водню (Н2) двічі: до та через 3 год після навантаження лактозою. Для діагностики ТЛН необхідно віднімати з максимального значення концентрації водню первісне, інакше результат може виявитися хибно позитивним (А. Abramowitz et al., 1986; G.R. Сorazza et al., 1993). Хибно негативний результат може бути при низькій кишковій колонізації, швидкому кишковому транзиті після оперативних втручань (В. Cochet et al., 1981).
У 2008 р. був прийнятий Римський консенсус із водневих тестів, де викладені рекомендації міжнародних експертів щодо клінічної практики стосовно показників та методів проведення Н2-дихальних тестів при захворюваннях шлунково-кишкового тракту (А. Gasbarrini et al., 2009).
Принцип ВДТ полягає у тому, що частина водню, який виділяється під час бактеріальної ферментації прийнятого субстрату у товстій кишці, потрапляє у кров та швидко виділяється з диханням, де може бути визначений кількісно. Склад газу, який знаходиться усередині просвіту, розрізняється по всій довжині шлунково-кишкового тракту. Так, склад газів у шлунку та атмосферного повітря схожі, тоді як кишкові гази різних індивідів істотно різняться, що є кінцевим результатом різних метаболічних процесів, які виникають усередині шлунково-кишкового тракту. Близько 99% газу складається з п’яти газів без запаху (N2, O2, CO2, H2 та CH2). Інші гази з запахом (NH3, сульфід, індол, скатол, летючі аміни та коротколанцюгові жирні кислоти) складають менш ніж 1% (M.D. Levitt, 1971). Газ потрапляє до кишечнику з трьох джерел: під час ковтання повітря, утворюється в просвіті кишечнику (хімічні реакції та бактеріальний метаболізм, для останніх характерним є утворення газу та його споживання) та дифундує у просвіт кишечнику з кровотоку. З урахуванням продукції, яка знаходиться усередині просвіту, було виявлено, що основними газами, створеними у різних відділах шлунково-кишкового тракту, є СО2, Н2 та СН2. У тонкій кишці велика кількість вуглецю діоксину (СО2) створюється при взаємодії іону водню та гідрокарбонату за наявності вугільної ангідрази. СО2 швидко абсорбується у верхніх відділах кишечнику й таким чином робить мінімальний внесок у загальний об’єм газу. Більш високу концентрацію СО2, що виділяється з прямої кишки, виявляли, коли концентрація Н2 у газах також була високою у зв’язку з бактеріальними ферментативними реакціями (А. Gasbarrini et al., 2009). Можливо, як Н2 та СН4, частина СО2 кишкового газу може утворюватися внаслідок ферментативних реакцій. На відміну від СО2 єдиним джерелом Н2 та СН2 у кишечнику є бактеріальні метаболічні процеси, тому що новонароджені у перші 12 год життя не можуть виділяти Н2 та СН4 (M.D. Levitt, J.H. Bond, 1970). При голодуванні продукування Н2 є низьким, але після вживання ферментативних та неперетравлених субстратів, переважно вуглеводів, бактерії, що знаходяться у середині просвіту, виділяють велику кількість Н2. При захворюваннях тонкої кишки та порушенні всмоктування велика кількість субстрату потрапляє у товсту кишку та стає доступною для бактеріальної ферментації – анаеробних процесів, з продукуванням СО2, Н2, СН4 та органічних кислот, таких як молочна кислота та коротколанцюгові кислоти.
Якщо гази утилізуються бактеріями, вони абсорбуються, а потім виділяються з диханням або під час випорожнення. Н2 може швидко всмоктуватися у кров та виділятися легенями, що є обґрунтуванням Н2-дихального тесту, який широко використовується для визначення мальабсорбції вуглеводів (M.D. Levitt, R.M. Donaldson, 1970). Абсорбований Н2 повністю видаляється з крові за один пасаж через легені, таким чином, рівень екскреції Н2 повинен бути еквівалентним його абсорбції у кишечнику (M.D. Levitt, J.H. Jr. Bond, 1970). Близько 14-20% Н2, що звільнився у товстій кишці, екскретується через легені: вимірювання концентрації Н2 у повітрі при видиху може бути прийнято за відображення кишкової продукції Н2 (M.D. Levitt, R.M. Donaldson, 1970).
За даними літератури, концентрація водню досягає максимальних показників через 3 год після навантажування лактозою. Це дозволяє виміряти концентрацію водню два рази: до та через 3 год після навантаження лактозою (A. Abramowitz, Е. Granot, I. Tamir et al., 1986).
За даними M. Ledochowski і співавт. (2008), показниками для проведення тесту на непереносимість лактози є:
- підозри на первинну та вторинну непереносимість лактози;
- дослідження синдрому подразнення товстої кишки;
- непереносимість молока та молочних продуктів;
- непереносимість кондитерських виробів та шоколаду;
- дослідження здуття, метеоризму, скупчення газів;
- дослідження діареї або хронічної діареї;
- дослідження стеатореї (жирові випорожнення);
- спостереження глютенової хвороби та інших випадків з атрофією кишкових ворсинок за умови, що первинна непереносимість лактози виключена шляхом проведення молекулярних генетичних тестів;
- хронічні запальні захворювання кишечнику (з порушенням засвоювання вуглеводів).
Для отримання достовірних результатів ВДТ необхідний правильний протокол ведення тесту, а також треба вести докладні записи. Необхідно звертати увагу на симптоми, що з’являються під час дослідження. Виявлення симптомів є важливим не тільки для інтерпретації результатів тесту, а й для визначення для клінічних наслідків.
Наприклад, виникнення після навантаження симптомів, що не супроводжуються виділенням водню, вказує на наявність мікроорганізмів, які не продукують водень. Але відсутність симптомів, за яких збільшується водень у видиху, може вказувати на порушення засвоєння, яке не обов’язково потребує дієтотерапії. Також важливе значення має час виникнення симптомів: якщо симптоми виникають дуже рано, це може вказувати на те, що скарги пов’язані не тільки з порушенням засвоєння, а ще й з синдромом надлишкового бактеріального росту. У такому випадку на доповнення до індивідуальної дієти необхідна відповідна терапія. Симптоми, що виникають під час тесту, не обмежені тільки такими проявами, як здуття, посилення перистальтики, діарея, біль у животі, що пов’язані зі шлунково-кишковим трактом. Частіше пацієнт відчуває позакишкові симптоми. Кожного пацієнта потрібно питати про скарги під час кожного вимірювання. Найчастіше виникають такі прояви, як урчання у животі, здуття, діарея, біль у животі, нудота, печія, відрижка, перевтомлення, головний біль.
Вимірювати водень у повітрі при видиху можна за допомогою двох типів газоаналізаторів: стаціонарних та переносних. У стаціонарних аналізаторах можна перевіряти дані разом з аналізом лінійності та відтворенням результатів (N.W. Solomonset et al., 1977).
Зараз в Україні зареєстрований портативний монітор для визначення Н2 у повітрі, що видихається, Gastro+Gastrolyzer виробництва Bedfont Scientific Limited (Велика Британія). Перевагою цього апарату є те, що в разі необхідності дослідження дітей та немовлят використовується спеціальна техніка відбору дихальних проб. Вона являє собою спеціальну систему, яка дозволяє спрямовувати повітря при видиханні у прилад. Маска для обличчя відповідного розміру одягається на рот та ніс пацієнта, при цьому відсутній витік повітря.
При проведенні тесту на ЛН дитина приймає навантаження 1-2 г лактози на 1 кг маси тіла (не більше 25 г), розчиненої у 10 мл води на 1 кг маси тіла, але не більше 250 мл (А. Gasbarrini et al., 2009). Лактоза погано розчиняється у холодній воді, тому рекомендується використовувати теплу воду. Водень вимірюють до навантаження (базальний рівень) та кожні 30 хв протягом 3 год (N.W. Solomons, C. Barillas, 1986). Трьохгодинна тривалість тесту була запропонована у зв’язку з тим, що діти не можуть перенести тривалий період голодування, а також з урахуванням коротшого часу кишкового транзиту у дитячому віці.
Дихальний тест на ЛН вважається позитивним при збільшенні рівня концентрації водню ≥20 ррm порівняно з базальним рівнем. При збільшенні рівня водню ≥10<20 ррm результати тесту вважають гранично позитивним. Крім цього збільшення рівня водню на ≥10 ррm порівняно з базальним рівнем протягом 30 хв може вказувати на лактозо-залежний надлишковий бактеріальний ріст у тонкому кишечнику. Максимальний бактеріальний ріст реєструється не раніше, ніж через 60 або 90 хв після здійснення навантаження – стільки часу необхідно незасвоєній частині лактози, щоб потрапити до товстого кишечнику (M. Ledochowski, Hydrogen Breath tests, V. Ledochowski, Innsbruck, 2008).
При ранньому прирості водню можливі два основних варіанти.
1. Характерні 2 максимуми змін рівня водню: за збільшенням у перші 30 хв спостерігається спад, а потім знову збільшення між 60-ю та 90-ю хв. Це вказує на надлишковий бактеріальний ріст у тонкому кишечнику, при цьому спостерігається нормальне функціонування ілеоцекального клапану, бактерії у тонкому кишечнику здатні до метаболізму лактози. Після 60-90 хв другий максимум кривої вказує, що більша частина лактози не може бути засвоєна, тому бродить у товстому кишечнику. Це випадок порушення засвоєння лактози. Якщо під час тесту хворий відчуває дискомфорт, то встановлюється діагноз кишкова непереносимість лактози з лактозо-залежним надлишковим бактеріальним ростом у тонкому кишечнику зі здоровим функціонуванням ілеоцекального клапану. Якщо під час тесту не відчувається дискомфорт, діагностується порушення засвоєння лактози з лактозо-залежним надлишковим бактеріальним ростом у тонкому кишечнику зі здоровим функціонуванням ілеоцекального клапану. Якщо симптоми спостерігаються протягом перших 60 хв, а потім достатньо швидко зникають, це свідчить про те, що вони були викликані надлишковим ростом у тонкому кишечнику, а не порушенням засвоєння лактози (B. Lembcke, Lactose-Toleranz-Test, 1998; F. Casellas, J.R. Malagelada, 2003).
2. Динаміка змін рівня водню має ранній приріст концентрації до 60 хв, яка залишається на рівні, що перевищує базальний мінімум на 20 ppm, до 90 хв без подальшого зниження. Це свідчить про те, що вміст товстого кишечнику переходить зворотно у тонкий кишечник через ілеоцекальний клапан; зустрічається часто тому, що в разі порушення засвоєння лактози у товстій кишці може створюватися великий тиск через процес бродіння. Ілеоцекальний клапан розтягується та починає «протікати». За такого стану у сліпій кишці виникає антиперистальтичний рух, який намагається «продавити» харчові маси. Таким чином, вміст кишечнику, насичений великою кількістю бактерій, викликає надлишковий ріст бактерій у кінцевому відділі здухвинної кишки, тоді як у термінальних відділах тонкого кишечнику надлишковий ріст не відбувається. Такий випадок описується терміном «ретроградний ілеїт» та спостерігається, коли ілеоцекальний клапан втрачає герметичність. Оскільки така ситуація майже завжди супроводжується скаргами, то встановлюється діагноз кишкова непереносимість лактози з ретроградним ілеїтом. Якщо під час проведення тесту хворий не скаржиться на дискомфорт, необхідно обстежити його на чутливість до тиску у правій нижній ділянці черева, у місці з’єднання тонкого та товстого кишечнику. Якщо чутливість відсутня, динаміка водню відповідає вищевказаним рівням, то встановлюється діагноз порушення засвоєння лактози з відтоком вмісту кишечнику через ілеоцекальний клапан без ретроградного ілеїту (B. Lembcke, 1998; F. Casellas, J.R. Malagelada, 2003).
У сучасних умовах є усі можливості для своєчасної діагностики лактазної недостатності. Але треба враховувати, що інформативні методи часто не можуть використовуватися у педіатричній практиці через їх недоступність та високу вартість.
Нами на базі ДКЛ № 5 м. Києва, що є клінічною базою кафедри педіатрії післядипломної освіти Національного медичного університету ім. О.О. Богомольця, проведено дослідження клінічного значення ВДТ для діагностики ТЛН у дітей грудного віку. Робота проводилася згідно з Наказом МОЗ України від 29.01.2013 р. № 59 «Уніфіковані клінічні протоколи медичної допомоги дітям із захворюваннями органів травлення». Було обстежено 306 дітей віком від 1 до 5 міс життя. Серед них 241 дитина з ТЛН. Всі діти були на грудному вигодовуванні. Всім пацієнтам проведено стандартне діагностичне обстеження за допомогою ВДТ з навантаженням харчовою лактозою. Для визначення Н2 у видихуваному повітрі використовували апарат Gastro+Gastrolyzer виробництва Bedfont Scientific Limited (Велика Британія). Нами розроблена методика проведення ВДТ з використанням масок відповідного розміру для грудних дітей. Водень вимірювали до навантаження лактозою (базальний рівень) та через 30 хв протягом 3 год. При проведенні тесту на лактазну недостатність дитина приймала навантаження 1,5 г лактози на 1 кг маси тіла, розчиненої у 10 мл теплої води на 1 кг маси тіла (А. Gasbarrini et al., 2009).
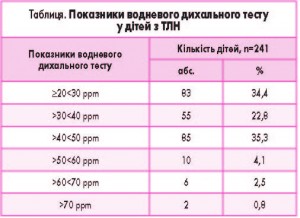
Показники збільшення рівня водню у дітей з ТЛН за даними ВДТ подано у таблиці.
Як видно з таблиці, найчастіше у дітей зустрічається підвищення рівня водню у межах ≥20<30 ppm (34,4%). Майже у однакової кількості дітей рівень водню складав >30<40 ppm та >40<50 ppm (22,8% та 25,3%). І тільки у поодиноких пацієнтів рівень водню перевищував >60<70 ppm (2,5% та 0,8%).
Діти, які мали виразні клінічні прояви ЛН та мали показники рівня водню >50ppm за даними ВДТ, були нами направлені на генетичне дослідження можливої вродженої ЛН.
При генетичному дослідженні у 4 із 18 дітей з ЛН та рівнем водню >50 ppm була підтверджена первинна (вроджена) ЛН. Аналіз показав наявність гомозиготного носійства С/С за алеллю 13910.
Таким чином, у 223 дітей грудного віку з ЛН рівень водню під час ВДТ з навантаженням харчовою лактозою становив ≥20<50 ppm.
З урахуванням клініки та ступенів збільшення рівня водню під час ВДТ нами виділено 3 ступеня тяжкості:
І ступінь (легкий) – збільшення рівня водню ≥20<30 ppm;
ІІ ступінь (середній) – збільшення рівня водню >30<50 ppm;
ІІІ ступінь (тяжкий) – збільшення рівня водню >50 ppm.
Такий розподіл дозволяє оптимізувати призначення ферменту лактази дітям грудного віку з ТЛН, що буде нами наведено в наступній публікації.
Література
- Gasbarrini A., Corazza G.R., Gasbarrini G., Montalto M.1st Rome H2-Breath Testing Consensus Conference Working Group. Methodology and indications of H2-breath testing in gastrointestinal diseases: the Rome Consensus Conference //Aliment. Pharmacol. Ther. – 2009, Mar 30. –29 (suppl. 1). – P. 1-49.
- Levitt M.D. Volume and composition of human intestinal gas determined by means of an intestinal washout technique //N. Engl. J. Med. –1971. – 284. – P. 1394-1398.
- Levitt M.D., Bond J.H. Jr. Volume, composition, and source of intestinal gas // Gastroenterology. – 1970. – 59. – P. 921-929.
- Levitt M.D., Donaldson R.M. Use of respiratory hydrogen (H2) excretion to detect carbohydrate malabsorption // J. Lab. Clin. Med. – 1970. – 75. – P. 937-945.
- Мухина Ю.Г., Чубарова А.И., Гераськина В.П. Современные аспекты проблемы лактазной недостаточности у детей раннего возраста. Вопросы детской диетологии 2003; 1, (1): 50-56.
- Abramowitz A., Granot E., Tamir I. et al. Two-hour lactose breath hydrogen test. J. Pediatr Gastroenterol Nutr. 1986 Jan; 5(1): 130-3.
- Сorazza G.R., Sorge M., Strocchi A. et al. Methodology of the H2 breath test.II. Importance of the test duration in the diagnosis of carbohydrate malabsorption Dig Dis Sci,1993 Nov; 38(11):2010-6.
- Solomons N.W., Viteri F.E., Hamilton L.H. Application of a sim-ple gas chromatographic technique for measuring breath hydrogen // J. Lab. Clin. Med. – 1977. – 90. – P. 856-862.
- Solomons N.W., Barillas C. The cut-off criterion for a positive hydrogen breath test in children: a reappraisal // J. Pediatr. Gastroenterol. Nutr. – 1986. – 5. – P. 920-925.
- Филиппский Г.К., Климов Л.Я., Возненко А.А. и др. Определение углеводов и органических кислот в кале у детей грудного возраста с непереносимостью лактозы, получающих высоколактозное питание. Педиатрия. – 1996. – том 4. – c. 22-259.
- Климов Л.Я. О генезе ложноотрицательных результатов лактозотолерантного теста у детей грудного возраста. Клиническая лабораторная диагностика 2000; № 7: 15-17.
- Cochet B., Griessen M., Balant L. et al. Schweiz Med Wochenschr. – 1981 Feb 7. – Vol.111. – № 6. – P. 192-3.
- Усенко Д.В. Лактазная недостаточность у детей / Д.В. Ксенко, А.В. Горелов // Педиатрия. – 2009. – № 1. – С. 33-36.
- Талалаев А.Г. Морфология и патогенез нарушений пищеварения и всасывания в тонкой кишке у детей. Автореф. дисс. ... д. мед. наук. – М. , 1992.
- Lerch M.M., Rieband H.C., Feldberg W., Matem S. Concordance of Indirect methods for the detection of lactose malabsorption in diabetic and nondiabetic subjects. Digestion . –1991. – Vol. 48. – № 2. – P. 81-88.
- Spender Q.W., Crone C.E., Stallings V.A. Assessment of linear growth of children with cerebral palsy, use of altenative measures to height or length. Development Med Child Neuroll. –1989. – Vol.31. – № 2. – P. 206-214.
- Heitlinger L.A., Rossi T.M., Lee P.C., Lebenthal E. Human intestinal disaccharidase activities: correlation with age, biopsy technique and degree of villus atrophy. J Ped Gastroenterol Nutr. – 1991. – Vol.12. – № 2. – P. 204-208.
- Sterch E.S., Mills P.R., Fransen J.A. Biogenesis of intestinal lactase-phlorizin hydrolas in adults with lactose intolerance. Evidence for reduces biosynthesis and slowed-down maturation in enterocytes. Journal of Clinical Investigation 1990; 86: 4: Р. 1329-1337.
- Чубарова А.И. Морфо-функциональные особенности тонкой кишки у детей грудного возраста с поражением центральной нервной системы. Автореф. дисс. ... канд. мед. наук. – М., 1996.
- Ledochowski М. Hydrogen Breath tests, Verlag Ledochowski, Innsbruck, 2008.
- Lembcke B. Lactose-Toleranz-Test. In: Thomas L, ed. Labor und Diagnose. Frankfurt: TH-Books-Verl. – Ges., 1998. – Р. 429-431.
- Casellas F., Malagelada J.R. Applicability of short hydrogen breath test for screening of lactose malabsorption. Dig Dis Sci 2003; 48:1333-8.