24 листопада, 2015
Гиперчувствительность к глютену без целиакии: дискуссионные вопросы
В последние годы произошло три существенных изменения в понимании глютеновой токсичности и целиакии. Во-первых, благодаря появлению новых стратегий диагностики понятие целиакии расширилось и теперь включает неклассические проявления заболевания, которые все чаще определяются у детей и взрослых [1]. Во-вторых, изменился подход к диагностике целиакии, и в новых руководствах указывается возможность в определенных случаях устанавливать диагноз у детей и подростков без биопсии двенадцатиперстной кишки [2, 3]. В других руководствах, сфокусированных на ведении заболевания у взрослых, дуоденальная биопсия остается неотъемлемой составляющей диагностического процесса [4]. В-третьих, возникла концепция непереносимости глютена без целиакии (НГБЦ). В Европе, США и Австралии значительная часть в целом здорового населения стала придерживаться безглютеновой диеты как части образа жизни [5], что указывает (но не доказывает) реальность НГБЦ как нозологии. В настоящей статье рассматриваются признаки, отличающие НГБЦ от целиакии, а также доказательная база наличия НГБЦ, включая исследования как с подтверждающими, так и с противоречащими результатами (табл.).
Определения
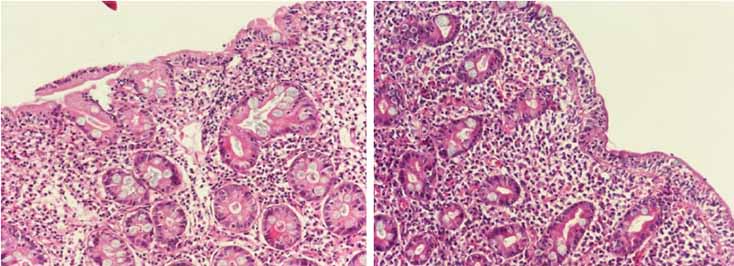
Целиакия определяется как хроническая иммуноопосредованная энтеропатия тонкого кишечника, вызываемая воздействием поступающего с пищей глютена у генетически предрасположенных лиц [6]. Старое определение включало термины «типичная», «атипичная» и «латентная» целиакия (сегодня их использование не рекомендуется). Целиакия характеризуется позитивностью по антителам класса иммуноглобулинов А (IgA) к тканевой трансглутаминазе 2 (TG2) в сыворотке, которые в настоящее время являются наиболее эффективным скрининговым тестом на целиакию. Наличие HLA-DQ2 (DQA1*0501, *0505) или HLA-DQ8 (DQB1*0201, *0202) может подтверждать диагноз целиакии, однако у большинства пациентов из стран Запада эти типы HLA присутствуют у 25 и 30% здоровых лиц соответственно. И наоборот, отсутствие этих типов HLA является очень сильным негативным предиктором в отношении целиакии, что делает эти тесты особенно полезными у пациентов, уже находящихся на безглютеновой диете. Тем не менее основу диагноза продолжают составлять результаты гистологического исследования биоптата слизистой двенадцатиперстной кишки, а именно наличие гипертрофии крипт и атрофии кишечных ворсинок [7]. Среди гистологических изменений наиболее индикативной в отношении целиакии является атрофия кишечных ворсинок, в то время как гипертрофия крипт как единственного признака и интраэпителиальный лимфоцитоз обладает значительно меньшей предиктивной ценностью. Так, интраэпителиальный лимфоцитоз чаще встречается при других, не связанных с глютеном состояниях и у клинически здоровых лиц [8]. Отдельным состоянием является аллергия на пшеницу, характеризующаяся IgE-опосредованным ответом; также описана реактивность на пшеницу, не связанная с IgE [9].
Характеристика непереносимости глютена без энтеропатии
Диагноз НГБЦ следует рассматривать только при отрицательных результатах тестов на целиакию, отсутствии TG2-IgA на фоне обычной диеты, а также отсутствии зависимости HLA DQ2 или DQ8, которые могут быть несколько повышены у пациентов с НГБЦ. Кроме того, при НГБЦ отсутствуют характерные для целиакии гистологические изменения дуоденальной слизистой. От аллергии на пшеницу НГБЦ отличает отсутствие специфических IgE-антител. Симптомы НГБЦ больше всего напоминают проявления синдрома раздраженного кишечника (СРК) с диареей и абдоминальной болью [9] (рис.). Некоторые авторы считают НГБЦ причиной психических нарушений, включая аутизм и шизофрению [10-12]. У взрослых пациентов для подтверждения диагноза НГБЦ или аллергии на пшеницу, не связанной с глютеном, использовалась двойная слепая плацебо-контролированная провокационная проба (ДСПКПП) с глютеном или пшеницей [13]. Популяцию пациентов набирали ретроспективно из амбулаторной группы больных СРК, авторы провели ДСПКПП 276 пациентам. Гиперчувствительность к глютену документировали не по объективным данным, а на основании субъективных жалоб по визуальной аналоговой шкале (ВАШ). В результате был сделан вывод о наличии четкой взаимосвязи появления симптомов и употребления пшеницы [14]. Однако при последующем наблюдении было продемонстрировано, что активный компонент гиперчувствительности не является глютеновой фракцией, а представляет собой так называемые FODMAP (ферментируемые олиго-, ди- и моносахариды и полиолы) [15]. Эти данные могут указывать на недостаточную чистоту ингредиентов, применяющихся в провокационных пробах, а также подчеркивают ограничения субъективных жалоб как основания для установления диагноза вместо объективных индикаторов, которые, к сожалению, для НГБЦ отсутствуют.
Дети
Имеющиеся на сегодня данные свидетельствуют о том, что у значительной части детей с подозрением на целиакию, но не имеющих серологических и гистологических признаков этого заболевания, может присутствовать НГБЦ. ВАШ в педиатрической популяции использовать трудно, особенно у детей младшего возраста. По данному вопросу было опубликовано довольно масштабное исследование [16]; тем не менее, насколько нам известно, ДСПКПП у детей с гастроэнтерологическими жалобами не изучалась. Исследования с участием детей с аутизмом показали, что симптомы заболевания могут уменьшаться на фоне безглютеновой диеты [12].
Патофизиология
Несмотря на огромный интерес к глютену и глютен-обусловленным заболеваниям, биологические механизмы патогенеза НГБЦ остаются малоизученными. Существуют данные, указывающие на повышенную клеточность слизистой тонкой кишки, повышенную иммунную реактивность слизистой у пациентов с НГБЦ. В норвежском исследовании биопсийный материал, полученный от пациентов с НГБЦ, сравнивали с таковым больных СРК [17]. Продукция цитокинов – γ-интерферона (IFNγ) и белка резистентности к миксовирусам А (MxA) – была достоверно повышенной у пациентов с СРК, в то время как у больных с НГБЦ наблюдались менее выраженные изменения (повышение клеточности CD3-положительных Т-клеток и мРНК IFNγ) после пробы с глютеном. В пшенице обнаружены ингибиторы трипсина и амилазы (ATI), являющиеся сильными стимуляторами врожденных иммунных реакций, прежде всего стимуляции Toll-подобных рецепторов 4 (TLR4) моноцитов, макрофагов и дендритических клеток, что сопровождается высвобождением в кровоток ряда цитокинов (интерлейкина‑8 – IL‑8, фактора некроза опухоли – TNF) как у здоровых лиц, так и у пациентов с целиакией [18]. В совокупности эти данные указывают на активацию общих патогенетических механизмов целиакии и НГБЦ, а также других воспалительных состояний. Тем не менее других доказательств роли ATI в развитии НГБЦ пока не получено.
Перспективы
Поскольку надежные биомаркеры НГБЦ отсутствуют, диагноз приходится устанавливать на основании клинических признаков и симптомов (например, оцениваемых с помощью ВАШ, но предпочтительно использовать объективные методы, а именно ДСПКПП (кроме младенцев и детей младшего возраста). ДСПКПП является хорошо изученной процедурой, широко применяющейся в диагностике пищевой аллергии [19]. Недостаток данного подхода состоит в том, что симптомы пищевой аллергии обычно проявляются в течении нескольких минут, часов или дней после специфической провокации, тогда как симптомы НГБЦ могут развиваться спустя более продолжительный период времени (точно не установлен). Кроме того, доза глютена при ДСПКПП должна быть эквивалентной дозам, употребляемым с обычной пищей. В теории, ДСПКПП следует повторить по крайней мере дважды для минимизации риска случайной позитивности. Также следует учитывать, что у пациентов, подозревающих у себя пищевую аллергию, воспроизводимая реакция на причинный продукт наблюдается только в 1 случае из 3 [20], а у больных с предполагаемой НГБЦ этот показатель может быть еще ниже. Таким образом, существует необходимость в разработке новых, более удобных подходов к проведению ДСПКПП, при этом следует продолжать поиск точных биомаркеров.
Литература
1. Garampazzi A. et al. Clinical pattern of celiac disease is still changing. J Pediatr Gastroenterol Nutr 2007, 45:611-4.
2. Husby S. et al. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. J Pediatr Gastroenterol Nutr 2012, 54:136-60.
3. Hill P.G., Holmes G.K.T. Coeliac disease: a biopsy is not always necessary for diagnosis. Aliment Pharmacol Ther 2008, 27:572-7.
4. DiGiacomo D.V. et al. Prevalence of gluten-free diet adherence among individuals without celiac disease in the USA: results from the Continuous National Health and Nutrition Examination Survey 2009-2010. Scand J Gastroenterol 2013, 48:921-5.
5. Rubio-Tapia A. et al. ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol 2013, 108:656-76; quiz 677.
6. Ludvigsson J.F. et al. The Oslo definitions for coeliac disease and related terms. Gut 2013, 62:43-52.
7. Oberhuber G. et al. The histopathology of coeliac disease: time for a standardized report scheme for pathologists. J Gastroenterol Hepatol 1999, 11:1185-94.
8. Pellegrino S. et al. Redefining the intraepithelial lymphocytes threshold to diagnose gluten sensitivity in patients with architecturally normal duodenal histology. Aliment Pharmacol Ther 2011, 33:697-706.
9. Sanders D.S., Aziz I. Non-celiac wheat sensitivity: separating the wheat from the chat!. Am J Gastroenterol 2012, 107:1908-12.
10. Potkin S.G. et al. Wheat gluten challenge in schizophrenic patients. Am J Psychiatry 1981, 138:1208-11.
11. Magistris L. de, Picardi A. et al. Antibodies against food antigens in patients with autistic spectrum disorders. Biomed Res Int 2013, 2013:729349.
12. Whiteley P. et al. The ScanBrit randomised, controlled, single-blind study of a gluten- and casein-free dietary intervention for children with autism spectrum disorders. Nutr Neurosci 2010, 13:87-100.
13. Carroccio A. et al. Non-celiac wheat sensitivity diagnosed by double-blind placebo-controlled challenge: exploring a new clinical entity. Am J Gastroenterol 2012, 107:1898-906; quiz 1907.
14. Biesiekierski J.R. et al. Gluten causes gastrointestinal symptoms in subjects without celiac disease: a double-blind randomized placebo-controlled trial. Am J Gastroenterol 2011, 106:508-14; quiz 515.
15. Biesiekierski J.R. et al. No effects of gluten in patients with self-reported non-celiac gluten sensitivity after dietary reduction of fermentable, poorly absorbed, short-chain carbohydrates. Gastroenterology 2013, 145:320-8.e1-3.
16. Francavilla R. et al. Clinical, serologic, and histologic features of gluten sensitivity in children. J Pediatr 2014, 164:463-7.e1.
17. Brottveit M. et al. Mucosal cytokine response after short-term gluten challenge in celiac disease and non-celiac gluten sensitivity. Am J Gastroenterol 2013, 108:842-50.
18. Junker Y. et al. Wheat amylase trypsin inhibitors drive intestinal inflammation via activation of toll-like receptor 4. J Exp Med 2012, 209:2395-408.
19. Bock S.A. et al. Double-blind, placebo-controlled food challenge (DBPCFC) as an office procedure: a manual. J Allergy Clin Immunol Pract 1988, 82:986-97.
20. Goldman A.S., Anderson D.W., Sellers W.A., Saperstein S., Kniker W.T., Halpern S.R. Milk allergy I. Oral challenge with milk and isolated milk proteins in allergic children. Pediatrics 1963, 32:425-43.
Перевел с англ. Алексей Терещенко



