6 липня, 2015
Мікробіота, метаболізм та неалкогольна жирова хвороба печінки (За матеріалами монотематичної конференції Європейської асоціації з вивчення захворювань печінки)

26-28 лютого 2015 року у м. Інсбрук (Австрія) відбулася монотематична конференція Європейської асоціації з вивчення захворювань печінки (EASL) «Мікробіота, метаболізм та неалкогольна жирова хвороба печінки», у роботі якої взяли участь делегати з багатьох країн світу, у тому числі з України. Провідні фахівці з країн Європи та Америки доповіли про сучасні досягнення у дослідженні мікробіоти, розвитку метаболічних порушень та неалкогольної жирової хвороби печінки (НАЖХП). Крім того, учасники конференції мали унікальну можливість обговорити новації з провідними гепатологами, мікробіологами, гастроентерологами.
У вступній промові голова організаційного комітету Herbert Tilg наголосив, що НАЖХП в останні роки розглядають як одне з найбільш поширених захворювань печінки у всьому світі паралельно з пандемією ожиріння. НАЖХП характеризується широким спектром проявів від простого стеатозу до цирозу печінки та гепатоцелюлярної карциноми (ГЦК). Встановлено, що порушення обміну речовин і запалення відіграють вирішальну роль у розвитку ожиріння та пов’язаних із ним розладів, у тому числі НАЖХП. Окрім того, на підставі результатів проведених досліджень можна припустити, що ключову роль у виникненні метаболічних та імунних процесів, які є рушійними силами при цих захворюваннях, відіграє кишкова мікробіота, що бере участь у розвитку печінкового стеатозу та запалення за участю певних toll-like рецепторів (TLR) і прозапальних цитокінів, таких як фактор некрозу пухлини α (TNFα). Доповідач зазначив, що на сьогодні більшість даних стосовно мікробіоти та ожиріння, НАЖХП отримано завдяки проведенню досліджень на тваринах. Однак останнім часом з’явилися докази стосовно ролі кишкової мікробіоти в розвитку НАЖХП у людей. Так, у пацієнтів з неалкогольним стеатогепатитом (НАСГ) спостерігаються синдром надмірного бактеріального росту, порушення кишкової проникності, збільшення рівня циркулюючих ендотоксинів та TNFα. Результати проведених клінічних досліджень кишкового мікробіома підтвердили наявність значних відмінностей за типами, сімействами та родами домінуючих мікроорганізмів у здорових осіб та хворих із НАСГ. Так, у пацієнтів з ожирінням, НАСГ і здорових осіб значно відрізняються співвідношення Proteobacteria, Enterobacteriaceae та Escherichia. Крім того, останнім часом дослідження підтверджують існування схожих для ожиріння і цукрового діабету 2 типу «кишковомікробіотичних ознак», які в майбутньому дадуть змогу диференціювати пацієнтів із жировою інфільтрацією печінки і НАСГ та з’ясувати, що лежить в основі патологічних механізмів НАСГ.
З доповіддю про значення про- та протизапальних типів харчування у розвитку НАСГ виступила професор Ina Bergheim з Німеччини. За її словами, результати низки досліджень, проведених у людей та на тваринах, свідчать про те, що переважання у раціоні продуктів із високим вмістом жиру та холестерину, а також вживання певних вуглеводів, таких як фруктоза, можуть призвести до розвитку НАЖХП. Було показано, що у пацієнтів з НАЖХП спостерігається не тільки підвищення калорійності раціону, а і вживання багатих на фруктозу продуктів. Надмірне споживання фруктози збільшує ризик розвитку більш пізніх стадій захворювання (фіброзу). Крім того, в деяких дослідженнях продемонстровано, що, окрім способу життя та генетичних факторів, у патогенезі НАЖХП певну роль може відігравати збільшення проникності бактеріальних ендотоксинів. Наприклад, встановлено, що пацієнти з різними стадіями НАЖХП страждають на ендотоксемію, яка пов’язана з підвищеною проникністю кишкової стінки і зменшенням вмісту протеїнів щільного зв’язку (tight junction proteins), а також підвищеною експресією TLR та сигнальних каскадів у тканині печінки. На підставі результатів досліджень, що проводилися на тваринах, у харчуванні яких переважали продукти, багаті на фруктозу, доведено, що підвищена транслокація бактеріальних ендотоксинів з просвіту кишечнику та подальша активація TLR-4-залежних сигнальних каскадів у печінці можуть бути критичними факторами у розвитку НАЖХП. З’ясовано, що при тривалому прийомі фруктози зменшується кількість протеїнів щільного зв’язку у слизовій оболонці верхніх відділів тонкої кишки, підвищується рівень ендотоксинів у портальній вені та індукуються TLR-4-залежні сигнальні каскади в печінці. Схожі результати були отримані в дослідах на тваринних моделях, коли використовували дієти, збагачені жиром. Дієти з обмеженням вживання цукру, але збагачені пробіотиками та іншими нутрієнтами (вторинними сполуками рослинного походження), можуть не тільки бути корисними при лікуванні порушень функції печінки, а й сприяти корекції рівнів ендотоксинів. Таким чином, модифікація дієти або прийом пробіотиків впливають на кишкову мікробіоту та проникність кишкової стінки і можуть бути ефективними під час лікування НАЖХП.
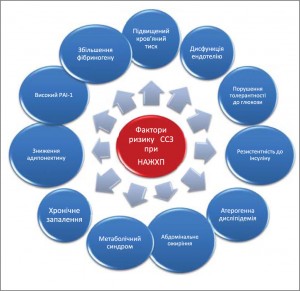
Доповідь Eleonora Scorletti з Великої Британії була присвячена зв’язку НАЖХП із серцево-судинними захворюваннями (ССЗ). Її презентація була сфокусована на клінічних даних, що підтверджують концепцію НАЖХП як мультисистемної хвороби з високим серцево-судинним ризиком. У хворих на НАЖХП дуже часто спостерігаються ознаки метаболічного синдрому (МС), а також безліч інших факторів ризику ССЗ (рис. 1).
Цей висновок має важливе клінічне значення для розвитку майбутніх серцево-судинних подій у таких пацієнтів. Згідно з результатами метааналізу 27 досліджень існує тісний зв’язок між НАЖХП і атеросклерозом, що підтверджують гістологічно або за допомогою методів візуалізації та кількох маркерів субклінічних проявів атеросклерозу, таких як збільшення товщини інтими-медії сонної артерiї (16 досліджень), збільшення кальцифікації сонної артерії (7 досліджень), порушення вазодилатації (7 досліджень) та артеріальної жорсткості (6 досліджень). Усі ці асоціації були незалежними від класичних факторів ризику ССЗ і МС у широкому діапазоні груп пацієнтів. Було проведено близько 20 ретроспективних і проспективних досліджень, встановлено зв’язок між НАЖХП, діагностованою за допомогою біопсії або візуалізації, та ризиком розвитку фатальних і нефатальних кардіоваскулярних подій. Крім того, НАЖХП є фактором ризику розвитку цукрового діабету 2 типу та гіпертензії – двох важливих факторів ризику виникнення ССЗ. Що стосується НАЖХП, діагностованої за допомогою візуалізації, результати низки великих перспективних досліджень також незмінно свідчать про те, що вона асоціюється з підвищеним ризиком фатальних і нефатальних СС-подій незалежно від встановлених СС-факторів ризику в осіб з або без цукрового діабету 2 типу. Автори метааналізу, опублікованого у 2011 році, дійшли висновку, що у хворих на НАЖХП ризик фатальних і нефатальних СС-подій був удвічі вищим.
Сьогодні стає очевидним, що розвиток НАЖХП пов’язаний з порушеннями обміну речовин у міокарді. Результати досліджень доводять, що у пацієнтів з підвищеним вмістом жиру у печінці одночасно спостерігається збільшення вмісту жиру в міокарді.
Цікаво, що кардіальний стеатоз є сильним предиктором діастолічної дисфункції; аналогічні результати також було отримано у дітей з НАЖХП. Нещодавно було показано, що помірно підвищений рівень печінкових трансаміназ незалежно пов’язаний із збільшенням частоти випадків фібриляції передсердь (ФП) у когорті Framingham Heart Study. Доповідач Eleonora Scorletti зазначила, що її група отримала докази підвищеного ризику виникнення ФП за наявності НАЖХП. Останні дані свідчать, що НАЖХП також незалежно пов’язана зі збільшенням інтервалу QT, тобто є потужним предиктором шлуночкових аритмій і раптової серцевої смерті, що може частково пояснити підвищену смертність від ССЗ у осіб із НАЖХП. Нарешті, наявність атеросклерозу аортального клапана також пов’язана з НАЖХП незалежно від встановлених факторів ризику ССЗ.
Mark Hull з Великої Британії присвятив свою доповідь зв’язку між НАСГ та розвитком ГЦК і позапечінкових злоякісних пухлин. Наявність НАЖХП асоціюється з підвищеним ризиком розвитку як ГЦК, так і деяких пов’язаних з ожирінням позапечінкових злоякісних пухлин, таких як колоректальний рак. НАЖХП є однією з головних причин виникнення ГЦК. У більшості випадків ГЦК розвивається на тлі цирозу, але хронічне запалення, пов’язане з НАСГ, також може стимулювати гепатоканцерогенез за відсутності цирозу. Етіологічний внесок місцевих проканцерогенних механізмів, пов’язаних із НАЖХП, включаючи запальну сигналізацію та ліпотоксичний мутагенез ДНК, порівняно із системними чинниками, пов’язаними з надмірною масою тіла, не з’ясований.
Наявність надмірної маси тіла асоціюється з підвищеним ризиком розвитку раку стравоходу і колоректального раку. Результати проведених досліджень свідчать про зв’язок між вісцеральним ожирінням, метаболічним синдромом та його біомаркерами при цукровому діабеті 2 типу і ризиком розвитку раку стравоходу (аденокарциноми) і колоректального раку (аденокарциноми), а також з передраковими ураженнями – метаплазією Барретта й аденомами прямої кишки. На сьогодні вважається, що етіологічні фактори, які спричиняють розвиток НАЖХП в осіб з надлишковою масою тіла, у тому числі хронічне запалення і кишковий дисбіоз, спільні для колоректального канцерогенезу. Таким чином, нічого дивного, що дані досліджень підтверджують зв’язок НАЖХП (зокрема НАСГ) із підвищеним ризиком розвитку колоректальної аденоми й аденокарциноми. Нині тривають масштабні дослідження з вивчення взаємозв’язку між НАЖХП і ризиком розвитку раку стравоходу у пацієнтів з ризиком виникнення стравоходу Барретта.
Незважаючи на те що існують певні методологічні проблеми під час проведення ретроспективних досліджень, зокрема сумнівність зворотного причинно-наслідкового зв’язку, надзвичайно важливо продовжувати дослідження впливу навмисної втрати ваги на пов’язаний з ожирінням ризик розвитку раку. Крім того, необхідно досліджувати ефект збільшення фізичних навантажень на перебіг НАЖХП та ризик розвитку позапечінкового (колоректального) раку.
Провідний європейський учений у галузі НАЖХП Vlad Ratziu із Франції висвітлив питання лікування НАСГ за допомогою сучасних та перспективних препаратів. На його думку, оптимальне лікування НАСГ має стати пріоритетом для гепатологів-практиків. Прогресування захворювання і труднощі, з якими стикаються пацієнти під час дотримання призначеної дієти і зміни способу життя, потребують розроблення спеціальної фармакотерапії НАСГ. Результати досліджень Trial PIVENS підтвердили, що інсуліносенситайзер піоглітазон і вітамін Е спроможні частково покращити гістологічну картину при НАСГ.
Тривають випробування з тестування препаратів із плейотропною дією. Обетихолева кислота – агоніст фарнезоїдних X рецепторів (FXR) – чинить метаболічну і гепатопротекторну дію. Ця речовина зменшує ліпогенез і збільшує β-окислення жирних кислот, знижує глюконеогенез і покращує секрецію інсуліну, а також має протизапальну і, можливо, антифібротичну дію на печінку, нирки і кишечник. Дослідження IIb фази показало значне поліпшення стосовно всіх гістологічних змін при НАСГ і навіть при фіброзі.
Професор Ratziu представив препарат-кандидат GFT505 – агоніст рецепторів PPARα i PPARσ. Результати клінічного випробування II фази, у якому взяли участь кілька сотень пацієнтів, продемонстрували підвищення у них чутливості до інсуліну, зменшення рівня дисліпідемії, системних запальних маркерів і активності печінкових ферментів.
Доповідач наголосив, що за результатами досліджень на тваринах в обох моделях із НАСГ та фіброзом печінки встановлено покращення не тільки при експериментальному стеатогепатиті, а й при фіброзі. Велике випробування IIb фази GFT505 триває.
Ще одним перспективним кандидатом у лікуванні захворювань печінки є сенiкривiрок (CVC) – селективний інгібітор рецепторiв CCR2 і CCR5. CVC пригнічує поповнення, міграцію та інфільтрацію прозапальних моноцитів до місця пошкодження печінки, що має вплинути на запалення в печінці, а також знизити активацію і міграцію клітин Купфера і зірчастих клітин печінки (антифібротичний ефект). Під час майбутніх досліджень необхідно визначити, чи чинить CVC вплив на інсулінорезистентність жирової тканини через модуляцію запалення. Зараз триває велике випробування IIb фази CVC у пацієнтів з гістологічно підтвердженим НАСГ.
Інші підходи спрямовані на пригнічення печінкового ліпогенезу через інгібування різних ферментів, які регулюють ліпогенез. Одним із таких кандидатів є арамхол, який продемонстрував виражений антистеатогенний ефект у щурів і здатний зменшувати вміст тригліцеридів у печінці людей. Нині триває велике дослiдження IIb фази арамхолу порівняно з плацебо. Враховуючи те, що деякі з цих сполук можуть мати антифібротичний ефект, можливо, їх дія буде спрямована і на лікування стеатогепатиту.
Зовсім інший підхід застосовують у дослідженнях, у яких перевіряються антифібротичні молекули. Симтузумаб – це гуманізовані моноклональні антитіла, спрямовані проти ферменту LOXL2, який керує зшиванням колагенових волокон, що є ключем до прогресування фіброзу в печінці людей. Імуногістохімічні дослідження довели збільшення експресії LOXL2 у пацієнтiв з фіброзом печінки, пов’язаним з вірусним гепатитом С і з НАСГ. У дослiдженнi III фази сьогодні тестують парентеральне введення симтузумабу у хворих на НАСГ як із цирозом, так і без нього.
Професор Ratziu вважає, що якщо антистеатогеннi i антифібротичні препарати виявляться ефективними, це дасть можливість розробити індивідуальну патогенетичну терапію у хворих на НАСГ, спрямовану на припинення прогресування захворювання і профiлактику цирозу печінки.

Українська делегація взяла активну участь у роботі конференції. Так, серед 82 постерних доповідей учених із різних країн світу 7 представили делегати з України. Е.Г. Манжалій та О.М. Бака, які є дійсними членами Європейської та Американської асоціацій з вивчення захворювань печінки, представили постерну доповідь «Клінічна ефективність комбінованої терапії в лікуванні ожиріння» (рис. 2). Мета нашого дослідження полягала в оцінці зниження ваги на тлі комбінованої терапії адеметіоніном та синбіотиком (1,5 млрд живих бактерій Lactobacillus rhamnosus з фруктоолігосахаридами).
 Рис. 2. Вигляд постерної доповіді українських науковців «Клінічна ефективність комбінованої терапії в лікуванні ожиріння», представленої на конференції
Рис. 2. Вигляд постерної доповіді українських науковців «Клінічна ефективність комбінованої терапії в лікуванні ожиріння», представленої на конференціїНами було обстежено 37 пацієнтів з ожирінням (серед них 22 жінки та 15 чоловіків віком 28-53 роки; середній вік 44±3,2 року). Індекс маси тіла (ІМТ), що відповідає ожирінню 1 ступеня, виявлено у 69% хворих середнього віку 31,2±2,1 року, 2 ступеня – у 31% пацієнтів середнього віку 36,4±3,1 року. Вміст лептину в сироватці крові хворих перед лікуванням становив 39,7±2,5 нг/мл, адипонектину (АДН) – 4,2±1,7 нг/мл, інтерлейкіну-6 (ІL-6) – 15,2±2,9 пг/мл. Наявність синдрому надмірного бактеріального росту виявлено у 79% хворих, жирову інфільтрацію печінки – у 93% пацієнтів. Залежно від лікування учасників розподілили на дві групи. В основній групі (ОГ) додатково до раціонального харчування було призначено адеметiонін 800 мг/добу та синбіотик упродовж 3 міс. Хворі контрольної групи (КГ) отримували лише збалансоване харчування, поведінкову терапію та адекватні фізичні навантаження впродовж 30 хв/добу.
У результаті обстеження у хворих на ожиріння 1 ступеня в ОГ ІМТ після лікування становив 27,1±2,7, з ожирінням 2 ступеня – 31,8±2,9. Середній показник зниження маси тіла становив 8,5±1,16 кг порівняно з таким у КГ – 4,5±2,2 кг. У пацієнтів ОГ спостерігалося статистично достовірне зниження рівнів лептину 27,5±2,1 нг/мл, ІL-6 до 2,7±1,2 пг/мл; зменшення жорсткості печінки та показника аланінамінотрансферази, підвищення вмісту АДН у 45,2% пацієнтів, покращення показників ліпідограми. Достовірних змін рівня цитокінів та мікрофлори кишечнику в КГ не виявлено.
Отже, включення адеметіоніну та синбіотика до терапії хворих з ожирінням може сприяти зниженню маси тіла, нормалізації мікрофлори кишечнику та підвищувати ефективність лікування зазначених захворювань. Визначення вмісту лептину, який є центральним регулятором енергетичного балансу та маси тіла, а також маркером ожиріння в організмі, допомагає оцінити ефективність лікування. Підвищення рівня лептину залежить від ступеня ожиріння. Роль АДН у патогенезі ожиріння підтверджується тим фактом, що при зниженні ваги, покращенні клінічного стану хворих після лікування спостерігається підвищення рівня АДН.
Наше дослідження є актуальним, оскільки встановлено, що жирова тканина є потужним ендокринним органом, а ожиріння розглядається як запалення жирової тканини, при якому різко збільшуються продукція та секреція прозапальних адипокінів, відбувається дисрегуляція імунної системи. Утворюється хибне коло: порушення мікрофлори кишечнику, накопичення ендотоксинів, дисбаланс цитокінової регуляції, надмірне накопичення вільних радикалів. Тема нашого дослідження співзвучна зі змістом доповідей багатьох європейських та американських фахівців, які були представлені на конференції.