6 липня, 2015
Пробиотики и антибиотик-ассоциированная диарея: вместе навсегда?
В настоящее время пробиотические препараты, обладающие относительно неплохой доказательной базой, прочно вошли в клиническую практику. К тому же в последние годы сфера применения пробиотиков значительно расширилась: живые микроорганизмы применяются в терапии и гастроэнтерологии, пульмонологии и оториноларингологии, неонатологии и педиатрии, акушерстве и гинекологии, хирургии и урологии. Самым распространенным поводом для назначения пробиотика является профилактика антибиотик-ассоциированной диареи (ААД). Сейчас уже трудно себе представить ситуацию, когда при назначении какого-либо антибактериального препарата врач не посоветует пациенту принимать пробиотик. Что касается того, какие пробиотические штаммы целесообразно применять в той или иной клинической ситуации, врачи а posteriori считают, что пробиотики всегда будут использоваться для профилактики ААД. Кажется, ничто не сможет разлучить пару «пробиотик-ААД». Так ли это? Обратимся к современным данным доказательной медицины и попытаемся найти ответ на этот вопрос.
Верь опыту
В последние годы все больше врачей предпочитают полагаться на данные доказательной медицины и использовать в своей практике препараты, эффективность которых доказана в рандомизированных контролированных исследованиях (РКИ). Однако порой не ясно, результатам каких РКИ можно доверять, ведь иногда они противоречат друг другу. Например, в течение трех последних лет было проведено большое количество РКИ, рассматривавших эффективность различных пробиотических штаммов при ААД. В подавляющем большинстве случаев результаты РКИ чрезвычайно оптимистичны, лишь в небольшом проценте случаев целесообразность назначения пробиотиков оценивается сдержанно и крайне редко констатируется полное фиаско живых микроорганизмов в профилактике и лечении ААД.
В качестве яркого примера очень высокой оценки применения пробиотиков при ААД можно привести работу S. Wong и соавт. (2014). В этом РКИ приняли участие больные с повреждением спинного мозга, которые нуждались в назначении антибиотика (n=164, средний возраст 50,1±17,8 года). Проводя рандомизацию пациентов, исследователи рекомендовали одним больным (n=76) одновременно с антибактериальным препаратом принимать пробиотик (6,5×109 живых Lactobacillus casei, штамм Shirota, один раз в сутки на протяжении 7 дней), а другим участникам назначали антибиотик без сопутствующей пробиотической поддержки (n=82). Оказалось, что распространенность ААД была значительно ниже у пациентов, получавших L. casei, по сравнению с группой отсутствия приема пробиотика (17,1 vs 54,9%; р<0,001). Исследователи подчеркнули интересный факт: ААД чаще страдали больные, имевшие недостаточную массу тела (64,1 vs 33,3%; р<0,01) или принимавшие ингибиторы протонной помпы (38,4% vs 12,1%; р=0,022). Перечислив независимые факторы риска развития ААД, S. Wong и соавт. подчеркнули, что отсутствие пробиотической поддержки (отношение рисков 8,46) может спровоцировать появление ААД.
С.Р. Selinger и соавт. (2013) не смогли дать однозначную оценку целесообразности профилактического применения пробиотика VSL#3. Сравнив частоту возникновения ААД у больных, получавших этот пробиотический препарат (n=117), с аналогичным показателем у пациентов, принимавших плацебо (n=112), исследователи оказались перед дилеммой: констатировать эффективность пробиотика или сделать нейтральный вывод? Ведь по данным анализа intention-to-treat (ITT – статистического анализа данных всех пациентов, получивших хотя бы одну дозу исследуемого препарата или плацебо), межгрупповые различия были недостоверными (4,3% в основной группе vs 8,9% в группе плацебо; р=0,19). И только по данным анализа per protocol (РР – статистического анализа данных пациентов, завершивших исследование в соответствии с протоколом), распространенность ААД была достоверно меньше у лиц, получавших пробиотик (0% в основной группе vs 11,4% в группе плацебо; р=0,006). В итоге авторы сделали выбор в пользу РР-анализа и заявили, что «VSL#3 предупреждает развитие ААД».
Отрицательные результаты при применении Saccharomyces boulardii (S. boulardii) получили Р. Pozzoni и соавт. (2012). Рекомендовав 7-дневный прием S. boulardii или плацебо 275 пожилым пациентам (средний возраст 79,2±9,8 года), исследователи диагностировали ААД у 13,3% больных, получавших плацебо, и 15,1% пациентов, принимавших пробиотик (ОР 1,16). Кроме того, ученые выявили 5 случаев Clostridium difficile-ассоциированной диареи (СD-АД), из них – 2 (2,0%) в группе плацебо и 3 (2,8%) в группе пробиотика (ОР 1,49). Проанализировав показатели смертности в обеих группах, авторы исследования также не выявили статистически значимых различий (12,7% в основной группе vs 15,6% в группе плацебо; р=0,60). Основываясь на полученных данных, Р. Pozzoni и соавт. констатировали, что пробиотические штаммы S. boulardii не эффективны в профилактике СD-АД у пожилых пациентов.
Пробиотики, ААД и пульмонология
Подобные разногласия были зафиксированы и в РКИ, исследовавших эффективность пробиотиков в профилактике ААД у пульмонологических больных. Так, в небольшом пилотном исследовании, выполненном L. Cimperman и соавт. (2011), была подтверждена целесообразность применения пробиотических штаммов. К этому выводу исследователи пришли, сравнив распространенность ААД у больных с различной пульмонологической патологией (пневмония, абсцесс легкого, хроническое обструктивное заболевание легких, бронхит), принимавших антибактериальные препараты. При проведении антибиотикотерапии пациентам рекомендовали дополнительно принимать пробиотик (n=13; Lactobacillus reuteri, штамм АТСС 55730) или плацебо (n=10) на протяжении 4 нед. Оказалось, что пациенты, принимавшие L. reuteri, реже страдали от ААД, чем больные, получавшие плацебо (соответственно 7,7 vs 50%; р=0,02).
Однако есть и работы, в которых были получены отрицательные результаты. Например, H.J. Song и соавт. (2010), отобрав 214 пациентов с различными инфекциями дыхательных путей и рандомизировав их для приема лактобацилл (n=103) или плацебо (n=111) на протяжении 14 дней, не смогли доказать преимущество использования живых микроорганизмов в профилактике ААД: эта патология была диагностирована у 3,9% больных, получавших пробиотик, и у 7,2% пациентов, принимавших плацебо (р=0,44).
Эффективность профилактики ААД с помощью пробиотиков исследовалась также и в педиатрической популяции. Например, Y.J. Zheng и соавт. (2012) установили, что применение комбинированного пробиотика, содержащего 5×109 КОЕ Clostridium butyricum и Bifidobacterium, позволяет снизить риск ААД у детей на 53,6% (ОР 0,419; р=0,008). К такому выводу исследователи пришли, обследовав популяцию детей, больных пневмонией, в возрасте от 3 мес до 3 лет (n=372). Частота развития ААД у пациентов, получавших пробиотик (n=193), была значительно ниже, чем у больных, принимавших плацебо (n=179): 7,8% vs 16,8% соответственно, р<0,05.
В другом РКИ, проведенном также с участием детей, были получены интересные данные (L.S. Shan и соавт., 2013). На протяжении 1-й фазы исследования всем детям внутривенно вводили антибактериальные препараты по поводу острого инфекционного заболевания нижних дыхательных путей (n=333). Детей рандомизировали для проведения монотерапии антибиотиком (группа В; n=166) либо для комбинированного назначения антибактериального препарата и пробиотика (группа А; 500 мг/сут S. boulardii, n=167) на протяжении 2 нед. Пациентов из группы В, у которых развился диарейный синдром в течение 2-недельного курса антибиотикотерапии или 2 нед спустя, дополнительно рандомизировали для проведения пероральной регидратационной терапии (группа В2) или для приема S. boulardii одновременно с регидратационными препаратами (группа В1). Оказалось, что распространенность диареи у детей, получавших пробиотик, была значительно ниже, чем в группе сравнения (7,9 vs 29,2%; ОР 0,27), а прием S. boulardii уменьшал риск развития ААД (4,3 vs 19,4%; ОР 0,22). У 42 детей, вошедших в состав группы В, развился диарейный синдром. Назначение им S. boulardii на протяжении 5 дней позволило уменьшить частоту опорожнения кишечника (р<0,05) и увеличить темпы выздоровления (91,3% в группе В1 vs 21,1% в группе В2; р<0,001). Средняя продолжительность диареи в группе В1 была короче, чем в группе сравнения (2,31±0,95 vs 8,96±1,07 дней; р<0,01). По мнению L.S. Shan, назначение S. boulardii детям, получающим внутривенные антибиотики, является эффективным методом профилактики ААД.
Статистика знает все: от метаанализа к рекомендациям
Некоторую ясность в вопрос целесообразности применения пробиотиков для профилактики ААД смогла внести такая наука, как статистика. Небольшой размер индивидуальных исследований и противоречивые результаты РКИ послужили поводом для проведения углубленного статистического анализа с использованием метаанализов. Среди ряда таких публикаций следует особо выделить работу G. Micklefield и соавт. (2014), в которой изучалась эффективность S. boulardii в профилактике ААД. Отобрав результаты 17 РКИ, отвечавших условиям включения в метаанализ, немецкие ученые установили, что эффективность пробиотика колебалась от 43,7 до 87,3% (данные 14 РКИ, n=4627). Метаанализ 5 РКИ с общим количеством пациентов 1076 человек продемонстрировал достоверное уменьшение риска развития ААД при применении S. boulardii с 17,2 до 6,7%. Метаанализ 4 РКИ, в которых пробиотик использовался при проведении эрадикации геликобактерий (n=1215), зафиксировал снижение вероятности ААД с 12,2 до 5,6%. Основываясь на полученных данных, G. Micklefield и соавт. рекомендуют использовать S. boulardii для профилактики ААД.
Проводя углубленный статистический анализ, другие исследователи не стали оценивать эффективность отдельных видов пробиотических бактерий, а анализировали целесообразность применения пробиотиков как таковых. Подобный подход использовали R. Pattani и соавт. (2013). В метаанализ, выполненный этими исследователями, вошли результаты 16 РКИ, при этом 4 РКИ были высокого качества, 5 РКИ – среднего, а 7 РКИ – низкого качества. Обобщенный анализ результатов указанных РКИ показал, что прием пробиотиков позволяет снизить риск как ААД (ОР 0,61), так и CD-АД (ОР 0,37). Показатель NNT (количество больных, которых необходимо пролечить для получения одного благоприятного исхода) для ААД был равен 11, а для CD-АД – 14. При проведении подгруппового анализа исследователи отметили, что наиболее значимое снижение указанных показателей имело место в хорошо спланированных исследованиях, в РКИ с длительным периодом наблюдения (не менее 4 нед), в исследованиях с комбинированной конечной точкой (ААД + CD-АД), а также в РКИ, в которых применялись только лактобациллы.
В одном из самых крупных метаанализов, посвященных проблеме профилактики ААД, пробиотики получили весьма высокую оценку. Проанализировав результаты 34 РКИ с общим количеством пациентов 4138 человек, E.J. Videlock и соавт. (2012) установили, что суммарное ОР развития ААД при приеме пробиотика было гораздо ниже, чем при применении плацебо (ОР 0,53; NNT 8).
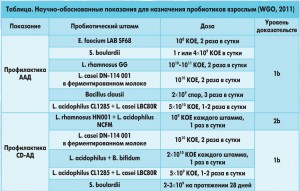
Суммируя все имеющиеся данные доказательной медицины, представители Всемирной гастроэнтерологической организации (WGO) в 2011 г. опубликовали Глобальное руководство «Пробиотики и пребиотики», где перечислили показания для назначения пробиотиков, указали вид и дозировку пробиотических штаммов (таблица), доказавших свою эффективность в профилактике ААД (F. Guarner и соавт., 2011).
Мнение экспертов Кокрановского сотрудничества
Эксперты Кокрановского сотрудничества, работы которых являются международным стандартом независимой оценки использования научных доказательств, также уделили пристальное внимание этой проблеме. Большую известность в медицинском научном мире получили результаты метаанализа, в котором исследовалась целесообразность профилактики ААД с помощью пробиотиков в педиатрической популяции (B.C. Johnston и соавт., 2011). В этот систематический обзор вошли результаты 16 РКИ с общим количеством пациентов 3432 человек. Эксперты Кокрановского сотрудничества отметили, что в РКИ использовались самые различные пробиотические штаммы: Bacillus, Bifidobacterium, Lactobacilli, Lactococcus, Leuconostoc cremoris, Saccharomyces и Streptococcus. При этом в 9 РКИ использовался препарат, содержащий один пробиотический штамм, в 4 РКИ применялась комбинация двух пробиотиков, в 2 РКИ назначали многокомпонентные пробиотические препараты, содержащие от трех до десяти штаммов бактерий. Эксперты установили, что распространенность ААД при приеме пробиотика была ниже, чем в контрольной группе (9% vs 18%; n=2874; ОР 0,52). Однако, по данным ITT-анализа, это превосходство не было статистически значимым, так как 60% детей, получавших пробиотик, и 20% детей, принимавших плацебо, выбыли из исследований на протяжении периода наблюдения. Значительно увеличив размер анализируемой выборки (n=3392), эксперты все равно получили похожие данные: распространенность ААД в группе пробиотика была меньшей, чем в контрольной группе (16% vs 18%; ОР 0,81). Проводя анализ гетерогенности исследований, ученые отметили интересный факт: оказалось, что высокие дозы пробиотиков (>5 млн КОЕ/сут) более эффективны в профилактике ААД, чем низкие (<5 млн КОЕ/сут; р=0,010). По данным РКИ, в которых применялись высокие дозы пробиотиков, распространенность ААД в основной группе составила всего 8%, а в контрольной группе – 22% (n=1474; ОР 0,40). В этих РКИ значение показателя NNT для предотвращения 1 случая диареи было достаточно высоким: он равнялся 7. При анализе результатов РКИ, в которых использовались низкие дозы пробиотика, выявленные межгрупповые различия были несколько ниже: распространенность ААД при применении пробиотика составила 8%, а в контрольной группе возросла до 11% (n=1382; ОР 0,80). «Несмотря на применение различных пробиотических штаммов, использование разнообразных схем и длительности их применения, а также разношерстное качество самих РКИ, суммарный статистический анализ свидетельствует о протекторном эффекте пробиотиков в отношении ААД», – отметили эксперты Кокрановского сотрудничества.
В 2012 г. корифеи Кокрановского сотрудничества представили результаты крупнейшего метаанализа, отбор РКИ для которого осуществляли два независимых эксперта (S. Hempel и соавт., 2012). В этот метаанализ вошли результаты 82 РКИ, в которых для профилактики или лечения ААД использовались разнообразные пробиотические штаммы (Lactobacillus, Bifidobacterium, Saccharomyces, Streptococcus, Enterococcus и/или Bacillus). Ученые подчеркнули, что в большинстве РКИ применялись лактобациллы в виде монотерапии или в комбинации с другими видами микроорганизмов. Объединенные результаты 63 РКИ с общим количеством пациентов 11 811 человек продемонстрировали достоверную взаимосвязь между приемом пробиотиков и уменьшением риска ААД (ОР 0,58; р<0,001). Показатель NNT был равен 13. В то же время из-за значительной гетерогенности объединенных результатов РКИ и недостаточности доказательств ученые не смогли определить, изменяется ли указанная взаимосвязь в зависимости от популяции, характеристики использованного антибиотика или вида назначенного пробиотического препарата. Констатируя, что применение пробиотиков приводит к снижению частоты ААД, эксперты Кокрановского сотрудничества указали на необходимость проведения хорошо спланированных исследований для уточнения, какие именно пробиотики обладают наибольшей эффективностью, и установления категории пациентов, нуждающихся в назначении пробиотиков для профилактики ААД при проведении антибиотикотерапии.
Еще один Кокрановский систематический обзор и метаанализ, выполненный под руководством J.Z. Goldenberg (2013), подтвердил эффективность пробиотиков в профилактике CD-АД у детей и взрослых. Отобрав 1871 РКИ, авторы включили в метаанализ результаты только 31 исследования с общим количеством пациентов 4492 человека. Анализ данных пациентов, завершивших исследование, продемонстрировал, что применение пробиотиков позволяет уменьшить риск CD-АД на 64% (данные 23 РКИ, n=4213). Распространенность CD-АД в группе пробиотика составила 2,0%, тогда как в группе плацебо или отсутствия лечения этот показатель был равен 5,5% (ОР 0,36). Несмотря на ряд выявленных недостатков, эксперты Кокрановского сотрудничества считают пробиотические штаммы эффективными в профилактике CD-АД.
Ахиллесова пята пробиотиков
Среди множества вышеописанных преимуществ пробиотиков у этих препаратов есть все же своя ахиллесова пята. В последние годы в медицинской прессе все чаще стали появляться публикации, рассматривающие безопасность пробиотиков и нежелательные реакции, возникающие при их применении. Известно, что побочные эффекты (метеоризм и дискомфорт в области живота) при применении пробиотиков развиваются достаточно редко, при этом они быстро и легко купируются. В то же время прием пробиотических штаммов может осложниться развитием пробиотик-ассоциированной бактериемии и фунгемии. В 2014 г. красочное описание подобного клинического случая представили турецкие ученые во главе с Z. Eren (2014). 88-летняя женщина поступила в стационар с жалобами на боли в левом бедре, гипотензию и спутанность сознания. В анамнезе жизни у этой пациентки имелись указания на артериальную гипертонию, хроническую почечную недостаточность, протезирование левого коленного сустава, рецидивирующие инфекции мочеполового тракта. Больная была госпитализирована в отделение интенсивной терапии с диагнозом «уросепсис», где ей назначили меропенем (500 мг 2 раза в сутки) и линелозид (600 мг 1 раз в сутки). В образцах мочи выделены штаммы Klebsiella pneumoniae и Escherichia coli, продуцирующие бета-лактамазу. На третий день антибиотикотерапии моча пациентки стала стерильной, а на четвертый день у больной развилась диарея, при этом тест на наличие токсина А/В Clostridium difficile был отрицательный. С целью купирования CD-АД пациентке был назначен пробиотик, содержащий подвид S. cerevisiae – S. boulardii (250 мг 2 раза в сутки). На второй день приема пробиотика уровень СРБ повысился с 23,2 мг/л до 100 мг/л без сопутствующей лихорадки, а в гемокультуре были обнаружены S. cerevisiae. После коррекции терапевтических назначений врачи смогли нормализовать состояние пациентки, снизить уровень СРБ и сывороточного креатинина до 9,1 мг/л и 1,2 мг/дл соответственно. Анализируя эту клиническую ситуацию, исследователи пришли к выводу, что фунгемия была обусловлена транслокацией из тонкого кишечника (ученые исключили вероятность контаминации центрального венозного катетера, так как пациентка принимала капсулы пробиотика, не вскрывая их). К предрасполагающим факторам ААД Z. Eren и соавт. отнесли старческий возраст пациентки и тяжелое течение основного заболевания.
Еще один случай развития S. boulardii-ассоциированной фунгемии описали немецкие ученые (J. Thygesen и соавт., 2012). У 79-летней женщины, страдавшей ревматоидным артритом и перенесшей резекцию толстого кишечника, течение постоперационного периода осложнилось развитием CD-АД. По этому поводу ей были назначены метронидазол, ванкомицин и пробиотик, содержавший штаммы S. boulardii. На 13-й день терапии у больной диагностирована фунгемия, вызванная S. boulardii. Врачи вынуждены были немедленно отменить пробиотик и использовать амфотерицин В для лечения фунгемии.
E.F. Zein и соавт. (2008) стали свидетелями пробиотик-ассоциированной септицемии у 54-летней женщины, больной сахарным диабетом 2 типа. Этот прецедент примечателен тем, что пациентка самостоятельно приняла решение о необходимости приема пробиотика для купирования явлений диспепсии. Больная приобрела и на протяжении 2 нед принимала многокомпонентный пробиотический препарат, основными составляющими которого были лактобактерии. Через 2 нед пациентка поступила в стационар с жалобами на повышение температуры до 40°С, тошноту, рвоту, головные боли. При бактериологическом обследовании в гемокультуре у нее выявлена Lactobacillus rhamnosus, чувствительная к пенициллину. Французским врачам удалось стабилизировать состояние пациентки и купировать явления септицемии при помощи амоксициллина.
К сожалению, описанные случаи далеко не полностью отражают все имеющиеся в мировой литературе данные о тяжелых осложнениях, развивающихся при приеме пробиотиков. Известны также случаи возникновения септического эндокардита и абсцесса печени при приеме лактобацилл и LGG соответственно. Проанализировав все доступные источники, описывавшие случаи пробиотик-ассоциированной бактериемии и фунгемии, R.J. Boyle и соавт. (2006) сформулировали концепцию идентификации лиц, имеющих большие и малые факторы риска возникновения этого осложнения. К большим факторам риска ученые отнесли иммуносупрессию (включая опухолевые процессы и общее истощение при тяжелых изнуряющих заболеваниях) и недоношенность у новорожденных; к малым – установку центрального венозного катетера, ухудшение функционирования эпителиального барьера тонкого кишечника (например, при диарее), клапанные пороки сердца (только для пробиотических штаммов Lactobacillus), введение пробиотиков через еюностому. Ученые рекомендуют с осторожностью назначать пробиотики пациентам, имеющим хотя бы один большой или ≥1 малого фактора риска. По данным N. Williams и соавт. (2010), чрезвычайно высокий риск развития пробиотик-ассоциированного сепсиса имеют тяжелобольные пациенты с выраженным иммунодефицитом и установленным центральным венозным катетером. В то же время S.P. Borriello и соавт. (2003) считают, что риск развития бактериемии при употреблении пробиотических штаммов лактобацилл чрезвычайно мал: меньше 1 случая на 1 млн потребителей, а риск развития фунгемии при приеме S. boulardii составляет всего 1 случай на 5,6 млн потребителей (K.D. Karpa и соавт., 2007).
Еще один «недостаток» пробиотиков зафиксировали M.G. Besselink и соавт. (2008). Немецкие ученые получили совершенно неожиданные данные, анализируя результаты многоцентрового РКИ, в котором исследовалась эффективность профилактического назначения пробиотиков больным с прогнозируемым тяжелым течением острого панкреатита. Первоначально ничто не предвещало каких-либо осложнений, все было буднично и рутинно. В спокойном рабочем порядке в исследование включали пациентов, у которых ожидалось тяжелое течение острого панкреатита (значение шкалы APACHE II ≥8 баллов, шкалы Imrie ≥3 баллов или уровень СРБ >159 мг/л). Также обыденно, в течение 72 ч от момента появления клинических симптомов заболевания, больных рандомизировали для приема плацебо (n=145) или многокомпонентного пробиотика (n=153) 2 раза в сутки на протяжении 28 дней. В качестве первичной конечной точки в этом РКИ выступали инфекционные осложнения (инфицированный панкреонекроз, бактериемия, пневмония, уросепсис или инфицированный асцит), развившиеся на протяжении 90 дней от момента включения в исследование. На этом привычная для исследователей обыденность закончилась. Полученные результаты повергли ученых в шок: оказалось, что назначение пробиотика не только не уменьшало риска инфекционных осложнений, но и приводило к возрастанию риска летального исхода. Вот какие данные были опубликованы в известном и авторитетном журнале Lancet: инфекционные осложнения чаще развивались у лиц, принимавших пробиотик, по сравнению с пациентами, получавшими плацебо (соответственно, 30% vs 28%; ОР 1,06). В группе пробиотика исследователи зафиксировали 24 (16%) летальных исхода, а в группе плацебо – 9 (6%) смертей (ОР 2,53). У 9 пациентов, вошедших в состав основной группы, диагностировали ишемию тонкого кишечника (в 8 случаях с фатальным исходом), тогда как в группе плацебо не было зафиксировано ни одного подобного случая (р=0,004). Резюмируя полученные данные, M.G. Besselink и соавт. рекомендуют отказаться от рутинного назначения пробиотиков больным острым панкреатитом, у которых прогнозируется тяжелое течение заболевания.
Еще одно РКИ преподнесло неприятный сюрприз своим создателям. Дизайн многоцентрового двойного слепого параллельно-группового исследования PLACIDE был тщательно продуман и спланирован в соответствии с рекомендациями экспертов Кокрановского сотрудничества (S.J. Allen и соавт., 2013). Самое широкомасштабное исследование в области изучения пробиотических штаммов продемонстрировало весьма неожиданные результаты, удивившие как своих создателей, так и представителей практической медицины. Нацеленное на сбор доказательств клинической эффективности высоких доз многокомпонентного пробиотика и определения соотношения «затраты/эффективность» при применении этого препарата в профилактике ААД и CD-АД, исследование PLACIDE было проведено в популяции пациентов старше 65 лет. В исследовании приняли участие больные, получавшие ≥1 антибактериального препарата (перорально или парентерально) и имевшие большую вероятность появления побочных эффектов при применении антибиотиков. Одной из отличительных особенностей PLACIDE является достаточно большой объем выборки: исследователи скринировали 17 420 пациентов и включили в исследование 2981 (17,1%) человек. Пациентов рандомизировали для приема пробиотика (n=1493; 50,1%) или плацебо (n=1488; 49,9%). Пробиотик представлял собой вегетарианскую капсулу, содержащую порошок из 6×1010 живых лиофилизированных бактерий: двух штаммов L. acidophilus (штамм 60 и 21; 3×1010 КОЕ) и двух штаммов бифидобактерий (B. bifidum и B. Lactis; 3×1010 КОЕ). Пробиотический препарат назначали по 1 капсуле в сутки и рекомендовали его принимать вместе с едой, между приемами антибактериальных препаратов, на протяжении 21 дня. Оказалось, что применение многокомпонентного пробиотика не влияло на такую первичную конечную точку, как распространенность ААД (включая CD-АД): этот показатель был сопоставим у лиц, принимавших пробиотик (159/1470; 10,8%) и плацебо (153/1471; 10,4%; ОР 1,04; р=0,71). При этом CD-АД была нехарактерной причиной ААД и имела место в 12/1470 (0,8%) случаях в группе пробиотика и в 17/1471 (1,2%) случаях в группе плацебо (ОР 0,71; р=0,35). Вторичные конечные точки, такие как длительность и тяжесть диареи, выраженность гастроинтестинальных симптомов, количество серьезных нежелательных явлений, качество жизни, также не отличались между двумя группами. Более того, анализ «затраты-эффективность» не подтвердил превосходства пробиотика над плацебо. Стоимость оказания общей медицинской помощи одному пациенту в группе пробиотика существенно не отличалась от таковой в группе плацебо. Прием пробиотика не влиял на стоимость стационарного лечения, длительность пребывания в стационаре, стоимость лечения диареи или антибиотикотерапии. К 8-й неделе лечения качество жизни у пациентов, получавших пробиотик, возросло на 0,01 QALY по сравнению с группой плацебо, однако выявленные различия были статистически недостоверными. Коэффициент эффективности дополнительных затрат (ICER) при приеме пробиотика через 1 год составил 22 701 фунтов стерлингов на 1 QALY (количество сохраненных лет качественной жизни). Таким образом, исследователи не получили доказательств эффективности приема пробиотиков при профилактике ААД. Несмотря на то что имела место тенденция к снижению CD-АД в группе пробиотика, применение пробиотических штаммов не приносило пользы пожилым пациентам, получавшим антибактериальные препараты.
Результаты исследования PLACIDE вызвали большой резонанс в медицинском сообществе. Одни ученые предлагают пересмотреть существующие рекомендации для назначения пробиотиков, другие, указывая на недостатки исследования (низкое этническое разнообразие пациентов и неохотное участие больных в исследовании из-за нежелания принимать дополнительный препарат), настаивают на проведении других широкомасштабных исследований. Пожалуй, самое оригинальное мнение высказал доктор медицины Nick Daneman (2013) из Университета Торонто (Канада): «PLACIDE – это самое крупное и самое безжалостное отрицательное исследование эффективности пробиотиков при ААД. Мы должны судить, смогут ли его результаты опрокинуть чашу весов со всей имеющейся доказательной базой пробиотиков. В то же время лактобациллы и бифидобактерии – это всего лишь два вида из огромного множества непатогенных бактерий, и мы должны решать, смогут ли они нарушить баланс различных экосистем кишечника». N. Daneman также подчеркнул, что результаты исследования PLACIDE, обладающего наивысшим, I уровнем доказательств, ставят под сомнение экономическую эффективность пробиотиков.
Зерно сомнения
Сомнения о целесообразности применения пробиотиков для профилактики ААД высказывают и авторы исследований, в которых с этой целью использовались другие препараты. Например, S. Rodriguez и соавт. (2014) предлагают применять метронидазол для профилактики CD-АД. К такому выводу исследователи пришли, выполнив ретроспективный когортный анализ 12 026 историй болезней пациентов, находившихся на стационарном лечении в одном из крупных американских госпиталей. Отобрав участников с высоким риском развития CD-АД (возраст ≥55 лет, прием антибактериальных – пиперациллин-тазобактам или ципрофлоксацин – и кислотосупрессивных – ингибиторы протонной помпы или блокаторы гистаминовых рецепторов – препаратов), ученые разделили больных на две группы. В первую группу вошли пациенты, которым по разным причинам назначали метронидазол до применения антибиотиков широкого спектра действия (n=811), а вторую группу составили больные, не принимавшие этот противомикробный препарат до проведения антибиотикотерапии (n=11215). Оказалось, что при приеме метронидазола распространенность CD-АД была гораздо ниже, чем при отсутствии назначения данного препарата: 1,4% (n=11) vs 6,5% (n=728) соответственно. Прием этого противомикробного препарата способствовал 80% снижению CD-АД (ОР 0,21; р<0,001).
Эксперты Американской коллегии гастроэнтерологов (ACG) также сомневаются в способности пробиотиков предупреждать развитие CD-АД (Surawicz C.M. и соавт., 2013). В практическом руководстве «Диагностика, лечение и профилактика инфекции Clostridium difficile» (2013) они отмечают: «Несмотря на имеющиеся доказательства о способности двух пробиотиков (Lactobacillus rhamnosus GG и S. boulardii) снижать распространенность ААД, в настоящее время недостаточно данных, подтверждающих эффективность пробиотиков в профилактике CD-АД».
Масло в огонь сомнений добавила и статья американского профессора D. Johnson (2014) под названием «Пробиотики: помощь или вред при ААД?». В этой публикации D. Johnson призывает практикующих врачей не спешить с назначением пробиотиков: «Не торопитесь рутинно назначать пробиотики пациентам, которым вы назначили антибактериальный препарат… Мы торопимся творить добро. Давайте остановимся и спросим себя, а не делаем ли мы зло. Несмотря на повсеместное использование пробиотиков, они могут и не быть правильным советом для пациентов».
Подводя итоги
В настоящее время сложилась достаточно противоречивая ситуация в отношении применения пробиотических препаратов. Одни ведущие ученые, руководствуясь данными доказательной медицины, поддерживают либеральное назначение пробиотических штаммов в соответствии с действующими рекомендациями. Другие авторитетные эксперты, учитывая данные недавно завершенных РКИ, рекомендуют отказаться от рутинного применения пробиотиков. Противники повсеместного использования пробиотиков подчеркивают, что следует относиться крайне осторожно к назначению этих препаратов пациентам с сопутствующим иммунодефицитом и недоношенным детям. Что же делать практикующему врачу? К какому лагерю примкнуть: продолжать активно использовать пробиотики или более взвешенно подходить к их назначению? Может быть, следует отказаться от применения пробиотиков и использовать другие препараты (метронидазол, ванкомицин или толевамер) для профилактики CD-АД? Ответы на все эти вопросы сокрыты в будущем, и только результаты новых РКИ, систематических обзоров и обновленных рекомендаций смогут подсказать, быть ли вместе паре «пробиотик-ААД» или ей суждено распасться?
Литература
1. Wong S. A Lactobacillus casei Shirota probiotic drink reduces antibiotic-associated diarrhoea in patients with spinal cord injuries: a randomised controlled trial // Br J Nutr. 2014 Feb; 111 (4): 672-8. doi: 10.1017/ S0007114513002973. Epub 2013 Sep 18.
2. Selinger C.P. Probiotic VSL#3 prevents antibiotic-associated diarrhoea in a double-blind, randomized, placebo-controlled clinical trial // J Hosp Infect. 2013 Jun; 84 (2): 159-65. doi: 10.1016/j.jhin.2013.02.019. Epub 2013 Apr 22.
3. Pozzoni P. Saccharomyces boulardii for the prevention of antibiotic-associated diarrhea in adult hospitalized patients: a single-center, randomized, double-blind, placebo-controlled trial // Am J Gastroenterol. 2012 Jun; 107 (6): 922-31. doi: 10.1038/ajg.2012.56. Epub 2012 Apr 3.
4. Guillemard E. Consumption of a fermented dairy product containing the probiotic Lactobacillus casei DN-114001 reduces the duration of respiratory infections in the elderly in a randomised controlled trial // Br J Nutr. 2010 Jan; 103 (1): 58-68.
5. Cimperman L. A randomized, double-blind, placebo-controlled pilot study of Lactobacillus reuteri ATCC 55730 for the prevention of antibiotic-associated diarrhea in hospitalized adults // J Clin Gastroenterol. 2011 Oct; 45 (9): 785-9. doi: 10.1097/MCG.0b013e3182166a42.
6. Fujita R. Decreased duration of acute upper respiratory tract infections with daily intake of fermented milk: a multicenter, double-blinded, randomized comparative study in users of day care facilities for the elderly population // Am J Infect Control. 2013 Dec; 41 (12): 1231-5. doi: 10.1016/j.ajic.2013.04.005. Epub 2013 Jul 23.
7. Smith T.J. Effect of Lactobacillus rhamnosus LGG® and Bifidobacterium animalis ssp. lactis BB-12® on health-related quality of life in college students affected by upper respiratory infections // Br J Nutr. 2013 Jun; 109 (11): 1999-2007. doi: 10.1017/S0007114512004138. Epub 2012 Oct 1.
8. Song H.J. Effect of probiotic Lactobacillus (Lacidofil® cap) for the prevention of antibiotic-associated diarrhea: a prospective, randomized, double-blind, multicenter study // J Korean Med Sci. 2010 Dec; 25 (12): 1784-91. doi: 10.3346/jkms.2010.25.12.1784. Epub 2010 Nov 24.
9. Kumpu M. Milk containing probiotic Lactobacillus rhamnosus GG and respiratory illness in children: a randomized, double-blind, placebo-controlled trial // Eur J Clin Nutr. 2012 Sep; 66 (9): 1020-3. doi: 10.1038/ejcn.2012.62. Epub 2012 Jun 13.
10. Zheng Y.J. Investigating Group for Prevention of AAD in Children with Pneumonia by Clostridium Butyricum and Bifidobacterium. [Multicenter, randomized, controlled clinical trial on preventing antibiotic-associated diarrhea in children with pneumonia using the live Clostridium butyricum and Bifidobacterium combined Powder]. Zhonghua Er Ke Za Zhi. 2012 Oct; 50 (10): 732-6.
11. Shan L.S. Prevention and treatment of diarrhoea with Saccharomyces boulardii in children with acute lower respiratory tract infections // Benef Microbes. 2013 Dec 1; 4 (4): 329-34. doi: 10.3920/BM2013.0008.
12. Micklefield G. Saccharomyces boulardii in the treatment and prevention of antibiotic-associated diarrhea // MMW Fortschr Med. 2014 Apr 17; 156 Suppl 1: 8-22.
13. Pattani R. Probiotics for the prevention of antibiotic-associated diarrhea and Clostridium difficile infection among hospitalized patients: systematic review and meta-analysis // Open Med. 2013 May 28; 7 (2): e56-67. eCollection 2013.
14. Videlock E.J. Meta-analysis: probiotics in antibiotic-associated diarrhoea // Aliment Pharmacol Ther. 2012 Jun; 35 (12): 1355-69. doi: 10.1111/j.1365-2036. 2012.05104.x. Epub 2012 Apr 24.
15. World Gastroenterology Organisation Global Guidelines. Probiotics and prebiotics. Francisco Guarner. 2011. http://www.worldgastroenterology.org/assets/ export/ userfiles/Probiotics_FINAL_20110116.pdf
16. Johnston B.C. Probiotics for the prevention of pediatric antibiotic-associated diarrhea // Cochrane Database Syst Rev. 2011 Nov 9; (11): CD004827. doi: 10.1002/ 14651858.CD004827.pub3.
17. Hempel S. Probiotics for the prevention and treatment of antibiotic-associated diarrhea: a systematic review and meta-analysis // JAMA. 2012 May 9; 307 (18): 1959-69. doi: 10.1001/jama.2012.3507.
18. Goldenberg J.Z. Probiotics for the prevention of Clostridium difficile-associated diarrhea in adults and children // Cochrane Database Syst Rev. 2013 May 31; 5: CD006095. doi: 10.1002/14651858.CD006095.pub3.
19. N. T. Williams. Probiotics // Am J Health Syst Pharm. 2010; 67 (6): 449-458.
20. Boyle R.J, Robins-Browne R.M., Tang M.L. Probiotic use in clinical practice: what are the risks? // Am J Clin Nutr 2006; 83: 1256-64.
21. Borriello S.P., Hammes W.P., Holzapfel W. et al. Safety of probiotics that contain lactobacilli or bifidobacteria // Clin Infect Dis. 2003; 36: 775-80.
22. Karpa K.D. Probiotics for Clostridium difficile diarrhea: putting it into perspective // Ann Pharmacother. 2007; 41: 1284-7.
23. Eren Z. Saccharomyces cerevisiae fungemia in an elderly patient following probiotic treatment // Mikrobiyol Bul. 2014 Apr; 48 (2): 351-5.
24. Thygesen J.B. Saccharomyces boulardii fungemia caused by treatment with a probioticum // BMJ Case Reports 2012; doi:10.1136/bcr.06.2011.4412
25. Zein E.F. Septicеmie а Lactobacillus rhamnosus chez une patiente diabеtique pregnant un traitement probiotique // Ann Biol Clin 2008; 66 (2) : 195-8.
26. Besselink M.G. Probiotic prophylaxis in predicted severe acute pancreatitis: a randomised, double-blind, placebo-controlled trial // Lancet. 2008 Feb 23; 371 (9613): 651-9. doi: 10.1016/S0140-6736(08)60207-X. Epub 2008 Feb 14.
27. Allen S.J. A high-dose preparation of lactobacilli and bifidobacteria in the prevention of antibiotic-associated and Clostridium difficile diarrhoea in older people admitted to hospital: a multicentre, randomised, double-blind, placebo-controlled, parallel arm trial (PLACIDE) // Health Technol Assess. 2013 Dec; 17(57): 1-140. doi: 10.3310/hta17570.
28. Daneman N. A probiotic trial: tipping the balance of evidence? // The Lancet, Vol. 382, Issue 9900. P. 1228-1230, 2013 Oct 12 .
29. Rodriguez S., Hernandez M.B., Tarchini G. et al. Risk of Clostridium difficile infection in hospitalized patients receiving metronidazole for a non-C difficile infection // Clin Gastroenterol Hepatol. 2014 Mar 27.
30. Surawicz C.M., Brandt L.J., Binion D.G. et al. Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections // Am J Gastroenterol. 2013; 108: 478-498.
31. David A. Johnson. Probiotics: Help or Harm in Antibiotic-Associated Diarrhea? // Medscape Gastroenterology > Disclosures September 10, 2014.
Подготовила Лада Матвеева