6 липня, 2015
Історичні аспекти та сучасні підходи до лікувальної тактики гострого панкреатиту
Гострий панкреатит – одне з найбільш поширених захворювань гастроінтестинального тракту, яке призводить до значних емоційних, фізичних та економічних втрат. За статистичними даними, у США в 2009 р. гострий панкреатит посів основне місце серед захворювань органів шлунково-кишкового тракту, а на його лікування з бюджету було виділено близько 2,6 млн доларів США [1]. Згідно з даними епідеміологічних досліджень, проведених з 1993 по 2003 р., виявлено зростання рівня захворюваності на гострий панкреатит із 40 до 73,4 випадку на 100 тис. населення [2].
У 70-80-х рр. минулого століття серед медичної спільноти помітно зростає інтерес до проблеми гострого панкреатиту. Причина полягала у суттєвому збільшенні захворюваності на гострий панкреатит, особливо його деструктивні форми. За статистичними даними тих років, гострий панкреатит у невідкладній хірургії посідав третє місце після гострого апендициту і гострого холециститу. Провідні фахівці вказували на збільшення частоти розвитку деструктивних форм гострого панкреатиту до 24,3-32,4% [3].
На той час існували різні типи класифікацій гострого панкреатиту. Деякі автори віддавали перевагу етіологічному фактору і поділяли панкреатити на інфекційні та неінфекційні. Інші (А.Н. Бакулєв, В.В. Виноградов, 1952; С.В. Лобачов, 1953) в основу класифікації поклали морфологічні зміни у паренхімі підшлункової залози. В.М. Глускіна (1972) вважала, що основою розвитку деструктивних процесів у підшлунковій залозі є етапність перебігу змін від гострого набряку до некрозу. В.В. Чаплинський і А.І. Гнатишак (1972) пропонували класифікації, що грунтувалися на клініко-анатомічних проявах гострого панкреатиту. Цей самий принцип покладено і в основу класифікації В.І. Філіна (1975), який виділяв: 1) гострий панкреатит у фазі набряку (серозний, серозно-геморагічний, або геморагічний); 2) гострий панкреатит у фазі некрозу (з геморагічним компонентом або без нього); 3) гострий панкреатит у фазі секвестрації. Крім того, автор виділяв 3 ступені інтоксикації: легкий, середній і тяжкий, з огляду на колір шкіри, пульс, рівень артеріального тиску, залишковий азот, активність трипсину та ліпази. В.С. Савельєв (1978) поділяв гострі панкреатити на набрякову форму, геморагічний і жировий панкреонекроз [3].
На той час переважали клінічні та лабораторні методи обстеження хворих. Велику увагу приділяли визначенню амілази крові та сечі. Серед методів інструментального обстеження переважно використовували оглядову рентгеноскопію черевної порожнини для диференційної діагностики гострого панкреатиту з перфоративною виразкою шлунка та дванадцятипалої кишки, а також диференційної діагностики з гострою кишковою непрохідністю. Для диференційної діагностики гострого панкреатиту та інфаркту міокарда проводили EКГ. Утім, частота діагностичних помилок коливалася в межах від 52% на долікарняному етапі до 17% в умовах хірургічного відділення (дані по м. Дніпропетровську, 80-ті рр. минулого століття) [3].
Згодом почали з’являтися роботи, які описували результати впровадження нових інформативних методів діагностики, – діагностичної лапароскопії та ангіографії. В цей час у діагностичний алгоритм впроваджуються достовірні і орієнтовні лапароскопічні симптоми гострого панкреатиту, що дає змогу суттєво покращити діагностику насамперед деструктивних форм [4].
З огляду на різноманітність клінічних проявів зазначеного захворювання розрізняють інтоксикаційний, інфарктоподібний, ілеусний та абдомінальний варіанти клінічного перебігу гострого панкреатиту. Цю класифікацію було опубліковано в монографії І.С. Білого, В.І. Десятерика, Р.Ш. Вахтангішвілі «Деструктивний панкреатит» (1986), а в її основу було покладено матеріали кандидатської дисертації В.І. Десятерика (1982).
Основними завданнями консервативної терапії тоді вважали: 1) вплив на місцевий патологічний процес; 2) дезінтоксикацію, профілактику та лікування порушень мікроциркуляції та реологічних властивостей крові; 3) коригуючу та замісну терапію, профілактику ускладнень [3]. В.М. Лащевкер (1982) визначив такі завдання консервативної терапії гострого панкреатиту: 1) боротьба с болем, нормалізація нейровегетативних функцій; 2) надання спокою підшлунковій залозі; 3) відновлення об’єму циркулюючої крові, корекція водно-електролітного і вуглеводного обмінів; 4) інактивація панкреатичних ферментів; 5) боротьба з інфекцією [5].
Під час лікування гострих панкреатитів широко використовували інгібітори протеаз. Медики вважали, що ефективність інгібіторів протеаз під час лікування набрякової форми панкреатиту значно вища, ніж при лікуванні деструктивного гострого панкреатиту. Проте багато авторів рекомендували введення інгібіторів протеаз і при панкреонекрозі, що сприяло зменшенню рівня інтоксикації, покращувало перебіг післяопераційного періоду [5]. Часто призначали апротинiн у дозі 40-100 тис. ОД протягом 3-4 діб. Нові можливості в лікуванні гострого панкреатиту з’явилися з використанням цитостатичних препаратів, які пригнічують синтез білка, зокрема внутрішньоклітинне утворення проферментів. Крім того, у комплексному лікуванні хворих на гострий панкреатит застосовували 5-фторурацил. Так, під нашим наглядом перебувало понад 200 хворих із гострим панкреатитом, які отримували в комплексному лікуванні 5-фторурацил. У переважній більшості випадків спостерігалося поліпшення стану хворих після застосування цих препаратів. Із 1978 року під час лікування тяжких форм гострого панкреатиту ми почали застосовувати локальну черезшлункову гіпотермію, яку проводили за допомогою апарата АЛГ-2 радянського виробництва. Вважалося, що гіпотермія була показана при тяжкому загальному стані хворого, виражених проявах інтоксикації, появі перитонеальних симптомів. Гіпотермію виконували на першу-другу добу після госпіталізації за відсутності ефекту від інтенсивної консервативної терапії [3].
Хірургічна тактика при гострому панкреатиті неодноразово змінювалася. На початку XX ст. вважали, що у хворих на гострий панкреатит показано оперативне втручання, так як і при перфоративній виразці шлунка та дванадцятипалої кишки чи при гострому апендициті. Висока післяопераційна летальність при гострому панкреатиті, а також певні успіхи консервативного лікування хворих з часом привели до того, що оперативного втручання з кожним роком потребувало все менше хворих. У 1980-ті рр. загальноприйнятою вважалася активно-вичікувальна тактика щодо хірургічного втручання при деструктивному панкреатиті. Переважна більшість авторів (А.А. Ширяев, 1975; А.А. Шалімов, 1978; В.І. Філін, 1979; Л.Д. Татаренко, А.Ф. Медведенко, 1985; Di Costanzo et al., 1974; Poy, Panuat, 1977; Poncelet, 1978) показаннями до оперативного втручання вважали: 1) сумніви у діагностиці та неможливість виключення іншого гострого хірургічного захворювання, яке потребувало б термінової операції (перфоративна виразка шлунка або дванадцятипалої кишки, кишкова непрохідність, гострий апендицит, деструктивний холецистит та ін.); 2) появу ознак перитоніту і відсутність ефекту від проведення консервативної терапії протягом 8-10 год. Необхідність оперативного втручання виникала при симптомах гнійного холангіту та рецидивуючій жовтяниці (А.А. Шалімов, В.І. Філін, 1971; Poncelet, 1978), при загальному тяжкому стані хворих і підозрі на геморагічні або некротичні ускладнення. Переважна більшість хірургів проводила операції в короткий термін хворим на гострий панкреатит при підозрі на захворювання жовчних шляхів (А.А. Шалімов, В.І. Філін, 1971; Poncelet, 1978).
Операції при деструктивному панкреатиті поділяли на три групи:
1) екстрені та негайні, які виконувалися у перші дні та години захворювання;
2) відстрочені, які виконувалися у фазі розплавлення і секвестрації некротичних осередків підшлункової залози і заочеревинної клітковини, через 10-14 та більше днів від початку захворювання;
3) планові, що виконувалися у період повної ліквідації гострого запалення у підшлунковій залозі, через 4-6 тижнів від початку захворювання, після завершення повного клінічного обстеження хворого (операції виконували для профілактики рецидиву гострого панкреатиту) [3].
На той час упровадження локальної черезшлункової гіпотермії і застосування 5-фторурацилу дало змогу майже удвічі зменшити хірургічну активність у лікуванні гострого панкреатиту, що сприяло зменшенню кількості випадків загальної летальності в 2 рази. Починаючи з 1985 р. лікувальну допомогу хворим з гострим панкреатитом почали надавати в міському центрі гострого панкреатиту на базі клінічної лікарні швидкої медичної допомоги. Ініціатором його створення, а потім і керівником був професор І.С. Білий. Вище описано наш досвід лікування гострого панкреатиту в умовах лікарні швидкої допомоги м. Дніпропетровська з 1977 по 1993 р.
Далі історія діагностики та лікування гострого панкреатиту продовжилася у м. Кривому Розі, яке у 1973 р. стало клінічною базою факультету удосконалення лікарів Дніпропетровського медичного інституту, а також в умовах спеціалізованого центру гострого панкреатиту на базі міської клінічної лікарні № 8, який почав діяти з 1994 р. Центр було започатковано за нашою ініціативою. В його становленні активну участь брав головний лікар міської клінічної лікарні № 8 В.І. Федін. На той час гострий панкреатит залишався важливою медичною та соціально-економічною проблемою. З одного боку, спостерігалося зростання рівня захворюваності, особливо серед людей працездатного віку, а з другого, – фіксувалися високі показники післяопераційної летальності, що характеризувало результати хірургічного лікування як незадовільні. За даними статистики, в Україні в 1999 р. гострий панкреатит у структурі ургентної хірургічної патології посідав, як і раніше, третє місце, поступаючись лише гострому апендициту та гострому холециститу, а за показником загальної післяопераційної летальності йому належало перше місце (В.Ф. Саєнко, 2000) [6]. Це пояснювалося несвоєчасним зверненням хворих за медичною допомогою, великою кількістю діагностичних помилок як на долікарняному етапі, так і в лікарні. Часто траплялися випадки недооцінки лікарем тяжкості перебігу захворювання, пізньої госпіталізації хворих до профільних хірургічних відділень, затримки із проведенням адекватних лікувальних заходів і, як наслідок, погіршення результатів хірургічного лікування. Так, у 1999 р. по Україні показник післяопераційної летальності при госпіталізації хворих на гострий панкреатит у термін понад 24 год від початку захворювання перевищував показник загальної летальності на 6% і становив 26,5% (В.Ф. Саєнко, 2000) [6]. У 97% випадків смерть була зумовлена розвитком ускладнень, які незалежно від перебігу запалення в підшлунковій залозі набували домінуючого характеру (В.С. Савельєв та співавт., 2001). Особливе місце серед таких ускладнень посідав парапанкреатит, тобто ураження клітковини заочеревинного простору навколо як підшлункової залози, так і більш віддалених ділянок. Парапанкреатит спостерігали у 84,2-100% хворих, що померли внаслідок прогресуючого гострого деструктивного панкреатиту (В.І. Філін та співавт., 1994; В.С. Земсков та співавт., 1998; Р.В. Вашетко та співавт., 2000).
Завдяки впровадженню сучасних науково-технічних досягнень за останні 10-15 років покращилися результати хірургічного лікування гострого деструктивного панкреатиту, майже втричі зменшився рівень післяопераційної летальності. Особливою проблемою в панкреатології залишаються гнійно-некротичні ускладнення гострого панкреатиту, які в більшості випадків є головною причиною летальних наслідків (Ю.Г. Бойко та співавт., 1998; В.А. Сипливий та співавт., 1999). Летальність серед хворих цієї групи найвища і коливається у межах від 33,3 до 88,3% (В.Н. Старосєк та співавт., 2000).
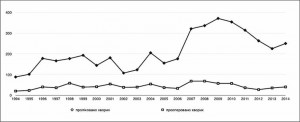
Наведемо основні показники роботи спеціалізованого центру з лікування гострого панкреатиту та як вони змінювалися за 20 років роботи центру на базі міської клінічної лікарні № 8 м. Кривого Рогу, яка є клінічною базою нашої кафедри. Всього було проліковано 4178 хворих, із яких 860 потребували хірургічного втручання (рис. 1).
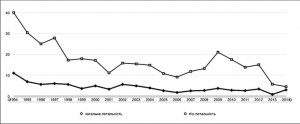
На початку роботи центру післяопераційна летальність становила 25-30%, загальна коливалася в межах 6% (рис. 2).
Починаючи з 1997 року до лікувальної схеми було внесено октреотид, синтетичний аналог соматотропного гормона, який сприяв значному зниженню секреторної активності шлунково-кишкового тракту та підшлункової залози, зменшував кровонаповнення черевного басейну. Одночасно із впровадженням октреотиду на фармацевтичному ринку з’явився перший представник карбапенемів – імiпенем/циластатин. Таке суттєве доповнення лікувальної схеми гострого панкреатиту на тлі накопиченого нами досвіду дало можливість починаючи з 1998 року суттєво зменшити кількість летальних випадків після операції.
На початку роботи центру переважала активна хірургічна тактика. Відпрацьовувалися методи своєчасної діагностики поширення запального процесу на парапанкреатичну клітковину. Було розроблено та впроваджено класифікацію парапанкреатитів, розроблено нові методи їх лікування. За матеріалами наших наукових досліджень асистент О.В. Котов успішно захистив кандидатську дисертацію «Хірургічне лікування гострого деструктивного панкреатиту, ускладненого парапанкреатитом» (м. Дніпропетровськ, 2002 р.).
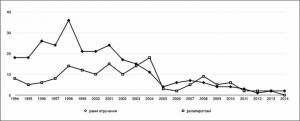
Водночас велику увагу приділяли післяопераційному перебігу хвороби, ранній діагностиці післяопераційних ускладнень та їх активному хірургічному лікуванню – релапаротомії. Матеріал знайшов відображення в кандидатській дисертації асистента В.В. Шаповалюка «Повторні оперативні втручання при деструктивному панкреатиті» (м. Київ, 2002 р.). Із накопиченням досвіду ранні втручання почали використовувати помітно менше (рис. 3).
Хворих, які страждали на деструктивний панкреатит, обов’язково направляли у відділення інтенсивної терапії та реанімації. Реаніматологи набували відповідного досвіду лікування таких хворих. Майже обов’язковим методом лікування тяжких форм гострого панкреатиту стало виконання епідуральної пролонгованої анестезії, використання методів ентеросорбції та плазмаферезу.
Суттєва зміна лікувальної тактики відбулася в 2006 р. після опублікування даних багатоцентрового дослідження [8], зокрема щодо важливості раннього ентерального харчування.
Так, змінилося ставлення до строків початку ентерального харчування у пацієнтів з гострим панкреатитом: початок такого харчування на 3-5-ту добу сприяв зменшенню кількості інфекційних ускладнень та летальних випадків. Також змінилося ставлення до холецистектомії. Згідно з Міжнародними рекомендаціями (2001 р.) холецистектомію бажано проводити після повного купірування запального процесу в підшлунковій залозі, краще в період поточної госпіталізації. Крім того, поступово зменшили використання холецистостомії, яку в перші роки роботи спеціалізованого центру гострого панкреатиту виконували майже всім пацієнтам з біліарним панкреатитом.
Щорічна кількість пацієнтів, які звертаються за допомогою, від часу заснування центру збільшилася майже втричі, до 300-400 хворих за останні роки. Водночас оперативна активність зменшилася майже вдвічі з 22,7% у 1995 р. до 10,2% у 2012 р.
На сьогодні у лікуванні хворих на гострий панкреатит широко використовуються малоінвазивні втручання. Поряд із лапароцентезом і лапароскопією у клініці застосовують діагностично-лікувальні пункції та дренування об’ємних утворень під ультразвуковим контролем.
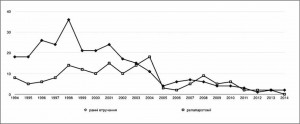
Впровадження малоінвазивних методів дозволило зменшити операційну травму та суттєво стримати прозапальний каскад реакцій, завдяки чому рідше виникає потреба в ранньому хірургічному втручанні (рис. 4).
В окремих випадках для визначення тактики ведення пацієнтів при панкреатиті біліарного ґенезу використовуємо ендоскопічну ретроградну холангіопанкреатографію (ЕРХПГ) та за потреби – ендоскопічну сфінктеротомію у пацієнтів з панкреатитом біліарного походження. Щороку вдосконалюється тактика лікування пацієнтів у відділенні інтенсивної терапії та реанімації: розрахунок об’єму інфузійної терапії, застосування антибіотикопрофілактики, модифікація антибіотикотерапії, показання до застосування штучної вентиляцiї легень.
Проаналізувавши дані роботи центру та порівнявши загальні показники летальності, яка у 1995 р. становила 6,9%, бачимо, що, наприклад, у 2012 р. цей показник дорівнював 3,4%, тобто зменшився вдвічі.
Завдяки використанню у роботі накопиченого нами досвіду, впровадженню сучасних наукових розробок, науковим дослідженням показники післяопераційної летальності з 30-40% у перші роки роботи центру зменшилися до 6-14% за останні роки.
Узагальнюючи наведені дані, можна сказати, що поступова динамічна зміна лікувальної тактики згідно із сучасними міжнародними рекомендаціями сприяла досягненню значних успіхів у боротьбі з такою тяжкою нозологією. Відмова від ранніх втручань, парадигма раннього ентерального харчування, зміщення акценту обсягу оперативних втручань у бік малоінвазивних, значні досягнення в галузі інтенсивної терапії, раціоналізація антибіотикотерапії сприяли високій якості лікування гострого панкреатиту. В основі цих змін лежить багаторічний досвід лікування великої кількості пацієнтів, постійна співпраця лікарів різних спеціалізацій, а також запровадження сучасних наукових досягнень та результатів досліджень.
Завершити екскурс в історію лікування гострого панкреатиту пропонуємо коротким оглядом сучасної тактики діагностики та лікування цієї патології за джерелами зарубіжної літератури з позиції доказової медицини.
Діагностика
Діагноз «гострий панкреатит» може бути поставлений за наявності як мінімум 2 критеріїв. Це абдомінальний біль, що відповідає захворюванню, і підвищення рівня амілази та/або ліпази крові як мінімум у 3 рази вище норми, та/або наявність ознак гострого панкреатиту на УЗД/КТ (рівень рекомендації В) [9].
Правильний діагноз гострого панкреатиту має бути встановлений у всіх пацієнтів протягом 48 год після госпіталізації (рівень рекомендації C) [10].
Етіологія гострого панкреатиту має бути визначена принаймні у 80% випадків, і не більш ніж у 20% захворювання має бути класифіковане як ідіопатичний гострий панкреатит (рівень рекомендації B) [10].
Хоч оцінка амілази широко доступна і забезпечує прийнятну точність діагнозу, де це можливо, проте оцінка ліпази має переваги для діагностики гострого панкреатиту (рівень рекомендації A) [10].
У сумнівних випадках може використовуватися візуалізація: на відміну від УЗД, яке часто буває неінформативним, візуалізація підшлункової залози за допомогою комп’ютерної томографії забезпечує більш точні свідчення наявності або відсутності панкреатиту (рівень рекомендації C) [10].
Пацієнти, у яких зберігається органна недостатність, спостерігаються ознаки сепсису або погіршення клінічного статусу через 6-10 днів після госпіталізації, потребують проведення КТ (рівень рекомендації B) [10].
Крім того, слід визначити ступінь тяжкості за Атлантськими критеріями. Однак органні порушення, що спостерігаються протягом першого тижня та ліквідуються упродовж 48 год, не можна вважати індикатором тяжкості гострого панкреатиту (рівень рекомендації B) [10].
Початкове ведення захворювання та запобігання ускладненням
Адекватне швидке заміщення рідини є найважливіший заходом для запобігання системним ускладненням. Хоч у більшості пацієнтів хвороба не перебігатиме тяжко і вирішуватиметься спонтанно, важливо на ранньому етапі виявити пацієнтів із ризиком розвитку ускладнень. Існують дані, що рання киснева підтримка і заміщення рідини можуть сприяти розрішенню органної дисфункції, що, у свою чергу, приводить до зниження смертності. Таким чином, слід рекомендувати, щоб усі пацієнти з гострим панкреатитом отримували адекватну кисневу підтримку і заміщення рідини доти, доки не будуть ліквідовані ознаки органних порушень. Сатурацію кисню слід вимірювати безперервно, кисневу підтримку необхідно призначати так, щоб підтримати артеріальну сатурацію більш як 95%. Рідини вводять внутрішньовенно (кристалоїди або колоїди, залежно від потреби) для забезпечення діурезу >0,5 мл/кг маси тіла на 1 год. Ступінь заміщення рідини має моніторуватися частим вимірюванням центрального венозного тиску у відповідних пацієнтів. Прийнято лікувати кожного пацієнта агресивно, допоки перебіг захворювання не стабілізується [10].
Агресивна інфузійна терапія необхідна всім пацієнтам, окрім хворих з кардіоваскулярними та/або нирковими коморбідними патологіями. Рання агресивна інфузійна терапія дає найбільший терапевтичний ефект у період від 12 до 24 год від початку захворювання (рівень рекомендації B) [9].
Рінгера лактат є найбільш доцільним ізотонічним кристалоїдом для проведення інфузійної терапії (рівень рекомендації B) [9].
Специфічна фармакотерапія
Не існує доведеної патогенетичної терапії для лікування гострого панкреатиту. Незважаючи на початкові позитивні результати, ефективність антипротеаз, антисекреторних агентів та протизапальних препаратів була спростована результатами великих рандомізованих досліджень [10, 12].
Використання антибіотиків
Інфікування некрозу – найтяжче місцеве ускладнення гострого панкреатиту, пов’язане з високою смертністю (до 40%). Існував великий інтерес до потенційного запобігання інфекції шляхом профілактичного призначення антибіотиків. Однак на підставі проведених на сьогодні досліджень не можна зробити однозначного висновку на користь доцільності антибіотикотерапії [10, 11].
Антибіотикотерапію слід призначати всім пацієнтам з екстрапанкреатичною інфекцією, такою як гострий холангіт, пневмонія, бактеріємія, інфекція сечового тракту (рівень рекомендації А) [9].
Рутинне призначення антибіотикопрофілактики не рекомендується (рівень рекомендації В) [9].
Крім того, не рекомендується призначення антибіотикотерапії у пацієнтів із неінфікованим панкреонекрозом (рівень рекомендації В) [9].
У разі якщо застосовується антибактеріальна профілактика, її потрібно проводити максимум 14 днів (рівень рекомендації B).
Нутритивна підтримка
Не існує ніякої переваги ентерального харчування при панкреатиті середнього ступеня тяжкості – такі пацієнти не потребують жодних дієтичних обмежень. У пацієнтів з тяжким перебігом хвороби звичайне харчування неможливе через нудоту. Штучне харчування може використовуватися при гострому панкреатиті для того, щоб запобігти ускладненням, або для забезпечення тривалої нутритивної підтримки. Вважається, що нутритивна підтримка допомагає зберегти функцію слизової оболонки і обмежує стимул для запальної відповіді. Ентеральне харчування є більш безпечним, ніж парентеральне, супроводжується меншою кількістю септичних ускладнень і менш дороге. За ефективністю між ними немає суттєвих відмінностей [10, 13].
Отже, якщо необхідна нутритивна підтримка, слід використовувати ентеральний шлях, якщо він не протипоказаний (рівень рекомендації A) [13].
Назогастральний шлях введення можна застосовувати, оскільки він є ефективним у 80% випадків (рівень рекомендації B).
Використання ентерального харчування може бути обмежене кишковою непрохідністю. Якщо вона збережеться протягом більш ніж п’яти днів, потрібно призначити парентеральне харчування [10].
Лікування біліарного панкреатиту
Термінова терапевтична ЕРХПГ має бути виконана пацієнтам із гострим панкреатитом з підозрюваною або доведеною жовчнокам’яною етіологією, які відповідають критеріям прогнозованого або фактичного тяжкого панкреатиту, або у випадках, коли є холангіт, жовтяниця, або доведено біліарну етіологію. Процедуру найкраще виконати протягом перших 72 год після появи болю. Всі пацієнти, що піддаються ранній ЕРХПГ при тяжкому біліарному панкреатиті, потребують ендоскопічної сфінктеротомії незалежно від того, знайдено чи ні камені у жовчній протоці (рівні рекомендації B і C) [10].
Пацієнтам з ознаками холангіту потрібно провести ендоскопічну сфінктеротомію або виконати дренування протоки стентом, щоб забезпечити розвантаження біліарної обструкції (рівень рекомендації A) [10].
Усі пацієнти з біліарним панкреатитом мають проходити радикальне лікування жовчнокам’яної хвороби протягом госпіталізації. Крім того, упродовж двох тижнів слід розробити чіткий план лікування (рівень рекомендації В) [4].
Хірургічне лікування
Пацієнти з тяжким гострим панкреатитом мають лікуватися у відділенні інтенсивної терапії з повним моніторингом та підтримкою систем (рівень рекомендації B) [13].
Пацієнтам з персистуючою симптоматикою і панкреонекрозом більш ніж 30% об’єму, а також з меншими ділянками некрозу та клінічною підозрою на сепсис слід виконувати візуально контрольовану тонкоголкову аспірацію, щоб отримати матеріал для культури через 7-14 діб після початку панкреатиту (рівень рекомендації B) [10].
Пацієнти з інфікованим некрозом потребують втручання для повного видалення всіх порожнин, що містять некротичний матеріал (рівень рекомендації B) [10].
Вибір хірургічної техніки для некрсеквестректомії та подальшого післяопераційного ведення залежить від індивідуальних особливостей та оцінки локального статусу (рівень рекомендації B) [10].
При виборі методу хірургічного втручання у пацієнтів з інфікованим панкреонекрозом малоінвазивні втручання мають суттєву перевагу (рівень рекомендації B) [9].
Таким чином, наш багаторічний досвід і сучасні дані літератури свідчать про те, що в тактиці лікування гострого панкреатиту, особливо його деструктивних форм, постійно відбуваються суттєві зміни.
Головними тенденціями цих змін є: раннє агресивне консервативне лікування в умовах відділень інтенсивної терапії та реанімації; показання до хірургічного лікування визначаються помітно менше та пізніше; серед методів хірургічного втручання все частіше перевагу віддають малоінвазивнним методам та визначенню факту інфікування панкреонекрозу; спостерігаються тенденції до більш широкого використання ендоскопічних методів вирішення протокової гіпертензії у хворих з біліарними панкреатитами.
Досвід лікування хворих на гострий панкреатит в умовах спеціалізованого центру свідчить про його перевагу.
Література
1. Fagenholz P.J. Direct medicalcosts of acute pancreatitis hospitalizations in the United States / Fagenholz P.J., Fernandez-del C.C., Harris N.S. et al. // Pancreas – 2007. – № 35. – P. 302-7.
2. Yadav D. Trends in the epidemiology of the first attack of acute pancreatitis: a systemic review / Yadav D. // Pancreas, 2006. – № 33. – P. 323-30.
3. Белый И.С., Десятерик В.И., Вахтангишвили Р.Ш. Деструктивный панкреатит: Библиотека практического врача. – К.: Здоровье, 1986.
4. Десятерик В.И. Диагностические критерии различных форм острого панкреатита. Диссертация … к.м.н., Днепропетровск, 1982, с. 142.
5. Лащевкер В.М. Острый панкреатит (клиника, диагностика, лечение). – К.: Здоров’я, 1982. – 666 с.
6. Котов О.В. Хірургічне лікування гострого деструктивного панкреатиту, ускладненого парапанкреатитом. Дисертація… к.м.н., Дніпропетровськ, 2002.
7. Шаповалюк В.В. Повторні оперативні втручання при деструктивному панкреатиті. Дисертація… к.м.н., Київ, 2002.
8. Besselink M.Y., De Bruin M.T., Rutter J.P., Boermeester M.A., Hofker H.S., Yooszen H.Y. // Surgical intervention in patients with necrotizing pancreatitis/ Dutch acute pancreatitis study group. – Br.j. Surg., 2006, May; 93(5) 593-9.
9. Tenner S. American College of Gastroenterology Guideline: Management of Acute Pancreatitis / S. Tenner, J. Baillie, J. DeWitt et al. // Am J Gastroenterol, 2013. – № 108. – P. 1400-1415.
10. Johnson С.D. UK guidelines for the management of acute pancreatitis / С.D. Johnson, R. Charnley, B. Rowlands et al. // Gut. – 2005. – № 54. – P. 1-9.
11. Isenmann R. Prophylactic antibiotic treatment in patients with predicted severe acute pancreatitis: a placebo-controlled, double-blind trial / Isenmann R., Runzi M., Kron M. et al. // Gastroenterology. – 2004. – № 126. – P. 997-1004.
12. Johnson C.D. Double blind, randomised, placebo controlled study of a platelet activating factor antagonist, lexipafant, in the treatment and prevention of organ failure in predicted severe acute pancreatitis / Johnson C.D., Kingsnorth A.N., Imrie C.W. et al. // Gut. – 2001. – № 48. – P. 62-90.
13. Gupta R. A randomised clinical trial to assess the effect of total enteral and total parenteral nutritional support on metabolic, inflammatory and oxidative markers in patients with predicted severe acute pancreatitis (APACHE II. or = 6) / Gupta R., Patel K., Calder P.C. et al. // Pancreatology. – 2003. – № 3. – P. 406-13.