24 грудня, 2019
Офтальмологічний дайджест: нові напрями в лікуванні хвороб органа зору
За матеріалами науково-практичної конференції з міжнародною участю «Рефракційний пленер’19», 17-19 жовтня, м. Київ
Рефракційний пленер, поза сумнівом, є однією з найочікуванішіх подій для офтальмологів й оптометристів України, адже ця традиційна щорічна конференція надає широкі можливості для професійного розвитку. У рамках заходу провідні вітчизняні спеціалісти галузі та закордонні фахівці представили доповіді, присвячені найцікавішим питанням сучасної офтальмології.

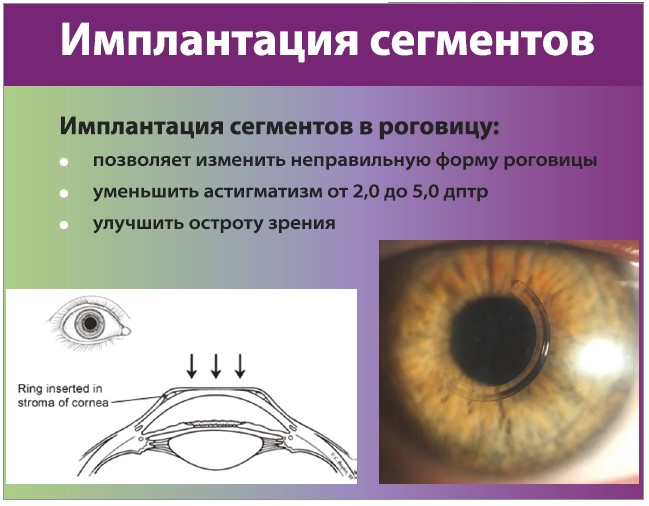 Заступник головного лікаря медичного центру «Новий зір» (м. Київ), кандидат медичних наук Тетяна Володимірівна Манойло ознайомила учасників із фемтолазерною імплантацією рогівкових сегментів для зорової реабілітації пацієнтів із кератоконусом. Вона нагадала присутнім, що крос-лінкінг рогівкового колагену є золотим стандартом терапії кератоконусу й інших ектазій рогівки. Це втручання дозволяє стабілізувати захворювання та підвищити міцність рогівки на 300%, однак у більшості випадків не покращує гостроту зору. Пацієнти з кератоконусом – переважно люди молодого віку, які потребують відновлення зорової функції. Однією з можливостей корекції в таких випадках є встановлення рогівкових сегментів (рогівкових кілець, кілець Феррара), які збільшують симетричність рогівки та покращують її форму. Кільця Феррара являють собою дугоподібні сегменти певної довжини з тригранним перерізом, зроблені з інертного для рогівки поліметилметакрилату. Імплантація цих сегментів дозволяє скоригувати форму рогівки, зменшити астигматизм і покращити гостроту зору. Згідно з результатами кератотопографічного дослідження, внутрішньорогівкові сегменти покращують регулярність поверхні рогівки та сприяють її ремоделюванню. Показаннями до імплантації сегментів є кератоконус 2-3 стадії; низька гострота зору в пацієнтів із кератоконусом, яка не підлягає корекції або коригується лише до 0,6-0,7; погана переносимість жорстких контактних і склеральних лінз; ектазія після ексимер-лазерної корекції; астигматизм високого ступеня після наскрізної кератопластики. Для встановлення сегментів товщина рогівки в найтоншому місці має бути не менше 380 мкм. Своєю чергою, протипоказаннями виступають помутніння строми рогівки на верхівці, кератометрія понад 70 діоптрій, гідропс, тонка рогівка, атопічні й алергічні захворювання, системна та місцева інфекційна патологія. Імплантація сегментів проводиться за допомогою фемтолазерної технології, перевагами якої є точна глибина формування тунелю, мінімальна травма рогівки, швидка імплантація сегмента, низький ризик його міграції. Підготовка пацієнтів передбачає відмову від контактних лінз на 2 тиж, місцеву крапельну анестезію під час операції, носіння м’яких контактних лінз упродовж 1 доби після втручання. Післяопераційне ведення пацієнтів включає топічні антибіотики та кортикостероїди протягом 1 тиж, зволожувальні краплі без консервантів (Теалоз® Дуо, Théa, Франція) протягом 3 міс, серветки для гігієни повік (Блефаклін®, Théa, Франція) протягом 2 тиж. Результат втручання оцінюють через 3 міс.
Заступник головного лікаря медичного центру «Новий зір» (м. Київ), кандидат медичних наук Тетяна Володимірівна Манойло ознайомила учасників із фемтолазерною імплантацією рогівкових сегментів для зорової реабілітації пацієнтів із кератоконусом. Вона нагадала присутнім, що крос-лінкінг рогівкового колагену є золотим стандартом терапії кератоконусу й інших ектазій рогівки. Це втручання дозволяє стабілізувати захворювання та підвищити міцність рогівки на 300%, однак у більшості випадків не покращує гостроту зору. Пацієнти з кератоконусом – переважно люди молодого віку, які потребують відновлення зорової функції. Однією з можливостей корекції в таких випадках є встановлення рогівкових сегментів (рогівкових кілець, кілець Феррара), які збільшують симетричність рогівки та покращують її форму. Кільця Феррара являють собою дугоподібні сегменти певної довжини з тригранним перерізом, зроблені з інертного для рогівки поліметилметакрилату. Імплантація цих сегментів дозволяє скоригувати форму рогівки, зменшити астигматизм і покращити гостроту зору. Згідно з результатами кератотопографічного дослідження, внутрішньорогівкові сегменти покращують регулярність поверхні рогівки та сприяють її ремоделюванню. Показаннями до імплантації сегментів є кератоконус 2-3 стадії; низька гострота зору в пацієнтів із кератоконусом, яка не підлягає корекції або коригується лише до 0,6-0,7; погана переносимість жорстких контактних і склеральних лінз; ектазія після ексимер-лазерної корекції; астигматизм високого ступеня після наскрізної кератопластики. Для встановлення сегментів товщина рогівки в найтоншому місці має бути не менше 380 мкм. Своєю чергою, протипоказаннями виступають помутніння строми рогівки на верхівці, кератометрія понад 70 діоптрій, гідропс, тонка рогівка, атопічні й алергічні захворювання, системна та місцева інфекційна патологія. Імплантація сегментів проводиться за допомогою фемтолазерної технології, перевагами якої є точна глибина формування тунелю, мінімальна травма рогівки, швидка імплантація сегмента, низький ризик його міграції. Підготовка пацієнтів передбачає відмову від контактних лінз на 2 тиж, місцеву крапельну анестезію під час операції, носіння м’яких контактних лінз упродовж 1 доби після втручання. Післяопераційне ведення пацієнтів включає топічні антибіотики та кортикостероїди протягом 1 тиж, зволожувальні краплі без консервантів (Теалоз® Дуо, Théa, Франція) протягом 3 міс, серветки для гігієни повік (Блефаклін®, Théa, Франція) протягом 2 тиж. Результат втручання оцінюють через 3 міс.
Теалоз® Дуо не лише відповідає вимогам до засобу для лікування та профілактики хвороби сухого ока (ХСО), а й перевищує їх, оскільки не містить консервантів і фосфатів. Гіпотонічний (гіпоосмолярний) Теалоз® Дуо коригує гіперосмолярність слізної плівки (СП), зменшує кількість запальних цитокінів у сльозі, регулює осмотичний баланс між СП і клітинами рогівки, зменшує пошкодження поверхні ока (ПО) при ХСО, у тому числі ятрогенній. Така потужність препарату Теалоз® Дуо пояснюється наявністю в складі двох активних речовин: трегалози та гіалуронової кислоти.
 Завідувач відділу вітреоретинальної та лазерної хірургії ДУ «Інститут очних хвороб і тканинної терапії ім. В.П. Філатова» НАМН України (м. Одеса), доктор медичних наук, професор Олексій Олексійович Путієнко у своїй доповіді представив сучасний підхід до лікування гемофтальму після вітректомії у хворих на проліферативну діабетичну ретинопатію (ПДР). За літературними даними, ПДР є основною причиною сліпоти в розвинених країнах (Abbate M. et al., 2017). Незважаючи на значний прогрес у хірургічному лікуванні цієї патології, частота післяопераційних геморагічних ускладнень (гемофтальмів) становить 25-75%. Кров у вітреальній порожнині, що не розсмоктується самостійно впродовж 2 міс, чинить токсичний вплив на сітківку ока і може призводити до офтальмогіпертензії, прогресування катаракти, розвитку хронічного увеїту тощо. Щонайменше в третини, а за даними D. H. Steel і співавт. (2015) – у половини таких пацієнтів виникає потреба в проведенні повторного оперативного втручання. Поствітректомічний гемофтальм значно сповільнює одужання та спричиняє зниження гостроти зору після операції.
Завідувач відділу вітреоретинальної та лазерної хірургії ДУ «Інститут очних хвороб і тканинної терапії ім. В.П. Філатова» НАМН України (м. Одеса), доктор медичних наук, професор Олексій Олексійович Путієнко у своїй доповіді представив сучасний підхід до лікування гемофтальму після вітректомії у хворих на проліферативну діабетичну ретинопатію (ПДР). За літературними даними, ПДР є основною причиною сліпоти в розвинених країнах (Abbate M. et al., 2017). Незважаючи на значний прогрес у хірургічному лікуванні цієї патології, частота післяопераційних геморагічних ускладнень (гемофтальмів) становить 25-75%. Кров у вітреальній порожнині, що не розсмоктується самостійно впродовж 2 міс, чинить токсичний вплив на сітківку ока і може призводити до офтальмогіпертензії, прогресування катаракти, розвитку хронічного увеїту тощо. Щонайменше в третини, а за даними D. H. Steel і співавт. (2015) – у половини таких пацієнтів виникає потреба в проведенні повторного оперативного втручання. Поствітректомічний гемофтальм значно сповільнює одужання та спричиняє зниження гостроти зору після операції.
Повторний крововилив у порожнину склоподібного тіла після операції поділяється на дві категорії: транзиторний (залишковий) і рецидивуючий. Транзиторним вважається крововилив, що виникає в перший день після операції (63-75% випадків). Причинами крововиливів є прогресуюча ретинальна неоваскуляризація, зумовлена ішемією сітківки; неоваскулярна глаукома; тромбоз центральної вени сітківки; екстракція катаракти тощо.
Авторські дослідження доповідача свідчать про те, що у 84% пацієнтів із ПДР і рецидивуючими гемофтальмами спостерігається перевищення норми фактора росту ендотелію судин (VEGF), що обґрунтовує доцільність застосування анти-VEGF препаратів у лікуванні цього ускладнення.
На сьогодні для терапії гемофтальму після вітректомії виконують повторну вітректомію з додатковою лазерною коагуляцією без тампонади вітреальної порожнини. Більшість хірургів при повторній вітректомії надає перевагу тампонаді склоподібного тіла стерильним повітрям або газом SF6 (Essex R. W. et al., 2018). P. T. Yang і співавт. (2016) запропонували повторні втручання з приводу рецидивуючого гемофтальму завершувати тампонадою вітреальної порожнини 10% газово-повітряною сумішшю перфторпропану.
На думку професора О. О. Путієнка, одним із найефективніших методів лікування рецидивуючих гемофтальмів після вітректомії у хворих на ПДР є методика замісної тампонади 20% газово-повітряною сумішшю перфторпропану. Використання зазначеної методики дозволяє найбільш тривало тампонувати поверхню сітківки, що запобігає рецидивам крововиливів. Результат втручання покращує комбінування замісної газової тампонади з анти-VEGF препаратами. У післяопераційному періоді рекомендоване додаткове застосування курсів консервативного лікування. Перевагу слід надавати комплексам з такими компонентами патогенетичного впливу, як ω3-поліненасичені жирні кислоти, ресвератрол, вітамін D. Ці компоненти доведено зменшують експресію VEGF факторів, покращують трофічні процеси в сітківці та підвищують ефективність лікування, саме тому в схему післяопераційного ведення хворих було включено відповідний комплекс – Нутроф® Форте.
 Доктор медичних наук Микола Миколайович Уманець (ДУ «Інститут очних хвороб і тканинної терапії ім. В.П. Філатова» НАМН України) охарактеризував ефективність вітректомії в лікуванні пацієнтів з епімакулярним фіброзом залежно від стадії захворювання. Клінічні прояви тракційного вітреомакулярного синдрому включають появу епімакулярної мебрани, тракційне відшарування макули, тракційний макулярний набряк (у тому числі діабетичний), ідіопатичний макулярний розрив (наскрізний, ламелярний). Класичні показання до вітректомії включають наявність епімакулярної мембрани 2 стадії, відчутне зниження гостроти зору, дискомфорт при читанні та роботі на близькій відстані.
Доктор медичних наук Микола Миколайович Уманець (ДУ «Інститут очних хвороб і тканинної терапії ім. В.П. Філатова» НАМН України) охарактеризував ефективність вітректомії в лікуванні пацієнтів з епімакулярним фіброзом залежно від стадії захворювання. Клінічні прояви тракційного вітреомакулярного синдрому включають появу епімакулярної мебрани, тракційне відшарування макули, тракційний макулярний набряк (у тому числі діабетичний), ідіопатичний макулярний розрив (наскрізний, ламелярний). Класичні показання до вітректомії включають наявність епімакулярної мембрани 2 стадії, відчутне зниження гостроти зору, дискомфорт при читанні та роботі на близькій відстані.
В авторському дослідженні вітректомію було доповнено препаратом Нутроф® Форте (Théa, Франція), який являє собою комплексний засіб для підтримання зору. Компонентами Нутроф® Форте є лютеїн і зеаксантин у необхідних дозах та потрібному співвідношенні, цинк, селен, вітаміни С, D та Е, ресвератрол, природні та захищені від окиснення ω3-поліненасичені жирні кислоти, виготовлені за запатентованою технологією Полярис (Silver synergy effect). Нутроф® Форте призначали по 1 капсулі 1 раз на 3-6 міс. У режим місцевого лікування було включено препарат Теалоз® Дуо, здатний достовірно знижувати рівень маркерів запалення ПО. Проаналізувавши отримані результати, автори зробили висновок, що вітректомія при лікуванні хворих з ідіопатичними епімакулярними мембранами найбільш результативна на ранніх стадіях захворювання.
 Сучасні аспекти лікування пацієнтів із запальними захворюваннями повік були розглянуті в доповіді професора кафедри офтальмології Національної медичної академії післядипломної освіти ім. П. Л. Шупика (м. Київ), доктора медичних наук Оксани Василівни Петренко. Блефарити – група захворювань повік різної етіології, в разі яких до патологічного процесу залучається вся повіка та/або її край. Частка блефаритів у структурі запальних захворювань органа зору становить 23,3%. Факторами ризику запальних уражень повік вважаються імунні порушення, гормональні розлади, інфекції, незбалансоване харчування, захворювання ендокринної системи та травного тракту, стреси. За перебігом блефарити підрозділяють на гострі, підгострі та хронічні, за клінічною картиною – на прості, лускаті й виразкові, за анатомічною локалізацією – на передні та задні. Передні блефарити включають неінфекційні (себорейні, токсичні, алергічні), інфекційні (бактеріальні, вірусні, паразитарні) та змішані, натомість причиною задніх блефаритів зазвичай є дисфункція мейбомієвих залоз або мейбоміїти (Gilbard J. P., 2009; Ben Ezra D., 2006).
Сучасні аспекти лікування пацієнтів із запальними захворюваннями повік були розглянуті в доповіді професора кафедри офтальмології Національної медичної академії післядипломної освіти ім. П. Л. Шупика (м. Київ), доктора медичних наук Оксани Василівни Петренко. Блефарити – група захворювань повік різної етіології, в разі яких до патологічного процесу залучається вся повіка та/або її край. Частка блефаритів у структурі запальних захворювань органа зору становить 23,3%. Факторами ризику запальних уражень повік вважаються імунні порушення, гормональні розлади, інфекції, незбалансоване харчування, захворювання ендокринної системи та травного тракту, стреси. За перебігом блефарити підрозділяють на гострі, підгострі та хронічні, за клінічною картиною – на прості, лускаті й виразкові, за анатомічною локалізацією – на передні та задні. Передні блефарити включають неінфекційні (себорейні, токсичні, алергічні), інфекційні (бактеріальні, вірусні, паразитарні) та змішані, натомість причиною задніх блефаритів зазвичай є дисфункція мейбомієвих залоз або мейбоміїти (Gilbard J. P., 2009; Ben Ezra D., 2006).
Загущення секрету мейбомієвих залоз призводить до утворення пробок у протоках. Густий секрет і зроговілі клітини епідермісу формують сприятливе середовище для розмноження кліщів та бактерій, які й провокують розвиток запалення (кісти, ячмені, флегмони, виразки, халязіони). Основні скарги при блефариті – відчуття печіння, свербіння та почервоніння повік, дискомфорт і сухість очей. Для діагностики застосовуються біомікроскопія, лабораторне вивчення вій тощо.
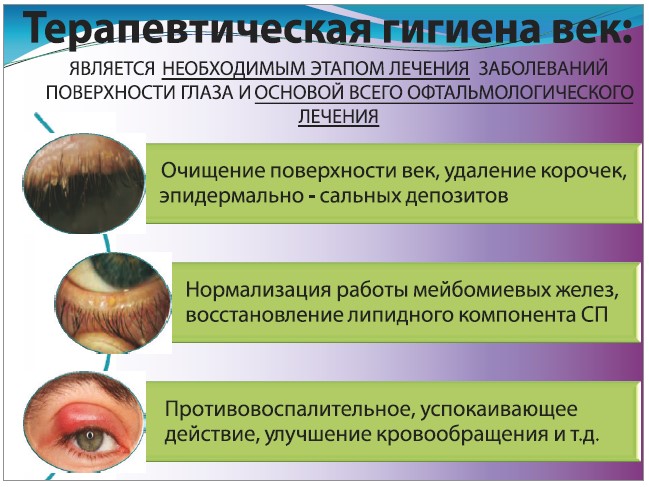 Базисними методами лікування є гігієна повік, фізіотерапія, медикаментозне лікування, корекція супутніх патологічних станів, дієта. Терапевтична гігієна повік – це науково-практичний напрям офтальмологічного лікування, спрямований на відновлення та покращення здоров’я повік, збільшення їхньої пружності (Полунин Г. С., 2014). Гігієна повік є необхідним етапом лікування хвороб ПО, оскільки дає можливість очистити поверхню повіки від кірочок й епідермально-сальних депозитів, нормалізувати роботу мейбомієвих залоз, відновити ліпідний компонент СП. Гігієна повік також має протизапальний, заспокійливий вплив і стимулює кровообіг. В арсеналі офтальмологічних засобів, які виробляє компанія Théa (Франція), наявні продукти для гігієни та нормалізації стану повік, а саме серветки Блефаклін® і гель Теагель®. Блефаклін® застосовується в комплексному лікуванні гострих і хронічних блефаритів, ячменів та халязіонів, мейбоміїтів, ХСО, демодекозу, дакріоциститів і кон’юнктивітів. Теагель® також є багатогранним засобом, що призначається при синдромі сухої повіки (блефарити, гіперкератози, наявність кірочок), мокнутті повік (екземи, виразковий блефарит, виворіт повіки), так званій палаючій повіці (алергічні ураження, сильна запальна реакція).
Базисними методами лікування є гігієна повік, фізіотерапія, медикаментозне лікування, корекція супутніх патологічних станів, дієта. Терапевтична гігієна повік – це науково-практичний напрям офтальмологічного лікування, спрямований на відновлення та покращення здоров’я повік, збільшення їхньої пружності (Полунин Г. С., 2014). Гігієна повік є необхідним етапом лікування хвороб ПО, оскільки дає можливість очистити поверхню повіки від кірочок й епідермально-сальних депозитів, нормалізувати роботу мейбомієвих залоз, відновити ліпідний компонент СП. Гігієна повік також має протизапальний, заспокійливий вплив і стимулює кровообіг. В арсеналі офтальмологічних засобів, які виробляє компанія Théa (Франція), наявні продукти для гігієни та нормалізації стану повік, а саме серветки Блефаклін® і гель Теагель®. Блефаклін® застосовується в комплексному лікуванні гострих і хронічних блефаритів, ячменів та халязіонів, мейбоміїтів, ХСО, демодекозу, дакріоциститів і кон’юнктивітів. Теагель® також є багатогранним засобом, що призначається при синдромі сухої повіки (блефарити, гіперкератози, наявність кірочок), мокнутті повік (екземи, виразковий блефарит, виворіт повіки), так званій палаючій повіці (алергічні ураження, сильна запальна реакція).
 Виступ доцента кафедри офтальмології Харківського національного медичного університету, кандидата медичних наук Олени Павлівни Мужичук стосувався ефективності та переносимості латанопросту без консервантів у пацієнтів із первинною відкритокутовою глаукомою (ПВКГ). ПВКГ – хронічна прогресуюча оптична нейропатія, яка супроводжується загибеллю гангліонарних клітин сітківки, що призводить до атрофії зорового нерва та втрати зорової функції. Оскільки ПВКГ є пожиттєвим захворюванням, прихильність до лікування відіграє провідну роль у контролі симптомів і запобіганні прогресуванню.
Виступ доцента кафедри офтальмології Харківського національного медичного університету, кандидата медичних наук Олени Павлівни Мужичук стосувався ефективності та переносимості латанопросту без консервантів у пацієнтів із первинною відкритокутовою глаукомою (ПВКГ). ПВКГ – хронічна прогресуюча оптична нейропатія, яка супроводжується загибеллю гангліонарних клітин сітківки, що призводить до атрофії зорового нерва та втрати зорової функції. Оскільки ПВКГ є пожиттєвим захворюванням, прихильність до лікування відіграє провідну роль у контролі симптомів і запобіганні прогресуванню.
Дослідження A. Arias і співавт. (2010), у якому взяв участь 191 пацієнт з ПВКГ, встановило, що найбільшу прихильність до лікування забезпечує латанопрост (81,6% проти 65,4% у групі травопросту, 60,4% у групі тимололу та 22,9% у групі біматопросту). Причинами низької прихильності можуть бути незручність у застосуванні та поява побічних ефектів, пов'язаних як із діючою речовиною, так і з наявністю консервантів. Так, консерванти здатні зумовлювати або збільшувати дискомфорт в очах, гіперемію, порушення з боку СП, ХСО.
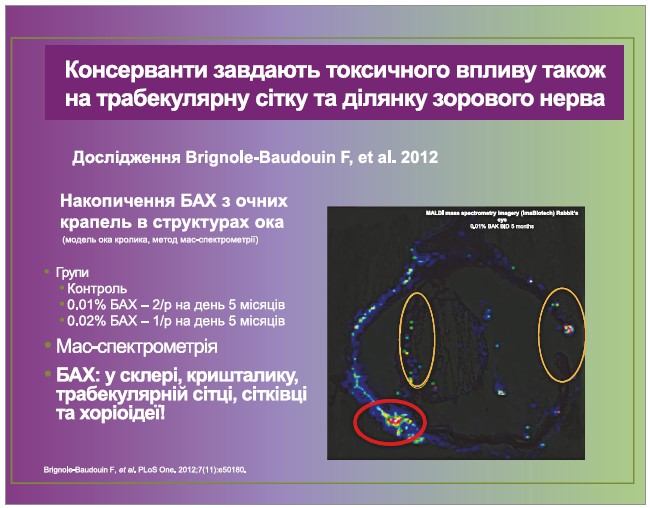 Один із найпоширеніших консервантів, що містяться в очних краплях, – бензалконію хлорид (БАХ) – характеризується широким спектром антимікробної й антимікотичної дії, проте має й низку недоліків, як-от виражений алергічний, токсичний, прозапальний та детергентний ефекти. БАХ індукує апоптоз, стимулює синтез супероксиду, збільшує рівень запальних медіаторів, зменшує щільність келихоподібних клітин, сприяє втраті мікроворсинок і розриву міжклітинних з’єднань клітин рогівки, руйнує СП, знижує сльозопродукцію. Але також ця речовина накопичується і токсично діє на епітеліальні клітини трабекули та ділянку зорового нерва, що несприятливо впливає на перебіг ПВКГ.
Один із найпоширеніших консервантів, що містяться в очних краплях, – бензалконію хлорид (БАХ) – характеризується широким спектром антимікробної й антимікотичної дії, проте має й низку недоліків, як-от виражений алергічний, токсичний, прозапальний та детергентний ефекти. БАХ індукує апоптоз, стимулює синтез супероксиду, збільшує рівень запальних медіаторів, зменшує щільність келихоподібних клітин, сприяє втраті мікроворсинок і розриву міжклітинних з’єднань клітин рогівки, руйнує СП, знижує сльозопродукцію. Але також ця речовина накопичується і токсично діє на епітеліальні клітини трабекули та ділянку зорового нерва, що несприятливо впливає на перебіг ПВКГ.
Порівняльні дослідження препаратів латанопросту з БАХ та без нього дозволили з’ясувати, що застосування латанопросту з консервантами асоціюється з більшою вираженістю гіперемії, а також із суттєвими змінами, деформаціями та потовщенням судин (Grupcheva C. et al., 2018).
В авторському дослідженні О. П. Мужичук, П.А. Бездітко та Т.В. Д'яконової вивчалися ефективність і переносимість препарату Монопрост, у пацієнтів з уперше виявленою ПВКГ. Монопрост – латанопрост без консервантів – інноваційна розробка компанії Thea, Франція. Сьогодні Монопрост є найбільш часто вживаним препаратом для лікування глаукоми серед продуктів без консервантів.
Через 3 міс лікування в групі з Монопрост середнє зниження внутрішньоочного тиску (ВОТ) становило 28,3±2,2 мм рт. ст., причому досягнутий показник був стабільним. У групі латанопросту з консервантом відповідний результат склав 26,9±1,2 мм рт. ст., однак у 4 учасників було зафіксовано рівень ВОТ, що перевищував цільовий, у зв’язку із чим їм було запропоновано додати до лікування дорзоламід. Ступінь гіперемії кон’юнктиви був істотно меншим у групі Монопросту (1,3 проти 2,9 бала в групі засобу з консервантом). Аналогічна закономірність простежувалася й стосовно рівня дискомфорту: 1,3 бала за суб’єктивною оцінкою в групі Монопрост (де 1 балл – відчуття повного комфорту, а 10 балів – нестерпний дискомфорт) та 6,5 балів – у групі консервантного аналога.
Автори дійшли висновку, що застосування Монопрост у пацієнтів із ПВКГ І-ІІ стадії сприяє досягненню вираженого стійкого гіпотензивного ефекту, завдяки відсутності консерванту Монопрост дуже добре переноситься і комфортний у застосуванні.
 Завідувач кафедри офтальмології Одеського національного медичного університету, доктор медичних наук, професор Людмила Віленівна Венгер привернула увагу аудиторії до показань до призначення аналогів простагландинів (АПГ), проілюструвавши виступ клінічними випадками. За прогнозами, кількість хворих на глаукому 2020 року становитиме 76 млн, а до 2040 р. зросте до 111,6 млн. Метою лікування глаукоми є підтримання зорової функції та прийнятної якості життя при доступних витратах. З‑поміж низки чинників ризику появи та прогресування глаукоми провідне місце посідають підвищення ВОТ та його добові флуктуації. Саме ці фактори призводять до розвитку ішемії та глаукомної оптичної нейропатії у зв’язку з порушенням перфузії ока та посиленим тиском на решітчасту пластину. Лікування глаукоми рекомендується розпочинати з монотерапії, при цьому відомо, що найбільш виражену гіпотензивну дію мають АПГ. Критеріями вибору препарату виступають ефективність у зниженні ВОТ, створення високої прихильності до лікування, місцева та системна безпека, зручність і комфорт у застосуванні, територіальна й фінансова доступність.
Завідувач кафедри офтальмології Одеського національного медичного університету, доктор медичних наук, професор Людмила Віленівна Венгер привернула увагу аудиторії до показань до призначення аналогів простагландинів (АПГ), проілюструвавши виступ клінічними випадками. За прогнозами, кількість хворих на глаукому 2020 року становитиме 76 млн, а до 2040 р. зросте до 111,6 млн. Метою лікування глаукоми є підтримання зорової функції та прийнятної якості життя при доступних витратах. З‑поміж низки чинників ризику появи та прогресування глаукоми провідне місце посідають підвищення ВОТ та його добові флуктуації. Саме ці фактори призводять до розвитку ішемії та глаукомної оптичної нейропатії у зв’язку з порушенням перфузії ока та посиленим тиском на решітчасту пластину. Лікування глаукоми рекомендується розпочинати з монотерапії, при цьому відомо, що найбільш виражену гіпотензивну дію мають АПГ. Критеріями вибору препарату виступають ефективність у зниженні ВОТ, створення високої прихильності до лікування, місцева та системна безпека, зручність і комфорт у застосуванні, територіальна й фінансова доступність.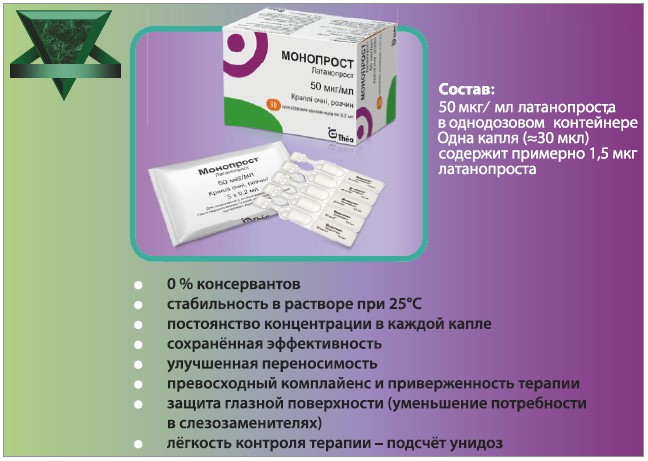
Метааналіз M. Cucherat і співавт. (2014) показав, що Монопрост (Théa, Франція) за своєю ефективністю не поступається іншим АПГ або навіть перевищує їхні результати та характеризується найкращою переносимістю серед вивчених препаратів. Переваги Монопросту включають відсутність консервантів, відмінну переносимість терапії, захист ПО та легкість контролю лікування за допомогою підрахунку унідоз. За даними дослідження PASSY, середнє покращення переносимості при переході з інших крапель на Монопрост дорівнює 46%. Важливо, що молекула латанопросту в складі Монопросту має нейропротекторні властивості, оскільки запобігає апоптозу гангліонарних клітин сітківки та сприятливо впливає на кровоток у ділянці диска зорового нерва.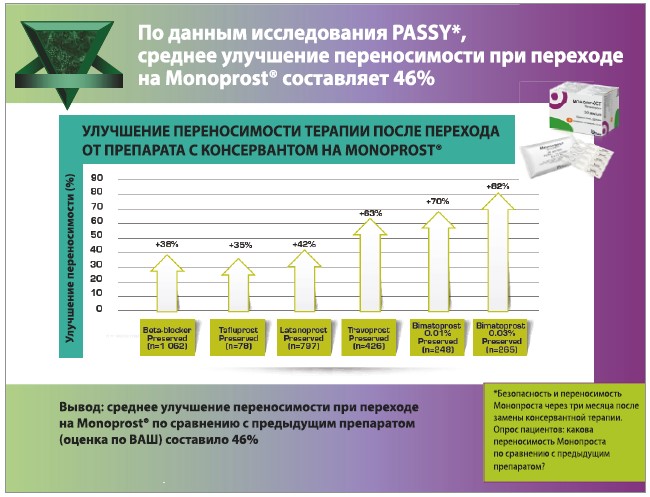
Згідно із сучасними поглядами, показання до призначення АПГ включають потребу в досягненні цільового ВОТ при ПВКГ, наявність глаукомної оптиконейропатії, високу осьову міопію (ВОМ) у віддаленому періоді після хірургічного втручання, прогресуючу ВОМ, наявність у пацієнта з глаукомою бронхіальної астми, недостатню ефективність терапії іншими препаратами, оперовану глаукому в стадії декомпенсації або в стадії компенсації у пацієнтів із вираженою глаукомною оптиконейропатією. Додатковими показаннями до застосування безконсервантних форм є захворювання ПО та носіння контактних лінз, ексимер-лазерна корекція або крос-лінкінг в анамнезі. Своєю чергою, протипоказання до лікування АПГ – вторинна та увеальна глаукома, макулярний набряк, волога форма вікової макулярної дегенерації, рецидивуючий увеїт, хронічні запальні захворювання повік, що не піддаються лікуванню, офтальмоонокологічні хвороби й індивідуальна непереносимість АПГ.
Ще одна доповідь професора Л. В. Венгер стосувалася рефракційних результатів катарактальної хірургії при ВОМ. Міопічна рефракція діагностується в 1,6 млрд населення світу. Однією з можливостей відновити зорову функцію в пацієнта з ВОМ є заміна кришталика. Одночасно з розвитком хірургічних технік і розробкою нових моделей штучних кришталиків зростають вимоги пацієнтів до якості отриманого в результаті операції зору.
Для розрахунку інтраокулярних лінз (ІОЛ) створено декілька формул. Згідно з рекомендаціями K. Hoffer, при виборі формули необхідно орієнтуватися на аксіальну довжину ока. Так, для очей <22 мм слід використовувати формули Haigis і Hoffer Q, для очей 22-24,5 мм – Haigis, Hoffer Q, Holladay I та SRK/T, 24,5-26 мм – Holladay I, >26 мм – SRK/T. Утім, розрахунок сили ІОЛ у пацієнтів із гіперметропією та міопією високого ступеня дотепер залишається складною проблемою. Для розрахунку ІОЛ для очей >26 мм L. Wang і D. Koch запропонували використовувати не оптимізацію А‑константи, а внесення поправки до довжини ока, виміряної суворо за допомогою оптичного біометра.
У дослідженні професора Л. В. Венгер і співавт. взяв участь 31 пацієнт з осьовою міопією. Усім пацієнтам було проведено стандартне офтальмологічне обстеження. Відомо, що стан ПО та слізної плівки може впливати на точність вимірів і розрахунок сили ІОЛ. Тому кератометричні та кератотопографічні дослідження, а також розрахунок оптичної сили ІОЛ виконувалися на системі оптичної біометрії та кератотопографії через 15 хв після обробки повік серветками Блефаклін® (Théa) й інстиляції безконсервантного препарату Теалоз® Дуо (Théa). Повторна оптична біометрія проводилася через 1 та 3 міс після втручання. Силу ІОЛ розраховували за формулами SRK II, SRK/T, Barrett Universal II та Hill RBF. Відповідно до рекомендацій L. Wang і D. Koch, були проведені оптимізація значень довжини ока для формули SRK/T та перерахунок сили ІОЛ. Усі операції виконував один хірург. Учасників було розподілено на групи з аксіальною довжиною ока до 28,0 мм та ≥28,1 мм.
Автори з’ясували, що оптимальної універсальної формули для розрахунку необхідної оптичної сили ІОЛ на очах з великою аксіальною довжиною (>28 мм) не існує. Для кращої задоволеності пацієнта рефракційним результатом факохірургії слід обговорити з ним усі нюанси операції та її наслідки до проведення втручання. У кожному конкретному випадку рішення стосовно сили імплантованої ІОЛ залишається за хірургом. Пацієнти з ВОМ можуть отримати високі зорові результати після факохірургії навіть за наявності виражених змін згідно з оптичною когерентною томографією.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 22 (467), листопад 2019 р.


