1 квітня, 2015
Бактериальные инфекции и цирроз печени (По материалам монотематической конференции EASL )
21 мая 2013 года в г. Барселоне под эгидой Европейской ассоциации по изучению болезней печени (EASL) состоялась монотематическая конференция, посвященная бактериальным инфекциям (БИ) у пациентов с циррозом печени. В ходе 2-дневного мероприятия делегаты ознакомились с современными представлениями о патогенетических механизмах возникновения БИ у больных циррозом, рассмотрели возможности ранней диагностики и адекватного лечения данной патологии, а также обсудили аспекты первичной и вторичной профилактики БИ. Осознавая клиническую значимость представленной информации, эксперты Европейской ассоциации по изучению печени (European Association for the Study of the Liver – EASL) опубликовали ключевые положения, которые были сформированы в ходе конференции, в Journal of Hepatology (2014). Предлагаем нашим читателям ознакомиться с основными тезисами этой публикации.
Клиническая значимость
Приступая к изложению материала, эксперты EASL подчеркнули значимость определения БИ, которые являются одной из главных причин прогрессирования печеночной недостаточности и летальности у больных циррозом печени. Кроме того, БИ могут спровоцировать развитие гастроинтестинального кровотечения, гиперволемической гипернатриемии, печеночной энцефалопатии, почечной недостаточности и острой печеночной недостаточности, развившейся на фоне уже имеющейся хронической (ОХПН). Значительно ухудшая качество жизни пациентов, БИ обусловливают также повышение экономических затрат на лечение: увеличивается количество повторных госпитализаций, возникает потребность в приеме дорогостоящих препаратов, растет стоимость медицинских услуг.
В рекомендациях EASL отмечается, что распространенность БИ у пациентов с циррозом в 4-5 раз выше, чем в общей популяции, при этом у 25-35% таких больных уже на момент госпитализации имеет место инфицирование или же развивается на протяжении стационарного лечения. Наиболее частыми инфекционными осложнениями являются спонтанный бактериальный перитонит (СБП) и инфекции мочевыводящих путей, к которым впоследствии могут присоединиться пневмония, инфекции кожи и мягких тканей, бактериемия. Вероятность летального исхода у больных декомпенсированным циррозом при наличии БИ возрастает в 3,75 раза, достигая 30% случаев в течение 1-го месяца и 63% случаев в течение 1 года.
Этиология
Большинство спонтанных инфекций при циррозе вызываются энтеробактериями и неэнтерококковыми стрептококками. Иногда БИ провоцируются мультирезистентными бактериями (патогенами, устойчивыми к ≥3 основным группам антибиотиков, включая β-лактамы). Основные мультирезистентные бактерии – это энтеробактерии, продуцирующие β-лактамазу широкого спектра действия (ESBL), неферментирующие грамотрицательные бациллы (Pseudomonas aeruginosa, Stenotrophomonas maltophilia или Acinetobacter baumannii), метициллинрезистентные штаммы Staphylococcus aureus (MRSA) и ванкомицинчувствительные (ВЧЭ) или ванкомицинрезистентные (ВРЭ) энтерококки. По данным последних эпидемиологических исследований, в странах Южной Европы и Азии доминируют ESBL, тогда как в США и странах Южной Америки преобладают MRSA и ВРЭ.
Патогенез
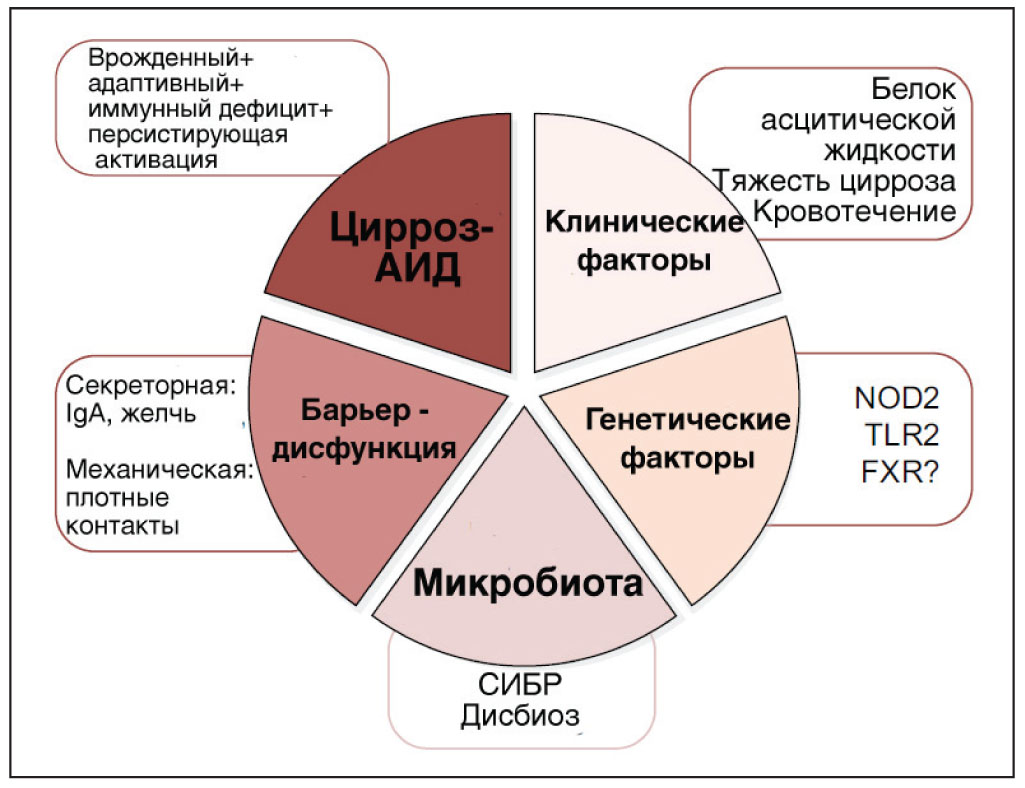
В публикации EASL перечисляются следующие ведущие патогенетические механизмы развития БИ при циррозе: патологические изменения состава и функции кишечного микробиома, нарушение кишечной проницаемости, бактериальная транслокация (БТ) и иммунологическая недостаточность (рис.).
Рассмотрев особенности количественных (синдром избыточного бактериального роста – СИБР) или качественных (дисбиоз) изменений микробиома, эксперты EASL подчеркнули, что у больных циррозом чаще развивается СИБР. На возникновение этого состояния влияют преимущественно модуляция желудочной секреции, снижение моторики тонкого кишечника, недостаток желчных кислот, антимикробные пептиды, а также портальная гипертензия. В подтверждение клинической значимости нарушения количественного состава кишечной микрофлоры эксперты привели интересный факт: у больных циррозом с сопутствующим СИБР чаще развивается СБП, чем у пациентов без СИБР.
Повышение кишечной проницаемости при патологии печени имеет место на поздних стадиях заболевания или при возникновении септических осложнений. Барьерная дисфункция обусловлена механическим и секреторным факторами. Ослабление функции плотных контактов между эпителиальными клетками приводит к увеличению парацеллюлярного проникновения и транслокации жизнеспособных бактерий посредством трансцитоза. Одним из ключевых регуляторов, модулирующих функцию плотных контактов и ускоряющих процесс трансцитоза, является фактор некроза опухоли, концентрация которого при циррозе печени значительно возрастает. В то же время количество секретируемых медиаторов, ограничивающих непосредственный контакт кишечных бактерий с поверхностью эпителиальной клетки (IgA, липиды желчи, антимикробные пептиды), существенно снижается. Комбинация этих факторов приводит к нарушению барьерной функции энтероцитов и проникновению патогенных микроорганизмов внутрь клетки.
По мнению экспертов EASL, в развитии БИ немаловажную роль играет генетическая предрасположенность. Мутация генов, ответственных за строение и функционирование Toll-подобных (TLR) и Nod-подобных рецепторов (NLR), приводит к нарушению распознавания внеклеточных бактерий: не происходит активация ядерного фактора k B, не стимулируется высвобождение антимикробных белков. Измененные TLR1 и TLR2 теряют способность распознавать триацилированный липопротеин грамположительных бактерий, TLR4 – не может обнаружить липополисахарид, NOD2 утрачивает специфичность к мурамилдипептиду (компоненту клеточной стенки грамотрицательных бактерий). Одновременное носительство двух вариантных генов TLR4 и NOD2 свидетельствует о высоком риске развития СБП и является суррогатным маркером патологической кишечной проницаемости и БТ.
Огромное значение в развитии БИ отводится циррозассоциированной иммунной дисфункции (цирроз-АИД), которая представляет собой иммунодефицитное состояние, протекающее на фоне персистирующей активации иммунной системы с продукцией провоспалительных цитокинов.
Цирроз-АИД приводит к изменению функции нейтрофилов, Th- и Tc-клеток, а также В-клеток памяти (CD27+). Одновременно с уменьшением численности мононуклеары и нейтрофилы теряют способность к фагоцитозу и мобилизации. Кроме того, при циррозе развивается ретикулоэндотелиальная дисфункция, обусловленная уменьшением количества ретикулоэндотелиальных мононуклеарных клеток и портосистемным шунтированием.
Определение органной недостаточности
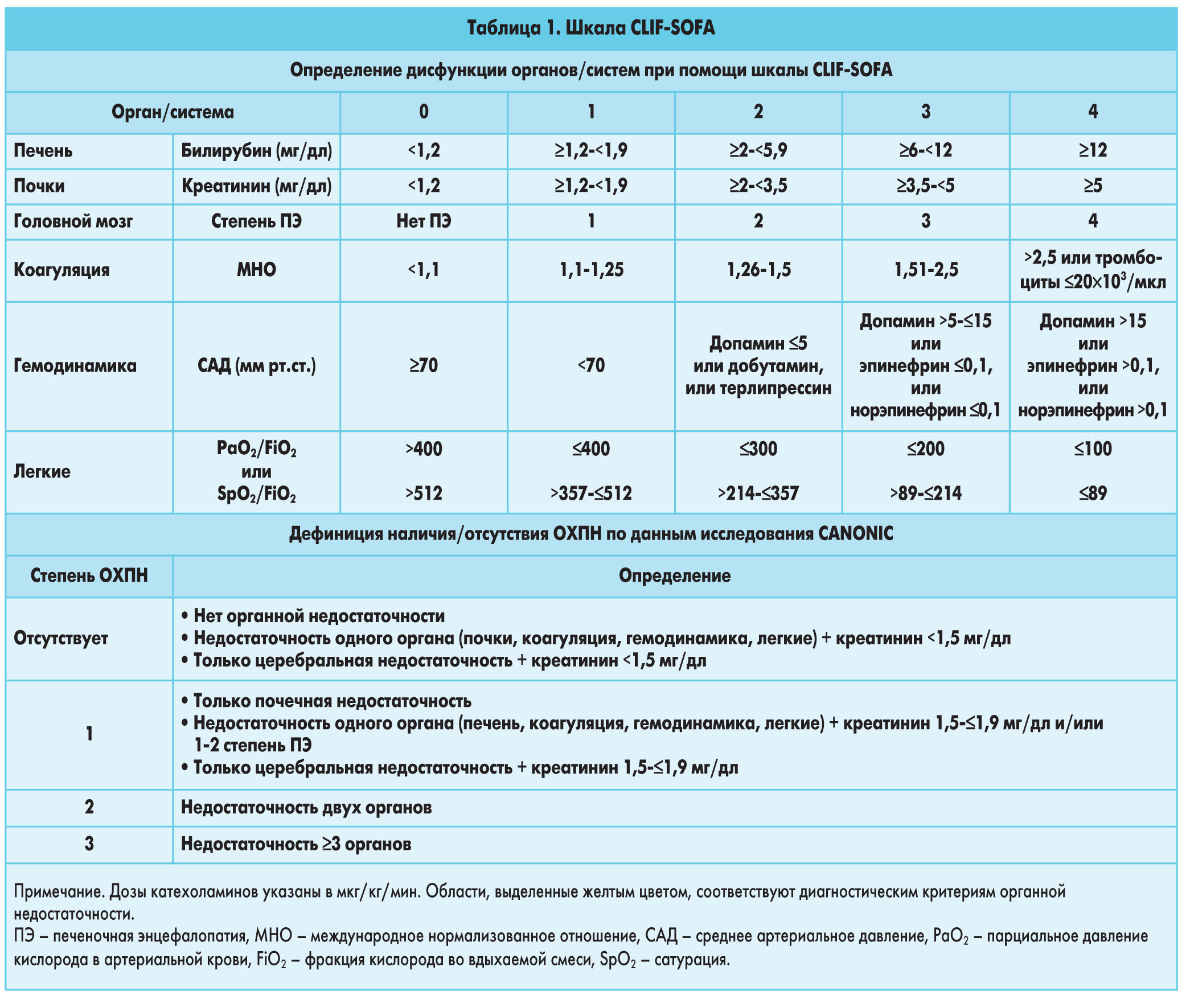
Для определения органной недостаточности эксперты EASL рекомендуют воспользоваться шкалой CLIF-SOFA (Chronic Liver Failure – Sequential Organ Failure Assessment), предназначенной для определения степени дисфункции органов и прогнозирования вероятности внутрибольничной летальности у больных циррозом (табл. 1).
Последствия БИ
Констатируя способность БИ провоцировать острую декомпенсацию у больных циррозом, эксперты EASL подчеркивают, что у одних пациентов острая БИ может привести только к декомпенсации цирроза, а у других осложниться развитием печеночной и/или внепеченочной органной недостаточности. Больные циррозом и острой органной недостаточностью относятся к высокой группе риска формирования ОХПН и внезапной смерти. По данным исследования CANONIC, при 1 степени ОХПН риск внезапной смерти составляет 22%, а при 3 степени ОХПН резко возрастает и достигает 77%.
Среди других клинически значимых последствий БИ в публикации EASL выделяют способность бактериальных компонентов инициировать чрезмерный воспалительный ответ иммунной системы организма-хозяина, что может приводить к повреждению тканей, органной недостаточности.
Еще одним возможным нежелательным последствием БИ для больных циррозом печени является развитие почечной недостаточности. Почечная недостаточность, как правило, возникает у пациентов с СБП, имеющих чрезмерный провоспалительный ответ иммунной системы. У таких больных клинические проявления почечной недостаточности фиксируют практически при разрешении инфекционного процесса на фоне проведения антибиотикотерапии.
БИ при циррозе может стать отправной точкой в развитии печеночной энцефалопатии и отека головного мозга, диссеминированного внутрисосудистого свертывания и кровотечения из варикозно расширенных вен, относительной надпочечниковой недостаточности и рефрактерного шока.
Ранняя диагностика
Настаивая на необходимости ранней диагностики БИ, эксперты EASL призывают врачей сохранять настороженность в отношении выявления стертых и атипичных форм БИ. В публикации рекомендуется всех госпитализированных больных циррозом печени считать потенциально инфицированными до тех пор, пока не будет доказано обратное. При поступлении в стационар или ухудшении состояния госпитализированных пациентов должно быть проведено тщательное обследование с целью обнаружения возможной инфекции.
Доказано, что БИ могут индуцировать развитие системного воспалительного ответа (СВО), который диагностируют у 57-70% инфицированных больных циррозом. Однако эти показатели, скорее всего, не отражают истинную распространенность СВО в данной популяции, так как низкая частота сердечных сокращений у таких пациентов может быть обусловлена приемом β-блокаторов. В то же время СВО может быть ошибочно диагностирован у больных циррозом при отсутствии БИ из-за гипердинамического типа кровообращения, печеночной энцефалопатии, напряженного асцита, гиперспленизма, которые изменяют частоту сердечных сокращений и дыхательных движений, температуру тела и количество белых клеток в крови.
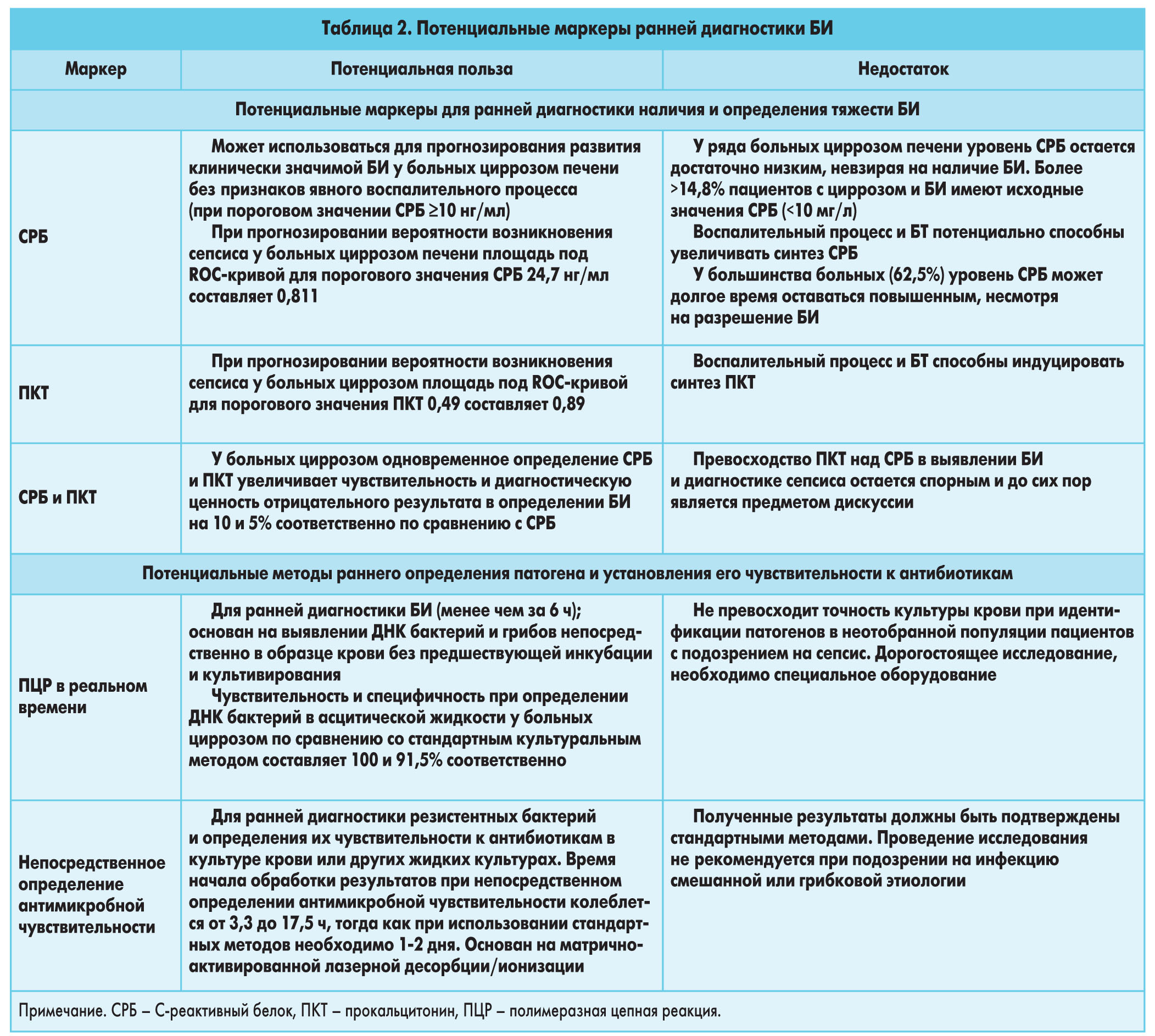
Недостаточное количество чувствительных и специфических маркеров для обнаружения СВО затрудняет своевременную диагностику сепсиса у этих пациентов. В публикации EASL отмечается, что в настоящее время для выявления и оценки тяжести БИ используются новые маркеры: проницаемость кишечной стенки, состояние кишечной микрофлоры, наличие/отсутствие продуктов жизнедеятельности бактерий, концентрация белков острой фазы воспаления, функционирование клеток врожденного иммунитета, активность клеточных рецепторов, ответственных за представление эндотоксинов (табл. 2).
Лечение
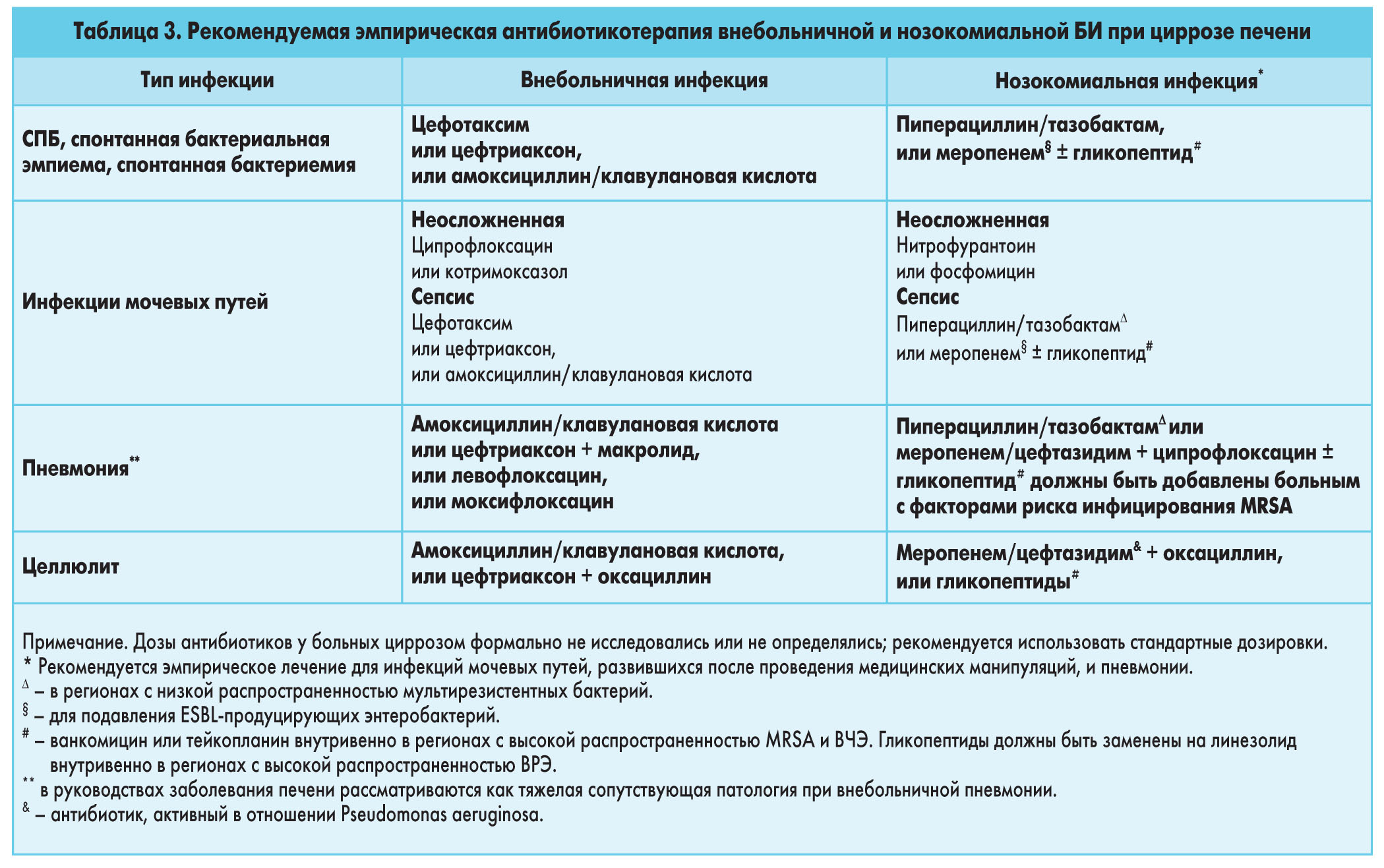
Основополагающими принципами в лечении больных циррозом и БИ являются ранняя диагностика и своевременное начало адекватной антибактериальной терапии, так как промедление в назначении антимикробного препарата ассоциировано с ростом летальности. Эксперты подчеркивают, что инициальный эмпирический выбор антибиотика должен основываться на сведениях о типе, тяжести и локализации инфекции (внебольничная, нозокомиальная, ассоциированная с проведением медицинских манипуляций), а также локальных эпидемиологических данных об антибиотикорезистентности. Золотым стандартом терапии большинства инфекций, развившихся во внебольничных условиях, остаются цефалоспорины третьей генерации (табл. 3). Неэффективность эмпирической антибиотикотерапии обусловлена некорректным выбором антибактериального препарата, инфицированием мультирезистентными штаммами, отсроченным началом лечения. Несмотря на то что длительность антимикробной терапии при циррозе формально не исследовалась и в настоящее время окончательно не определена (за исключением СБП), минимальный срок приема антибиотиков, по мнению экспертов EASL, составляет 5 дней. Эффективность антибактериальной терапии при СБП оценивается через 48 ч от момента установления предположительного диагноза и назначения антибиотика и проявляется уменьшением количества полиморфноядерных лейкоцитов в асцитической жидкости. В случае неэффективности терапии эксперты рекомендуют заменить антибактериальный препарат.
Эксперты EASL рекомендуют дополнять антибиотикотерапию внутривенным введением альбумина. Данная рекомендация основана на результатах одного открытого рандомизированного клинического исследования, в котором больные циррозом с СБП и высоким риском летального исхода получали цефотаксим и 20% альбумин. Оказалось, что дополнительное введение альбумина уменьшает вероятность возникновения почечной недостаточности и снижает уровень летальности с 29 до 10%. Этот эффект не наблюдался у пациентов с низким риском летальности (показатели общего билирубина составляли <4 мг/дл и креатинина <1 мг/дл).
Профилактика
В большинстве случаев СБП у больных циррозом развивается вследствие бактериальной транслокации кишечных грамотрицательных микроорганизмов. Исходя из этого постулата, эксперты EASL считают, что профилактические препараты должны эффективно снижать концентрацию указанных бактерий в кишечнике, сохраняя при этом популяцию протекторной анаэробной флоры. Именно поэтому для профилактики БИ при циррозе используют норфлоксацин – плохо адсорбирующийся хинолон, селективно воздействующий на грамотрицательные бактерии (табл. 4). В публикации EASL отмечено, что профилактический прием антибиотиков должен быть рекомендован только больным, имеющим высокий риск развития БИ: с гастроинтестинальным кровотечением, прогрессирующим циррозом и низким содержанием общего белка в асцитической жидкости, а также с отягощенным анамнезом по СБП.

У 55-66% больных циррозом с верхним гастроинтестинальным кровотечением в течение первых 5-7 дней от его начала развивается БИ. Прием системных антибактериальных препаратов (пенициллина, цефалоспорина, хинолонов) снижает вероятность возникновения БИ на 10-20%, повышает контроль над гемостазом, способствует профилактике повторных кровотечений и увеличивает выживаемость. Золотым стандартом антибиотикопрофилактики у больных с сохраненной функцией печени является прием норфлоксацина per os (400 мг/12 ч на протяжении 7 дней). Больным, инфицированным ESBL-продуцирующими штаммами Enterobacteriaceae, показано назначение нитрофурантоина или эртапенема. В публикации EASL отмечается, что идеальным является начало антибиотикопрофилактики до проведения эндоскопического исследования или непосредственно после его завершения.
Пациенты с низким содержанием белка в асцитической жидкости (10-15 г/л), печеночной недостаточностью (сывороточный билирубин >3,2 мг/дл) и низким количеством тромбоцитов (<98 000/мм3) относятся к группе высокого риска развития СБП. По данным одного рандомизированного клинического исследования, у пациентов с циррозом и высоким риском СБП назначение норфлоксацина по сравнению с плацебо способствует снижению вероятности возникновения СБП в течение 1 года (соответственно, 7 vs 61%), гепаторенального синдрома (соответственно, 28 vs 41%; р=0,02) и улучшает 3-месячную выживаемость (соответственно, 94 vs 62%). В этой популяции больных альтернативой норфлаксацину является пероральный прием ципрофлоксацина в дозе 500 мг/сут.
Пациенты, перенесшие один эпизод СБП, имеют очень высокий риск рецидива СБП. Длительный прием норфлоксацина (400 мг/сут per os) эффективен в качестве вторичной профилактики: его применение позволяет снизить вероятность рецидива СБП в течение 1 года с 60 до 3% (при приеме плацебо с 68 до 20%). Эксперты EASL также отмечают, что пролонгированная терапия норфлоксацином может обусловить формирование штаммов бактерий, резистентных к хинолонам, триметоприм-сульфаметоксазолу. Длительный профилактический прием норфлоксацина в 2,7 раза увеличивает риск возникновения мультирезистентных бактерий и в 4 раза – инфекции, вызванной ESBL-продуцирующими штаммами Enterobacteriaceae. По мнению специалистов EASL, для того чтобы избежать таких негативных последствий, можно заменить норфлоксацин на рифаксимин (антибиотик широкого спектра действия, неселективно воздействующий на кишечную флору), так как его назначение больным печеночной энцефалопатией не ассоциировано с риском появления мультирезистентных бактерий. В то же время, отмечают эксперты, необходимо учитывать отсутствие данных сравнительных исследований, в которых сопоставлялась эффективность норфлоксацина и рифаксимина.
Ключевые положения
• Распространенность и тяжесть БИ у больных циррозом печени превышает таковую в общей популяции.
• БИ, вызванные мультирезистентными организмами, часто развиваются у пациентов с циррозом печени; их возникновение ассоциировано с более высокими показателями летальности по сравнению с таковыми у пациентов без сопутствующего цирроза.
• У больных циррозом печени повреждения органов-мишеней при БИ развиваются значительно чаще (вследствие измененной чувствительности), что обычно приводит к ОХПН.
• Поздняя диагностика и несвоевременно начатое лечение ассоциированы с высокими показателями летальности, особенно у больных циррозом печени с сопутствующей гипотонией.
• Дополнительное назначение альбумина к антибактериальным препаратам у пациентов с СБП снижает показатели летальности.
• Первичная профилактика СБП с использованием норфлоксацина показана пациентам с варикозным кровотечением, крайне декомпенсированным циррозом и содержанием белка в асцитической жидкости <15 г/л.
• Внутривенное введение цефалоспоринов III поколения пациентам с варикозным кровотечением улучшает показатели выживаемости.
• Прием норфлоксацина с целью профилактики рецидивов СБП снижает летальность у больных циррозом.
Подготовила Лада Матвеева