1 квітня, 2015
Воспалительные заболевания кишечника: от современной классификации к эффективной терапии
Во второй день V съезда Украинской гастроэнтерологической ассоциации (19 сентября 2014 года) отдельная секция была посвящена проблеме заболеваний кишечника. Предлагаем читателям краткий обзор выступлений украинских и зарубежных ученых по поводу современных возможностей диагностики и лечения неспецифического язвенного колита (НЯК) и болезни Крона (БК).
Открыл работу секции директор Института гастроэнтерологии НАМН Украины (г. Днепропетровск), доктор медицинских наук, профессор Юрий Миронович Степанов. В содержательной лекции, посвященной современным тенденциям диагностики и лечения функциональных и органических заболеваний толстой кишки, было уделено внимание и проблеме воспалительных заболеваний кишечника (ВЗК). Долгое время в Украине не велся статистический учет этих нозологий. Приказом МЗ Украины № 511 от 17.06.2013 г. в формы статистической отчетности № 12 и № 20 наряду с другими гастроэнтерологическими заболеваниями внесены НЯК и БК, что открывает возможности реальной оценки распространенности этих заболеваний и планирования ресурсов здравоохранения. За 2013 г. в Украине зарегистрирован 9421 случай НЯК, что соответствует распространенности 20,8 на 100 тыс. населения. В 1296 случаях этот диагноз был установлен впервые.
В соответствии с современными представлениями о роли аутоиммунного воспаления в патогенезе ВЗК наиболее прогрессивным и эффективным методом терапии в настоящее время является биологическая терапия препаратами моноклональных антител к провоспалительным факторам. Позиции лидера на рынке иммунобиологических препаратов удерживает Хумира (адалимумаб) – рекомбинантное человеческое моноклональное антитело (IgG1) с высокой степенью сродства и специфичностью к растворимому фактору некроза опухоли (ФНО). Связываясь с ФНО, адалимумаб нейтрализует его биологические эффекты путем блокирования его взаимодействия с рецепторами на поверхности клеток.
Адалимумаб одобрен Европейским агентством по лекарственным средствам (EMA) и Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA) для использования у пациентов с активной формой язвенного колита (ЯК) среднетяжелого и тяжелого течения и тех больных, которые не отвечают либо не переносят традиционную терапию, на основании результатов рандомизированных плацебо-контролируемых двойных слепых исследований ULTRA 1 и ULTRA 2.
Ранее была накоплена убедительная доказательная база применения адалимумаба у пациентов с БК. На фоне поддерживающей терапии адалимумабом на протяжении года частота оперативных вмешательств в группе плацебо была до 6 раз выше, чем в группе адалимумаба (Feagan B.G. et al., 2008).
Доказательная база биологической терапии ВЗК более подробно проанализирована в следующих лекциях. Что касается реального положения дел в Украине, то, как отметил Ю.М. Степанов, существующая сегодня практика подходов к диагностике и, соответственно, к лечению заболеваний кишечника не учитывает разновидности и формы заболевания, связанные с различной этиологией. Этим объясняются неудовлетворительные результаты лечения у значительной части пациентов.
Доктор медицинских наук, профессор Андрей Эдуардович Дорофеев (Донецкий национальный медицинский университет им. М. Горького) прочел две лекции – об особенностях течения НЯК и БК у больных. Лектор отметил принципиальные различия между этими заболеваниями. Если при БК могут сегментарно поражаться любые отделы ЖКТ, причем воспалительные изменения распространяются на все слои стенки кишки, обусловливая предрасположенность к формированию стенозирующих и пенетрирующих осложнений, то при ЯК локализация поражения ограничена исключительно толстой кишкой и воспаление редко распространяется глубже слизистой оболочки. Соответственно, и подходы к ведению пациентов с разными формами ВЗК существенно различаются.
В лекции относительно особенностей ЯК профессор А.Э. Дорофеев представил Монреальскую классификацию заболевания, которая учитывает возраст больных, распространенность колита, активность воспаления и другие параметры. В отличие от БК для ЯК не существует единого индекса активности заболевания, поэтому нет точного определения ремиссии. На практике чаще используется неполный индекс Мейо. Полный индекс Мейо требует проведения эндоскопии, что возможно не на всех визитах пациента.
На основании собственных исследований лектор выделил дополнительные предикторы тяжелого течения НЯК:
• генетическая предрасположенность;
• выраженность аутоиммунной агрессии;
• степень метаболических нарушений (абсорбции, детоксикации);
• нарушения кишечной микрофлоры.
В качестве генетических маркеров предрасположенности к НЯК и раку кишечника изучены гены NOD2/CARD15, VDR, TLR3, TLR4. Если у большой части (42%) пациентов с дистальными формами и легким течением НЯК мутации указанных генов отсутствовали, то у всех больных с тяжелыми распространенными формами заболевания были выявлены полные или неполные мутации.
Специфическими аутоиммунными маркерами НЯК являются антитела к бокаловидным клеткам и гранулоцитам (выявлены у 28 и 67% пациентов соответственно), а при БК – антитела к протокам поджелудочной железы и S. cerevisiae (39 и 67% соответственно).
Целями лечения НЯК являются индукция и поддержание ремиссии (не только клинической, но и гистологической), повышение качества жизни больных и профилактика рака кишечника. На выбор терапии НЯК влияют распространенность, локализация, клиническая форма, степень тяжести, клиническая, эндоскопическая и гистологическая активность заболевания, а также наличие внекишечных поражений (чаще всего суставов, кожи и печени).
Алгоритмы выбора лечения в настоящее время регламентированы рекомендациями Европейского общества болезни Крона и колита (ECCO) и рабочей группы Украинской гастроэнтерологической ассоциации. Ведение пациентов с НЯК и другими формами ВЗК должно осуществляться совместно гастроэнтерологом и хирургом-колопроктологом.
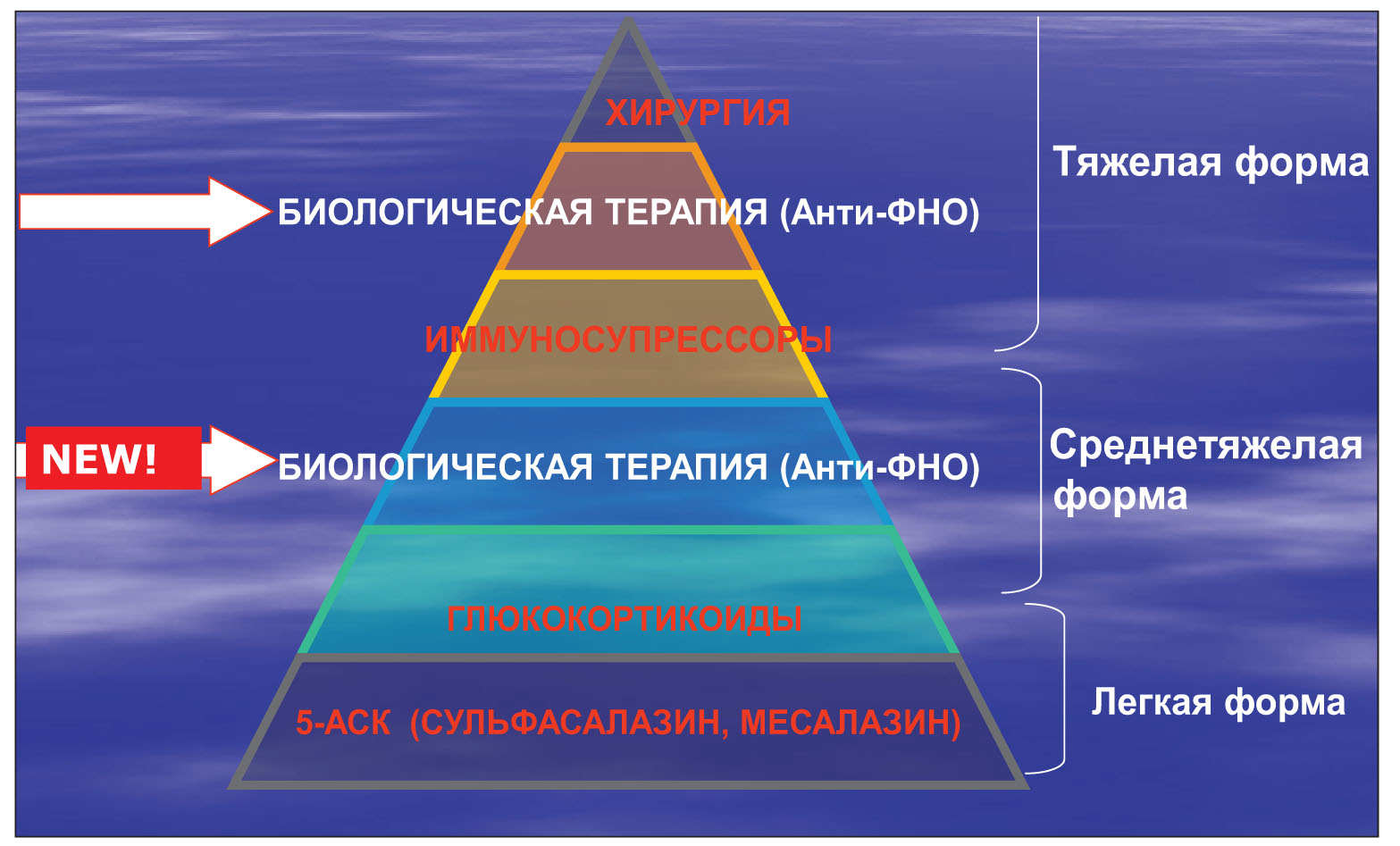
Пирамида лечения НЯК в зависимости от тяжести заболевания представлена на рисунке 1 . Препараты месалазина остаются первой линией терапии всех форм НЯК. При дистальном колите лечение должно начинаться с топических форм месалазина (ректальные суппозитории), а при недостаточной эффективности следует присоединять пероральный прием. Это повышает биодоступность препарата и эффективность лечения, особенно у больных с левосторонним и тотальным колитом. Аналогично кортикостероиды в качестве второй линии терапии могут применяться в топических формах (при легком течении НЯК) или в комбинации топические + системные формы.
Лектор отметил, что в развитых странах наблюдается тенденция к более раннему назначению биологической терапии. В настоящее время препараты моноклональных антител к ФНО являются терапией второй линии при неэффективности препаратов месалазина и глюкокортикоидов у пациентов со среднетяжелыми и тяжелыми формами ЯК. Биологическая терапия ЯК средней и высокой активности способствует репарации слизистой оболочки толстой кишки и индукции ремиссии уже в первые недели лечения у пациентов, резистентных к терапии кортикостероидами и/или иммуносупрессорами, что было показано в исследовании ULTRA 1 с адалимумабом. В исследовании ULTRA 2 длительный прием препарата позволял удерживать пациентов в ремиссии до 52 недель. Доказано, что комбинированная терапия любыми иммуносупрессорами менее эффективна по сравнению с монотерапией анти-ФНО. Использование биологической терапии является альтернативой колэктомии у больных с тяжелым стероидорезистентным НЯК. Также раннее назначение анти-ФНО терапии целесообразно пациентам с внекишечными проявлениями НЯК: при наличии поражений суставов и позвоночника, гангренозной пиодермии, склерозирующего холангита.
В лекции, посвященной БК, профессор А.Э. Дорофеев также акцентировал внимание на Монреальской классификации клинических форм заболевания, которая учитывает:
• возраст больных (чем раньше дебютирует БК, тем агрессивнее ее течение);
• локализацию воспалительного процесса (в отличие от НЯК при БК могут поражаться любые отделы ЖКТ – от полости рта до прямой кишки);
• клинические проявления БК (неосложненное, стенозирующее или пенетрирующее течение);
• наличие перианальных изменений.
Тяжесть (клиническую активность) БК оценивают по индексу Беста (CDAI). Клиническая ремиссия констатируется при значениях CDAI <150. Значения выше 450 свидетельствуют о высокой активности (тяжелом течении) БК. К неудобствам этой методики лектор отнес необходимость ведения пациентом дневника самонаблюдения, определения гематокрита и массы тела в момент расчета индекса.
Кроме того, при выборе терапии БК, как и в случае с НЯК, следует учитывать наличие внекишечных поражений.
Цели лечения БК созвучны целям лечения НЯК – индукция ремиссии, поддержание ремиссии без кортикостероидов, профилактика осложнений, предупреждение операций и повышение качества жизни больных.
Ориентиром для выбора лечения служит основанный на доказательствах Второй европейский консенсус по диагностике и лечению БК (ECCO, 2010). Терапия назначается в соответствии с локализацией, клиническим вариантом и активностью БК согласно Монреальской классификации. При терминальном илеите (L1) показаны топические стероиды и/или месалазин перорально; при изолированном поражении толстой кишки (L2) – присоединение к этой терапии ректальных форм месалазина; при комбинированном поражении тонкой и толстой кишки (L3) – топические стероиды, месалазин перорально и ректально и/или системные кортикостероиды, цитостатики, биологическая терапия; при локализации процесса в верхних отделах ЖКТ (L4) показаны системные кортикостероиды и/или цитостатики, а также биологическая терапия.
При подозрении на стенозирование, пенетрирующее течение или при наличии перианальных изменений в обязательном порядке необходима консультация хирурга. Однако современная биологическая терапия во многих случаях является альтернативой хирургическому вмешательству.
БК - прогрессирующее заболевание, в естественном континууме которого можно выделить окно терапевтических возможностей. Это промежуток времени от постановки диагноза до развития рецидивов и формирования осложнений, когда есть возможность замедлить прогрессирование воспаления, достичь глубокой ремиссии путем назначения биологической терапии, предотвратить или отсрочить таким образом оперативное вмешательство и инвалидизацию пациента.
Своевременное назначение моноклональных антител к ФНО, в частности адалимумаба, эффективно для индукции клинической ремиссии (по данным исследования CHARM), а также достижения эндоскопической ремиссии БК (по данным исследования EXTEND). Раннее назначение дает лучший клинический эффект. Кроме того, в исследованиях CHARM и ADHERE было доказано, что длительная поддерживающая монотерапия адалимумабом снижает частоту госпитализаций и хирургических вмешательств.
При фистулизирующем течении БК антибиотикотерапия эффективно уменьшает выраженность симптомов, но редко приводит к закрытию фистул. Эффективность по закрытию фистул и поддержанию ремиссии продемонстрировали азатиоприн и анти-ФНО препараты (адалимумаб, инфликсимаб). При наличии осложненных фистул при БК согласно обобщенным данным консенсуса ECCO назначение антагонистов ФНО рекомендуется в качестве второй линии терапии после применения антибиотиков, азатиоприна и адекватного дренирования.
Особое внимание лектор уделил послеоперационному ведению пациентов с БК. Резекционным операциям подвергается до 80% больных на разных этапах течения заболевания, однако резекция не обеспечивает излечения, и вновь развиваются обострения болезни. Их частота при отсутствии лечения или неправильном ведении пациентов в послеоперационном периоде составляет 65-90% в первый год и 80-100% в течение 3 лет. Самым точным предиктором обострений является эндоскопическая картина БК. В исследовании POCER была показана эффективность поддерживающей терапии адалимумабом для профилактики послеоперационных обострений БК, при этом адалимумаб оказался эффективнее 6-меркаптопурина: частота достижения эндоскопической ремиссии на 6-м месяце после резекции составила 93,8 против 62,2%; р=0,024 (De Cruz P. et al., 2012).
Таким образом, ведение пациентов с ВЗК должно осуществляться совместно терапевтами и хирургами. Биологическая терапия (адалимумаб, инфликсимаб) является современной и эффективной терапией 2-3-й линии у пациентов со среднетяжелым и тяжелым течением ВЗК, но при наличии неблагоприятных прогностических признаков рекомендуется раннее применение антагонистов ФНО.
Центральным событием секции по заболеваниям кишечника стали две онлайн-лекции профессора медицины, микробиологии и иммунологии, руководителя медицинского факультета Университета Калгари (Канада) Subrata Ghosh. В первой презентации были более подробно рассмотрены доказательная база и возможности биологической терапии ВЗК.
С внедрением биологической терапии профессор Ghosh связывает тенденцию к уменьшению числа плановых колэктомий у пациентов специализированных клинических центров США и Канады, которая прослеживается с 2002 г. У многих больных хроническим ЯК биологическая терапия позволяет добиться стабильной ремиссии, отказаться от инвалидизирующей операции с возможными осложнениями или отсрочить ее выполнение.
Биологические препараты у больных ЯК изучались в плацебо-контролируемых клинических исследованиях ULTRA 1 и ULTRA 2 (адалимумаб), ACT1 и ACT2 (инфликсимаб), PURSUIT (голимумаб) и GEMINI (ведолизумаб). Лектор отметил, что из-за различий в дизайне и критериях включения пациентов по результатам этих исследований нельзя напрямую сравнивать эффективность разных биологических препаратов. Так, в исследовании ULTRA 1 оценивалась только частота индукции ремиссии на 8-й неделе терапии адалимумабом, а затем открыто проводилась поддерживающая терапия в течение года, а в исследовании ULTRA 2 первичными конечными точками были и индукция ремиссии на 8-й неделе, и ремиссия на 52-й неделе поддерживающей терапии, причем плацебо-контроль присутствовал на протяжении всего исследования. В исследованиях PURSUIT и GEMINI с новыми анти-ФНО препаратами проводили две рандомизации пациентов: в фазу поддерживающей терапии рандомизировали только тех участников, которые достигли ремиссии в первые 6 недель.
Важно отметить, что в оба исследования адалимумаба включали пациентов, которые плохо отвечали на предыдущую терапию стероидами и/или иммуномодуляторами, то есть с тяжелым течением ЯК. Кроме того, в исследовании ULTRA 2 участвовали пациенты с опытом неудачной анти-ФНО терапии.
В исследовании ULTRA 1 был определен оптимальный режим дозирования адалимумаба для индукции ремиссии ЯК в первые 8 недель: 160 мг в первый день и 80 мг через 2 недели. Этот же режим индукции применяли в исследовании ULTRA 2. Для поддерживающей терапии препарат назначали по 40 мг через неделю в обоих исследованиях.
В результате частота терапевтического ответа в исследовании ULTRA 2 была достоверно выше, чем при использовании плацебо, уже со 2-й недели: 39,1 против 19,9% по частичному индексу Мейо (p<0,001), что расценивается как быстрое начало действия адалимумаба. На 52-й неделе ремиссия ЯК по критериям частичного индекса Мейо была достигнута у 22,2% пациентов, что достоверно выше результата в группе плацебо (11,0%; p<0,001)
Профессор Ghosh обратил внимание на то, что эффективность адалимумаба в исследовании ULTRA 2 была выше у тех пациентов, которые ранее не получали анти-ФНО препаратов, и, таким образом, подчеркнул важность раннего использования эффективной биологической терапии ЯК.
В ходе дополнительного анализа результатов исследования было установлено, что на фоне поддерживающей терапии адалимумабом значительно снижается потребность пациентов в кортикостероидах (Sandborn W. et al., 2012) и, что особо подчеркнул лектор, достоверно по сравнению с плацебо уменьшается как общая частота госпитализаций, так и частота госпитализаций по причине обострений и осложнений ЯК (Feagan B.G. et al., 2012).

Опираясь на результаты исследований биологических препаратов, профессор Ghosh представил алгоритм ведения больных ЯК, который уже применяется в клинике Университета Калгари. Основной принцип сводится к раннему назначению анти-ФНО терапии при неэффективности кортикостероидов (определяется в течение 2-4 недель лечения) или азатиоприна (определяется в течение 8-12 недель терапии).
Подобный подход лектор представил и в части доклада, посвященной БК. 5-аминосалицилаты при БК не эффективны, за исключением самых легких форм колита. При отсутствии ответа на терапию адекватными дозами кортикостероидов в течение 2-4 недель или азатиоприном в течение 3 мес следует рассмотреть возможность назначения анти-ФНО терапии.
Кандидатами на назначение ранней анти-ФНО терапии являются пациенты с предикторами неблагоприятного прогноза: с ранним дебютом БК (особенно моложе 20 лет), с поражением тонкой кишки на большом протяжении, с тяжелым поражением верхних отделов ЖКТ, с перианальными фистулами и абсцессами, ранним развитием стриктур и пенетраций, глубокими язвами толстой кишки.
В пользу раннего назначения анти-ФНО терапии свидетельствуют результаты плацебо-контролируемых исследований адалимумаба. В исследовании CHARM у пациентов с длительностью БК менее 2 лет доля достижения ремиссии на 56-й неделе терапии адалимумабом составила 51%, а у пациентов, которые начали получать биологическую терапию через 5 лет и более от момента постановки диагноза, результат был существенно скромнее – 35% (Schreiber S. et al., 2007). В исследовании EXTEND раннее назначение адалимумаба чаще способствовало полному заживлению слизистых оболочек пораженных органов ЖКТ, чем при использовании у пациентов со стажем БК 5 лет и более (Sandborn W. et al., 2010).
Результаты терапии во многом зависят от фенотипа или клинической формы БК. При 5-летнем наблюдении за больными БК частота выполнения резекционных операций на фоне анти-ФНО терапии оказалась наименьшей у пациентов с клинической формой В1 (воспаление слизистой оболочки без стриктур и пенетраций) по сравнению с пациентами с наличием стенозов (клиническая форма В2), пенетраций (В3) (Moran G.W. et al., 2014).
Данные других исследований позволяют получить ответы на вопросы, как долго можно поддерживать ремиссию БК на биологической терапии и что произойдет после ее отмены. Согласно результатам исследования ADHERE, в котором продолжалось открытое лечение адалимумабом пациентов с ремиссией на 56-й неделе исследования CHARM, ремиссия БК оставалась стабильной в течение 4 последующих лет (Panaccione R. et al., 2013). Прекращение анти-ФНО терапии может привести к рецидиву. По данным T. Molnar et al. (2013), почти половина больных с ремиссией БК, достигнутой в результате 1 года лечения анти-ФНО препаратами, после их отмены нуждалась в возобновлении биологической терапии в среднем через 6 мес.
В ходе метаанализа исследований, в которых препараты анти-ФНО терапии назначались в комбинации с азатиоприном (Jones et al., 2013), было установлено, что комбинирование с иммуносупрессантами повышало эффективность инфликсимаба, чего не наблюдалось в случае применения адалимумаба или цертолизумаба (последний не зарегистрирован в Европе). Против использования адалимумаба с иммуносупрессантами свидетельствует повышение риска развития злокачественных новообразований по сравнению с монотерапией адалимумабом (Osterman M.T. et al., 2013).
Что касается выбора конкретного препарата биологической терапии, профессор Ghosh констатировал сопоставимую эффективность адалимумаба и инфликсимаба по частоте достижения ремиссии в клинических исследованиях, но обратил внимание на потребности и предпочтения самих пациентов, так как режимы терапии и способы введения препаратов отличаются. По данным опроса 36 больных БК, проведенного Peake et al. (2011), 67,6% респондентов (23 пациента) предпочли терапию адалимумабом по причине удобства применения (подкожные инъекции, которые можно делать дома самостоятельно). Однако 11 пациентов все же выбрали терапию инфликсимабом (внутривенные инъекции), поскольку предпочитали более длительный интервал между введениями препарата и регулярные контакты с медперсоналом. При этом подавляющее большинство пациентов (82,4%) предпочитали, чтобы решение принималось совместно пациентом и лечащим врачом. Похожее соотношение предпочтений больных профессор Ghosh наблюдает в собственной клинической практике.
Лектор представил алгоритм терапии в слубольных БК в зависимости от тяжести заболевания, который используется в клинике г. Калгари. Препараты будесонида и сульфасалазина используются только при легком течении БК с поражением толстой кишки. При умеренной активности заболевания препаратом первого выбора является преднизолон. При стероидзависимой БК к преднизолону могут присоединяться метотрексат или азатиоприн, а при их неэффективности на третьем шаге применяется анти-ФНО терапия: самостоятельно (адалимумаб) или в сочетании с иммуномодулятором (инфликсимаб). При этом до начала анти-ФНО терапии может пройти до 16 недель.
При рефрактерности БК к преднизолону сразу переходят к назначению анти-ФНО монотерапии или сочетания анти-ФНО препарата с иммуномодулятором. В последнем случае решение о назначении анти-ФНО терапии может быть принято быстрее – уже через 2-4 недели неэффективного лечения преднизолоном. Раннее присоединение азатиоприна к терапии кортикостероидами не повышает шансы больных БК на достижение устойчивой ремиссии, что было показано в исследованиях AZTEC и RAPID GETAID (Panes J. et al., 2013; Cosnes J. et al., 2013).
При тяжелой БК 1-2 недели неэффективного лечения преднизолоном дают повод для размышлений о целесообразности назначения анти-ФНО препарата в комбинации с иммуносупрессором, особенно у пациентов с предикторами неблагоприятного исхода.
Вторая лекция профессора S. Ghosh была посвящена общим принципам и моделям оказания специализированной помощи пациентам с ВЗК.
Стандарты ведения пациентов с ВЗК различаются в разных странах и регионах в зависимости от места оказания помощи, опыта специалистов, доступности диагностических методов и препаратов и других факторов. Стандартизация процессов повышает качество помощи, как это продемонстрировал лектор на примере клиники г. Калгари. К какому бы врачу не обратился пациент с ВЗК, он получает стандартизированное лечение в соответствии с едиными алгоритмами и доказательной базой. В г. Калгари наблюдаются 9600 больных с ВЗК. Из них 4500 пациентов получают биологическую терапию: 65% адалимумабом, 35% инфликсимабом.
Потенциал оптимизации помощи больным ВЗК состоит в ранней диагностике, прогнозировании течения заболевания и исходов, раннем терапевтическом вмешательстве с применением наиболее эффективных на данный момент препаратов биологической терапии, объективном контроле ремиссии с эндоскопической оценкой заживления слизистой оболочки кишечника.
Для начала следует уяснить, каковы цели терапии ВЗК. Купирования симптомов и клинической констатации ремиссии уже недостаточно. Высшими целями лечения являются замедление прогрессирования заболевания и достижение глубокой гистологической ремиссии. В последнее время происходит изменение концепции терапии ВЗК: на смену стратегии острого реагирования на симптомы и подавления воспаления приходит долгосрочная стратегия, которая ставит целью недопущение воспалительного повреждения тканей и стабильное удержание пациента в состоянии без воспаления.
Большое значение имеет индивидуальная оценка течения заболевания и прогноза. У пациентов с легкими проявлениями ВЗК без осложнений может быть целесообразной стратегия ступенчатого повышения интенсивности терапии (step-up) без применения иммуносупрессоров на начальном этапе во избежание развития побочных эффектов, в то время как у лиц с агрессивным течением заболевания оправдана стратегия top-down – раннее применение анти-ФНО препаратов, возможно, в сочетании с иммуносупрессорами во избежание возникновения осложнений, с последующим снижением интенсивности терапии по мере наступления ремиссии.
На агрессивное течение БК указывают ранний дебют заболевания (в возрасте до 40 лет), наличие перианальных осложнений, стриктур и пенетраций, глубоких дефектов слизистой оболочки, покрывающих более 10% одного сегмента толстой кишки.
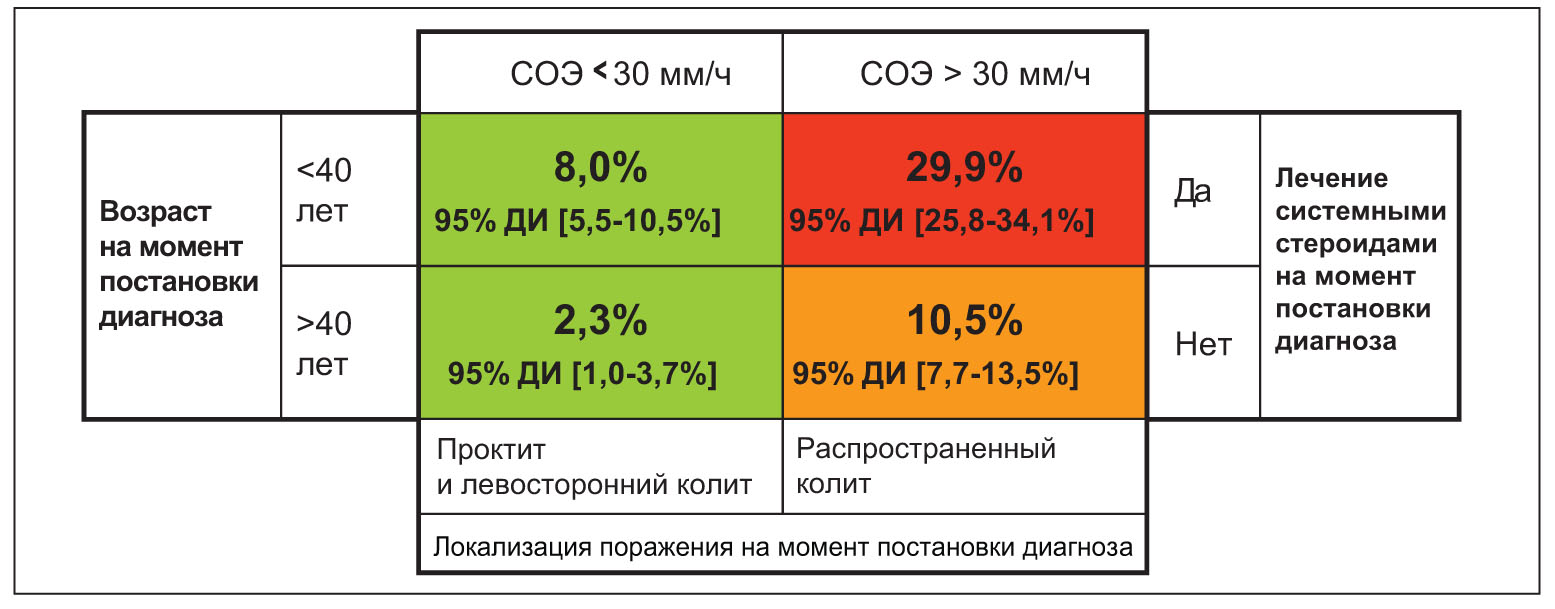 Рис. 2. Модель прогнозирования потребности в колэктомии у пациентов с ЯК, созданная на основании результатов исследования IBSEN (Cvancarova M. et al. UEGW 2010, Abstract OP161)
Рис. 2. Модель прогнозирования потребности в колэктомии у пациентов с ЯК, созданная на основании результатов исследования IBSEN (Cvancarova M. et al. UEGW 2010, Abstract OP161)На рисунке 2 показана модель прогнозирования потребности в колэктомии у пациентов с ЯК, созданная на основании результатов исследования IBSEN (Cvancarova N. et al., 2010). Самый высокий риск колэктомии в течение 10 лет отмечается у пациентов моложе 40 лет с распространенным колитом, СОЭ >30 мм/ч, которые получали терапию кортикостероидами сразу после постановки диагноза.
Что касается организационных аспектов помощи больным ВЗК, то на примере клиники г. Калгари лектор акцентировал внимание на двух ключевых принципах – мультидисциплинарном подходе и стандартизации работы медперсонала путем составления клинических протоколов, алгоритмов принятия решений и контроля их выполнения. Вовлечение врачей разных специальностей в алгоритмы обследования и лечения пациентов с ВЗК, особенно в специализированных клинических центрах, необходимо в связи с тем, что ВЗК часто имеют внекишечные проявления: ревматологические, дерматологические, офтальмологические. Локальный протокол оказания помощи больным ВЗК основывается на национальном протоколе, международной доказательной базе и учитывает особенности и ресурсы конкретного лечебного учреждения. Грамотно составленный локальный протокол синхронизирует действия медперсонала и структурных подразделений (поликлиники, стационара, лаборатории, отделения радиологической диагностики и др.), сводит к минимуму визиты и лишние передвижения пациентов. Протокол регламентирует последовательность принятия решений в разных клинических ситуациях, включая отсутствие ответа на терапию, а также содержит индикаторы (критерии) качества помощи. Протоколы, которые используются в клинике г. Калгари, построены по принципу минимизации неэффективной терапии, снижения дозы кортикостероидов и раннего назначения анти-ФНО препаратов пациентам, которые могут получить от них максимальную пользу.
В заключение профессор Ghosh обратил внимание слушателей на то, что, кроме протоколов, важно учитывать ожидания и персональные цели пациентов, которые могут различаться даже в разные периоды лечения.
Мнение пациента также было представлено в рамках заседания. С короткой презентацией выступил лидер объединения пациентов с ВЗК Юрий Анатольевич Петров – врач по образованию, который перенес все тяготы болезни в поисках оптимальной для себя терапии.
«Надежда на будущее» – молодая всеукраинская организация пациентов, образованная в этом году. Цели деятельности организации – привлечение внимания общества к проблеме ВЗК, налаживание взаимодействия «пациент-врач», образовательная работа среди больных. Первыми шагами станут создание школы пациентов с регулярными встречами (1 раз в квартал), создание группы психологической поддержки, разработка информационных материалов.
Подготовил Дмитрий Молчанов