16 грудня, 2016
Иммунобиотики в комплексной терапии воспалительных дерматозов
Многообразие функций нормобиоты желудочно-кишечного тракта (ЖКТ) – в последние годы одна из популярных тем многих исследований и публикаций, авторами которых стали украинские и зарубежные ученые. Такое пристальное внимание обусловлено открытием иммунобиологических свойств нормальной микрофлоры кишечника, обеспечивающих правильное функционирование всех органов и систем организма.
 12-14 октября в Киеве проходили «11-е Киевские дерматологические дни» – масштабное мероприятие в жизни отечественной дерматологии. В этом году конференция носила мультидисциплинарный характер, в частности были подняты вопросы, затрагивающие иммунологическую функцию нормобиоты и роль нарушений последней в патогенезе воспалительных заболеваний, а также возможности терапии современными препаратами-иммунобиотиками. В частности, доклад «Плейотропное действие пробиотиков при хронических воспалительных дерматозаx» был представлен заведующей кафедрой дерматовенерологии Харьковской медицинской академии последипломного образования, доктором медицинских наук, профессором Людмилой Анатольевной Болотной.
12-14 октября в Киеве проходили «11-е Киевские дерматологические дни» – масштабное мероприятие в жизни отечественной дерматологии. В этом году конференция носила мультидисциплинарный характер, в частности были подняты вопросы, затрагивающие иммунологическую функцию нормобиоты и роль нарушений последней в патогенезе воспалительных заболеваний, а также возможности терапии современными препаратами-иммунобиотиками. В частности, доклад «Плейотропное действие пробиотиков при хронических воспалительных дерматозаx» был представлен заведующей кафедрой дерматовенерологии Харьковской медицинской академии последипломного образования, доктором медицинских наук, профессором Людмилой Анатольевной Болотной.
– Реализация защитной функции кишечника невозможна без нормальной микрофлоры, которая сегодня признана новым метаболически активным органом. Ежегодно появляются описания все новых и новых функций симбионтной флоры. В кишечнике человека обитает >1 тыс. видов бактерий, общее количество которых достигает 1014. Нормальная микрофлора на 95% состоит из анаэробов (бифидо- и лактобактерий), при этом аэробы (кишечная палочка, энтерококки и др.) рассматриваются как сопутствующая флора. Также встречаются стафилококки, клостридии, протей.
Среди основных функций нормальной микрофлоры следует упомянуть:
- колонизационную;
- дезинтоксикационную;
- биосинтетическую;
- пищеварительную;
- терморегуляционную;
- трофическую;
- энергетическую;
- регуляторную и т. д.
Важно отметить, что примерно 80% всех иммунокомпетентных клеток локализовано именно в слизистой оболочке ЖКТ, а каждый метр кишечника содержит около 1010 лимфоцитов. Именно в лимфоидной ткани кишечника (GALT – gut-associated lymphoid tissue) происходит иммунная регуляция специализированных клеток, обеспечивающих как клеточный, так и гуморальный иммунный ответ.
Иммунотропная функция микробиоты кишечника реализуется за счет:
- пролиферации иммунных клеток и стимуляции синтеза иммуноглобулинов;
- потенцирования механизмов неспецифической резистентности (синтез компонентов системы комплемента, лизоцима), системного и локального иммунитета;
- стимуляции созревания Т- и В-лимфоцитов, системы фагоцитирующих мононуклеаров и лимфоидного аппарата кишечника.
Нормальная работа микрофлоры кишечника обеспечивает деление и дифференциацию регуляторных Т-клеток; сегментированные филаментные бактерии способствуют развитию Th-17, защищающих организм от внеклеточных патогенов. Микробиота кишечника регулирует процесс т. н. хоминга – рециркуляцию лимфоцитов, а также дифференцировку Т-клеток в различных отделах кишечника.
Дисбактериоз можно описать как клинико-лабораторный синдром, характеризующийся изменением состава нормальной микрофлоры, метаболическими и иммунными нарушениями. Для дисбактериоза характерно появление значительного количества микроорганизмов в тонком кишечнике и изменение микробного профиля толстого кишечника. Защитная микрофлора кишечника фактически перестает полноценно выполнять свои функции, формируя т. н. синдром избыточного бактериального роста. Примечательно, что нарушения состава даже одного биотопа способны вызывать нарушение резистентности в других биотопах, в результате чего достаточно быстро повышается вероятность возникновения дезадаптационных иммунных состояний.
Ведущим механизмом развития хронических воспалительных дерматозов сегодня признан дисбаланс иммунной системы. В частности, при псориазе и алопеции изменено количество Th-1, при атопическом дерматите – Th-2, при аутоиммунных расстройствах – Th-17. Также при дерматозах обнаруживается дисбаланс в системе про- и противовоспалительных цитокинов. Форма и выраженность изменений кишечной нормобиоты влияют на такие дерматологические показатели, как увлажненность, тургор, липидный обмен, пигментация кожи, состояние микроциркуляторного русла, ногтей, волос, стабильность микробиоты, иммунный статус и др. Следовательно, рациональным решением множества дерматологических проблем является комплексный подход к терапии, включающий выявление и коррекцию дисбиотических нарушений.
Какие же изменения нормальной микрофлоры характерны для воспалительных дерматозов? У 89-94% детей с атопическим дерматитом (АД) диагностируется дисбиоз кишечника. Также отмечаются:
- уменьшение разнообразия симбионтной флоры;
- появление условно-патогенной и патогенной флоры, провоцирующей аутосенсибилизацию организма с развитием преимущественно IgЕ-зависимых реакций;
- повышение проницаемости эпителиального барьера кишечника для макромолекул пищи;
- усиление пищевой сенсибилизации;
- дефицит секреторного Ig A.
Замедление колонизации кишечника вызывает изменение ответа Т-хелперов. Микробиота кожи больных с АД зачастую содержит Staphylococcus epidermidis, S. aureus, грибы рода Candida, Malassezia.
При акне отмечается изменение качественного и количественного состава микробиоты (кишечной палочки, бифидо- и лактобактерий, рост и развитие условно-патогенной флоры), что соответствует дисбактериозу 1-3 степени. Дефицит микрофлоры ЖКТ осложняется усугублением выраженности патологии кожи, торпидностью к проводимой терапии.
Себорейный дерматит сопровождается уменьшением количества облигатной микрофлоры, ростом и развитием условно-патогенной флоры. Примечательно, что в клинических исследованиях отмечена прямая корреляция тяжести заболевания со степенью дисбиоза.
При генерализованной и диссеминированной формах витилиго обнаруживают дисбиоз 3-4 ст. Характерна ассоциация нескольких условно-патогенных биотопов, высокая частота выделения протея.
В качестве средства коррекции иммунобиотических нарушений, сопровождающих воспалительные дерматозы, сегодня широко используются пробиотики, обладающие плейотропным действием (плейотропность – способность препарата влиять одновременно на несколько мишеней, запускающих различные биохимические процессы в организме). Разнонаправленность эффектов пробиотиков при воспалительных дерматозах реализуется с помощью:
- стимуляции естественного иммунитета, подавления активности патогенной микрофлоры путем синтеза бактериоцинов;
- усиления неспецифических барьерных функций эпителия за счет стимуляции синтеза муцина и увеличения числа плотных межклеточных контактов;
- •предотвращения активации Т-хелперов и последующей продукции цитокинов из-за конкурирующего действия с патогенами на дендритные антигенпредставляющие клетки;
- усиления синтеза регуляторного интерлейкина (IL)-10, ответственного за иммунологическую толерантность.
Наиболее хорошо изученным иммунобиотическим штаммом на сегодняшний день является Lactobacillus rhamnosus GG. Данный микроорганизм является представителем нормальной микрофлоры ЖКТ. Важно отметить, что проводились многочисленные исследования в различных возрастных группах, в т. ч. у беременных и новорожденных. Культура LGG получила документально подтвержденный статус безопасности от научного комитета Управления по контролю качества пищевых продуктов и лекарственных средств США (FDA). Штамм соответствует значительному количеству характеристик и обладает свойствами, рекомендованными в качестве критериев выбора оптимального пробиотика. LGG способствует повышению колонизационной резистентности (это подразумевает как предотвращение адгезии патогенов, так и препятствие их транслокации).
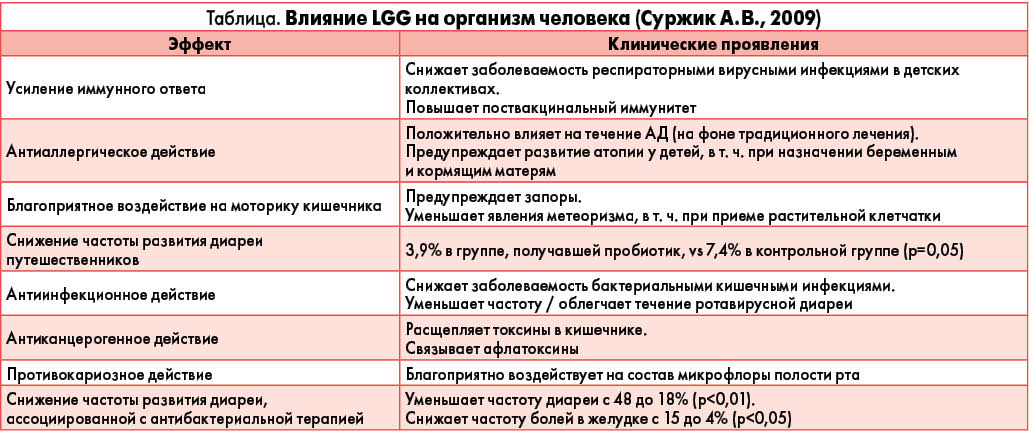
Важнейшим свойством LGG является способность модифицировать иммунный ответ. В частности, пробиотики, содержащие LGG, реализуют следующие иммунотропные эффекты (табл.):
- активация универсального фактора транскрипции NF-B и Toll-like рецепторов (механизмы врожденного иммунитета);
- повышение активности фагоцитов за счет усиления экспрессии на поверхности клеток рецепторов СR1, CR3, FcyRIII, FCaR, участвующих в распознавании антигенов патогенов;
- усиление продукции IL-12 и IL-15, ответственных за созревание и активацию NK-клеток;
- возрастание уровня сывороточного IgA;
- снижение активности CD4+ и синтеза провоспалительных цитокинов.
Известным комплексом на основе LGG, разработанным для применения в дерматологической практике, является ДермаПРО® (Schonen; Delta Medical Promotions). В его состав также входят фруктоолигосахариды – идеальный питательный субстрат для полезной микрофлоры.
ДермаПРО® содержит уникальный штамм L. rhamnosus GG, отличающийся повышенной адгезией к эпителиоцитам. Наличие в составе комплекса только одного штамма обеспечивает низкую аллергенность, что является дополнительным преимуществом в терапии аллергических заболеваний. Каждая капсула ДермаПРО® содержит 1,5 млрд бактерий, высокая выживаемость которых обеспечивается с помощью технологии микроинкапсулирования. Средство можно рекомендовать пациентам с АД, экземой, акне, аллергическим дерматитом, стрептококковой пиодермией, красным плоским лишаем, себорейным дерматитом и др. в режиме по 1 капсуле в сутки. ДермаПРО® целесообразно использовать как в случае острых состояний, так и с целью профилактики обострений и удлинения периодов ремиссии при хронической патологии. Рекомендованный курс лечения – 1 мес. ДермаПРО® разрешен к применению у детей с 2 мес.
Таким образом, назначение иммунобиотиков в составе комплексной терапии воспалительных дерматозов обеспечивает плейотропный эффект, нормализуя состояние метаболизма и иммунный статус пациентов.
Постоянное углубление знаний о механизмах патогенеза различных заболеваний все чаще заставляет практикующих врачей и ученых рассматривать человеческий организм как единое целое. Главный постулат целителей древности, подтверждаемый сегодня результатами серьезных научных исследований, – «Лечить нужно не болезнь, а больного» – становится основой врачебной практики, а использование средств с широким спектром терапевтических эффектов – требованием времени.
Подготовила Александра Меркулова
Медична газета «Здоров’я України 21 сторіччя» № 21 (394), листопад 2016 р.