6 лютого, 2020
Останні досягнення медикаментозного лікування раку нирки
 Рак нирки – порівняно нечастий тип злоякісних пухлин. В економічно розвинених країнах він становить 2,0-2,5% усіх випадків онкологічної патології. В Україні щороку близько 4800 осіб захворіває, а близько 2000 помирає від раку нирки. Захворюваність складає 8,2 на 100 тис. населення (11,3 у чоловіків і 6,0 у жінок) [1]. У США та Західній Європі показники захворюваності вищі на 40-50%. Прогнозувалося, що у 2018 р. у світі захворіє 403,3 тис. осіб, а 175,1 тис. помре від раку нирки [2].
Рак нирки – порівняно нечастий тип злоякісних пухлин. В економічно розвинених країнах він становить 2,0-2,5% усіх випадків онкологічної патології. В Україні щороку близько 4800 осіб захворіває, а близько 2000 помирає від раку нирки. Захворюваність складає 8,2 на 100 тис. населення (11,3 у чоловіків і 6,0 у жінок) [1]. У США та Західній Європі показники захворюваності вищі на 40-50%. Прогнозувалося, що у 2018 р. у світі захворіє 403,3 тис. осіб, а 175,1 тис. помре від раку нирки [2].
Тривожним фактом є те, що з невідомих причин захворюваність на рак нирки в усьому світі упродовж останніх 50 років щороку зростає на 2-4%, тобто швидше, ніж при багатьох інших типах пухлин. За цей час захворюваність на рак нирки в США підвищилася більш ніж у 2 рази, але смертність знизилася на 1/3. Такий значний поступ зумовлений головним чином успіхами своєчасної діагностики (зокрема ультразвуковими методами), без чого неможливе радикальне хірургічне лікування. Це дало можливість істотно підвищити показники 5-річної виживаності, наприклад, у США – від 20,0% у 1974‑1976 рр. до 63,9% у 1995-2000 рр. Однак в Україні упродовж останніх років цей показник є нижчим за 40%.
Рак нирки частіше уражає немолодих людей – медіана віку пацієнтів становить 65 років. Понад 90% первинних пухлин нирок є злоякісними, а 80-85% у зазначеній групі – це нирковоклітинний рак (НКР).
Класифікацію НКР здійснюють за загальноприйнятими принципами: виділяють I-IV стадії, які відповідають показникам за системою TNM. Нині застосовується 8-ма редакція (2017), яка не зазнала великих змін порівняно з 6-ю (2002) і 7-ю (2010) редакціями [3]. Стадія є найважливішим фактором прогнозу у хворих; при виявленні хвороби у порівняно ранній стадії, яка дає можливість провести радикальне оперативне втручання, хворий має значні шанси на повне одужання. Проте близько 1/3 первинних хворих на НКР і майже така сама частка прооперованих пацієнтів мають віддалені метастази [4].
Хворих на метастатичний НКР також можна розподілити на кілька підгруп за прогнозом. Наприкінці 1990-х рр. американський онкоуролог Роберт Мотцер (Robert J. Motzer) запропонував враховувати п’ять несприятливих факторів: низький індекс Карновського (<80%), високий рівень лактатдегідрогенази (понад 1,5 норми), анемію, високий рівень кальцію в плазмі крові, відсутність нефректомії. Згодом до них додали такий фактор, як ураження метастазами 2 органів і більше. За наявністю факторів ризику виділяють три групи. Упродовж останніх років використовують уточнені міжнародні критерії (табл. 1) [5].
У хворих з віддаленими метастазами радикальне лікування досі неможливе. НКР резистентний до опромінення та хіміотерапії. За даними 83 клінічних досліджень (понад 4000 хворих), загальна ефективність хіміотерапії склала лише 6%. Променеву терапію застосовують у двох випадках – для зменшення вираженості болю при кісткових чи абдомінальних метастазах, а також при метастазах у мозку.
Ще на початку 2000-х рр. єдиним методом лікування занедбаного НКР була інтерферонотерапія, яку застосовували від 1980-х рр. Інтерферон альфа активує B- і T-клітини, макрофаги та дендритні клітини, підвищує експресію Fc-рецепторів. Безпосередня протипухлинна активність інтерферонів незначна – 12-15%, повне регресування пухлини відбувалося дуже рідко (1-2%), а медіана виживаності у загальній групі не перевищувала 1 року. Від середини 1980-х рр. поширеним засобом лікування НКР став інтерлейкін‑2, який є T-клітинним ростовим фактором. Запропоновано кілька режимів його введення – високодозовий, низькодозовий, у комбінації з інтерфероном альфа. Однак, як і у випадку з інтерфероном, безпосередня ефективність імунотерапії інтерлейкіном‑2 була порівняно невисокою (15‑20%).
Незважаючи на відносні успіхи терапії із застосуванням інтерферонів чи інтерлейкіну‑2, НКР до 2000-х рр. вважався резистентним до медикаментозної терапії. Така оцінка почала змінюватися після запровадження в клінічну практику так званих таргетних (англ. targeted – мішеневий) препаратів. До таргетних належать лікарські засоби, дія яких спрямована на шляхи, процеси та фізіологічні особливості, що унікально пошкоджені в злоякісних клітинах: поверхневі рецептори, ангіогенез, специфічні гени і їх мутації тощо.
З’ясовано, що розвиток НКР, який є високоваскуляризованою пухлиною, асоційований з підвищеною експресією рецепторів ендотеліального та епідермального факторів росту (VEGFR та EGFR), у ньому також важливу роль відіграють шляхи, пов’язані з мішенню рапаміцину у ссавців (mTOR). Таргетні препарати групи інгібіторів тирозинкінази блокують внутрішньоклітинний домен рецептора VEGF, а VEGF, що циркулює у сироватці крові, може інактивуватися специфічними антитілами.
Перші значні успіхи таргетної терапії при НКР, які дали можливість втілити ці теоретичні концепції у практичне русло, здобуто у 2007 р. (його деякі експерти навіть назвали роком нирки), коли було зареєстровано одразу кілька препаратів для паліативної терапії занедбаного НКР – сунітиніб, сорафеніб, темзиролімус, комбінація бевацизумабу з інтерфероном. Згодом додалися інгібітор mTOR (еверолімус), ще кілька інгібіторів тирозинкінази (пазопаніб, акситиніб, ленватиніб), а у 2019 р. – сучасні засоби імунотерапії анти-PD-L1 та анти-CTLA‑4 (ці методи лікування потребують окремого аналізу).
Такий широкий спектр препаратів для паліативної терапії НКР поставив на порядок денний важливі клінічні завдання вибору найефективнішої терапії першої лінії, а також оптимальної послідовності застосування різних засобів з груп інгібіторів тирозинкіназ та mTOR. Справа в тому, що на відміну від цитостатичної терапії, при таргетній терапії нерідко послідовно застосовують препарати з подібним механізмом дії (зокрема різні інгібітори тирозинкіназ), бо вони мають свої особливості щодо спектра сигнальних шляхів, які можуть блокувати. Загальним правилом є те, що ширший (і унікальніший) спектр дії дає можливість досягнути вищої ефективності, хоча може спричиняти і вищу токсичність. Тому пошуки нових молекул групи інгібіторів тирозинкіназ продовжуються.
Серед останніх досягнень у цьому напрямі відзначимо кабозантиніб – інгібітор тирозинкіназ із вираженою активністю проти множинних тирозинкіназ, які беруть участь у рості пухлини, ангіогенезі, аномальному ремоделюванні кісток, метастазуванні та формуванні резистентності до лікарських засобів. При тестуванні in vitro інгібіторну активність кабозантинібу перевіряли приблизно на 270 кіназах людини. Важливими мішенями кабозантинібу є VEGFR‑1, VEGFR‑2, VEGFR‑3, AXL (anexelekto, що означає «неконтрольований»), MET (рецептор фактора росту гепатоцитів), RET, рецептор фактора стовбурових клітин KIT, FLT3, ROS1, MER, TYRO3, TRKB, TIE‑2. Зокрема, інгібування AXL та MET може бути критично важливою характеристикою, яка відрізняє кабозантиніб від інших мультирецепторних інгібіторів тирозинкінази, таких як сунітиніб та пазопаніб [6]. Надмірна експресія MET та AXL спостерігається при багатьох злоякісних новоутвореннях і асоціюється з несприятливим прогнозом у пацієнтів із занедбаним НКР. Більше того, у доклінічних моделях лікування сунітинібом призводило до посилення сигналу MET та AXL, тим самим сприяючи метастазуванню та ангіогенезу, тоді як при використанні кабозантинібу сигналізація MET та AXL знижувалася, а ріст пухлини інгібувався на ксенотрансплантатах НКР, які стали резистентними до лікування сунітинібом. Отже, шлях МЕТ та AXL відіграє важливу роль у первинній резистентності, а також у розвитку стійкості до інгібування шляху VEGF сунітинібом. Одночасне блокування MET та AXL додатково до шляху VEGF може сприяти ефективності лікування занедбаного НКР. Таким чином, маємо теоретичне підґрунтя для застосування кабозантинібу не лише у пацієнтів, хвороба у яких прогресувала після попереднього лікування анти-VEGF, а й у першій лінії терапії, оскільки є дані про порушення регуляції МЕТ у не лікованих раніше хворих на НКР.
Опубліковано результати кількох клінічних досліджень кабозантинібу І-ІІІ фаз. Зокрема у дослідженні І фази, проведеному за участю 25 пацієнтів з гістологічно підтвердженим метастатичним світлоклітинним НКР після принаймні однієї лінії терапії інгібітором шляху VEGF, доза кабозантинібу становила 140 мг. Часткової відповіді досягнуто у 28% пацієнтів, а у 52% пацієнтів зафіксовано стабілізацію. У 19 з 21 пацієнтів спостерігалося певне регресування пухлини. Медіана виживаності без прогресування (ВБП) становила 12,9 міс, а медіана загальної виживаності (ЗВ) – 15,0 міс [7].
У квітні 2016 р. Управління з контролю якості харчових продуктів і лікарських препаратів США (FDA) схвалило кабозантиніб для лікування резистентного до попередньої терапії інгібіторами тирозинкіназ метастатичного НКР. Це рішення базувалося на результатах дослідження ІІІ фази METEOR, у якому порівнювали ефективність кабозантинібу та еверолімусу. Усі пацієнти мали отримувати попереднє лікування щонайменше одним засобом з групи інгібіторів тирозинкіназ, орієнтованим на VEGFR, а прогресування захворювання фіксували протягом 6 міс до рандомізації. Не було обмежень щодо кількості чи типу попередніх методів терапії з приводу раку. Пацієнти з відомими метастазами в мозку, які були адекватно ліковані та перебували у стабільному стані, також мали право на лікування. Пацієнтів рандомізували у співвідношенні 1: 1 у групи кабозантинібу 60 мг щодня (n=330) або еверолімусу 10 мг на добу (n=328). Лікування продовжували до втрати клінічної користі або до розвитку побічних явищ чи токсичності. Кросовер між групами заборонявся. Первинною кінцевою точкою була тривалість ВБП за оцінкою незалежної комісії. Вторинні кінцеві точки включали тривалість ЗВ та швидкість розвитку ефекту, а також час виникнення та ступінь побічних ефектів.
Після закінчення дослідження METEOR з’ясувалося, що у групі кабозантинібу медіана ВБП становила 7,4 міс, тоді як у групі еверолімусу – 3,8 міс (рис. 1). Показник прогресування захворювання або смерті був на 42% нижчим у групі кабозантинібу (коефіцієнт ризику – HR – 0,58). Медіана тривалості лікування становила 7,6 міс у групі кабозантинібу та 4,4 міс у групі еверолімусу.
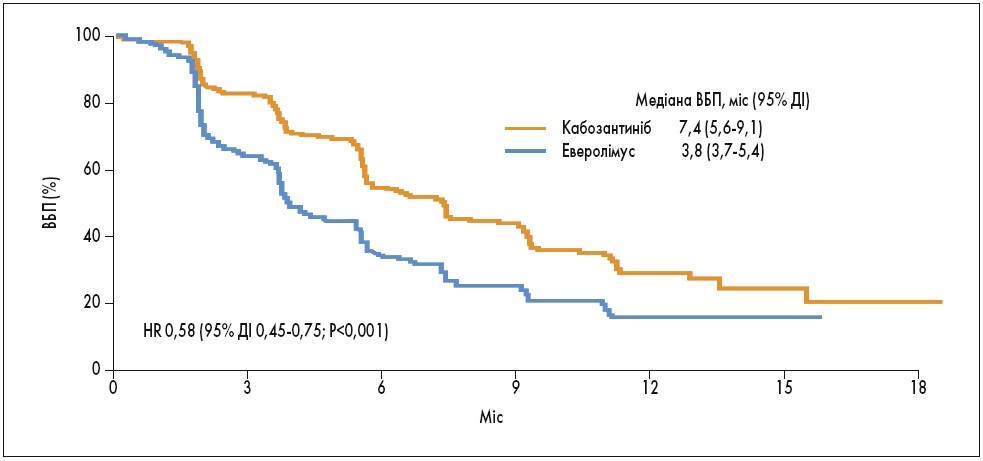 Рис. 1. Кабозантиніб vs еверолімус при метастатичному НКР (друга лінія терапії – METEOR): ВБП (Choueiri T.K. et al. N Engl J Med. 2015; 373: 1814-23; Choueiri T.K. et al. Lancet Oncol. 2016; 17: 917-27)
Рис. 1. Кабозантиніб vs еверолімус при метастатичному НКР (друга лінія терапії – METEOR): ВБП (Choueiri T.K. et al. N Engl J Med. 2015; 373: 1814-23; Choueiri T.K. et al. Lancet Oncol. 2016; 17: 917-27)
У дослідженні METEOR були досягнуті і вторинні кінцеві точки. ЗВ не перетнула межу значущості при проміжному аналізі, але була статистично достовірно довшою при застосуванні кабозантинібу порівняно з еверолімусом при остаточному аналізі (21,4 проти 16,5 міс; HR 0,66; рис. 2). Загальна ефективність після аналізу даних перших 375 пацієнтів за оцінкою незалежної рентгенологічної комісії становила 21% у групі кабозантинібу та 5% у групі еверолімусу (p<0,001), стабілізація стану спостерігалася у 62% пацієнтів у кожній групі, тоді як прогресування захворювання зафіксовано у 14% хворих у групі кабозантинібу та 27% – у групі еверолімусу. Побічні явища призвели до зниження дози у 60% пацієнтів, які отримували кабозантиніб, та 25% пацієнтів, які приймали еверолімус. Дев’ять відсотків пацієнтів припинили лікування кабозантинібом через несприятливі явища порівняно з 10% пацієнтів, які отримували еверолімус [8, 9].
 Рис. 2. Кабозантиніб vs еверолімус при метастатичному НКР (друга лінія терапії – METEOR): ЗВ (Choueiri T.K. et al. Lancet Oncol. 2016; 17: 917-27)
Рис. 2. Кабозантиніб vs еверолімус при метастатичному НКР (друга лінія терапії – METEOR): ЗВ (Choueiri T.K. et al. Lancet Oncol. 2016; 17: 917-27)
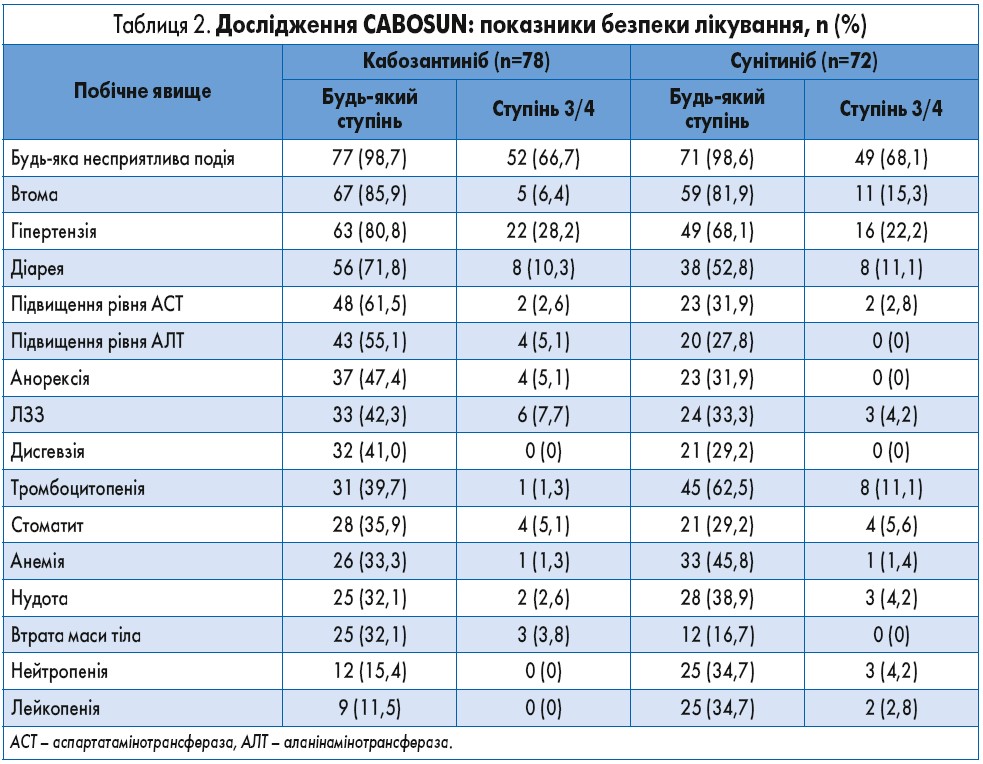
У грудні 2017 р. FDA схвалило застосування кабозантинібу при первинному метастатичному НКР. Це базувалося на результатах рандомізованого дослідження ІІ фази CABOSUN, у якому порівнювали ефективність введення сунітинібу та кабозантинібу пацієнтам із метастатичним НКР середнього та низького ризику. Первинною кінцевою точкою була ВБП за оцінкою дослідника, тоді як загальна ефективність, ЗВ та безпека були вторинними кінцевими точками. Порівняно з сунітинібом застосування кабозантинібу сприяло значному збільшенню медіани ВБП (5,6 і 8,2 міс відповідно; рис. 3), а також подовженню часу до прогресування захворювання або смерті на 34% (HR 0,66). ЗВ у групах на момент публікації результатів дослідження істотно не відрізнялася. Частота побічних явищ була однаковою у двох групах лікування, при цьому профілі безпеки обох препаратів відповідали таким у попередніх дослідженнях за участю пацієнтів з НКР. З медіаною спостереження 34,5 міс медіана ЗВ становила 26,6 міс у групі кабозантинібу та 21,2 міс у групі сунітинібу (HR 0,80) [10, 11].
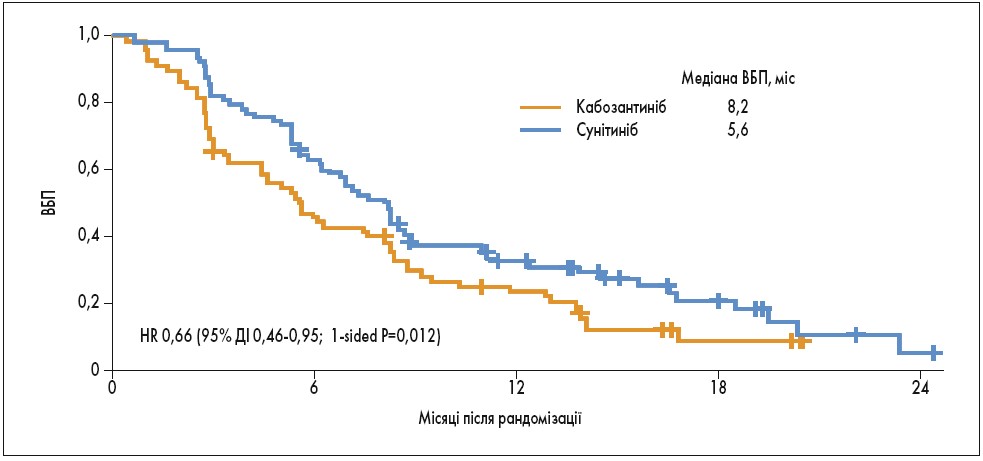 Рис. 3. Кабозантиніб vs сунітиніб при метастатичному НКР (перша лінія терапії – CABOSUN): ВБП (Choueiri T.K. et al. J Clin Oncol. 2017; 35: 591-7)
Рис. 3. Кабозантиніб vs сунітиніб при метастатичному НКР (перша лінія терапії – CABOSUN): ВБП (Choueiri T.K. et al. J Clin Oncol. 2017; 35: 591-7)
Дуже важливими є показники безпеки лікування. Як видно з даних таблиці 2, побічні ефекти, зумовлені введенням кабозантинібу, трапляються приблизно з такою ж частотою і вираженістю, як і при лікуванні сунітинібом. З точки зору повсякденної клінічної практики дуже важливими є заходи і засоби, які розроблено для профілактики та лікування цих побічних ефектів.
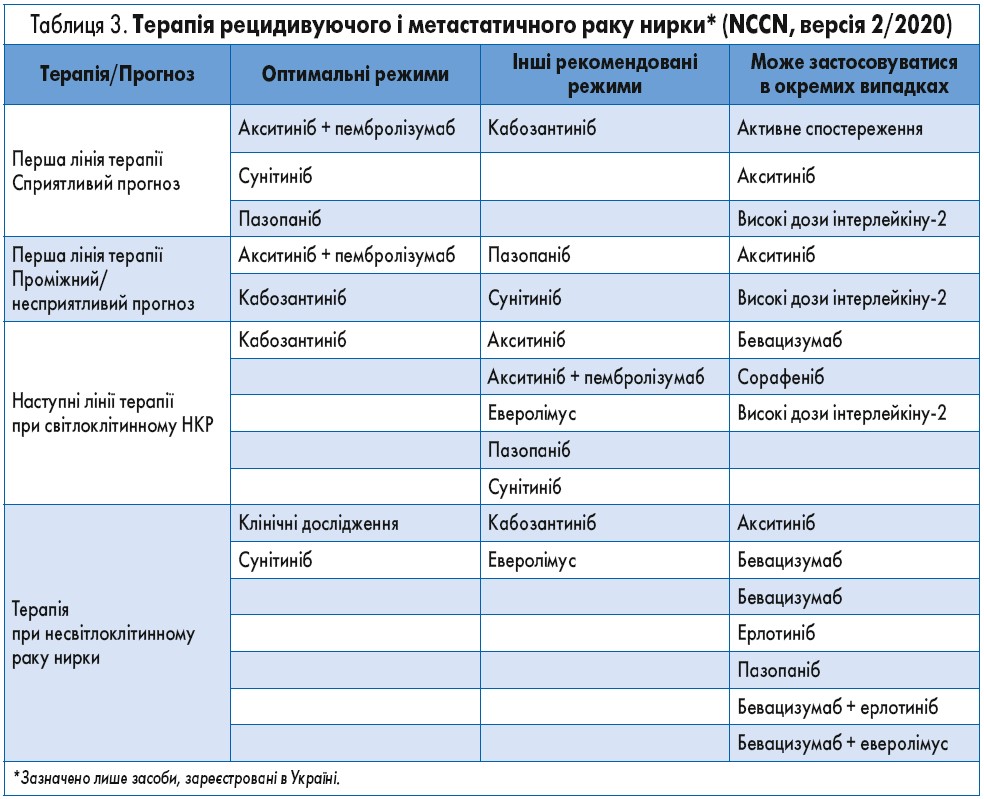
Таким чином, світлоклітинний рак нирки поступово переходить у групу пухлин, при яких навіть у занедбаному стані можна досягнути істотного подовження тривалості життя та підтримати його якість. Це стало можливим завдяки все ширшому застосуванню в клінічній практиці таргетних препаратів (табл. 3).
Література
- Рак в Україні. 2017-2018. Захворюваність, смертність, показники діяльності онкологічної служби. Бюлетень Національного канцер-реестру україни. Видання № 20. – К., 2019.
- Ferlay J., Colombet M., Soerjomataram I., Mathers C., Parkin D.M., Pineros M., Znaor A., Bray F. Estimating the global cancer incidence and mortality in 2018: GLOBOCAN sources and methods. Int J Cancer. 2019 Apr 15; 144(8): 1941-53. / укр. переклад Oncology Group. 2019; 3.
- Swami U., Nussenzveig R.H., Haaland B., Agarwal N. Revisiting AJCC TNM staging for renal cell carcinoma: quest for improvement. Ann Transl Med. 2019 Mar; 7 (suppl. 1): S18.
- Osawa T., Takeuchi A., Kojima T., Shinohara N., Eto M., Nishiyama H. Overview of current and future systemic therapy for metastatic renal cell carcinoma. Jpn J Clin Oncol. 2019 May 1; 49(5): 395-403.
- Ko J.J., Xie W., Kroeger N., Lee J.L., Rini B.I., Knox J.J., Bjarnason G.A., Srinivas S., Pal S.K., Yuasa T., Smoragiewicz M., Donskov F., Kanesvaran R., Wood L., Ernst D.S., Agarwal N., Vaishampayan U.N., Rha S.Y., Choueiri T.K., Heng D.Y. The International Metastatic Renal Cell Carcinoma Database Consortium model as a prognostic tool in patients with metastatic renal cell carcinoma previously treated with first-line targeted therapy: a population-based study. Lancet Oncol. 2015 Mar; 16(3): 293-300.
- Yakes F.M., Chen J., Tan J., Yamaguchi K., Shi Y., Yu P., Qian F., Chu F., Bentzien F., Cancilla B., Orf J., You A., Laird A.D., Engst S., Lee L., Lesch J., Chou Y.C., Joly A.H. Cabozantinib (XL184), a novel MET and VEGFR2 inhibitor, simultaneously suppresses metastasis, angiogenesis, and tumor growth. Mol Cancer Ther. 2011 Dec; 10(12): 2298-308.
- Choueiri T.K., Pal S.K., McDermott D.F., Morrissey S., Ferguson K.C., Holland J., Kaelin W.G., Dutcher J.P. A phase I study of cabozantinib (XL184) in patients with renal cell cancer. Ann Oncol. 2014 Aug; 25(8): 1603-8.
- Choueiri T.K., Escudier B., Powles T., Mainwaring P.N., Rini B.I., Donskov F., Hammers H., Hutson T.E., Lee J.L., Peltola K., Roth B.J., Bjarnason G.A., Geczi L., Keam B., Maroto P., Heng D.Y., Schmidinger M., Kantoff P.W., Borgman-Hagey A., Hessel C., Scheffold C., Schwab G.M., Tannir N.M., Motzer R.J.; METEOR Investigators. Cabozantinib versus Everolimus in Advanced Renal-Cell Carcinoma. N Engl J Med. 2015 Nov 5; 373(19): 1814-23.
- Choueiri T.K., Escudier B., Powles T., Tannir N.M., Mainwaring P.N., Rini B.I., Hammers H.J., Donskov F., Roth B.J., Peltola K., Lee J.L., Heng D.Y.C., Schmidinger M., Agarwal N., Sternberg C.N., McDermott D.F., Aftab D.T., Hessel C., Scheffold C., Schwab G., Hutson T.E., Pal S., Motzer R.J.; METEOR investigators. Cabozantinib versus everolimus in advanced renal cell carcinoma (METEOR): final results from a randomised, open-label, phase 3 trial. Lancet Oncol. 2016 Jul; 17(7): 917-27.
- Choueiri T.K., Halabi S., Sanford B.L., Hahn O., Michaelson M.D., Walsh M.K., Feldman D.R., Olencki T., Picus J., Small E.J., Dakhil S., George D.J., Morris M.J. Cabozantinib Versus Sunitinib As Initial Targeted Therapy for Patients With Metastatic Renal Cell Carcinoma of Poor or Intermediate Risk: The Alliance A031203 CABOSUN Trial. J Clin Oncol. 2017 Feb 20; 35(6): 591-7.
- Choueiri T.K., Hessel C., Halabi S., Sanford B., Michaelson M.D., Hahn O., Walsh M., Olencki T., Picus J., Small E.J., Dakhil S., Feldman D.R., Mangeshkar M., Scheffold C., George D., Morris M.J. Cabozantinib versus sunitinib as initial therapy for metastatic renal cell carcinoma of intermediate or poor risk (Alliance A031203 CABOSUN randomised trial): Progression-free survival by independent review and overall survival update. Eur J Cancer. 2018 May; 94: 115-25.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (60), 2019 р.