30 березня, 2016
Дерматит рук: дифференциальный диагноз, возможности диагностики и терапии

Дерматит рук (ДР) является полиэтиологическим заболеванием, в развитии которого играют роль как наследственные, так и экологические факторы. Несмотря на относительно небольшую площадь поражений (максимум 4% поверхности тела в соответствии с «правилом девяток»), данное заболевание имеет большое экономическое и социально-медицинское значение. Так, в структуре профессиональных кожных заболеваний ДР занимает лидирующую позицию. Цели данной статьи – суммирование современных знаний о причинах этого генетически и морфологически гетерогенного заболевания, дифференциальной диагностике, а также предоставление практической информации о выявлении и лечении ДР.
Распространенность
ДР является достаточно часто встречающимся заболеванием. Основываясь на данных 36 исследований (1964-2007), средняя распространенность его в общей популяции составляет 4%. Анализ 7 современных исследований определил среднюю заболеваемость на уровне 5,5 случаев / 1000 человеко-лет – 9,6 у женщин и 4,0 у мужчин (Thyssen J. P. et al., 2010). Согласно данным популяционного исследования, проведенного в г. Гейдельберге (Германия) в случайной выборке (n=2500), распространенность заболевания достигает 3,4% (Berg S., 2005).
Факторы риска
Атопический дерматит, пол, возраст, контактная аллергия и работа во влажной среде
В многочисленных исследованиях изучали частоту и факторы риска возникновения ДР. Так, более высокая частота заболеваемости ассоциируется с женским полом, наличием контактной аллергии, атопического дерматита и работой во влажной среде. Атопический дерматит был идентифицирован как наиболее важный фактор риска возникновения ДР, при этом для некоторых профессиональных групп ключевой является работа во влажной среде. Наиболее важные причины длительного течения ДР – значительная выраженность заболевания, аллергическое или атопическое происхождение, детский возраст, а также дебют в возрасте до 20 лет (Thyssen J. P. et al., 2010).
Генетические факторы
Помимо атопического дерматита, описаны и другие генетические факторы риска развития ДР. Различные формы заболевания на сегодня связывают с однонуклеотидными полиморфизмами (SNP), делециями и мутациями на различных сайтах генов. Чаще всего атопический дерматит ассоциируется с мутациями гена филаггрина, обусловливающими полную или частичную утрату его функции. Филаггрин играет ключевую роль в терминальной дифференцировке корнеоцитов, способствует увеличению механической прочности кожного барьера и является отправной точкой для продукции натурального увлажняющего фактора. В то время как гомозиготные или сложные гетерозиготные мутации с полной потерей функции филаггрина были определены в качестве основной причины ихтиоза, у гетерозиготных носителей мутации обнаруживаются структурные изменения кожи различной степени выраженности (например, уменьшение плотности, нарушение организации, функциональные изменения, повышение рН, снижение гидратации рогового слоя). Из-за упрощения проникновения аллергена через поврежденный кожный барьер носители мутации филаггрина имеют повышенный риск развития атопического дерматита, бронхиальной астмы, аллергического ринита и пищевой аллергии. Частое развитие реакций гиперчувствительности IV типа в ответ на воздействие никеля и ранние клинические проявления аллергии на никель у лиц с мутацией гена филаггрина объясняются сниженным количеством остатков гистидина (основного метаболита филаггрина), формирующих хелатную связь с никелем, что обусловливает быстрое проникновения ионов никеля сквозь кожный барьер. В целом мутации гена филаггрина связывают с ранним началом и устойчивостью дерматита к терапии, неблагоприятным течением заболевания и значительно более частой необходимостью прекращения профессиональной деятельности (Landeck L. et al., 2012; Thyssen J. P., 2012; Kaae J. et al., 2012). Мутации гена TNF повышают риск развития ДР за счет усиленного высвобождения провоспалительного цитокина – фактора некроза опухоли – поврежденными и стимулированными интерлейкином-1 кератиноцитами и макрофагами кожи (Landeck L. et al., 2012). Изменения структуры генов позднего ороговения (LCE3B и LCE3C) приводят к дисфункции эпидермального барьера, защищающего от потери воды и проникновения экзогенных факторов, что создает предпосылки к возникновению атопического дерматита и ДР (Molin S. et al., 2011). Мутации гена SPINK5 сопряжены с нарушением процесса дифференцировки кератиноцитов за счет отсутствия ингибирующего воздействия на экзогенные сериновые протеазы типа Kazal-5, что связывают с развитием неатопического ДР (Lan C. C. et al., 2011).
Исследования с участием близнецов показали, что причинами развития ДР в 41% случаев могут быть генетические факторы, в 59% – влияние окружающей среды. В целом в популяции 31% случаев заболевания определяются генетическими факторами и 69% – факторами окружающей среды, что подчеркивает важность превентивных производственных и экологических мероприятий (Lerbaek А. et al., 2007).
Никель
Хотя связь никеля с развитием атопического дерматита и ДР является доказанной, в последние годы значению этого иона в возникновении кожных заболеваний приписывается меньшая роль. Это связано с регуляторной политикой, ограничивающей включение никеля в состав ювелирных украшений.
Табакокурение
На сегодня связь табакокурения и ДР считается спорным вопросом, однако в датском исследовании с участием 7931 пациента в возрасте от 18 до 69 лет отмечалась более высокая распространенность ДР среди курильщиков (как нынешних, так и бывших) по сравнению с таковой в группе ранее не куривших участников (Thyssen J. P. et al., 2010). В систематическом обзоре публикаций за 1980-2013 гг. и метаанализе не удалось показать существенную связь между курением и заболеванием. Учитывая разнородность исследований, авторы все же сделали вывод о невозможности исключения курения из перечня факторов риска развития ДР (Lukács J. et al., 2015).
В другом недавнем обзоре 20 опубликованных статей по корреляции между табакокурением и ДР 3 из 7 статей и 4 из 8 эпидемиологических исследований свидетельствуют о значительной степени ассоциации между курением и распространенностью заболевания; 2 из 5 испытаний продемонстрировали положительную связь между курением и клинической степенью заболевания, в то время как ни в одной из работ не отмечено защитного влияния курения (Sorensen J. A. et al., 2015). Таким образом, влияние табакокурения на развитие и течение ДР не может быть окончательно оценено в настоящее время. Тем не менее попытка отказа от этой вредной привычки с целью клинического наблюдения течения ДР может быть весьма полезной. Связь ДР с употреблением алкоголя в исследованиях не прослеживается (Thyssen J. P. et al., 2010).
Рискассоциированные профессии и вещества
Рискассоциированные роды деятельности
В исследовании с участием пациентов с ДР в 10 европейских медицинских центрах у 52% выявлена положительная корреляция с родом деятельности. Профессиями, связанными с высоким риском (≥7 новых случаев заболевания на 10 тыс. рабочих в год) приобретения профессионального дерматоза (из которых ДР составляет более 90% случаев), названы парикмахер, пекарь, флорист, кондитер, плиточник, сварщик, паяльщик, зубной техник, механик, металлист, работник здравоохранения. Перечень специальностей высокого риска (3-7 новых случаев заболевания на 10 тыс. рабочих в год) включает в себя поваров, маляров, работников лакокрасочной промышленности, сферы общественного питания, механиков, монтажников, строителей и бетонщиков, лиц, занимающихся обработкой кожи и меха, домработниц, а также технический персонал (Dickel H. et al., 2001).
Рискассоциированные вещества
Согласно принятому в Германии нормативу «TRGS401. Опасность при контакте с кожей: определение, оценка, меры», вещества или смеси веществ, обладающие агрессивным раздражающим или сенсибилизирующим эффектом, должны быть маркированы буквой R. Дополнительно описаны особые условия работы и вещества, контакт с которыми не оказывает прямого повреждающего воздействия на кожу, однако при длительном влиянии способен провоцировать развитие дерматита. К этой категории относятся работы, связанные с сильным загрязнением или механическим напряжением, приводящим к микротравмам кожи; контакт с такими веществами, как растворители, дезинфицирующие, смазочно-охлаждающие и моющие жидкости; длительное воздействие мягких кислот и щелочей, а также воды.
Работа во влажной среде
Такие виды работ являются доказанным фактором развития ДР, поскольку предусматривают:
- регулярное нахождение рук во влажной среде ≥2 ч/день;
- необходимость частого или особо тщательного мытья рук;
- ношение защитных перчаток с окклюзионным эффектом.
ДР как профессиональное заболевание
ДР составляет около 1/3 всех случаев профессиональной патологии. В 2013 г. из общего числа (71 579) уведомлений о профессиональных заболеваниях в Германии 24 033 относились к дерматозам. Профессиональная связь была подтверждена в 36 202 случаях, из которых 20 643 классифицированы как кожные заболевания (Deutsche Gesetzliche Unfallversicherung Spitzenverband, 2013).
Экономическая составляющая ДР
Согласно данным за 2010 г., 70% пациентов с ДР обращаются за медицинской помощью. Более 20% из них теряют трудоспособность более чем на 7 дней, 10% вынуждены менять работу. Ежегодные затраты на 1 случай лечения хронического ДР оцениваются в 9000 евро, 30% из которых составляет стоимость медицинской помощи (прямые затраты), а 70% – косвенные расходы (потеря производительности). Кроме того, у большинства пациентов, перенесших ДР, возникают негативные психосоциальные последствия (нарушения сна, перепады настроения, дискомфорт при повседневной деятельности) и снижение качества жизни (Diepgen T. et al., 2013).
Этиология
У некоторых пациентов с ДР обнаруживают только одну причину заболевания, но в большинстве случаев данное заболевание является многофакторным (33 vs 66%).
Основные причины развития ДР:
- генетические факторы;
- раздражающее воздействие на кожу (работа во влажной среде, контакт с химическими веществами, окклюзионные эффекты перчаток, механическое напряжение);
- контактные аллергены (профессиональные или экологические);
- контакт с белком (особенно в пищевой промышленности);
- идиопатический вариант (например, идиопатический гиперкератоз).
Дифференциальный диагноз
При установлении диагноза ДР необходимо выполнять общий осмотр. При этом важно помнить, что наличие псориаза не исключает развития ДР.
Заболевания, с которыми следует дифференцировать ДР:
- микозы (отрубевидный лишай рук);
- псориаз, в т. ч. ограниченный;
- красный плоский лишай;
- индуцированный химиотерапией ладонно-подошвенный синдром;
- чесотка;
- туберкулез кожи;
- поздняя кожная порфирия;
- буллезный пемфигоид;
- паранеопластический акрокератоз;
- злокачественный черный акантоз (тип Acral);
- наследственные ладонно-подошвенные кератозы.
Диагностика
Диагностика ДР предусматривает детальное изучение анамнеза, включающее:
- оценку существующих профессиональных и экологических воздействий;
- изучение личного и семейного анамнеза в отношении аллергических и кожных заболеваний (особенно атопических болезней и псориаза);
- уточнение продолжительности и временных характеристик дерматита (в частности, с учетом периодов работы и отдыха);
- оценку сопутствующей патологии и используемых препаратов;
- определение статуса курения.
Для оценки риска работы во влажной среде необходимо получить информацию о продолжительности прямого контакта кожи с водой (>2 ч/день?), ношении водонепроницаемых перчаток (>2 ч/день?), частоте и интенсивности мытья рук
(>10 р/день?; применение абразивных веществ с этой целью?), использовании защитных перчаток в работе.
Обследование включает в себя общий осмотр поверхности тела, в т. ч. стоп.
Патч-тестирование с коммерческой серией и материалами пациента
Контакт с аллергенами – причина не менее половины случаев дерматитов, поэтому выполнение патч-тестов является необходимым при длительности заболевания более 3 мес. Метод основан на реакции гиперчувствительности IV типа, в качестве стандартной коммерческой серии контактных аллергенов используются предполагаемые провоцирующие агенты: резиновые смеси, эпоксидные смолы, производные меркаптобензотиазола и др.
Использование стандартных аллергенов для патч-тестирования считается недостаточным, так как не позволяет выявить взаимосвязь заболевания и профессиональных факторов. В ряде случаев чрезвычайно информативно изучение смесей аллергенов с рабочего места пациента. Важную роль в патч-тестировании играет концентрация аллергена в смеси. Так, она не должна превышать рекомендуемую концентрацию, однако и высокое разведение может стать причиной ложноотрицательного результата.
Патч- и прик-тестирование с белоксодержащими материалами
Для диагностики контактного дерматита белкового генеза используется прик- и патч-тестирование, также необходимым является определение уровня IgE в сыворотке крови. Зачастую результаты патч-теста оказываются отрицательными, это объясняется тем, что реакция гиперчувствительности возникает только при проникновении аллергена сквозь кожный барьер, что возможно при нарушении его целостности (мацерации, микротравмах кожи рук). В такой ситуации для установления диагноза профессионального контактного дерматита необходимо провести прик-тест с целью индуцирования реакции немедленного типа, определить уровень IgE в сыворотке крови, обнаружить в анамнезе указания на взаимодействие с данным аллергеном. Ввиду очевидной сложности стандартизация и оптимизация методов диагностики контактного дерматита белкового генеза являются предметом текущих исследований.
Исследования содержания никеля и кобальта
Информационная сеть дерматологических отделений сообщает, что никель обусловил развитие 0,7% случаев ДР в период 2009-2013 гг. (Kickinger-Lorsch A. et al., 2015). В датском исследовании показано, что из 200 исследованных рабочих инструментов около 5% содержат никель (Thyssen J. P. et al., 2011), однако данная статистика не применима к Германии. Так, в недавней работе, в рамках которой изучали 600 различных инструментов, установлено наличие никеля в 32,5% из них. Причем в 22,9% случаев никель содержался в области ручки либо во всех частях инструмента, в то время как функциональная часть, имеющая минимальный контакт с руками рабочих, содержала данный элемент только в 9,7% (Kickinger-Lorsch A. et al., 2015). Эти результаты созвучны с данными шведского исследования, в котором никель обнаружили в 27% из 565 исследованных инструментов (Lidén C. et al., 1998). Известно, что большинство замочных ключей содержат никель. При этом его концентрация в рабочих инструментах и замочных ключах не подпадает под регуляторную директиву Европейского союза (документ REACH).
У пациентов с ДР и подозрением на сенсибилизацию никелем следует проводить тестирование с диметилглиоксимом. Такие тест-наборы, а также стандартные реакции для выявления кобальта (с 1-нитрозо-2-нафтол-3,6-дисульфокислотой динатриевой соли) выпускаются с указанием цветной реакции, коммерчески доступны и просты в использовании (Hamann D.
et al., 2013).
Лечение
Устранение контакта с причинным фактором
Лечение ДР должно начинаться с выявления и устранения триггерного фактора. Особое внимание следует уделять защитным мерам на производстве, замене рабочих инструментов на аналогичные, но не содержащие сенсибилизирующие компоненты, оптимизации влажности, температуры и других условий труда. Важно отметить, что «защитные перчатки» – это не обобщенное понятие. Для каждого химического вещества существуют показатели проницаемости через те или иные протекторные материалы. Начиная работу с химикатами, необходимо сначала изучить данные упаковки по требованиям к материалу и толщине защитных перчаток. Например, смотровые медицинские перчатки не предохраняют от попадания дезинфицирующих растворов, что необходимо учитывать, рекомендуя пациенту меры производственной защиты (Liskowsky J. et al., 2011).
В случаях доказанной провоцирующей роли конкретных производственных условий в развитии ДР в качестве профессионального заболевания дерматологический отчет должен быть направлен в страховую компанию с целью инициации проведения профилактических мероприятий. Доказано, что средства вторичной (производственные меры, амбулаторные семинары) и третичной (модификация диагностики и лечения) индивидуальной профилактики позволяют достигать ремиссии, улучшать качество жизни и сохранять рабочие места за сотрудниками (Skudlik C., Weisshaar E., 2015).
Топическое лечение
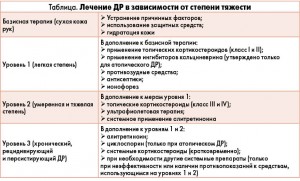
Терапия ДР базируется на оценке степени тяжести заболевания (табл.).
При необходимости топической терапии кортикостероидами в качестве стартовых средств рекомендуются препараты II класса, у которых соотношение польза/риск является наиболее оптимальным. Однако следует помнить, что лечение сильными стероидами коротким курсом предпочтительнее длительных схем использования более слабых препаратов (Diepgen P. et al., 2009). Существуют данные о благоприятном влиянии на длительность безрецидивного периода использования крема для рук на основе мометазона фуроата (воскресенье – вторник – четверг). Похожие данные накоплены и относительно положительного влияния топических препаратов циклоспорина, флутиказона пропионата и метилпреднизолона с частотой 2-4 раза в неделю (Veien N. K. et al., 1999; Schmitt J. et al., 2011).
При необходимости используются ингибиторы кальциневрина и другие вещества: антисептики (клиохинол, хлоргексидин, триклозан, полигексанид, сульфадиазин серебра) в случае суперинфекции; вяжущие и дубильные вещества при везикулярных поражениях; кератолитические и антипролиферативные вещества (в т. ч. салициловая кислота, мочевина, дитранол) в случае гиперкератоза, а также каменноугольные смолы, например полидоканол и ихтаммол, в качестве противозудных и противовоспалительных средств. Кроме перечисленных эффектов, ихтаммол, как недавно было обнаружено, увеличивает экспрессию филаггрина (van den Bogaard E. et al., 2013). Ионофорез водопроводной воды показан при везикулярном ДР в сочетании с гипергидрозом (Stege H., 2008).
Ультрафиолетовая терапия
В случае хронического и рецидивирующего течения при отсутствии противопоказаний целесообразно использовать ультрафиолетовую терапию (UVB, крем или ванна PUVA).
По данным большинства исследований, ванны PUVA превосходят по эффективности широкополосную UVB-терапию (Stege H., 2008).
Системная терапия
Системное лечение ДР оправдано в случае неэффективности базисной и топической терапии, о которой свидетельствует отсутствие положительной динамики в соответствии с одной из принятых шкал (Clinical Photo Guide – использование фото с целью 4-балльной оценки динамики процесса; Osnabruck Hand Dermatitis Severity Index – детальная 18-балльная оценка 6 морфологических критериев: эритема, размер, папула, глубина, трещины, везикулы; Occupational Contact Dermatitis Disease Severity Index – 10-балльная оценка эффективности проводимых мероприятий и т. д.). «Застывший» на протяжении нескольких недель показатель, отражающий активность процесса, является показанием к дополнению терапевтических схем системной терапией. Алитретиноин с 2008 г. лицензирован в Европе для лечения дерматитов, устойчивых к терапии кортикостероидами. Максимальный эффект достигается у пациентов с явлениями гиперкератоза. Механизм действия препарата заключается в стимуляции дифференциации, пролиферации и миграции Т- и В-лимфоцитов (Schindler M., 2014). Однако, несмотря на преимущества препарата, не следует забывать о его тератогенности. Так, женщинам фертильного возраста в период приема препарата и в течение 30 дней до и после лечения необходимо применять повышенные меры контрацепции с целью исключения возможной беременности.
Лечение системными кортикостероидами должно проводиться исключительно при неэффективности топической терапии и только короткими курсами.
Заключение
Оценивая динамику терапии ДР, врачам следует помнить, что при использовании анкет и субъективных шкал пациенты склонны оценивать свое состояние необъективно, характеризуя его как более тяжелое. Поэтому рекомендуется трактовать результаты, в большей мере ориентируясь на клиническую картину. Иными словами, морфологическая тяжесть заболевания должна влиять на концепцию лечения в большей степени, чем его длительность и влияние на качество жизни пациента. Стандартизированная оценка степени тяжести позволяет осуществлять мониторинг динамики и эффективности терапии не только в клинических исследованиях, но и в реальной практике (Agner T. et al., 2013).
Тем не менее недавнее исследование показало, что не удается достичь полной удовлетворенности пациентов лечением только лишь при улучшении кожных проявлений заболевания. Поэтому, помимо клинических проявлений, врач также должен учитывать степень комплайенса, проявлять сопереживание и не забывать о стрессе, индуцированном болезнью, в высокой степени влияющем на качество жизни пациентов (Herschel S. et al., 2013).
Mahler V. Journal der Deutschen Dermatologischen Gesellschaft. 2016 Jan; 14, Issue 1.
Подготовила Александра Меркулова