29 березня, 2020
Вплив кишкової мікрофлори на роботу жовчовивідної системи
Функціональні розлади травної системи у дітей – це актуальна проблема сучасної педіатрії, яка завжди активно обговорюється в рамках вітчизняних та міжнародних наукових конференцій. Принципи ведення пацієнтів з функціональною патологією періодично переглядаються і відображаються в оновлених настановах та рекомендаціях, зокрема у Римських критеріях. Проте за авторитетністю міжнародних рекомендацій вітчизняні лікарі применшують важливість напрацювань українських науковців, які часто випереджають своїх зарубіжних колег. Така ситуація склалася і з оновленими Римськими критеріями IV, які перегукуються з роботами українських вчених XIX-XX ст. Так, в усьому світі активно обговорювати роль мікробіоти кишечнику в забезпеченні нормальної роботи всіх органів та систем стали лише на початку ХХІ ст., хоча І.І. Мечников про це говорив ще на початку ХХ ст.
 У рамках науково-практичної конференції з міжнародною участю «Інновації в дитячій гастроентерології та нутриціології в практиці дитячого та сімейного лікаря» доповідь «Захворювання жовчовивідної системи та Римські критерії IV: нові терміни і старі визначення» представив завідувач кафедри терапії, ревматології та клінічної фармакології Харківської медичної академії післядипломної освіти, доктор медичних наук, професор Олексій Анатолійович Опарін.
У рамках науково-практичної конференції з міжнародною участю «Інновації в дитячій гастроентерології та нутриціології в практиці дитячого та сімейного лікаря» доповідь «Захворювання жовчовивідної системи та Римські критерії IV: нові терміни і старі визначення» представив завідувач кафедри терапії, ревматології та клінічної фармакології Харківської медичної академії післядипломної освіти, доктор медичних наук, професор Олексій Анатолійович Опарін.
– В Україні часто прослідковується тенденція, коли міжнародні рекомендації чи критерії сприймаються лікарями як непорушна догма, якою слід керуватися під час лікування тих чи інших захворювань. Після прийняття Римських критеріїв IV пройшло вже декілька років, що дозволяє проаналізувати їх основні переваги та недоліки, а найголовніше – відповісти на питання, чи всі іноземні критерії слід беззаперечно впроваджувати у вітчизняну клінічну практику, тим самим відкидаючи напрацювання власної школи гастроентерологів.
Коментар 1
Автори нових Римських критеріїв IV пропонують не використовувати функціональну термінологію всюди, де це можливо.
Уже кілька десятиліть тривають дебати між експертами щодо цього питання. Проте слово «функціональний» міцно закріпилося в сучасній медичній термінології і знайти йому альтернативу важко. Тим не менше, його застосування має певні обмеження, оскільки термін є неспецифічним.
Коментар 2
У Римських критеріях IV були переглянуті діагностичні критерії дисфункції сфінктера Одді (ДСО).
Згідно з попередніми Римськими критеріями ІІІ, при ДСО як діагностичне обстеження проводилася папілосфінктеротомія, однак це втручання підвищує ризик розвитку панкреатиту та кровотечі, тому ця рекомендація була виключена з наступних критеріїв. Слід зазначити, що при прийнятті Римських критеріїв ІІІ українські гастроентерологи були стурбовані включенням цієї інвазивної діагностичної маніпуляції, оскільки її ризики не є виправданими при ДСО. Зарубіжні експерти та автори Римських критеріїв дійшли такого висновку набагато пізніше.
Коментар 3
У Римських критеріях IV були запропоновані 12 кроків для посилення терапевтичного впливу, які анонсувалися як нові принципи ведення пацієнтів з гастроентерологічними захворюваннями.
Перший крок передбачав підвищення вдоволеності пацієнта, яке значною мірою залежить від сприйняття лікаря як особистості та компетентного спеціаліста, що цікавиться психологічним станом пацієнта та подає йому достовірну медичну інформацію. Важливою також є невербальна комунікація. Цей алгоритм передбачає збір анамнезу за допомогою інтелігентного інтерв’ю з пацієнтом. Рекомендується уважно слухати скарги хворого, ставити питання стосовно його почуттів, думок та досвіду, оминаючи стандартні «сухі» питання. Завдання лікаря – з’ясувати мету візиту пацієнта: нові чи минулі фактори ризику (похибки в дієті, супутні хвороби), наявність спадкових захворювань у пацієнта та членів його родини, наявність стресових факторів (смерть родича, проблеми на роботі, зловживання алкогольними напоями тощо), виявити погіршення психологічного стану (депресивний настрій, тривожність) та щоденної діяльності (зниження фізичної активності, працездатності). Якщо можливо, лікар повинен встановити зв’язок між симптомами та дією стресового фактора, оскільки більшість хворих не можуть зробити це самостійно, хоча і визнають негативний вплив стресу на емоційний стан.
Слід зазначити, що ці постулати були закладені ще фундаторами сучасної української медицини, котрі сформулювали усім добре відому фразу: «Лікувати потрібно пацієнта, а не хворобу». В той час як автори цих критеріїв оголосили «12 кроків» принципово новим підходом, вітчизняна школа гастроентерологів була знайома з ним уже давно.
Коментар 4
Римськими критеріями IV рекомендоване психологічне лікування, що включає когнітивно-поведінкову терапію, релаксацію, гіпноз тощо.
У деяких пацієнтів з гастроентерологічними симптомами може спостерігатися психопатологічна симптоматика, яка істотно знижує якість життя та часто є причиною проведення непотрібних діагностичних маніпуляцій та необґрунтованого призначення низки лікарських засобів. У таких випадках лікарю необхідно призначати додаткові методи обстеження відповідно до об’єктивних даних, та терапію з метою покращення якості життя хворого. Зазвичай проводиться психологічна терапія та призначаються трициклічні антидепресанти.
Ця рекомендація об’єднує як сумнівні методи лікування (гіпноз), так і «важку артилерію» (трициклічні антидепресанти). Призначення цієї групи препаратів без урахування першопричини та індивідуальних особливостей формування патології у конкретного пацієнта не вирішить основну проблему. Питання доцільності застосування антидепресантів у цієї категорії хворих є дуже суперечливим.
Таким чином, за 10 років після публікації Римських критеріїв ІІІ накопичені нові знання щодо природи захворювань, їх діагностики та нових підходів ведення пацієнтів, які втілені у Римських критеріях IV і одночасно повторюють принципи, закладені ще в теорії нервізму І.П. Павлова.
Сьогодні увага лікарів та науковців світу прикута до порушення роботи осі «головний мозок – кишечник» як основного механізму функціональних розладів шлунково-кишкового тракту. Цей механізм є класичним проявом теорії нервізму І.П. Павлова, яка виникла ще наприкінці ХІХ ст. Стосовно позитивної ролі мікробіоти у здоров’ї людини та впливу дисбіозу на якість та тривалість життя писав ще професор І.І. Мечников на початку ХХ ст.
Патологія жовчовивідної системи та кишкова мікробіота
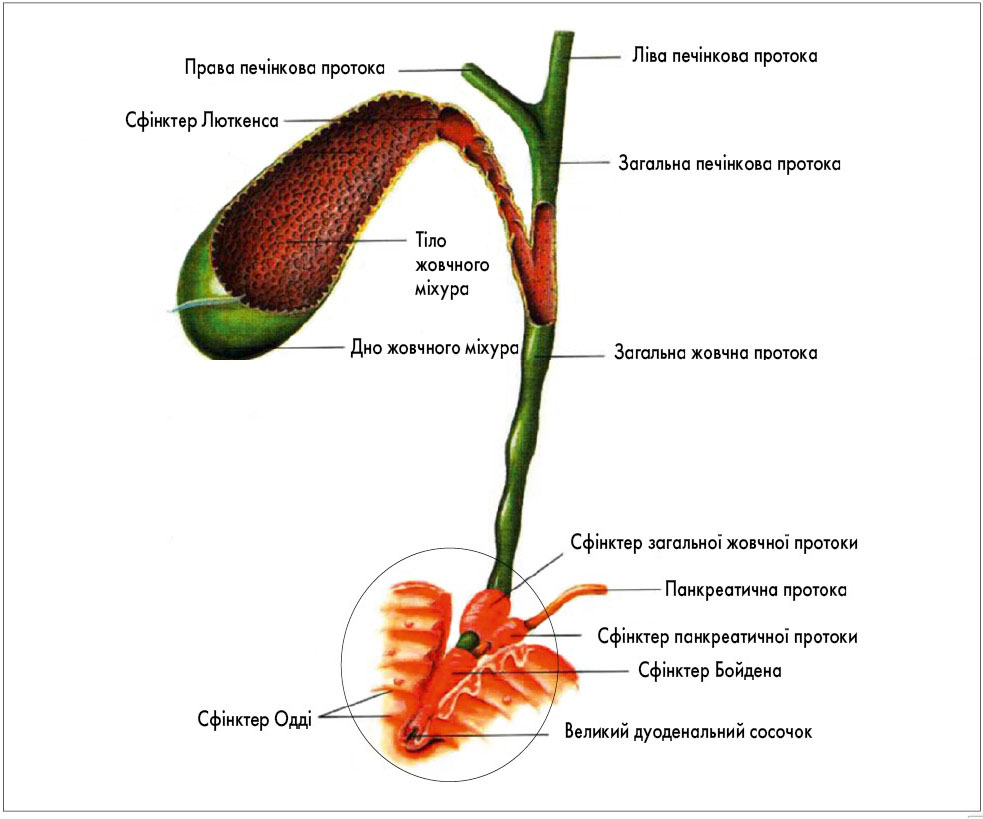
Одним з найчастіших функціональних розладів жовчовивідної системи є ДСО. Серед лікарів поширена думка, що сфінктер Одді – це окреме анатомічне утворення. Насправді він представляє собою комплекс сфінктерів загальної жовчної протоки, вірсунгової протоки та сфінктера великого дуоденального сосочка (рис. 1). Відповідно, патологія сфінктера Одді може бути зумовлена ураженням будь-якого його компонента.
Рис. 1. Жовчовивідні шляхи
Поряд із вдосконаленням візуалізаційних методів обстеження жовчовивідної системи зросла частота виявлення аномалій форми жовчного міхура у дітей та дорослих. Також збільшилася кількість випадків аномалій розташування жовчної та загальної печінкової проток. Це значно ускладнює диференційну діагностику патології жовчовивідної системи, адже вона супроводжується некласичними біліарними симптомами, зокрема наявністю у пацієнта кількох больових точок на поверхні живота, що не збігаються із проєкціями певних анатомічних структур біліарного тракту.
Сучасна ультразвукова діагностика є основним методом виявлення функціональних та структурних уражень жовчовивідних шляхів та жовчного міхура. Сьогодні почастішали випадки візуалізації у підлітків жовчного міхура із сильним потовщенням стінки та зменшенням порожнини органа, що поступово заміщується сполучною тканиною. Такий жовчний міхур називають порцеляновим.
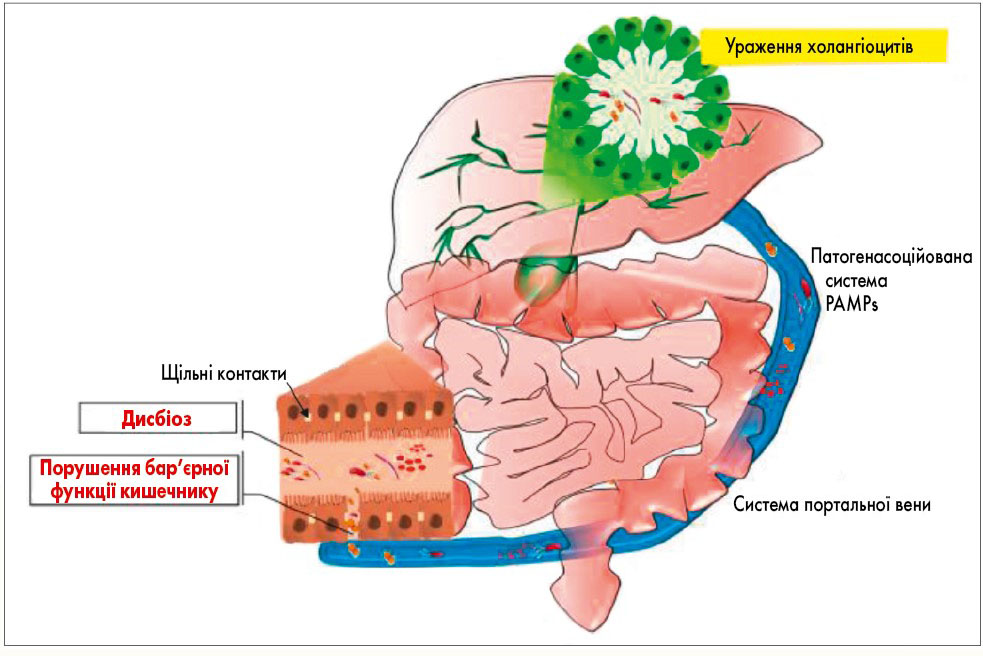
Функціональний та морфологічний стан гепатобіліарної системи значною мірою залежить від мікрофлори кишечнику. У нормі шлунково-кишковий тракт має фізичний (кишковий бар’єр та слизовий шар) та хімічний (секреторний IgA та антимікробні пептиди) бар’єри, котрі перешкоджають транслокації бактеріальних агентів та їх токсинів у бік печінки. Лише невелика кількість бактерій потрапляє до портальної вени та досягає печінки, проте завдяки механізму імунотолерантності цей процес не супроводжується імунною відповіддю. У випадку порушення кишкового бар’єра до печінки надходить велика кількість бактерій та їх метаболітів, які здатні потенціювати запалення гепатобіліарної зони та фіброз (рис. 2). Цей принцип лежить в основі гіпотези кишкової проникності. Система портальної вени забезпечує метаболічний зв’язок між кишечником та печінкою. Запальні процеси в кишечнику призводять до порушення кишкового бар’єра (порушення цілості тісних контактів між ентероцитами) та дисбактеріозу, сприяють надходженню до печінки мікроорганізмів та патогенасоційованих молекул PAMPs, які здатні ініціювати ураження гепатобіліарної системи.
Рис. 2. Гіпотеза кишкової проникності
У роботі D.M. Giordano і співавт. (2018) показаний зв’язок дисбактеріозу з розвитком та прогресуванням холангіопатій. Виявлено, що у хворих з холангіопатіями склад мікрофлори кишечнику істотно відрізняється від такого у здорових людей. У нормальних умовах холангіоцити, які вистилають жовчовивідні шляхи, беруть участь у формуванні кінцевого складу та об’єму жовчі. Під дією певних екзо- чи ендогенних чинників холангіоцити можуть зазнавати деяких фенотипічних змін. Реактивні холангіоцити провокують вивільнення прозапальних молекул та активують вроджену імунну відповідь на дію мікроорганізмів чи продуктів їх життєдіяльності, які надходять до гепатобіліарної системи шляхом ентерогепатичної циркуляції. Дисбіоз кишечнику асоційований з розвитком двох найпоширеніших холангіопатій: первинного склерозуючого холангіту та первинного біліарного холангіту.
У дослідженні T. Wu, Z. Zhang та співавт. (2013) було показано, що у хворих з жовчнокам’яною хворобою (ЖКХ) склад мікрофлори кишечнику відрізняється від складу мікрофлори у здорових людей. Так, при ЖКХ виявляли збільшення кількості протеобактерій Escherichia, Salmonella, Helicobacter spp. та зменшення Faecalibacterium, Lachnospira, Roseburia spp. Точно з’ясувати, є ця відмінність причиною чи наслідком ЖКХ, поки не вдалося.
Таким чином, доведений зв’язок між кишковою мікрофлорою та гепатобіліарною системою відкриває ще одну ціль терапевтичного впливу у складі комплексного лікування осіб з ураженням жовчовивідних шляхів, що спрямована на корекцію дисбіозу.
Сьогодні на фармацевтичному ринку представлено багато бактеріальних препаратів, проте доведеною пробіотичною активністю володіють лише деякі з них. Одним з найбільш відомих та добре вивчених пробіотиків є Saccharomyces boulardii (S. boulardii) – непатогенні одноклітинні дріжджові гриби роду Saccharomyces.
Мікроорганізми S. boulardii мають низку переваг: вони стійкі до дії соляної та жовчної кислот, не колонізують кишечник (через 2-5 днів після припинення прийому препарату у випорожненнях їх вже не виявляють), не проникають через кишковий бар’єр, володіють природною антибіотикорезистентістю, не пригнічують ріст облігатної мікрофлори кишечнику. Ліофілізовані дріжджі S. boulardii входять до складу препарату Нормагут. Завдяки стійкості S. boulardii до агресивного середовища шлунково-кишкового тракту пробіотики потрапляють до місця призначення у високій концентрації. Препарат можна застосовувати одночасно з антибіотиками.
S. boulardii мають такі властивості:
- антимікробні – запобігають адгезії хвороботворних бактерій до слизової оболонки кишечнику, інгібують розмноження патогенної та умовно-патогенної флори, не впливають на корисні бактерії кишечнику;
- антисекреторні – шляхом зниження продукції цАМФ в ентероцитах зменшують секрецію води та солей у кишечнику;
- антитоксичні – розщеплюють бактеріальні токсини завдяки синтезу протеази та фосфатази;
- ферментативні – сприяють підвищенню активності лактази, сахарази, мальтази;
- трофічний ефект – завдяки вивільненню поліамінів у тонкій кишці відбувається стимуляція травних ферментів, які сприяють розщепленню та всмоктуванню поживних речовин;
- опосередкований противірусний ефект, пов’язаний із синтезом поліамінів та антитіл у кишечнику;
- неспецифічний імуномодулюючий ефект – пробіотик сприяє підвищенню секреції IgA, зменшенню синтезу прозапальних цитокінів.
Згідно з офіційною інструкцією, препарат Нормагут може застосовуватися у дітей з 2 років, проте у деяких сучасних публікаціях описується досвід застосування пробіотика у недоношених немовлят (O. Serce, 2013). Він значно знижує рівень білірубіну в сироватці здорового новонародженого з неонатальною жовтяницею, не викликаючи жодних побічних реакцій (V. Suganthi, 2016).
Проведений метааналіз 21 рандомізованого контрольного дослідження (РКД) показав, що застосування пробіотика S. boulardii знижує ризик виникнення антибіотикасоційованої діареї (ААД) у дітей та дорослих (H. Szajewska et al., 2015). Згідно з висновками мультицентрового РКД, пробіотик S. boulardii є одним з препаратів вибору для профілактики ААД у новонароджених та дітей раннього віку (C.M. Wan et al., 2017). Найновіший метааналіз щодо ефективності S. boulardii у веденні педіатричних пацієнтів з гострим ентероколітом (H. Szajewska et al., 2020) показав, що порівняно з плацебо чи відсутністю лікування пробіотик знижує тривалість діареї (n=3450; середня різниця -1,06 дня; 95% ДІ -1,32 до -0,79), скорочує час перебування в стаціонарі (n=999; середня різниця -0,85 дня; 95% ДІ -1,35 до -0,34).
Сьогодні сфера застосування пробіотиків набагато ширша, ніж раніше. Корекція мікрофлори кишечнику у хворих з патологією жовчовивідної системи є патогенетично обґрунтованою та доречною. Згідно з настановами Європейського товариства педіатричної гастроентерології, гепатології та нутриціології та Європейського товариства дитячих інфекційних хвороб (ESPGHAN/ESPID, 2014), S. boulardii (Нормагут) та Lactobacillus GG належать до пробіотиків з позитивною рекомендацією.
Підготувала Ілона Цюпа
Тематичний номер «Педіатрія» №1 (52) 2020 р.