8 грудня, 2016
Поддерживающая диуретическая терапия у пациентов с ХСН: вопросы и ответы
В настоящей публикации мы попытались в сжатой форме ответить на наиболее характерные вопросы со стороны клиницистов, касающиеся длительной диуретической терапии (ДТ) у пациентов с хронической сердечной недостаточностью (ХСН).
Каковы цели, которые преследует врач, назначающий пациенту поддерживающую ДТ (ПДТ)?
Главной целью ПДТ является перманентный контроль (недопущение появления) субъективных и объективных признаков задержки жидкости, которые ранее имели место у пациента и были ранее устранены с помощью активной, обычно стационарной, ДТ (здесь подразумевается, что упомянутая активная ДТ была адекватной, т.е. проводилась до достижения эуволемического состояния). Правильно осуществляемой ДТ обычно сопутствует улучшение качества жизни за счет улучшения самочувствия и повышения толерантности пациентов к физической нагрузке [1].
Продлевает ли жизнь пациентам с ХСН ПДТ?
Данный вопрос выглядит вполне резонным, поскольку хорошо известно, что, в отличие от нейрогуморальных антагонистов, петлевые и тиазидные диуретики не влияют на патофизиологические механизмы прогрессирования ХСН.
С сугубо формальных позиций, базирующихся на стандартах доказательной медицины, на вопрос о том, улучшают ли диуретики выживаемость пациентов с ХСН, не существует ответа, поскольку соответствующие масштабные рандомизированные клинические исследования – РКИ (плацебо-контролируемые либо сравнительные) не проводились по этическим мотивам. Причиной их непроведения было базирующееся на клиническом опыте допущение об a priori более высоком ближайшем риске декомпенсации кровообращения (и ассоциированном с ней риске смерти) в группе пациентов, не принимающих диуретик. В качестве примера, иллюстрирующего справедливость такого допущения, можно привести результаты одного из ранних исследований, в котором замена у пациентов с умеренно выраженными симптомами ХСН диуретика на каптоприл в структуре ПДТ уже спустя несколько недель приводила к развитию отека легких в 1/3 случаев [2]. В повседневной практике клиницисты регулярно сталкиваются с ситуацией, когда пропуски в приеме или отказ от диуретиков у пациента с тяжелой ХСН довольно быстро заканчиваются госпитализацией, нередко ургентной. Поэтому, если отбросить казуистическую «шелуху», на поставленный вопрос есть все основания ответить утвердительно. Каждый очередной прием диуретика склонными к гиперволемии пациентами с насосной недостаточностью левых отделов сердца предотвращает за счет «механического» уменьшения объема циркулирующей плазмы (ОЦП) появление застойных явлений в легких, включая угрожающий жизни их альвеолярный отек. Точно так же у пациентов с правожелудочковой СН регулярная ДТ, предупреждая или ограничивая гиперволемию большого круга кровообращения и, соответственно, системную венозную гипертензию, отдаляет во времени терминальную дисфункцию печени и почек. Несмотря на вышеупомянутое отсутствие РКИ, в двух крупных Кокрановских метаанализах, базирующихся на данных пилотных и обсервационных исследований, продемонстрировано свойство диуретиков снижать и долговременную смертность, и риск госпитализаций по поводу клинической декомпенсации при ХСН [1, 3].
Вместе с тем сама постановка вопроса о характере влияния длительной ДТ на прогноз жизни пациентов с ХСН отнюдь не случайна и имеет прямое отношение к практическим аспектам их применения. Суть заключается в том, что такие фундаментально присущие салуретикам фармакодинамические эффекты, как увеличение экскреции ионов К+ и Mg2+ и рефлекторное (в ответ на снижение ОЦП) активирование симпатоадреналовой и ренин-ангиотензиновой систем (РАС), потенциально сопряжены с увеличением риска развития жизнеугрожающих желудочковых аритмий и стимуляцией системных патофизиологических путей прогрессирования ХСН. В итоге это может ограничивать продолжительность жизни таких пациентов
и, таким образом, нивелировать благоприятное влияние регулярного их приема на системную и внутрисердечную гемодинамику. «Ключом» к недопущению такой ситуации является строгое соблюдение современных условий длительного применения диуретиков у пациентов с ХСН. В соответствии с действующими новыми (2016 г.) Европейскими рекомендациями по лечению ХСН таковыми являются сочетание диуретиков с ингибиторами РАС (ингибиторами ангиотензинпревращающего фермента – ИАПФ или сартанами), бета-адреноблокаторами и антагонистами минералокортикоидных рецепторов (АМР); контроль электролитов крови (прежде всего, К+) на фоне подбора их дозы; использование той минимальной ежедневной дозы диуретика, которая позволяет поддерживать состояние эуволемии [4].
Обратим Ваше внимание также и на пункт вышеупомянутых рекомендаций, в котором речь идет
о том, что назначение ДТ противопоказано пациентам с ХСН, ранее не имевшим признаков задержки жидкости [4]. По удачному выражению одного из ведущих экспертов, лечение этой категории пациентов диуретиками «впрок» – бессмысленно и не может быть оправдано [5]. Более того, оно вредно, поскольку не имеет своим результатом ничего иного, кроме стимуляции механизмов прогрессирования ХСН через активацию нейрогуморальных систем. Иллюстрацией этого, в частности, может быть более высокая смертность пациентов с ХСН, принимавших диуретики, в сравнении с больными, их не принимавшими, в субанализе базы данных исследования DIG (1997), в котором основная часть (80%) пациентов исходно относились ко II функциональному классу (легкая СН) по NYHA и, по ретроспективной оценке аналитиков, на самом деле в большинстве случаев не нуждались в ДТ.
Каковы факторы, ограничивающие эффективность ДТ?
Условно разделим такие факторы на несколько групп: а) патофизиологические; б) связанные с самой ДТ; в) связанные с одновременным приемом других медикаментов; г) связанные с несоблюдением правил ДТ; д) связанные с некоторыми сопутствующими состояниями.
А. Патофизиологические факторы
Почечный кровоток (ПК) является важной детерминантой диуретического ответа. При ХСН снижению ПК способствует констрикция приносящих (афферентных) артериол, обусловленная высокой активностью РАС, и низкое системное артериальное давление (АД) [6]. Сочетание последних двух факторов, характеризующее многих пациентов с тяжелой ХСН, является наиболее неблагоприятным, поскольку в большинстве случаев из-за низкого уровня АД адекватной блокады РАС с помощью ингибиторов АПФ либо сартанов у них достичь не удается, а возрастание диуретического ответа при увеличении дозы мочегонного препарата может обусловить дальнейшее снижение АД, замыкая таким образом соответствующий «порочный круг». Определенную роль в преодолении подобной ситуации может сыграть выбор петлевого диуретика для ПДТ – в пользу торасемида с его менее выраженным гипотензивным ответом в сравнении с фуросемидом в сопоставимой по диуретической эффективности дозировке [7].
Нельзя забывать и о том, что пациенты со скоростью клубочковой фильтрации (СКФ) <30 мл/мин/1,73 м2 хуже отвечают на петлевые диуретики, как правило, требуя назначения более высоких доз, и слабо реагируют на мочегонные средства тиазидного ряда, применяемые в качестве монотерапии [8].
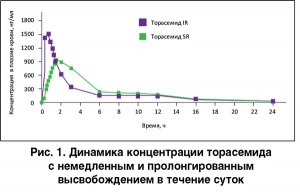
Фактором, способным негативным образом повлиять на суммарный диуретический ответ за сутки, выступает так называемый рикошетный эффект постдиуретической задержки Na+, состоящий в усилении реабсорбции последнего (а следовательно, и в угнетении диуреза) после окончания периода диуретического действия мочегонного препарата. Вышеуказанный эффект реализуется через рефлекторную активацию РАС и существенно выражен у фуросемида. Торасемид, характеризующийся слабой активацией РАС либо отсутствием таковой, демонстрирует меньшую выраженность указанного эффекта [9]. В то же время имеются данные о том, что инновационная пролонгированная форма торасемида (торасемид SR) рикошетного Na+-ретенционного эффекта практически не проявляет [10], что связывают с наиболее «плавным», в сравнении с другими диуретиками (включая торасемид с немедленным высвобождением – торасемид IR), характером его фармакокинетического профиля (рис. 1).
Б. Факторы, сопряженные с самой ДТ
Неадекватность режима приема диуретика и неправильно выбранная для поддерживающей терапии его дозировка выступают важными самостоятельными факторами, определяющими недостаточную эффективность ПДТ. Необходимо помнить, что единственно приемлемым режимом приема диуретика в амбулаторных условиях является ежесуточный, а ежедневная его доза должна быть такой, которая бы обеспечивала стабильное поддержание так называемой «сухой» массы тела пациента, достигнутой в результате преодоления предшествующей клинической декомпенсации. Важнейшим технологическим «приемом», способствующим решению данной задачи, является взвешивание пациента не менее 3 раз в неделю на домашних весах. Увеличение массы тела на 1,5-2 кг за последние 3-4 дня выступает сигналом к консультированию (в том числе и в телефонном режиме) с врачом относительно дозировки диуретика, либо к самостоятельной ее коррекции, наряду с упорядочиванием питьевого режима, до восстановления исходной массы тела. Вышеупомянутая схема действий в обязательном порядке должна быть транслирована пациенту в виде устной и письменной (желательно в виде одного из пунктов рекомендаций) при выписке из стационара.
Учитывая, что адекватная суточная дозировка диуретика для амбулаторного приема далеко не всегда может быть правильно «заблаговременно» определена врачом, крайне важную роль играет амбулаторный визит пациента, вне зависимости от самочувствия, в ближайшие сроки (от 7 до 14 дней) после выписки из стационара, на котором, сообразуясь с данными регистрации массы тела в домашних условиях, врач, при необходимости, осуществляет корректировку дозы препарата для ПДТ в сторону увеличения либо, в ряде случаев, – уменьшения. Вышеуказанный «7-дневный» визит закреплен в качестве стандарта ведения пациентов с ХСН в рекомендациях Американской коллегии кардиологов/Американской Ассоциации сердца [11]. Вполне приемлем и амбулаторный визит в срок до 30 дней после выписки, поскольку позволяет снизить риск госпитализации по поводу декомпенсации кровообращения в ближайшие 6 мес вдвое по сравнению с пациентами, такой визит не осуществившими [12].
Фактором, в ряде случаев обусловливающим снижение диуретического ответа при длительной ДТ, является развитие так называемой поздней резистентности к диуретикам, патофизиологической основой которой является компенсаторная гипертрофия эпителиальных клеток дистальных канальцев, направленная на повышение реабсорбции Na+ и опосредуемая циркулирующим альдостероном [8]. Наконец, имеет значение и выбор диуретика: как правило, для ПДТ назначается петлевой диуретик, поскольку тиазиды характеризуются более слабым мочегонным эффектом и, как уже указывалось выше, малодейственны при СКФ <30 мл/мин/1,73 м2.
В. Лекарственные средства, угнетающие диуретический ответ
Наиболее опасной для пациентов с ХСН, нуждающихся в ДТ, группой препаратов являются нестероидные противовоспалительные средства (НПВП). Блокируя синтез вазодилататорных простагландинов, выполняющих при ХСН важнейшую роль регуляции почечного кровотока, НПВП могут резко снижать диурез, вплоть до анурии, проявляя при этом достаточно продолжительный «следовой» эффект [8, 9]. В международных клинических документах их использование при ХСН отнесено к рекомендациям III класса, т.е. квалифицировано как вредное и противопоказанное [4, 11]. При трансляции пациенту основных положений, касающихся модификации образа жизни и основ самопомощи, врачом должны отдельно быть освещены риски применения НПВП. Это тем более важно, что большинство среди пациентов с ХСН составляют лица пожилого возраста, как правило, страдающие нарушениями со стороны опорно-двигательного аппарата и нередко рассматривающие НПВП как банальные «обезболивающие» средства. Нефротоксическим действием обладают также триметоприм, гентамицин, некоторые другие средства.
Г. Сопутствующие состояния
Сопутствующие заболевания почек с нефротическим синдромом, характеризующиеся макропротеинурией и выраженным (<20-30 мл/мин/1,73 м2) снижением СКФ резко уменьшают эффективность диуретической терапии, нередко требуя максимальных доз петлевых диуретиков [13].
Сопутствующий гипотиреоз способствует задержке жидкости во внеклеточном пространстве и может являться неидентифицированной причиной недостаточного диуретического ответа у пациентов с ХСН. Особое значение гипотиреоз как преципитирующий фактор ретенции жидкости имеет у пожилых (старше 65 лет) пациентов с ХСН, поскольку доля этой патологии среди них достигает 20% [14].
Какова тактика врача в случаях возникновения резистентности к ПДТ?
О формирующейся резистентности к ПДТ можно говорить тогда, когда при надлежащем соблюдении пациентом водного баланса и неупотреблении им препаратов, способных ухудшить функцию почек (НПВП и др.), снижается диуретический ответ на ранее эффективную ежедневную дозу диуретика, что сопровождается нарастанием массы тела. Подобную ситуацию нет оснований расценивать как устойчивость к диуретическому препарату как к таковому – правильнее говорить о резистентности пациента к конкретной его дозе. Ее причинами могут быть, с одной стороны, упомянутый механизм поздней резистентности, с другой же – естественный процесс прогрессирования насосной недостаточности сердца, обычно требующий усиления диуретической терапии на том или ином этапе длительного наблюдения пациента. При своевременном обращении пациента к врачу данная проблема может быть разрешена в амбулаторных условиях. Восстановление должного диуретического ответа и возврат к состоянию эуволемии могут быть достигнуты путем: а) добавления АМР (если таковой не был назначен ранее); б) увеличения дозы петлевого диуретика и/или комбинирования последнего с тиазидами [4]. Реализация вышеуказанных подходов, как правило, должна сочетаться с повторным обсуждением с пациентом вопросов контроля водного баланса, солевого режима и массы тела.
Рекомендация, касающаяся добавления ацетазоламида (диакарба) на срок до 3-4 дней к петлевому диуретику с целью восстановления диуретического ответа [15], не имеет под собой реальной доказательной базы и не представлена ни в одном из международных документов по лечению СН, в связи с чем использование такого подхода вряд ли оправдано.
В случаях позднего обращения пациента, которое, как правило, сопровождается явными застойными явлениями в легких и/или выраженным периферическим отечным синдромом, больного следует направить на стационарное лечение, подразумевающее, прежде всего, внутривенное введение диуретиков до достижения эуволемического состояния.
Может ли сама по себе ДТ вызывать повреждение почек?
От повреждения почек следует отличать так называемую преренальную азотемию в виде транзиторного повышения уровня креатинина крови на фоне активной диуретической терапии, обусловленную относительно быстрым уменьшением объема циркулирующей плазмы, приводящей к снижению почечного кровотока. У пациентов с ХСН эта проблема может возникать в процессе стационарного лечения клинической декомпенсации и не очень характерна для грамотно проводимой амбулаторной ПДТ.
В то же время на сегодняшний день накоплены данные о прямом повреждающем влиянии быстрого массивного натрийуреза на тубулоинтерстициальную ткань почек. Поражение канальцевого аппарата является ранним маркером ренального повреждения, предшествующего выраженному снижению клубочковой фильтрации [16]; при дальнейшем прогрессировании оно характеризуется развитием истерстициального фиброза и гибелью канальцев («атубулярные нефроны»), чему уже сопутствует снижение азотовыделительной функции почек [17]. Назначение быстродействующего петлевого диуретика с коротким периодом полувыведения характеризуется вышеупомянутым пикообразным натрийурезом, повреждающим канальцевый аппарат [18]. При быстром и избыточном выведении натрия эти микроповреждения канальцевого аппарата имеют необратимый характер [16,19]. За пикообразным натрийурезом неизбежно следует «рикошетный» период компенсаторной задержки Na+, что, как уже говорилось ранее, может обусловливать необходимость повторного введения препарата либо увеличения его дозы.
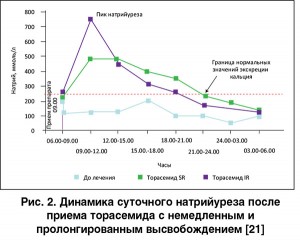
Вышеизложенная картина достаточно характерна для ежедневного использования фуросемида в тех немалых ежедневных дозах, которые обычно требуются для поддержания эуволемического/субэуволемического состояния у пациентов с тяжелой ХСН. С позиций ограничения повреждения ренального тубулоинтерстициального аппарата теоретически более привлекательным выглядит торасемид с его несколько более продолжительным периодом полувыведения [20]. Однако сравнение широко применяемой рутинной лекарственной формы торасемида с его современной пролонгированной формой показало, что его применение сопряжено с той же пикообразной конфигурацией кривой натрийуретического ответа (рис. 2). В то же время прием торасемида замедленного высвобождения характеризовался значительно менее выраженными крутизной нарастания и амплитудой кривой натрийуреза, не носящей формы пика (рис. 2). При этом статистически значимых различий между суммарным натрийурезом за сутки в обеих группах не отмечено [21].
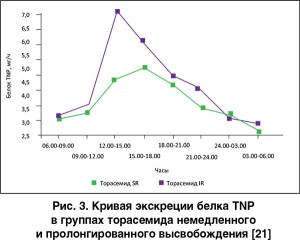
В свете вышеизложенных данных о роли пикообразного натрийуреза в повреждении канальцевого аппарата с указанными различиями соответствующих кривых должны согласовываться и различия в реакции тубулоинтерстициальной ткани на прием обычной и пролонгированной форм торасемида. Данное предположение было подтверждено при анализе в вышеуказанных группах экскреции белка ТНР, выполняющего защитную роль в отношении повреждения канальцев [22, 23] и используемого в качестве маркера такого повреждения. Оказалось, что экскреция ТНР была существенно выше в группе обычного торасемида, и ее пик практически соответствовал по конфигурации пику натрийуреза [21] (рис. 3).
Таким образом, терапии петлевыми диуретиками сопутствует определенный риск латентного повреждения канальцевого аппарата почек. Вместе с тем сегодня имеются доказательства в пользу того, что такой риск может быть нивелирован использованием лекарственной формы торасемида с замедленным высвобождением.
Как обеспечить безопасность ПДТ?
Начинать следует с момента инициации ПДТ – обычно в период перед выпиской пациента из стационара. На данном этапе целесообразно: 1) проконтролировать уровень К+ и креатинина, рассчитав СКФ; 2) оценить уровень систолического АД; 3) оценить сопутствующую поддерживающую фармакотерапию с позиций ее взаимодействия с ПДТ.
При гипокалиемии (К+ <3,5 ммоль/л) следует рассмотреть возможность увеличения дозы АМР и оценить возможность замены фуросемида на торасемид; при этом, если Вы планировали комбинировать петлевой диуретик с тиазидным – рассмотреть возможность уменьшения дозы последнего либо даже его отмены. При величине СКФ <30 мл/мин/1,73 м2 акцент в назначаемой ПДТ следует сделать на петлевой диуретик, хотя у наиболее тяжелых пациентов, склонных к быстрому накоплению жидкости, комбинирование с последним мочегонного средства тиазидного ряда может не иметь альтернативы.
При артериальной гипотензии (систолическое АД <90 мм рт. ст.) оптимальным может быть использование пролонгированной формы торасемида с его «плавной» кривой суточного диуреза, отличающейся от традиционных петлевых диуретиков. В случае необходимости использования больших доз диуретиков для поддержания эуволемического состояния у тяжелых пациентов с ХСН, склонных к гипотензии, вынужденной (хотя и крайне нежелательной) мерой может стать временное уменьшение дозы ИАПФ (сартана).
Уже в процессе длительной ПДТ могут возникать клинические проблемы, алгоритм реагирования на каждую из которых представлен в действующих (2016 г.) Европейских рекомендациях по лечению ХСН.
Симптомная гипотензия:
а) попробовать уменьшить дозу диуретика (-ов), если отсутствуют застойные явления; б) оценить потребность в продолжении приема препаратов с вазодилатирующим действием (нитраты, антагонисты кальция и пр.).
Гипокалиемия/гипомагниемия:
а) увеличить (если позволяет АД! – Прим. авт.) дозу ингибитора АПФ (сартана); б) добавить АМР, препараты калия/магния.
Гипонатриемия: при отсутствии гиповолемии – если пациент принимает тиазидный диуретик – отменить его, уменьшить дозу петлевого диуретика; если есть задержка жидкости: а) ограничить прием последней внутрь; б) увеличить дозу петлевого диуретика; в) рассмотреть возможность назначения антагониста вазопрессина (в Украине данная группа средств пока отсутствует. – Прим. авт.); г) рассмотреть целесообразность инфузионного лечения инотропными препаратами; д) рассмотреть целесообразность ультрафильтрации крови.
Гиповолемия/дегидратация: оценить волемический статус, уменьшить дозу диуретика.
Повышение уровня креатинина/азота мочевины:
а) убедиться, нет ли дегидратации; б) исключить использование нефротоксических агентов (НПВП, триметоприм и др.); в) отменить АМР; г) в случае комбинирования петлевого и тиазидного диуретика – отменить последний; д) рассмотреть целесообразность уменьшения дозы ИАПФ/сартана.
Гиперурикемия/подагра:
а) рассмотреть возможность приема аллопуринола; б) при симптомах подагры – назначить колхицин для уменьшения боли.
Советы пациенту:
Избегать приема НПВП; научиться корректировать дозу диуретика с учетом данных регулярного взвешивания и самочувствия; оговорить целесообразность уменьшения дозы диуретика при развитии состояний, характеризующихся потерей жидкости, – диареи, рвоты, обильного потоотделения [4].
Может ли длительная ПДТ отрицательным образом влиять на качество жизни пациента?
Поддерживая эуволемическое (или близкое к таковому) состояние, диуретики улучшают самочувствие и, соответственно, качество жизни пациентов с ХСН, о чем говорилось выше. Вместе с тем назначение ПДТ имеет обратную сторону в виде определенного ограничения бытовой активности пациентов вследствие возникновения императивных позывов к мочеиспусканию в первой, наиболее социально активной половине дня [24]. Это выступает потенциальным фактором ухудшения качества жизни, поддержание приемлемого уровня которого является одной из фундаментальных целей лечения ХСН. С другой стороны, как показало одно из исследований, потребность в реализации своих социальных функций нередко заставляет пациентов отказываться от планового приема диуретика, что может инициировать рецидив гиперволемии и, соответственно, ухудшение клинического состояния [25].
Оптимизм касательно возможности преодоления данного недостатка ПДТ появился после внедрения в клиническую практику упоминавшейся ранее, пока что единственной, пролонгированной (или с так называемым модифицированным высвобождением) формы торасемида (Бритомар). Данная форма, созданная на основе гидроколлоидного матрикса, характеризуется, в сравнении с обычным торасемидом, более медленной абсорбцией в кишечнике при сохранении аналогичной биодоступности. В результате этого примерно вдвое возрастает период достижения максимальной концентрации препарата в крови (Cmax), а сама Cmax уменьшается примерно на треть в сравнении с обычной формой торасемида. Следствием этого является меньший объем мочи в первые 5-6 ч после приема Бритомара при сопоставимом для обеих форм препарата объеме мочи за сутки [26]. Как показали исследования с участием здоровых добровольцев, этому отвечают меньше частота и интенсивность позывов к мочеиспусканию при приеме пролонгированной лекарственной формы [27].
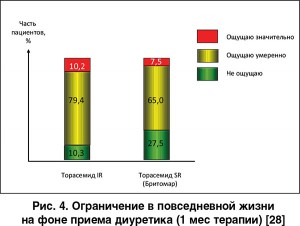
В выполненном в Украине мультицентровом исследовании КОМФОРТ-СН (2014) сопоставлялись эффекты Бритомара и обычного (с немедленным высвобождением) торасемида у амбулаторных пациентов с ХСН [28]. Обе лекарственные формы препарата при регулярном приеме эффективно контролировали волемический статус пациентов. В то же время обработка заполнявшихся пациентами специальных стандартизованных опросников показала, что прием Бритомара характеризовался достоверно меньшим количеством мочеиспусканий в первые 3-6 ч, меньшим ограничением бытовой активности (рис. 4) и достоверно большей комфортностью диуретической терапии (рис. 5).
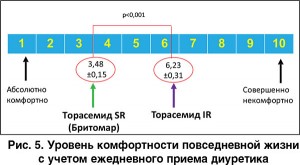
В контексте ответа на заданный выше вопрос результаты исследования КОМФОРТ-СН представляются достаточно важными – прежде всего в свете современной доктрины обеспечения наилучшего, насколько это возможно, качества жизни и сохранения социальной активности пациентов с ХСН. Исходя из такого подхода, из двух препаратов, которые проявляют соизмеримое терапевтическое влияние на симптоматику и течение заболевания, преимущество следует отдавать тому из них, который характеризуется лучшей переносимостью. С постепенным совершенствованием подходов к лечению и, соответственно, с улучшением клинико-гемодинамического контроля «амбулаторной» ХСН существенно возрастает число физически активных пациентов, на социальных функциях которых в той или иной степени может нежелательным образом сказываться регулярный прием диуретиков [29]. Если преимущество торасемида над фуросемидом в данном аспекте продемонстрировано давно [30], то теперь становится очевидным факт лучшей субъективной переносимости пациентами с ХСН пролонгированной формы торасемида над рутинной формой этого препарата. Следовательно, есть все основания рассматривать торасемид модифицированного высвобождения в качестве оптимальной «стартовой» опции при назначении ПДТ пациентам с ХСН.
В заключение заметим, что обеспечение эффективной и безопасной поддерживающей диуретической терапии больных с ХСН на амбулаторном этапе является далеко не простой и весьма ответственной функцией врача, призванного оказывать помощь таким пациентам. Эта функция требует твердых навыков, базирующихся на знании современных рекомендаций и текущих достижений клинической науки. От грамотности ее реализации может зависеть как качество, так и прогноз жизни наших с Вами пациентов.
Литература
1. Faris R.F., Flather M., Purcell H. et al. Diuretics for heart failure // Cochrane Dotabase Syst. Rev. – 2012. – V. 2. – CD003838.
2. Richardson A., Scriven A., Poole-Wilson P. et al. Double blind comparison of captopril alone against frusemide plus amiloride in mild heart failure // Lancet. – 1987. – V. 2. – P. 709-711.
3. Faris R., Purcell H., Henein M. et al. Current evidence supporting the role diuretics in heart failure: a meta analysis of randomised controlled trials // Int. J. Cardiol. – V. 82. – P. 149-158.
4. Ponikowski P., Voors A.A., Anker S.D. et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure – Wed Addenda // Europ. Heart J. doi:10.1093/eurheartj/ehw128.
5. Беленков Ю.Н., Мареев В.Ю., Агеев Ф.Т. Хроническая сердечная недостаточность. Избранные лекции по кардиологии. Москва, 2006, 432 с.
6. Boerrigter G., Costello-Boerrigter L., Burnett J.C. Alterations of renal function in heart failure // In. Heart Failure. Second Edition: Ed.D.L.Mann.Elsvier, 2011. – P. 291-299.
7. Воронков Л.Г., Дудник А.В., Ляшенко А.В. та ін. Клініко-фармакодинамічні ефекти внутрішньовенної діуретичної терапії торасемідом та фуросемідом у пацієнтів з декомпенсованою ХСН // Серцева недостатність. – 2015. – № 1. – C. 25-27.
8. Opie L.H., Kaplan N.M. Diuretics. In.: Drugs for the Heart. Eds: L.Opie, J. Gersh.-Saunders, 2009, p. 88-111.
9. Gottlieb S. Management of volume overload in heart failure / In.: Heart Failure. Second Edition: Ed.D.L.Mann.Elsvier, 2011. – P. 650-658.
10. Арутюнов Г.П., Оганезова Л.Г., Драгунов Д.О. Взаимосвязь периода полувыведения петлевого дируетика, выраженности натрийуреза и показателей центральной гемодинамики у больных ХСН (пилотное исследование) // Сердечная недостаточность. – 2013. – № 2. – С. 1-7.
11. Yancy C.W., Jessup M., Bozkurt B. et al. 2013 ACCF/AHA Guideline for the Management of Heart failure // Circulation. – 2013. – V. 128. – e240-e327. DOI:10.116.1161/CIR.0b013e31829e8776.
12. Basoor A., Doshi N.S., Cotant J.F. et al. Decreased readmissions and improved quality of care with the use of an inexpensive checklist in heart failure // Congest. Heart failure. – 2013. – V. 19. – P. 200-206.
13. Воронков Л.Г., Ильницкая М.Р. Диуретики при хронической сердечной недостаточности. – К., 2011. – 95 с.
14. Lien C.T., Gillespie N.D., Struthers A. Et al. Heart failure infrail eiderly patients : diagnostic difficulties, co-morbidites, polypharmacy and treatment dilemmas // Eur. J. Heart Failure. – 2002. – V. 38. – P. 806-813.
15. Агеев Ф.Т., Арутюнов Г.П., Беленков Ю.Н. и др. Назначение мочегонных препаратов при синдроме задержания жидкости // Сердечная недостаточность. – 2013. – Т. 14. – № 5. – С. 293-296.
16. Арутюнов Г.П., Оганезова Л.Г. Новые параметры в оценке эффективности мочегонной терапии у больных с ХСН // Росс. мед. журнал. – 2012. – № 4. – С. 144-146.
17. Арутюнов Г.П., Оганезова Л.Т. Тубулоинтерстициальный аппарат почки и его поражениe при артериальной гипертензии // Клин. нефрология. – 2011. – № 1. – С. 52-57.
18. Roson M.J., Cavallero S. Acute sodium overload producec renal tubuloitnerstitial inflammation in normal rats // Kidney Int., 2006, v. 70, p. 1439-1447.
19. Elzinga L.W., Rosen S. Dissociation of glomerular filtration rate from tubolointerstitial fibrosis in experimental chronic nephropathy: role of sodium intake // J. Amer. Sci. Nephrol. – 1993. – V. 4(2). – P. 214-221.
20. Амосова К.М. Петлевые диуретики в лечении хронической сердечной недостаточности: новые возможности // Серце і судини. – 2005. – № 4. – C. 8-14.
21. Арутюнов Г.П., Драгунов Д.О., Соколова А.В. Оценка влияния петлевых диуретиков с разными периодами полувыведения на ретенцию натрия // Клиническая нефрология. – 2013. – № 5. – C. 43-44.
22. Bates J., Raffi H., Prasadan K. et al. Tamm-Horsfall protein knockout mice are more prone to urinary tract infection : rapid communication // Kidney Int. – 2004. – V. 65. – P. 791-797.
23. Mutig K., Kahl T., Saritas T. Activаtion of the bumetanide-sensitive Na+, K+, 2Cl-Cotransporter (NKCC2) is facilitated by Tamm-Horsfall protein in a chloride-sensitive manner // J. Biological Chemistry. – 2011. – V. 286(34): 30200-30210.
24. Gropper S., Rojas M.J., Guglietta A. et al. Single and repeated-dose, randomized,, cross-over, biovailability clinical trial of torasemide immediate release compared to a new prolonged release formulation of torasemide (abstract).
25. Rogers A., Addington-Hall J.M., McCoy ASM, Edmonds P.M. et al. A qualitative study of chronic heart failure patients understanding of their symptoms and drug therapy // European J. heart Failure. – 2002. – № 4. – P. 283-7.
26. Gropper S., Albet C., Guglietta A. et al. Single-dose, randomized, cross-over, biovailability clinical trial of torasemide immediate release compared to new prolonged release formulation of torasemide (abstract) // Basic. Clin. Pharmacol. Toxicol. – 2006. – V. 99 (Suppl.1). – P. 48
27. Barbanoj M.J., Ballester M.R. et al. A bioavailability/bioequivalence and pharmacokinetic study of two oral doses of torasemide (5 and 10 mg): prolonged-release versus the conventional formulation // Clin. Exp. Pharmacol. Physiol. – 2009. – V. 36 (5-6). – P. 469-477.
28. Науковий комітет дослідження КОМФОРТ-СН Воронков Л.Г. (співголова), Багрій А.Е. (співголова), Коваль О.А., Тащук В.К., Целуйко В.Й. – від імені колективу дослідників. Українська Асоціація фахівців із серцевої недостатності. Обґрунтування, протокол та результати українського мультицентрового дослідження КОМФОРТ-СН (Кооперативне випробування звичайної та з Модифікованим вивільненням ФОРм Торасеміду при хронічній Серцевій Недостатності) // Серцева недостатність. – 2014. – № 1. – 15 с.
29. Berry C., McMurrаy J. A review of quality-of-life evaluations in patients with congestive heart failure // Pharmacoeconomiсs. – 1999. – Vol. 16. – P. 247-71.
30. Muller K., Camba G., Jaquet F. еt al. Torasemide vs. Furosemide in primary care patients with chronic heart failure NYHA II to IV – efficacy and quality of life // European J. Heart Failure. – 2003. – № 5. – P. 793-801.
UA/XMP/0816/0174