25 вересня, 2016
Европейский спиронолактон делает доступнее прогноз-модифицирующую терапию для украинских пациентов c ХСН
Спиронолактон – хорошо знакомый многим клиницистам калийсберегающий диуретик, по новой классификации относящийся к антагонистам минералокортикоидных рецепторов (АМР), с патогенетически обоснованными механизмами действия и доказанным положительным влиянием на клинический прогноз при хронической сердечной недостаточности (ХСН). Несмотря на рекомендацию I класса от Европейского общества кардиологов (ЕОК), в клинической практике препараты класса АМР используются недостаточно. Пробел между реальным применением АМР и количеством пациентов, которые могли бы получить пользу от их назначения, указывает на нераскрытый потенциал снижения смертности, частоты повторных госпитализаций и сокращения расходов на лечение ХСН. Заполнить этот пробел в нашей стране могут качественные генерики спиронолактона.
Спиронолактон был синтезирован в 1957 г. как молекула со свойствами конкурентного антагониста эффектов альдостерона в почечных канальцах. С 1960-х годов препарат применялся в качестве вспомогательного калийсберегающего диуретика для лечения отечного синдрома у пациентов с ХСН. В 1980-х годах интерес к нему несколько снизился в связи с синтезом и внедрением в практику ингибиторов ангиотензинпревращающего фермента (ИАПФ), у которых также был открыт эффект блокады альдостерона (Ю.Ф. Осмоловская и соавт., 2013). И только в 1999 г. в исследовании RALES было установлено положительное влияние спиронолактона на выживаемость пациентов с тяжелой систолической ХСН.
В этом исследовании добавление спиронолактона в низких, недиуретических дозах (12,5-50 мг/сут) к стандартной на тот момент терапии (дигоксин, диуретики и ингибиторы АПФ) приводило к достоверному снижению смертности от всех причин на 30% и частоты госпитализаций – на 35% за 2 года наблюдения. Указанные результаты послужили поводом для досрочного завершения исследования. Общая смертность снижалась за счет уменьшения частоты как смерти от прогрессирования ХСН, так и внезапной кардиальной смерти (B. Pitt et al., 1999). Исследование RALES стало поворотным пунктом в формировании современных взглядов на место АМР в лечении ХСН.
В настоящее время известно, что прогноз-модифицирующее действие спиронолактона обусловлено не диуретическим и калийсберегающим эффектами, а блокадой неблагоприятных биологических эффектов альдостерона путем конкурентного связывания с минералокортикоидными рецепторами. Воздействуя на эти рецепторы, обнаруженные в сосудах, сердце, почках и других органах, альдостерон вызывает повышение артериального давления, увеличивает реабсорбцию натрия, задержку жидкости и снижает уровень калия (Ю.Ф. Осмоловская и соавт., 2013). Альдостерон рассматривается как один из важнейших нейрогуморальных факторов, запускающих процессы фиброза и ремоделирования миокарда, а также вызывает изменения реполяризации и функции ионных каналов мембраны кардиомиоцитов, приводящие к возникновению опасных для жизни сердечных аритмий (B. Greenberg et al., 2006; B. Pitt et al., 2014).
К доказанным полезным эффектам блокады альдостерона относятся замедление формирования фиброза миокарда, подавление ренин-ангиотензиновой и симпатоадреналовой систем, нормализация функции эндотелия, угнетение системного воспаления. Эти эффекты трансформируются в улучшение клинического прогноза пациентов с ХСН, связанное со снижением риска фатальных аритмий, замедлением процессов ремоделирования сердца, блокадой системных механизмов прогрессирования СН, снижением риска развития тромбоза (А.Э. Багрий и соавт., 2010).
В условиях избыточного образования свободных радикалов, сопровождающего все сердечно-сосудистые заболевания, минералокортикоидные рецепторы становятся чувствительными также к кортизолу – гормону хронического стресса. Поэтому термин «антагонисты минералокортикоидных рецепторов» применяется чаще, чем «антагонисты альдостерона» (Л.Г. Воронков, 2016).
Согласно последним рекомендациям ЕОК по ведению пациентов с СН (обновлены в июле 2016 г.) АМР показаны в сочетании с бета-адреноблокатором и ИАПФ или с блокатором рецепторов ангиотензина ІІ (БРА) при непереносимости ИАПФ пациентам с клиническими проявлениями ХСН II-IV функциональных классов по NYHA и фракцией выброса левого желудочка (ФВ ЛЖ) ≤35% с целью облегчения симптомов, предотвращения эпизодов ухудшения СН, приводящих к повторным госпитализациям, и повышения выживаемости.
Рекомендуемая ЕОК стартовая доза АМР – 25 мг/сут, целевая – 50 мг/сут. Терапию спиронолактоном можно начинать в стационаре и продолжать длительно в амбулаторных условиях. Положительное влияние на прогноз сохраняется столько времени, сколько продолжается блокада неблагоприятных сердечно-сосудистых эффектов альдостерона.
Диуретические дозы спиронолактона выше, чем болезнь-модифицирующие. Некоторым пациентам может потребоваться доза ≥75-150 мг/сут для потенцирования эффекта петлевых диуретиков и преодоления терапевтической резистентности отечного синдрома. Калийсберегающий эффект спиронолактона также может быть полезным для профилактики гипокалиемии у пациентов, принимающих дигоксин.
Учитывая и без того сложные схемы лечения ХСН, которых предстоит придерживаться пациенту, ему следует объяснить пользу от назначения еще одного препарата для длительной терапии (увеличение продолжительности жизни, снижение частоты декомпенсаций ХСН, повторных госпитализаций, а значит, и суммарных расходов на лечение).
Несмотря на доказанное положительное влияние на прогноз, АМР все еще недостаточно используются в клинической практике. По данным первого национального срезового исследования UNIVERS (Л.Г. Воронков и соавт., 2012), среди почти 3 тыс. амбулаторных пациентов с ХСН 28,8% принимали АМР, преимущественно спиронолактон. В подгруппе пациентов с систолической ХСН этот показатель составил 47,8%, а среди пациентов с ФВ ЛЖ ≤35% (то есть с жесткими показаниями к назначению АМР по рекомендациям ЕОК) АМР принимали чуть больше половины – 51,2% (рис.). Таким образом, каждый второй пациент не получал терапию, которая могла бы увеличить продолжительность жизни и сократить частоту госпитализаций по поводу обострения СН еще на 25-30% сверх того положительного эффекта, который обеспечивают ИАПФ и бета-адреноблокаторы.
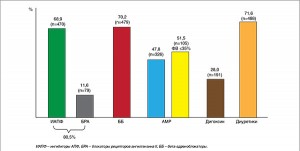 Рис. Структура терапии нейрогуморальными антагонистами, диуретиками, АМР и дигоксином у амбулаторных пациентов с ХСН с систолической дисфункцией в украинской популяции (n=682) по данным исследования UNIVERS
Рис. Структура терапии нейрогуморальными антагонистами, диуретиками, АМР и дигоксином у амбулаторных пациентов с ХСН с систолической дисфункцией в украинской популяции (n=682) по данным исследования UNIVERSЗарубежные эксперты склонны объяснять недостаточное применение АМР боязнью развития гиперкалиемии и ее фатальных осложнений в результате калийсберегающего действия эплеренона и спиронолактона (B. Pitt, 2014). Вместе с тем в исследовании RALES не было зафиксировано ни одного случая фатальной гиперкалиемии у пациентов, принимавших спиронолактон; в средней дозе (25 мг/сут) он редко, всего в 2% случаев, вызывал значимое повышение уровня калия. То же самое справедливо в отношении эплеренона, который продемонстрировал отличный профиль безопасности в крупных клинических исследованиях.
Хотя гиперкалиемия в повседневной практике встречается чаще, чем в контролируемых клинических исследованиях с жестким протоколом, меры безопасности, основанные на доступных методах лабораторного контроля, сводят риски к минимуму. Опасность развития гиперкалиемии при тщательном мониторинге функции почек и содержания электролитов в крови минимальна по сравнению с пользой, которую могут получить пациенты (B. Pitt, 2014).
Принципы отбора пациентов для назначения АМР и последующего наблюдения с выполнением повторных анализов для контроля уровня электролитов в крови и функции почек подробно изложены в соответствующем разделе рекомендаций ЕОК по медикаментозной терапии ХСН (2016). Анализы крови на креатинин, азот мочевины и электролиты являются общедоступными и не отнимают много времени. Следует отметить, что по рекомендациям ЕОК исходно повышенный уровень калия и сниженная функция почек не являются абсолютными противопоказаниями к назначению АМР. Если уровень калия составляет >5,5 ммоль/л или креатинина >221 мкмоль/л при скорости клубочковой фильтрации (СКФ) <30 мл/мин/1,73 м2, рекомендуется уменьшить дозу в 2Jраза и продолжать отслеживать электролитные и биохимические показатели. И только при гиперкалиемии >6,0 ммоль/л, уровне креатинина >310 мкмоль/л или СКФ <20 мл/мин/1,73 м2 рекомендуется отменить АМР, при этом следует иметь в виду возможность возобновления терапии после нормализации показателей.
Вероятно, в нашей стране недостаточное применение АМР в большей степени обусловлено высокой стоимостью терапии ХСН в целом. С момента публикации результатов исследования UNIVERS прошло больше трех лет, но с учетом сложившейся в Украине социально-экономической ситуации за последние три года структура назначений прогноз-модифицирующих препаратов вряд ли изменилась в лучшую сторону. Пробел между реальным применением АМР и количеством пациентов, которые могли бы получить пользу от их назначения, могут заполнить доступные генерики.
Несмотря на более чем 50-летнюю клиническую историю молекулы спиронолактона, выбор препаратов на отечественном фармацевтическом рынке очень ограничен. Оптимальным соотношением цены и качества выделяется генерик европейского производства Спиронолактон Сандоз. Препарат производится в таблетках по 50 и 100 мг спиронолактона, которые можно делить, получая дозировки с интервалом в 25 мг. Это позволяет соблюдать рекомендации ЕОК по назначению АМР в режиме прогноз-модифицирующей терапии низкими дозами (начальная доза – 25 мг, с повышением через 4-8 нед до 50 мг).

Как видно из таблицы, компания Сандоз предлагает наименьшую стоимость дозировки 50 мг среди трех представленных на рынке препаратов спиронолактона. Таблетку Спиронолактон Сандоз (100 мг) удобно делить пополам, таким образом, стоимость терапии дозой 50 мг составит менее 2 грн в сутки.
На основании вышеизложенного можно сделать вывод, что Спиронолактон Сандоз, обладающий оптимальным соотношением стоимости и качества, является самым доступным европейским препаратом класса АМР в Украине. Его применение в составе прогноз-модифицирующей терапии систолической ХСН (вместе с бета-адреноблокатором и ингибитором АПФ или БРА) отвечает современным рекомендациям ЕОК и помогает обеспечить дополнительную пользу для украинских пациентов.
Подготовил Дмитрий Молчанов
3-09-СПИ-РЕЦ-0916


