4 липня, 2016
Транскатетерна алкогольна септальна абляція – сучасна альтернатива у лікуванні пацієнтів з обструктивною формою гіпертрофічної кардіоміопатії
Гіпертрофічна кардіоміопатія (ГКМП) – генетично детерміноване первинне захворювання міокарда, яке характеризується асиметричною гіпертрофією міжшлуночкової перегородки (МШП) різної локалізації, збільшенням площі стулок мітрального клапана, порушенням проведення збудження, стадійністю перебігу з подальшим порушенням внутрішньосерцевої гемодинаміки і високим ризиком раптової смерті [1].
У педіатричних реєстрах відсутня інформація щодо частоти діагностування зазначеного захворювання серед дітей, але дані популяційних досліджень свідчать про захворюваність від 0,3 до 0,5% на 100 тис. населення на рік [4], в Україні – 0,47% [3]. Частота розвитку ГКМП серед хворих різних рас майже аналогічна [2, 4].
Вибір методу лікування
Вибір методу лікування при ГКМП утруднений внаслідок варіабельності клінічних і гемодинамічних проявів захворювання та його природного перебігу. Лікування включає терапевтичні, електрофізіологічні, хірургічні методи й ендоваскулярне лікування. До загальних рекомендацій належить обмеження фізичних навантажень, які стимулюють прогресування гіпертрофії та посилення обструкції вихідного тракту (ОВТ) лівого шлуночка (ЛШ) з формуванням градієнта систолічного тиску (ГСТ) і, відповідно, підвищують ризик раптової смерті. Усі пацієнти з ОВТ ЛШ мають уникати дегідратації та прийому значної кількості алкоголю, також має заохочуватися зниження маси тіла. Основу медикаментозної терапії становлять препарати з негативним інотропним ефектом (бета-блокатори й антагоністи кальцію групи фенілалкіламінів), антиаритмічні препарати III класу (з метою лікування порушень ритму та профілактики раптової аритмічної смерті). Препарати, які розширюють артерії та вени, в тому числі нітрати й інгібітори фосфодіестерази 5 типу, можуть збільшувати ОВТ ЛШ, і при можливості їх застосування необхідно уникати. У разі розвитку серцевої недостатності (СН) внаслідок зменшення порожнин серця, систолічної та діастолічної дисфункції ЛШ показане лікування СН за загальними принципами.
Інвазивне лікування з метою зниження ОВТ ЛШ потрібно розглядати у пацієнтів з градієнтом ОВТ ЛШ ≥50 мм рт. ст., із симптомами СН від помірно виражених до тяжких (III-IV функціональний клас [ФК] за NYHA) та/або повторними синкопальними станами, індукованими фізичним навантаженням, незважаючи на максимально переносиму медикаментозну терапію [4]. У деяких центрах інвазивне лікування також розглядається для пацієнтів із помірно вираженою симптоматикою (II ФК за NYHA), у яких максимальний або індукований градієнт ≥50% мм рт. ст. (під час навантаження чи проби Вальсальви) поєднується з опосередкованою систолічним рухом передньої стулки (SAM) мітральною регургітацією (МР)помірного/вираженого ступеня, фібриляцією передсердь або дилатацією лівого передсердя від середнього до тяжкого ступеня, проте даних на підтримку такої практики небагато [2, 4].
Хірургічне лікування донедавна вважали методом вибору у пацієнтів з обструктивною формою ГКМП, рефрактерною до медикаментозного лікування. Найчастішим оперативним втручанням для лікування ОВТ ЛШ є шлуночкова септальна міоектомія (процедура Морроу), під час якої формується прямокутне поглиблення, яке продовжується дистально за межі контакту між мітральною стулкою і перегородкою нижче аортального клапана. Це дає змогу усунути або істотно знизити ГСТ на вихідному тракті (ВТ) ЛШ у понад 90% випадків, зменшити SAM-опосередковану МР і покращити толерантність до фізичного навантаження. Тривалий симптоматичний ефект досягається у 70-80% пацієнтів, а результати щодо віддаленого виживання співставні з такими у загальній популяції. Проте розвиток інтервенційних технологій поступово змінює підходи до хірургічного лікування ГКМП, хоча проведення септальної міоектомії залишається золотим стандартом у випадках симультанних операцій (наприклад, у комбінації з аортокоронарним шунтуванням або протезуванням мітрального клапана). Летальність при хірургічному лікуванні обструктивних форм ГКМП становить 3-4% [2, 4].
Щодо послідовної двокамерної електрокардіостимуляції (ДЕКС) із вкороченою атріовентрикулярною (АВ) затримкою, то лише три невеликі, рандомізовані плацебо-контрольовані дослідження, присвячені зазначеному методу лікування, і декілька тривалих обсерваційних спостережень підтверджують зниження ГСТ на ВТ ЛШ і варіабельне поліпшення симптоматики та якості життя [2, 4]. У нещодавньому Кокранівському огляді стверджується, що дані про користь стимуляції базуються на фізіологічних вимірах і не містять результатів про клінічно-релевантні кінцеві точки [4]. Таким чином, постійну послідовну стимуляцію з коротким АВ-інтервалом можна рекомендувати пацієнтам зрілого віку з наявністю симптомів, які не підходять (або незгодні) для інших методів інвазивного зниження ГСТ, і пацієнтам, які мають інші показання до кардіостимуляції. Параметри стимуляції мають бути оптимізовані для досягнення максимального перезбудження правого шлуночка (ПШ) з мінімальним порушенням наповнення ЛШ (зазвичай досягається з АВ-інтервалом спокою 100±30 мс). Для того, щоб упевнитись у повному залученні шлуночків при навантаженнях, має бути доступне динамічно задане значення АВ-інтервалу, і програмована верхня межа має бути вищою, ніж найшвидший ритм, який досягається при фізичному навантаженні [4].
Як альтернативу хірургічним методам лікування при відповідній анатомії коронарних артерій можна застосовувати транскатетерну алкогольну септальну абляцію (АСА). Вперше зазначена процедура була проведена в 1989 р. Brugada і співавт. з метою лікування шлуночкової тахіаритмії [5]. При обструктивній формі ГКМП методику застосував лише в 1994 р. Sigwart [6]. АСА передбачає зниження обструкції шляхом зменшення товщини гіпертрофованої МШП у віддаленому періоді та зниження скоротливості цієї ділянки, модифікації скорочення ЛШ внаслідок етанол-індукованої оклюзії однієї або кількох септальних гілок – СГ (іноді в інші гілки передньої міжшлуночкової гілки [ПМШГ] лівої коронарної артерії [ЛКА]) і розвитку локального інфаркту міокарда. У зв’язку з варіабельністю септального кровообігу до проведення ін’єкції алкоголю необхідно виконати міокардіальну контрастну (МК) ехокардіографію (ЕхоКГ). Результативність ендоваскулярного лікування ОВТ ЛШ при ГКМП близька до такої при хірургічному лікуванні щодо зменшення ГСТ, поліпшення симптоматики і толерантності до фізичних навантажень. Основне нефатальне ускладнення – це АВ-блокада у 7-20% пацієнтів [2, 4], а смертність в результаті процедури співставна з такою при ізольованій міоектомії. В Україні перша процедура транскатетерної АСА з метою лікування ОВТ ЛШ у пацієнта з ГКМП була проведена у 2000 р. в ДУ «Національний інститут серцево-судинної хірургії ім. М.М. Амосова НАМН України» під керівництвом Ю.В. Панічкіна, проте більш широке використання ендоваскулярного лікування стало доцільним після аналізу результатів її застосування щодо користі/ризику провідними установами в усьому світі, які займаються лікуванням хворих з ГКМП, та поступового зростання ролі зазначеної процедури у світових рекомендаціях з лікування ГКМП [2, 4, 7, 8], адаптації та вдосконалення методики виконання АСА практично через десятиліття з моменту її впровадження у практику.
Мета роботи – аналіз результатів транскатетерної АСА у хворих з обструктивною формою ГКМП.
Матеріали та методи
З 01.01.2009 р. по 01.05.2016 р. виконано 132 процедури транскатетерних АСА у 123 пацієнтів у ДУ«Національний інститут серцево-судинної хірургії ім. М.М. Амосова НАМН України»; серед них 75 (57%) чоловіків і 57 (43%) жінок. Середній вік пацієнтів становив 44 роки. Середнє значення пікового ГСТ на ВТ ЛШ – 91,7±8,3 мм рт. ст., реєструвалась помірна та виражена SAM-асоційована МР. У 3 пацієнтів визначено піковий ГСТ <50 мм рт. ст. у стані спокою, проте наявні виражена SAM-асоційована МР і синкопальні стани в анамнезі. Середня товщина МШП – 2,4 см [1, 3, 6].
Діагноз і визначення морфологічних особливостей захворювання базувались на даних двомірної ЕхоКГ, коронаровентрикулографії (КВГ), МК ЕхоКГ, у разі необхідності – трансезофагеальної ЕхоКГ, магнітно-резонансної томографії (МРТ), та даних, отриманих безпосередньо під час виконання транскатетерної АСА. Оцінка біохімічного дослідження крові здійснювалася до процедури, через 1, 3 та 7 діб після її проведення. ЕхоКГ виконували на цифровому ультразвуковому діагностичному (УЗД) апараті Aplio SSА-700А (Toshiba) секторальним датчиком зі змінною частотою випромінювання 2,0-5,0 МГц, за стандартною методикою в положенні хворого лежачи на спині з індивідуальним позиціонуванням датчика для найякіснішої локалізації внутрішньосерцевих структур. Під час проведення двомірної ЕхоКГ оцінювали локалізацію, поширеність та ступінь гіпертрофії стінок ЛШ. Рівень обструкції в ЛШ визначали при кольоровому допплерівському контрастуванні за місцем виникнення високошвидкісного мозаїчного потоку. Ступінь обструкції визначали за ГСТ, розрахованим за допомогою методу безперервно-хвильової допплер-ЕхоКГ за максимальною швидкістю потоку з п’ятикамерної апікальної позиції. В умовах операційної під час коронарографії проводили ЕхоКГ на УЗД-апараті ACUSON Cypress (Siemens).
Процедура АСА виконувалась на ангіографічних установках COROSKOP та AXIOM ARTIS (Siemens), AXIOM ARTIS BIPLANE (Siemens) зі швидкістю реєстрації кадрів зображення 12,5-25 кадрів на секунду під комбінованою анестезією. З метою профілактики тромбоемболічних ускладнень пацієнтам проводилась гепаринізація з розрахунку 80-100 ОД/кг маси тіла під контролем активованого часткового тромбопластинового часу. На випадок розвитку повної АВ-блокади перед проведенням АСА трансюгулярним (чи трансфеморальним) доступом у верхівку ПШ імплантували та налаштовували в режим «за потребою» тимчасовий штучний водій ритму серця (ШВРС). ЕхоКГ-моніторинг ГСТ на ВТ ЛШ та ступеня МР здійснювали під час виконання, після процедури та через 1 добу.
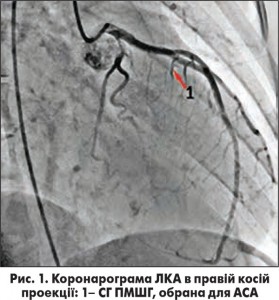
Після проведення КВГ, встановлення показань та уточнення анатомічних даних щодо можливості виконання АСА, ангіографічного визначення СГ (рис. 1), яка забезпечує кровопостачання гіпертрофованої ділянки ЛШ, в зазначену гілку вводився коронарний провідник, 0,014-дюймовий і двопросвітний балонний катетер (БК). Техніка виконання процедури передбачала проведення МК ЕхоКГ в апікальній чотири- або п’ятикамерній позиції з метою визначення зони перфузії цільової СГ перед введенням спирту через один із каналів інфльованого (відповідним до діаметра СГ тиском) двопросвітного БК. Це було необхідним для визначення артерії, що забезпечує кровопостачання зони міокарда, яка, власне, і створювала ОВТ ЛШ і, відповідно, ГСТ, а також для перевірки, чи прилягає контрастований міокард до ділянки максимального наростання швидкості виносного потоку. Крім цього, МК ЕхоКГ дає змогу окреслити можливу зону інфаркту, пересвідчитись у відсутності ретроградного потоку крові та виявити можливе залучення до процесу папілярних м’язів, вільної стінки ЛШ [5, 7], дозволяє встановити протипоказання до виконання процедури – контрастування правої частини МШП, оскільки в зазначеному випадку є можливим розвиток небезпечних для життя порушень ритму серця [5, 7].
З метою контрастування міокарда під час проведення МК ЕхоКГ у цільову СГ через один з каналів інфльованого двопросвітного БК перед введенням 96% етилового спирту вводили 1-2 мл ехоконтрастної речовини. Безпосередньо у момент введення препарату спостерігався виражений ефект візуалізації міокарда у вигляді яскравого ехопозитивного контрастування фрагмента МШП.
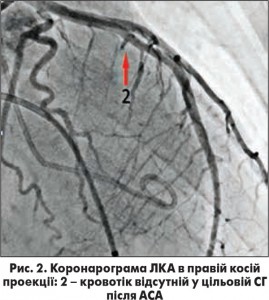
Після виконання вищезгаданої МК ЕхоКГ та за умови відсутності протипоказань до процедури вводився 96% етиловий спирт у дозі 1-3 мл з ЕхоКГ-контролем після введення кожного мілілітра. Через 10 хв після введення спирту видалявся дефльований БК і коронарний провідник, виконувалися контрольні коронарографії (рис. 2), оцінка безпосередніх результатів процедури. ЕхоКГ, електрокардіографічний контроль здійснювався щодня до виписки пацієнта.
Результати
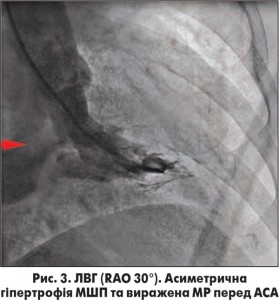
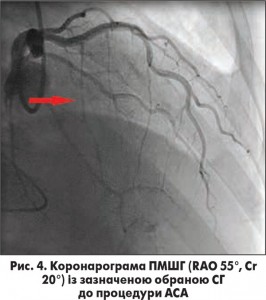
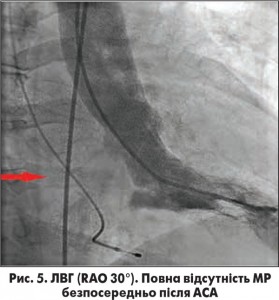
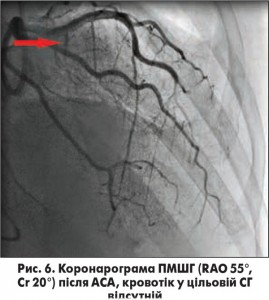
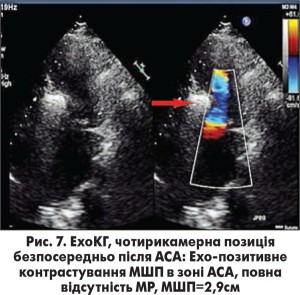
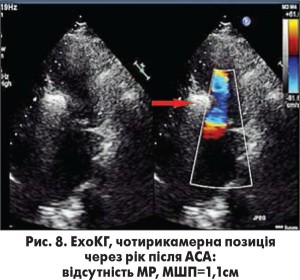
Середнє значення піковогоГСТ на ВТ ЛШ в результаті АСА знизилось з 91,7±8,3 мм рт. ст. до 34,3±4,6 мм рт. ст., ступінь МР зменшився переважно від помірного до незначного чи тривіального. У 3 випадках було зафіксовано повне зникнення МР після АСА. На рисунках 3 та 4 зображено ліву вентрикулографію (ЛВГ) та коронарограму ЛКА в правій косій проекції із зазначеною обраною для АСА СГ у пацієнтки з ОВТ ЛШ при ГКМП та вираженою SAM-асоційованою МР. На рисунках 5 і 6 зображено ЛВГ і ЛКА після процедури, де зареєстровано повну відсутність МР та кровотоку по цільовій СГ. При ЕхоКГ також зафіксовано відсутність МР безпосередньо після транскатетерної АСА (рис. 7), а також виявлено стоншення МШП з 2,9 до 1,1 см та відсутність МР через рік після процедури.
Середній термін спостереження за 123 (100%) пацієнтами становив 52±3,7 міс. Під час 107 (81%) процедур зареєстровано зменшення ОВТ ЛШ та ступеня МР, зниження ГСТ (≤30 мм рт.ст.), що розглядалося як позитивний результат процедури. Безпосередньо після АСА позитивний результат отримано при 124 (94%) процедурах. Зареєстровано 1 (0,76%) летальний випадок у ранньому післяопераційному періоді внаслідок комбінації оклюзії ПМШГ та кровотечі з поперечного розриву підключичної артерії, травмованої, очевидно, при імплантації тимчасового ШВРС, а також геморагічного шоку. У 9 (6,8%) випадках АСА виконувалася повторно в термін від 6 міс до 3 років у зв’язку із залишковим ГСТ ≥50 мм рт. ст., у 7 (78%) з них вдалося досягти вищезазначених критеріїв позитивного результату. Двом (1,5%) пацієнтам проведено хірургічне втручання у зв’язку з неефективністю ендоваскулярного лікування. Варто зазначити, що 6 (4,5%) процедур АСА здійснювали після попереднього лікування ОВТ ЛШ за допомогою методу ДЕКС, 4(3%) – після попереднього хірургічного лікування в умовах штучного кровообігу.
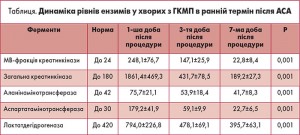
Під час аналізу біохімічних досліджень крові реєстрували підвищення рівня МВ-фракції креатинкінази, загальної креатинкінази, лактатдегідрогенази, аланінамінотрансферази, аспартатамінотрансферази через 1 добу та подальший спад рівнів досліджуваних ензимів на 3-й день з наступною нормалізацією до 7-ї доби (табл.).
В одному випадку спостерігався рефлюкс спирту до ПМШГ з подальшою аспірацією та відсутністю великих кардіальних подій. Серед інших нефатальних ускладнень після 9 (6,8%) АСА виникла необхідність в імплантації постійного ШВРС з приводу повної АВ-блокади. Крім того, нами зареєстровано 1 випадок фібриляції шлуночків на 10-й день після процедури з успішною серцево-легеневою реанімацією. Спостерігався 1 (0,76%) випадок раптової смерті через 6 міс після процедури. Після 25 (19%) процедур у віддаленому періоді визначено залишковий ГСТ >30 мм рт. ст., але зафіксовано значне поліпшення симптоматики.
Середня товщина стінки МШП зменшилася з 2,6±0,4 до 1,9±0,1 см. Ступінь МР знизився від переважно помірного до незначного або повного зникнення. ФК за NYHA зменшився в цілому з 2,9 до 1,1, під час збору анамнезу в переважної більшості пацієнтів виявлено підвищення толерантності до фізичних навантажень, клінічне покращення загального стану.
Висновки
1. Транскатетерна АСА є ефективним та безпечним методом лікування обструктивної форми ГКМП зі стабільними результатами у віддаленому періоді при правильному відборі пацієнтів.
2. Транскатетерну АСА можна застосовувати і як незалежний метод та альтернативу хірургічному лікуванню, і в етапному лікуванні хворих з ГКМП.
3. Скорочення тривалості процедури, зменшення кількості ускладнень і загальне поліпшення результатів ендоваскулярного лікування обструктивної форми ГКМП можливі з накопиченням досвіду центром та лікарем-ендоваскулярним хірургом.
Література
1. Knyshov G., Lazoryshynets V., Rudenko K., Kravchuk B., Beshlyaga V., Zalevsky V. et al. Is surgery the gold standard in the treatment of obstructive hypertrophic cardiomyopathy? Interact Cardio Vasc Thorac Surg 2013; 16: 5-10.
2. Gersh B.J., Maron B.J., Bonow R.O., Dearani J.A., Fifer M.A., Link M.S. et al. 2011 ACCF/AHA Guideline for the Diagnosis and Treatment of Hypertrophic Cardiomyopathy: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2011; 58: e212-60 [PubMed].
3. Тодуров Б.М. Эндоваскулярное лечение гипертрофической обструктивной кардиомиопатии / Б.М. Тодуров, А.В. Хохлов, С.Н. Фуркало, А.А. Максаков, Сохраб Хоррам, М.В. Шиманко, А.Н. Грицай, И.Н. Кузьмич, В.Ю. Кундин, Г.И. Ковтун // Кардіохірургія та інтервенційна кардіологія. – 2012. – № 1. – С. 29-33 [Електронний ресурс]. – Режим доступу: http://nbuv.gov.ua/UJRN/karx_2012_1_5.
4. Elliott P.M., Anastasakis A., Borger M.A., Borggrefe M. et al. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy European Heart Journal (2014), 35, 2733-2779, doi:10.1093/eurheartj/ehu284, Online publish-ahead-of-print 29 August 2014.
5. Brugada P., de Swart H., Smeets J.L. et al. Transcoronary chemical ablation of ventricular tachycardia. Circulation 1989; 79:475-82.
6. Sigwart U. Non-surgical myocardial reduction for hypertrophic obstructive cardiomyopathy // Lancet. – 1995. – Vol. 346. – P. 211-214.
7. Barry J. Maron, William J. Mckennaet al. 2003. American College of Cardiology / European Society of Cardiology Clinical Expert Consensus Document on Hypertrophic Cardiomyopathy Journal of the AmericanCollege of Cardiology. Vol. 42, No. 9, 2003.
8. Transcatheter Alcohol Septal Ablation in Patient with Hypertrophic Obstructive Cardiomyopathy: the Immediate and Long-Term Results / S.M. Fanta, V.V. Lazoryshynets, K. Rudenko et al. // Journal of the American College of Cardiology. – 2015 [Електронний ресурс]. – Режим доступу: J Am Coll Cardiol. 2015; 66(15_S): doi:10.1016/j.jacc.2015.08.1080.