30 червня, 2016
Целевой уровень артериального давления и антигипертензивная терапия пациентов с сахарным диабетом
По материалам научно-практической конференции «Современный профиль кардиометаболического риска в Украине: от диагностики до лечения» (6 апреля, г. Днепропетровск)
Сочетание артериальной гипертензии (АГ) и сахарного диабета (СД) – достаточно распространенная во всем мире проблема.
Также известно, что СД и АГ независимо друг от друга приводят к поражению органов-мишеней, а при их сочетании значительно чаще развиваются осложнения. В результате у больных с АГ и диабетом в 3 раза выше риск развития ишемической болезни сердца (ИБС) и в 2 раза выше риск возникновения других сердечно-сосудистых (СС) осложнений (инфаркта миокарда, инсульта, сердечной недостаточности) по сравнению с больными СД без АГ.
 СД и АГ признаны наиболее частыми причинами развития нефропатии и хронической почечной недостаточности.
СД и АГ признаны наиболее частыми причинами развития нефропатии и хронической почечной недостаточности.
Особенности ведения пациентов с СД и АГ рассмотрела в своем докладе доктор медицинских наук, профессор Анна Дмитриевна Радченко (отдел симптоматических артериальных гипертензий, ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины).
– Частота встречаемости АГ у пациентов с СД колеблется от 71 до 93% в зависимости от наличия и степени поражения почек (L. Tarnow et al., 1994). Пациенты с СД являются значительно более чувствительными к повышению АД, чем пациенты без СД, – уже начиная с величины систолического АД (САД) 120 мм рт. ст. и выше резко возрастает кардиоваскулярная смертность у пациентов с СД, тогда как при отсутствии СД этот риск увеличивается при уровне САД ≥140 мм рт. ст. (J. Stamler et al., 1993).
В настоящее время эффективный контроль АД рассматривается как одно из главных условий снижения риска возникновения СС-осложнений, которые занимают ведущее место в структуре причин смерти пациентов с СД. Так, в работе C.A. Emdin и соавт. (2015) показано, что снижение САД всего на 10 мм рт. ст. обеспечивает снижение риска развития СС-заболеваний на 11%, смерти – на 13%, инсульта – на 27%, альбуминурии – на 17%. Более того, еще в 1998 г. авторы крупного исследования (UKPDS Group) сделали вывод, что более жесткий контроль АД имеет большее значение для улучшения прогноза пациентов с СД, чем более жесткий контроль гликемии.
В дальнейших клинических рандомизированных исследованиях (ACCORD, ADVANCE), ретроспективных анализах (исследование INVEST), метаанализах (R. Gianpaoloa et al., 2011; K. McBrien et al., 2012) были сделаны попытки определить целевой уровень АД для пациентов с СД. Оказалось, что в настоящее время нет клинических доказательств, свидетельствующих о том, что снижение САД <130 мм рт. ст. с помощью антигипертензивной терапии ассоциируется со значительным снижением риска СС-осложнений. И единственным преимуществом более активного снижения АД стало уменьшение относительного риска развития инсульта на 30%, но при этом снижение абсолютного риска составило всего 1%. Эти данные отличаются от таковых, полученных в популяции пациентов с АГ без СД, – в недавнем исследовании SPRINT (2015) было продемонстрировано значительное уменьшение частоты развития фатальных и нефатальных СС-событий, а также смерти от любых причин при снижении САД <120 мм рт. ст. по сравнению со снижением САД <140 мм рт. ст.

Поэтому на сегодня рекомендовано всем пациентам с СД и АГ снижать АД до уровня <140/90 мм рт. ст. (в европейских рекомендациях ESC/ESH 2013 г. указывается уровень <140/85 мм рт. ст.). Возможно достижение более низкого уровня САД <130 мм рт. ст. и диастолического АД <80 мм рт. ст. у молодых пациентов, которые хорошо его переносят и при условии, что оно может быть достигнуто без чрезмерного усиления терапии (т.е. назначения большого количества антигипертензивных препаратов).
Согласно рекомендациям Американской диабетической ассоциации 2014-2016 гг. всем пациентам с СД и уровнем АД ≥120/80 мм рт. ст. уже следует рекомендовать мероприятия по модификации образа жизни и пищевых привычек:
• физические нагрузки (≥30 мин/сут);
• ограничение потребления соли до <1,5 г/сут;
• ограничение потребления алкоголя;
• снижение веса.
При уровне АД >140/90 мм рт. ст. эти мероприятия обязательно должны сочетаться с антигипертензивной терапией:
• основой антигипертензивной терапии должны быть блокаторы ренин-ангиотензиновой системы (РАС) – ингибиторы ангиотензинпревращающего фермента (ИАПФ) или блокаторы рецепторов ангиотензина ІІ (БРА);
• в большинстве случаев для контроля АД требуется назначение двух и более препаратов;
• рекомендовано назначение одного или более антигипертензивного препарата в вечернее время;
• при назначении ИАПФ, сартанов или диуретиков необходимо контролировать скорость клубочковой фильтрации (СКФ) и уровень калия в крови;
• для беременных с СД и хронической АГ целевой уровень АД составляет 110-129/65-79 мм рт. ст. для обеспечения здоровья матери и минимизации повреждения плода. Блокаторы РАС противопоказаны беременным.
Блокаторы РАС рекомендованы в качестве препаратов выбора при лечении АГ у пациентов с СД в связи с наличием широкой доказательной базы, свидетельствующей о благоприятных эффектах лекарственных средств этой группы для данной категории больных. Так, в Консенсусе Американской ассоциации клинических эндокринологов (2006) указывается, что ИАПФ и БРА положительно влияют на функцию почек и могут улучшать чувствительность к инсулину, благодаря чему они являются препаратами первого выбора у пациентов с СД и АГ. Такой же вывод можно сделать, если проанализировать международные рекомендации по антигипертензивной терапии у пациентов с диабетической и недиабетической нефропатией, особенно это касается больных с признаками почечной недостаточности.
Прямые сравнительные исследования эффективности ИАПФ и БРА в отношении влияния на частоту СС-осложнений у пациентов с СД и АГ не проводились. Данные же ряда метаанализов свидетельствуют об отсутствии существенных различий по влиянию на прогноз у пациентов с АГ. Так, в одном из последних метаанализов 2016 г. показано, что влияние ИАПФ и БРА на частоту развития СС-осложнений у пациентов без сердечной недостаточности существенно не отличается (рис. 1).
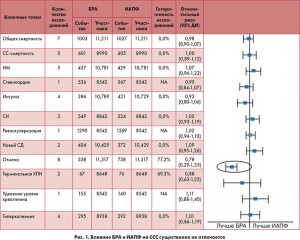
В большинстве рекомендаций нет четких указаний, кому следует назначать ИАПФ, а кому – БРА. Есть лишь указания в рекомендациях National Kidney Foundation KDOQI Diabetes and CKD: 2012 о том, что «у пациентов с макроальбуминурией и умеренно сниженной СКФ существуют строгие доказательства, что ИАПФ предпочтительны при СД 1 типа, БРА – при СД 2 типа». В рекомендациях Американской диабетической ассоциации 2016 г. отмечено, что при наличии почечной дисфункции и проблем с уровнем калия предпочтение может быть отдано БРА, так как они в меньшей степени влияют на этот показатель.
В большом ретроспективном бразильском исследовании продемонстрировано, что при СД БРА обеспечивают лучший показатель выживаемости без поражения почек по сравнению с ИАПФ (рис. 2)
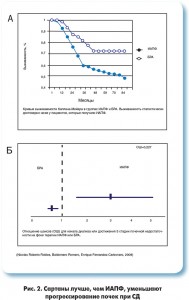
Таким образом, БРА существенно не отличаются от ИАПФ по влиянию на прогноз, могут оказывать более выраженное благоприятное влияние на почки и, кроме того, им свойственен лучший профиль переносимости среди антигипертензивных препаратов. Принимая решение о назначении БРА для контроля АД у больного СД, следует обратить внимание на представителя последнего поколения группы сартанов – азилсартан (в Украине зарегистрирован под торговым названием Эдарби), многообещающий и перспективный препарат для лечения пациентов с АГ при СД.
Азилсартана медоксомил является пролекарством и после приема внутрь быстро гидролизуется до активного вещества в желудочно-кишечном тракте. Биодоступность составляет 60%, а максимальная концентрация в крови достигается на протяжении 1,5-3 ч. Период полувыведения – 11 ч.
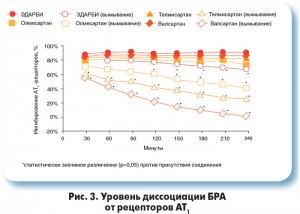
Азилсартан обладает мощным и длительным (24 ч) антигипертензивным эффектом и обеспечивает лучший суточный профиль АД по сравнению с другими антигипертензивными препаратами, такими как рамиприл, валсартан, олмесартан (G. Bonner, 2013; W.B. White, 2011). Эта важная особенность объясняется тем, что молекула азилсартана медоксомила обеспечивает наиболее стойкую связь с АТ1-рецепторами и наиболее медленную диссоциацию комплекса блокатор/АТ1-рецептор, (М. Ojima et al., 2011) (рис. 3). На сегодня известно, что от степени связывания БРА с АТ1-рецепторами зависит выраженность их антигипертензивного эффекта, именно поэтому препараты данной группы различаются между собой по антигипертензивной эффективности (M.J. Fabia et al., 2007; Eimfeldt et al., 2012).
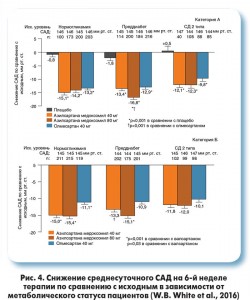
В 2016 году были опубликованы новые данные в отношении эффективности азилсартана. В прямом сравнительном исследовании у пациентов с АГ и СД 2 типа получены результаты, свидетельствующие о преимуществах азилсартана перед валсартаном и олмесартаном в снижении АД. По данным повторных полуавтоматических измерений АД в условиях клиники, азилсартана медоксомил в дозе 80 мг достоверно превзошел олмесартан в снижении САД в подгруппе пациентов с преддиабетом. В подгруппе пациентов с СД 2 типа азилсартана медоксомил в дозе 40 мг снижал САД более значимо по сравнению с олмесартаном. В подгруппах пациентов без метаболических нарушений и пациентов с СД 2 типа азилсартана медоксомил при использовании в дозах 40 и 80 мг продемонстрировал достоверное превосходство над валсартаном в снижении офисного САД. В подгруппе преддиабета отмечены преимущества азилсартана при применении в дозе 80 мг. В этой же работе было установлено положительное влияние терапии азилсартаном на показатели гликемии натощак и уровень секреции инсулина, как у нормогликемических пациентов, так и в подгруппе больных СД 2 типа (рис. 4).
Азилсартан относится к мультифункциональным БРА, являясь частичным агонистом ядерных рецепторов PPAR, которые регулируют метаболизм липидов и углеводов, и антагонистом рецепторов АТR1. Антагонизм к рецепторам ATR1 – один из механизмов повышения чувствительности тканей к инсулину. Установлено также, что азилсартан увеличивает потребление глюкозы инсулинчувствительными тканями у больных с СД. Эти преимущества дают основания для выбора азилсартана для пациентов с АГ и СД.
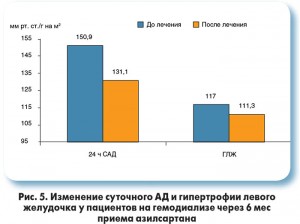
Одним из ведущих осложнений у больных с СД является возникновение и прогрессирование хронической почечной недостаточности. Поэтому в развитых странах основную массу пациентов которым необходимо проведение гемодиализа, составляют именно больные с СД. В связи с этим важными представляются результаты исследования Takanori Kusuyama и соавт. (2014) по изучению антигипертензивной эффективности азилсартана у пациентов на гемодиализе (45% участников исследования имели СД). Больные, которые принимали любой БРА на протяжении последних 6 мес, были переведены на прием азилсартана с периодом наблюдения 6 мес. В работе продемонстрировано, что азилсартан более эффективен в снижении АД по сравнению с другими БРА у пациентов, находящихся на гемодиализе (рис. 5).
Недавно опубликованы экспериментальные данные, свидетельствующие о наличии у азилсартана еще одного уникального эффекта – способности улучшать солевую чувствительность. Известно, что центральные механизмы регуляции обмена Na реализуются в почках, а нарушения этих механизмов приводят к компенсаторным сдвигам экскреции Na с мочой, нарушению водно-солевого баланса и, как следствие, – повышению АД, которое служит компенсаторным механизмом, обеспечивающим надлежащую экскрецию Na. Таким образом, АГ может развиваться в результате неспособности почек выделять адекватное количество Na при нормальном уровне системного давления. Солевая чувствительность зависит от соотношения уровня клубочковой фильтрации и канальцевой реабсорбции Na. Чем меньше СКФ и больше реабсорбция Na, тем выше солевая чувствительность. В экспериментальном исследовании азилсартан не только более выраженно по сравнению с кандесартаном снижал АД, но и улучшал солевую чувствительность (увеличивал экскрецию Na) у животных с субтотальной нефрэктомией, что, по мнению авторов исследования, может означать появление в будущем новых терапевтических опций для этого препарата (Masaki Hatanaka et al., 2016).
В настоящее время активно проводятся исследования молекулы азилсартана как в эксперименте, так и в клинике. Описаны церебро- и ангиопротекторные механизмы эффективности азилсартана при СД (Mohammed Abdelsaid et al., 2014; Sachiko Matsumoto et al., 2014). По данным сайта ClinicalTrials.gov, на сегодня выполняются 5 различных клинических исследований по изучению азилсартана у пациентов с СД.
Данные, которые накоплены в отношении особенностей течения АГ у пациентов с СД, а также результаты изучения эффектов азилсартана (Эдарби), позволяют сделать следующие выводы.
– АГ у пациентов с СД 2 типа во многом значительно увеличивает вероятность возникновения СС-событий.
– Контроль АД крайне важен у больных с СД, поскольку улучшает прогноз даже в большей степени, чем контроль гликемии.
– Блокаторы РАС являются основой лечения АГ при СД.
– Благодаря выраженному антигипертензивному эффекту и положительному влиянию на патогенетические механизмы поражения СС-системы при СД азилсартан (Эдарби) является перспективным препаратом для лечения АГ у пациентов с СД 2 типа.
Подготовила Наталья Очеретяная
UA/AZI/0616/0009


