24 травня, 2016
Дисфункция щитовидной железы и сердечная недостаточность

Хроническая сердечная недостаточность (ХСН) является самым распространенным кардиологическим заболеванием в мире, и в настоящее время наблюдается неуклонный рост частоты данной патологии [1]. В США количество пациентов с ХСН составляет 5,8 млн при ежегодной заболеваемости 670 тыс. случаев и ежегодной смертности – более 56 тыс. случаев [2-4]. Из более 900 млн населения Европы примерно у 15 млн выявляются клинические признаки СН [5-7].
Заболевания щитовидной железы широко распространены и являются наиболее частой эндокринной патологией, особенно в регионах с недостаточным содержанием йода в окружающей среде. Дисфункция щитовидной железы выявляется у 5-10% населения, чаще – у женщин и в возрастной группе старше 60 лет [8, 9]. В данной статье рассмотрены вопросы эпидемиологии дисфункции щитовидной железы, взаимосвязь указанного состояния с сердечно-сосудистым риском, влияние гормонов щитовидной железы на сердечно-сосудистую систему в норме и при дисфункции щитовидной железы, а также особенности патогенеза СН у пациентов с гипотиреозом и тиреотоксикозом.
Исходя из данных метаанализа [10], в котором оценивалась эпидемиология дисфункции щитовидной железы в Европе на основании публикаций за период с 1975 по 2012 г., распространенность недиагностированной дисфункции щитовидной железы составила в среднем 6,71% (при 95% доверительном интервале от 6,49 до 6,93); недиагностированного гипотиреоза и гипертиреоза – 4,94% (от 4,75 до 5,13) и 1,72% (от 1,66 до 1,88) соответственно. Распространенность как ранее диагностированной, так и недиагностированной дисфункции щитовидной железы составила 3,82% (от 3,77 до 3,86); гипотиреоза и гипертиреоза – 3,05 (от 3,01 до 3,09) и 0,75% (от 0,73 до 0,77) соответственно. Заболеваемость дисфункцией щитовидной железы составила 259,12 (от 254,39 до 263,9) случая на 100 тыс. населения в год; для гипотиреоза и гипертиреоза – 226,2 (от 222,26 до 230,17) и 51 (от 49,23 до 52,88) случая на 100 тыс. населения в год соответственно. В США распространенность субклинических нарушений функции щитовидной железы составляет 5% среди женщин и 3% – среди мужчин [11], примерно у 0,5% населения выявляется недиагностированная патология щитовидной железы [9, 12].
Субклиническая дисфункция щитовидной железы определяется как увеличение или снижение уровня тиреотропного гормона – ТТГ (норма – 0,45-4,50 мМЕ/л) при нормальных значениях гормонов щитовидной железы. Манифестация заболевания щитовидной железы диагностируется при аномальных уровнях гормонов щитовидной железы (свободного тироксина, с или без трийодтиронина) (табл. 1) [13, 14].

В ходе анализа данных исследований по изучению взаимосвязи сердечно-сосудистого риска с патологией щитовидной железы были получены противоречивые результаты [8, 9, 16-18]. В ряде исследований установлено, что субклинический гипотиреоз ассоциируется с повышенным риском развития ишемической болезни сердца (ИБС) [17, 19] и ХСН [20], а субклинический гипертиреоз – общей смертности и смертности вследствие ИБС; с фибрилляцией предсердий [21] и со снижением плотности костной ткани [14]. Клинически выраженные проявления заболеваний щитовидной железы связаны с отрицательным влиянием изменения уровня тиреоидных гормонов на сердечно- сосудистую систему, опорно-двигательный аппарат, кожу, желудочно-кишечный тракт и др., причем клинические маски весьма разнообразны и зависят от тяжести нарушения функций щитовидной железы [15]. Скрининг заболеваний данного органа позволяет выявить пациентов с субклинической и недиагностированной клинически выраженной дисфункцией щитовидной железы. Медикаментозная коррекция указанных состояний потенциально могла бы уменьшить риск возникновения неблагоприятных клинических исходов.
J. Rugge и соавт. [15] выполнили анализ базы данных MEDLINE и Кокрановского сотрудничества рандомизированных контролируемых клинических исследований по оценке эффективности скрининга и медикаментозной терапии. Прямых исследований по оценке преимуществ скрининга обнаружено не было. Проанализированы результаты 11 исследований и 1 ретроспективного когортного исследования, посвященных лечению субклинического гипотиреоза. Терапия проводилась левотироксином в различных режимах дозирования. Длительность лечения составила 4-12 мес, за исключением когортного исследования, в котором период наблюдения составил 7,6 года. Количество участников исследований – от 14 до 120 пациентов; в когортном исследовании анализировались данные 4735 больных. В большинстве исследований исходную группу сравнивали с группой плацебо и в 3 – с группой, которой терапия не проводилась. В когортном исследовании [22], включавшем пациентов с субклиническим гипотиреозом (на основании повышения уровня ТТГ – 4,1-11,0 мМЕ/л), установлено, что лечение больных левотироксином по сравнению с лицами, которым терапия не проводилась, ассоциировалось с более низким риском возникновения фатальных и нефатальных сердечно-сосудистых событий (4,2 против 6,6%; относительный риск 0,61; 95% ДИ от 0,39 до 0,95), общей смертности (3,4 против 6,4%; ОР 0,36; 95% ДИ от 0,19 до 0,66), сердечно-сосудистой смертности (1,4 против 2,4%; ОР 0,54; 95% ДИ от 0,37 до 0,92) и смертности вследствие онкологических заболеваний (1,2 против 2,2%; ОР 0,59; 95% ДИ от 0,21 до 0,88) в возрастной группе от 40 до 70 лет. При этом у пациентов старше 70 лет не выявлено взаимосвязи между применением левотироксина и риском возникновения сердечно- сосудистых событий (ОР 0,99; 95% ДИ от 0,59 до 1,33), общей смертностью (ОР 0,71; 95% ДИ от 0,56 до 1,08) или смертностью вследствие новообразований (ОР 0,51; 95% ДИ 0,24 до 1,09) [22]. Ни в одном из 5 исследований на фоне терапии не отмечено улучшения качества жизни, когнитивных функций, нормализации уровня артериального давления (АД) или индекса массы тела по сравнению с лицами, которым лечение не проводилось. В лечебной ветви в целом выявлено благоприятное влияние на уровни общего холестерина и холестерина липопротеинов низкой плотности (ЛПНП), однако данные были противоречивы и в большинстве исследований не достигли достоверных различий, а клиническая значимость величины влияния не была точно определена.
J. Mitchell и соавт. [23] изучили взаимосвязь между уровнем ТТГ и прогнозом у больных с систолической ХСН, включенных в многоцентровое клиническое исследование SCD-HeFT (Sudden Cardiac Death in Heart Failure Trial) [24]. В исследовании принимали участие пациенты со стабильной ХСН ишемического или неишемического генеза II или III функционального класса (ФК) по NYHA (Нью-Йоркская ассоциация сердца) и фракцией выброса (ФВ) левого желудочка (ЛЖ) <35%, рандомизированные на прием плацебо (n=847), амиодарона (n=845) или имплантацию однокамерных кардиовертеров-дефибрилляторов (ИКД) (n=829). Уровень ТТГ определяли в исходных условиях и далее каждые 6 мес на протяжении 5 лет. Из 2225 больных у большинства (87%) в исходных условиях выявлены нормальные значения содержания ТТГ в крови (0,3-5,0 мкЕд/мл), в 12% случаев – значения, указывающие на гипотиреоз, и у 1% – значения, свидетельствующие в пользу гипертиреоза. Пациенты с гипотиреозом были старше и среди них было больше женщин (р<0,05). Период наблюдения в среднем составил 45,5 мес. В процессе лечения у 89 участников с исходно нормальной функцией щитовидной железы было обнаружено снижение уровня ТТГ в крови и у 341 больного – значительное повышение указанного показателя. У пациентов, рандомизированных на прием амиодарона (средняя доза – 300 мг), определен повышенный риск изменения уровня ТТГ по сравнению с группами ИКД или плацебо (р<0,0001). У больных с дисфункцией щитовидной железы в исходных условиях или в процессе терапии установлен более высокий уровень смертности, чем у лиц с нормальной функцией щитовидной железы, причем даже после поправки на другие известные предикторы смертности (для гипотиреоза ОР составил 1,58; 95% ДИ от 1,29 до 1,94; р<0,0001; для гипертиреоза – ОР 1,85; 95% ДИ от 1,21 до 2,83; р=0,0048). Польза от ИКД не зависела от функции щитовидной железы. Итак, нарушение функции щитовидной железы у пациентов с симптоматической ХСН и ФВ ЛЖ ≤35% ассоциируется со значительным увеличением риска смерти, даже с учетом известных предикторов смертности.
В исследованиях, в которых оценивались клинические исходы у пациентов с сердечно-сосудистыми заболеваниями в зависимости от состояния щитовидной железы, были обнаружены значительно отличающиеся результаты. В обсервационном исследовании Framingham Heart Study [25] с участием 4331 пациента не выявлено взаимосвязи между субклиническими нарушениями функции щитовидной железы по данным измерения уровня ТТГ и риском развития сердечно-сосудистых заболеваний и смертности. В то же время в проспективном 4-летнем исследовании [17], включившем 2730 мужчин и женщин в возрасте от 70 до 79 лет, установлено, что у больных с умеренным или тяжелым субклиническим гипотиреозом риск развития ХСН был в 2-3 раза выше, чем в популяции с нормальной функцией щитовидной железы.
B. Gencer и соавт. [20] провели объединенный анализ 6 когортных исследований, включивших 25 390 участников, в которых оценивали функцию щитовидной железы и изучали клинические исходы, в частности развитие ХСН. У 2068 (8,1%) участников выявлен субклинический гипотиреоз и у 648 (2,6%) – субклинический гипертиреоз. Анализ, скорректированный по возрасту и полу, показал, что частота возникновения ХСН возрастала у лиц как с повышенными, так и со сниженными уровнями ТТГ, особенно при уровне ТТГ ≥10 и <0,10 мМЕ/л. Так, в ходе объединенного анализа отмечено, что у пациентов с уровнем ТТГ ≥10 мМЕ/л увеличивалась частота случаев СН (ОР 1,86; 95% ДИ от 1,27 до 2,72) в сравнении с эутиреоидным контролем [20]. В то же время скорректированный на факторы риска развития сердечно-сосудистых заболеваний риск возникновения ХСН оставался без изменений.
В проспективном когортном исследовании PROSPER (Prospective Study of Pravastatin in the Elderly at Risk) [26] изучено влияние субклинического гипертиреоза и гипотиреоза на риск развития СН и сердечно-сосудистых заболеваний у пожилых лиц. В исследовании принимали участие 5316 лиц в возрасте 70-82 лет с факторами риска или сердечно- сосудистыми заболеваниями, из которых у 71 участника выявлен субклинический гипертиреоз (ТТГ <0,45 мМЕ/л), у 199 – субклинический гипотиреоз (ТТГ ≥4,5 мМЕ/л, обе группы с нормальным уровнем свободного Т4); у остальных – эутиреоз (ТТГ=0,45-4,5 мМЕ/л). Длительность наблюдения составила 3,2 года. Изучались следующие показатели: частота госпитализаций в связи с обострением СН, фибрилляцией предсердий, сердечно-сосудистыми событиями, уровень смертности в зависимости от исходного состояния щитовидной железы. Установлено, что частота госпитализаций в связи с обострением СН была выше у лиц с субклиническим гипертиреозом по сравнению с участниками с эутиреозом (скорректированный по возрасту и полу ОР составил 2,93; 95% ДИ от 1,37 до 6,24; р=0,005; при многофакторном анализе скорректированный ОР 3,27; 95% ДИ от 1,52 до 7,02; р=0,002). Субклинический гипотиреоз (ТТГ >10 мМЕ/л) ассоциировался с СН (скорректированный по возрасту и полу ОР составил 3,01; 95% ДИ от 1,12 до 8,11; р=0,029; при многофакторном анализе ОР 2,28; 95% ДИ от 0,84 до 6,23). Не выявлено убедительных доказательств существования взаимосвязи между субклинической дисфункцией щитовидной железы, частотой развития сердечно-сосудистых событий и показателем смертности, за исключением больных с уровнем ТТГ <0,1 или >10 мМЕ/л и не принимавших правастатин. Таким образом, у пожилых лиц с высоким риском возникновения сердечно-сосудистых событий, с низким или очень высоким уровнем ТТГ и нормальным уровнем свободного Т4 увеличен риск частоты госпитализаций в связи с СН.
Гормоны щитовидной железы и сердечно-сосудистая система
Синтез и секреция тиреоидных гормонов регулируется тиреотропин-рилизинг-гормоном гипоталамуса, который осуществляет контроль над синтезом ТТГ и концентрацией тиреоидных гормонов в крови.
Тиреоидным гормонам принадлежит ключевая роль в регуляции разнообразных физиологических функций, включая рост, дифференцировку тканей и метаболический гомеостаз, в частности контроль синтеза и активности регуляторных белков и ключевых ферментов метаболизма.
Основной формой тиреоидных гормонов, синтезируемых щитовидной железой, является прогормон тироксин (Т4, тетрайодтиронин), который биологически малоактивен, однако может превращаться в организме в биологически активную форму – трийодтиронин (Т3) посредством удаления иодида с помощью дейодиназ (семейство селенсодержащих ферментов йодтирониндейодиназы 1-го, 2-го и 3-го типов, которые катализируют дейодинацию тироксина и его производных). Щитовидная железа секретирует Т4 в 10 раз больше, чем Т3; до 80% биологически активной формы Т3 образуется под действием дейодиназ 1-го (D1) и 2-го типа (D2) в периферических тканях [27]. Инактивация тиреоидных гормонов осуществляется путем дейодирования их внутреннего кольца. Данную реакцию катализирует дейодиназа 3-го типа (D3) [28].
В крови Т4 и Т3 циркулируют в двух формах: в свободной и связанной с транспортными белками. Между связанными и свободными фракциями гормонов установлено динамическое равновесие. Уменьшение концентрации свободного гормона приводит к снижению связывания и наоборот. В клинической практике можно определять и свободные, и связанные с белками фракции гормонов. Уровень общих Т4 и Т3 в большей степени зависит от концентрации связывающих белков, чем от степени нарушения функции щитовидной железы. В случае повышения уровня транспортных белков (беременность, прием контрацептивов) или их уменьшения (цирроз печени, нефротический синдром, прием андрогенов, генетические нарушения) общая концентрация гормонов изменяется, однако содержание свободных фракций остается прежним. Изменения уровня связывающих белков может осложнять интерпретацию результатов исследования общих Т4 и Т3. Поэтому особую диагностическую значимость имеет определение свободных фракций Т4 и Т3 [29].
Сердечно-сосудистая система особенно чувствительна к снижению локального уровня Т3, который имеет фундаментальное значение в поддержании морфологии и функций сердца с помощью геномных и негеномных эффектов. Многочисленные геномные эффекты гормонов щитовидной железы на сердце опосредуются путем взаимодействия со специфическими рецепторами к тиреоидным гормонам (TRs). TRs кодируется двумя генами – THRA и THRB, расположенными в хромосомах 17 и 3 соответственно. Т3 – активная форма тиреоидных гормонов – оказывает большинство своих эффектов при участии следующих TRs: TRa1, TRa2, TRb1. Установлено, что экспрессия TRs, за исключением TRb2, осуществляется во всех тканях; при этом паттерн экспрессии варьирует в различных типах тканей.
Экспрессия TRa1 выявлена преимущественно в миокарде. Предполагается, что TRa1 регулирует важные гены, которые связаны с дифференцировкой и ростом клеток, сократительной функцией, пейсмекерной активностью и проводимостью. Для трех основных изоформ TRs (TRa1, TRb1 и TRb2) установлена тканеспецифичная экспрессия и отмечено участие в регуляции ряда метаболических функций и процессах клеточного роста. Кроме того, TRs являются членами суперсемейства ядерных рецепторов и выполняют роль транскрипционных факторов, индуцируемых Т3. В кардиомиоцит Т3 поступает при участии специфичных транспортных белков, расположенных на его клеточной мембране [30], и далее в ядро, где связывается с ядерным рецептором (TRs), и данный комплекс, в свою очередь, связывается с элементами, отвечающими за гормональный ответ (TREs) на промоутерных зонах регуляторных генов [31].
Кроме геномного (ядерного) действия гормонов щитовидной железы, опосредованного TRs, негеномные эффекты тиреоидных гормонов часто ассоциируются с активацией сигнальных путей. Классические геномные эффекты Т3 опосредованы высокоаффинными ядерными рецепторами, которые регулируют экспрессию генов-мишеней. В настоящее время выделен ряд генов, чувствительных к действию тиреоидных гормонов (табл. 2). Тиреоидные гормоны могут оказывать как позитивную, так и негативную регуляцию. Позитивная регуляция приводит к возрастанию транскрипционной активности гена и увеличению продукции мРНК. Результатом негативной регуляции является угнетение транскрипционной активности гена и снижение образования мРНК.

Негеномные эффекты тиреоидных гормонов на кардиомиоциты и общее периферическое сосудистое сопротивление (ОПСС) не предполагают связывания с ядерными рецепторами [33]. Указанные эффекты развиваются довольно быстро и обусловлены влиянием на транспорт ионов кальция, натрия и калия через клеточную мембрану, а также транспорт глюкозы, на функции митохондрий и различные внутриклеточные сигнальные пути [34]. Таким образом, влияние Т3 на сердце и центральную гемодинамику осуществляется при участии геномных и негеномных механизмов.
Экспрессия генов Са-АТФ-азы саркоплазматического ретикулума и ее ингибитора фосфоламбана находится под контролем Т3. Вход кальция и его перераспределение в саркоплазматическом ретикулуме являются критическими детерминантами систолической сократительной функции и диастолического расслабления [35, 36]. Активный транспорт кальция Са-АТФ-азой в пластинку саркоплазматического ретикулума регулируется фосфоламбаном, активность которого, в свою очередь, зависит от уровня фосфорилирования [36]. Следовательно, изменения относительного количества указанных белков и степень фосфорилирования фосфоламбана при патологии щитовидной железы оказывают влияние на диастолическую функцию.
Т3 уменьшает ОПСС, что вызывает рефлекторный положительный инотропный и хронотропный эффекты. Вследствие прямого расслабляющего действия на гладкомышечные клетки и увеличения синтеза оксида азота эндотелиальными клетками отмечается уменьшение среднего артериального и диастолического давления (постнагрузки на ЛЖ). Это, в свою очередь, приводит к активации ренин-ангиотензиновой системы (РАС), увеличению реабсорбции натрия и воды в почках, повышению объема циркулирующей крови (ОЦК) и преднагрузки на ЛЖ [37]. Таким образом, Т3 посредством значительного снижения ОПСС (до 50% от исходного уровня), с одной стороны, и повышения венозного возврата к сердцу – с другой, повышает сердечный выброс [38].
Сердечно-сосудистая система при гипертиреозе
Тиреоидные гормоны модулируют каждый компонент сердечно-сосудистой системы, необходимый для ее нормального функционирования. Избыток тиреоидных гормонов вызывает значительные изменения со стороны сердечно-сосудистой системы. Для гипертиреоза характерны следующие проявления: увеличение частоты сердечных сокращений (ЧСС) в покое (у половины пациентов с гипертиреозом выявляется синусовая тахикардия >100 уд/мин), объема крови, ударного объема, сократимости миокарда и ФВ ЛЖ, улучшение диастолического расслабления. Повышение уровня тиреоидных гормонов индуцирует тахикардию в покое и сердцебиение, которые являются наиболее распространенными симптомами при манифестном гипертиреозе. У 10-15% больных с гипертиреозом диагностируется фибрилляция предсердий [39]. Частое нерегулярное сокращение предсердий увеличивает риск образования тромбов в полости сердца, которые, в конечном счете, могут привести к системной эмболии, инсульту и другим осложнениям. Симптомы тиреотоксикоза часто неспецифичны, развиваются медленно, а фибрилляция предсердий может быть первым клиническим проявлением дисфункции щитовидной железы [37, 40].
В проспективном когортном исследовании [41], включившем 84 пациента с впервые зарегистрированным гипертиреозом, проведен анализ симптомов тиреотоксикоза в зависимости от возраста. В группе больных ≥70 лет (средний возраст 80,2 года) более 50% предъявляли 3 жалобы: тахикардия, усталость и потеря веса; реже – гиперрефлексия, повышенная потливость, непереносимость жары, тремор, нервозность, полидипсия и повышенный аппетит. По сравнению с молодыми пациентами (≤50 лет, средний возраст 37,4 года) у пожилых больных более часто диагностировали анорексию (32 против 4%) и фибрилляцию предсердий (35 против 2%). Зоб выявлялся у 94% молодых пациентов и у 50% пожилых больных. По сравнению со здоровыми сверстниками установлено, что с тиреотоксикозом ассоциировались следующие симптомы: апатия, тахикардия и потеря веса (отношение шансов 14,8, 11,2 и 8,7 соответственно).
Как правило, отмечается постоянная форма фибрилляции предсердий, которая чаще обнаруживается у пожилых пациентов, что, по-видимому, отражает снижение порога обнаружения данной аритмии с возрастом. Определяется высокое пульсовое давление, повышение сердечного выброса, увеличение симпатического тонуса вегетативной нервной системы. При аускультации выявляют усиление тонов сердца (особенно на верхушке), акцент второго тона над легочной артерией, систолические шумы в области основания сердца и на верхушке.
При тиреотоксикозе определяется положительный хронотропный и батмотропный эффекты, по-видимому, ассоциированные с вегетативным дисбалансом вследствие уменьшения парасимпатической активности, гиперактивности симпатико- адреналовой системы, увеличения количества
β-адренорецепторов гуанидин-нуклеотид-регулирующего белка, а также повышенной чувствительности к катехоламинам. Тиреоидные гормоны могут действовать независимо от катехоламинов, но подобными путями, что, возможно, связано с их структурной схожестью. Так, катехоламины и тиреоидные гормоны являются аналогами тирозина, они подвергаются действию одних и тех же ферментов. Исходя из вышесказанного, можно предположить, что аналоги адреналина и норадреналина, образовавшиеся из тиреоидных гормонов, могут функционировать как псевдокатехоламины, взаимодействуя с β-адренорецепторами [42]. Считается, что трийодтиронин высвобождается из нервных синапсов и действует как симпатомиметический нейротрансмиттер [43, 44].
Наблюдается увеличение систолической функции ЛЖ в покое, а также скорости релаксации и диастолического наполнения ЛЖ [45]. При гипертиреозе отмечается незначительное снижение уровня среднего АД вследствие повышения систолического АД, связанного с увеличением ударного объема, и снижения диастолического АД в результате периферической вазодилатации. Под влиянием тиреоидных гормонов происходит уменьшение ОПСС вследствие дилатации артериол и повышенной скорости метаболизма в периферических тканях [46]. Ускоренная утилизация кислорода увеличивает образование конечных продуктов обмена, а расслабление гладкой мускулатуры артериальных волокон под влиянием тиреоидных гормонов, вызывающих периферическую вазодилатацию, приводит к снижению ОПСС и способствует дальнейшему повышению ЧСС. При этом наблюдается селективное увеличение кровотока в коже, скелетных мышцах и сердце. Вазодилатация наряду с отсутствием увеличения почечного кровотока приводит к снижению перфузионного давления в почках и активации ренин-ангиотензин-альдостероновой системы (РААС) с повышением почечной задержки натрия и увеличением ОЦК. Указанные изменения ведут к повышению преднагрузки и снижению постнагрузки, что приводит к значительному росту ударного объема [47]. Установлено, что увеличение преднагрузки оказывает стимулирующее влияние на секрецию предсердного натрийуретического пептида (ПНУП). Предполагается, что у здоровых лиц секреция ПНУП, индуцированная тиреоидными гормонами, является не следствием прямого действия на миокард, а возникает в ответ на изменения состояния сердечно- сосудистой гемодинамики, приводящей к увеличению растяжения предсердий [48]. Итак, при тиреотоксикозе наблюдается тахикардия с высоким сердечным выбросом, увеличение преднагрузки, наряду со снижением ОПСС, что сопровождается развитием гиперкинетического типа гемодинамики.
Кроме того, в ответ на повышение давления в левом предсердии и стимуляцию барорецепторов увеличивается давление в легочных венах, что, в свою очередь, стимулирует рефлекторное сужение легочных артериол (рефлекс Китаева) [49]. Вследствие сужения артериол малого круга кровообращения повышается давление в легочной артерии и увеличивается нагрузка на правый желудочек, которому необходимо больше усилий для проталкивания крови в легочный ствол, что способствует дальнейшему увеличению резистентности легочных сосудов и повышению легочной гипертензии [50]. Также развитию легочной гипертензии при тиреотоксикозе способствуют аутоиммунные процессы, ассоциированные с повреждением эндотелия или эндотелиальной дисфункцией, увеличением сердечного выброса и повышением интенсивности процессов метаболизма сосудорасширяющих веществ в легочных сосудах [51]. Следует отметить, что у пациентов с тиреотоксикозом после достижения эутиреоидного состояния обнаружено реверсирование легочной гипертензии [52]. Таким образом, у больных с тиреотоксикозом, которые предъявляют жалобы на одышку, нужно учитывать возможность наличия легочной гипертензии.
Сердечная недостаточность при гипертиреозе
Понимание патофизиологических механизмов развития СН при гиперфункции щитовидной железы является важным для врачей, особенно для кардиологов и эндокринологов. Это обусловлено тем, что пациенты с манифестным и субклиническим гипертиреозом имеют высокий риск развития сердечно-сосудистой смерти. В двух метаанализах [53, 54] оценивалась сердечно-сосудистая летальность при манифестном гипертиреозе. В первом [53], включавшем 7 когортных исследований, установлено увеличение риска сердечно- сосудистой смертности в 1,7 раза при манифестном гипертиреозе. В более позднем метаанализе, проведенном F. Brandt и соавт. [54] с включением данных 31 138 больных с гиперфункцией щитовидной железы, обнаружено, что ОР общей смертности составил 1,21 (95% ДИ от 1,05 до 1,38). Авторы сделали заключение, что у пациентов с гипертиреозом уровень смертности увеличивается примерно на 20% от исходного.
Противоречивые результаты были получены в больших проспективных исследованиях, посвященных оценке сердечно-сосудистой заболеваемости и смертности у больных с субклиническим гипертиреозом, что, по-видимому, отражает гетерогенность анализируемых популяций [55]. Тем не менее в двух последних метаанализах установлено, что субклинический гипертиреоз может увеличить сердечно-сосудистую смертность, особенно у пациентов с неопределяемыми уровнями ТТГ. Так, в метаанализе [56], включившем 17 когортных исследований, у больных с субклиническим гипертиреозом продемонстрировано значительное повышение риска общей и сердечно-сосудистой смертности: ОР составил 1,25 (95% ДИ 1,00-1,55) и 1,52 (95% ДИ 1,08-2,13) соответственно.
Увеличение риска сердечно-сосудистой смерти может быть результатом повышения риска нарушений ритма [57], в частности предсердных аритмий и риска развития СН, особенно у пожилых пациентов [58]. Установлено, что возникновение фибрилляции предсердий при тиреотоксикозе ассоциировалось с повышенным риском развития мозгового инсульта и эмболии легочной артерии [59, 60]. Важно отметить, что при аутоиммунном гипертиреозе аутоиммунные процессы часто затрагивают сердечно-сосудистую систему. Так, у пациентов с болезнью Грейвса выявляются легочная гипертензия, миксоматозное поражение клапанного аппарата сердца и тиреотоксическая кардиомиопатия [61].
Установлено, что распространенность ХСН при диффузном токсическом зобе составляет 12-68% [63]. При этом почти у 90% пациентов с тиреотоксикозом и ХСН отмечалась фибрилляция предсердий [64]. В исследовании Т. Гома [65], включившем 89 больных с диффузным токсическим зобом, сердечно-сосудистые нарушения зарегистрированы в 80,9% случаев. При этом артериальная гипертензия (АГ) отмечена у 34,8% пациентов, фибрилляция предсердий и ХСН – у 21,3% больных. Выявлено, что у пациентов с диффузным токсическим зобом и с АГ, фибрилляцией предсердий и ХСН наблюдается ремоделирование миокарда, расширение полостей сердца, легочная гипертензия и снижение ФВ ЛЖ. Продемонстрировано, что с возникновением ХСН у больных с диффузным токсическим зобом ассоциированы наличие постоянной формы фибрилляции предсердий и АГ, возраст старше 40 лет, мужской пол, длительность течения диффузного токсического зоба ≥10 лет, наличие более 6 эпизодов тиреотоксикоза.
Под действием тиреоидных гормонов происходит изменение диастолической и систолической функции ЛЖ; сократительная способность миокарда изменяется в соответствии с гемодинамическим паттерном, вторичным по отношению к эффектам гормонов щитовидной железы на ОПСС. Оптимальный баланс тиреоидных гормонов поддерживает положительное желудочково-артериальное взаимодействие, являющееся важнейшей детерминантой функционирования сердечно-сосудистой системы [37]. Тиреотоксикоз усиливает работу сердца посредством модуляции гемодинамических нагрузок. Усиление метаболизма и потребления кислорода путем оптимизации механико-энергетических процессов повышает производительность ЛЖ. Изменения гемодинамики, обусловленные гипертиреозом, уменьшают сократительный резерв миокарда и не позволяют повышаться ФВ ЛЖ и сердечному выбросу при физической нагрузке, по-видимому, вследствие невозможности снижения и так низкого ОПСС, хотя констрикция венозных сосудов возрастает. Результатом уменьшения ОПСС является активация РААС, ведущая к задержке натрия и жидкости [66].
Увеличение преднагрузки и ОЦК активирует работу сердца и стимулирует прогрессирование гипертрофии миокарда. Вследствие увеличения ЧСС и повышения ударного объема возрастает сердечный выброс, усиливается венозный возврат крови к сердцу. Указанные изменения приводят к увеличению среднего гемоциркуляторного давления наполнения, что способствует ретроградному притоку крови к правому предсердию [35]. Причиной увеличения ОЦК при тиреотоксикозе является изменение сывороточного уровня эритропоэтина в соответствии с изменением сывороточного уровня тироксина, что приводит к увеличению массы эритроцитов [42]. Кроме того, транскрипционные эффекты тиреотропных гормонов способствуют повышению контрактильности миокарда через регуляцию транспорта кальция в кардиомиоцитах и фосфорилирование фосфоламбана. Нетранскрипционные эффекты гормонов щитовидной железы связаны с их влиянием на различные ионные каналы.
Вышеперечисленные кардиальные влияния в сочетании с низким ОПСС и увеличением ОЦК ведут к состоянию высокого сердечного выброса, так называемой «сердечной недостаточности с высоким выбросом» (табл. 3).

Больные с гипертиреозом предъявляют жалобы на снижение переносимости физических нагрузок, одышку при незначительной физической нагрузке при отсутствии в анамнезе заболеваний сердца. Это может быть обусловлено неадекватным увеличением сердечного выброса при физической нагрузке [67]. Таким образом, нарушение толерантности к физической нагрузке можно интерпретировать как первый симптом ХСН у пациентов с гипертиреозом, что отражает неспособность сердца при гипертиреозе адекватно реагировать на возрастающие требования к сердечно-сосудистой системе при физической нагрузке [61].
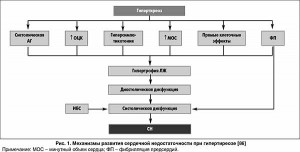
В то же время у больных с тиреотоксикозом также может развиваться СН с низким сердечным выбросом. В соответствии с клиническими данными [68] такой тип ХСН выявляется у 6-15% пациентов. Отмечено, что наряду со снижением сердечного выброса увеличивается системное сосудистое сопротивление, уменьшается контрактильность ЛЖ и его наполнение при увеличенном ОЦК (табл. 4, рис. 1). Риск возникновения СН с низким сердечным выбросом возрастает при наличии у пациентов с тиреотоксикозом сопутствующих заболеваний сердечно-сосудистой системы, в частности ИБС, АГ, пороков сердца и/или фибрилляции предсердий.
При тиреотоксикозе наблюдается укорочение фазы диастолической деполяризации, снижение потенциала действия клеток синусового узла, неравномерное укорочение рефрактерных периодов предсердных миоцитов, что обусловливает возникновение электрической гетерогенности миокарда предсердий. Отмечается также укорочение рефрактерного периода АВ-узла, повышается чувствительность к адренергической стимуляции, что может провоцировать возникновение наджелудочковых аритмий, прежде всего фибрилляции предсердий [69]. В результате возможно развитие кардиомиопатии, индуцированной тахикардией. Последняя являет собой вторичную дисфункцию ЛЖ, вызванную длительной тахикардией, которая полностью или частично восстанавливается после нормализации сердечного ритма. Диагноз подтверждается после восстановления функции ЛЖ, достижения контроля ЧСС и эутиреоидного состояния [70]. Как правило, при кардиомиопатии, индуцированной тахикардией, размеры сердца значительно увеличиваются, уменьшается толщина стенок ЛЖ, а снижение контрактильности ЛЖ подобно дилатационной кардиомиопатии. Указанные показатели улучшаются после достижения контроля ЧСС и СН.
Отмечено, что у пациентов с тиреотоксикозом после достижения состояния эутиреоза наблюдалось улучшение течения ХСН, в частности быстрое улучшение клинических симптомов и признаков ХСН, наряду с корригирующим влиянием на функции сердца. Тем не менее в некоторых ситуациях ХСН может становиться необратимой [58]. Продемонстрировано, что примерно у 1/3 больных может развиться тиреотоксическая кардиомиопатия [58].
Тиреотоксическое сердце или тиреотоксическая кардиомиопатия являет собой повреждение миокарда, вызванное токсическими эффектами избытка гормонов щитовидной железы, приводящими к нарушению энергообразующей функции кардиомиоцитов (окислительное фосфорилирование, гликолиз), внутриклеточного метаболизма (синтез белковых структур) и сократительной функции миофибрилл. Выделяют 3 стадии тиреотоксической кардиомиопатии (табл. 5).

Основные проявления включают гипертрофию ЛЖ, нарушения ритма сердца, фибрилляцию предсердий, расширение полостей сердца, СН, легочную гипертензию и диастолическую дисфункцию. В исследовании А.С. Карась [72] отмечено, что особенностями тиреотоксической кардиомиопатии являются: частичная субъективная манифестация синдрома поражения мышцы сердца; развитие электрической негомогенности миокарда как предсердий, так и желудочков; увеличение размеров полостей сердца и массы миокарда ЛЖ; ускорение расслабления ЛЖ и увеличение вклада левого предсердия в диастолическое наполнение ЛЖ.
Несмотря на то что у пациентов с тиреотоксикозом выявляется снижение ОПСС и уровня диастолического АД, среднее давление в легочной артерии обычно возрастает и возможно развитие правожелудочковой СН вследствие перегрузки объемом правого желудочка, что обусловлено увеличением ОЦК и венозного возврата. При этом отмечается дилатация правого желудочка и трикуспидальная недостаточность вследствие растяжения клапанного кольца трикуспидального клапана, часто в сочетании с легочной гипертензией.
Сердечно-сосудистая система при гипотиреозе
Дефицит тиреоидных гормонов влияет на многие физиологические функции и метаболические процессы в организме. При дефиците тиреоидных гормонов снижается активность клеточных ферментов, участвующих в регуляции обратного захвата кальция, и экспрессия сократительных белков в кардиомиоцитах, что ведет к снижению ЧСС, ослаблению контрактильности и нарушению процесса релаксации миокарда. Наиболее очевидным эффектом дефицита тиреоидных гормонов на сердечную мышцу является удлинение временных характеристик систолы и ранней диастолы [73]. При гипотиреозе отмечается уменьшение сердечного выброса, ударного объема и ОЦК, однако в отличие от застойной СН давление в легочной артерии не возрастает.
Клинические симптомы и признаки нарушения со стороны сердечно-сосудистой системы при гипотиреозе ассоциированы с брадикардией, увеличением ОПСС, уменьшением пульсового давления и незначительной АГ [50]. Наблюдается увеличение времени циркуляции крови (замедление кровообращения), однако давление наполнения правых и левых отделов сердца, как правило, остается в пределах нормальных значений, если не увеличивается в случае перикардиального выпота. Повышение ОПСС при нормальном венозном давлении приводит к перераспределению кровотока с существенным снижением мозгового, почечного и кожного кровотока [74]. При гипотиреозе потребность миокарда в кислороде снижается в большей степени, чем его кровоснабжение. Однако гиперхолестеринемия с увеличением уровня липопротеинов низкой плотности (ЛПНП) и аполипопротеинов В [75] повышает риск развития атеросклероза. У пациентов с гипотиреозом ХСН может развиваться и при отсутствии основного заболевания сердца [50]. В то же время у таких пациентов часто выявляются ИБС, АГ, нарушения проводимости и перикардит [76].
Экспериментально [77] установлено, что гипотиреоз приводит к тяжелой прогрессирующей систолической дисфункции и увеличению соотношения толщины стенки к размеру полости ЛЖ наряду с уменьшением массы миокарда ЛЖ. Дилатация камер сердца ассоциировалась с увеличением числа саркомеров, что характерно для СН. Кроме того, отмечено ухудшение миокардиального кровотока вследствие значительного уменьшения количества артериол [77].
В клинических исследованиях [73, 78] установлено, что у больных с манифестным и субклиническим гипотиреозом изменения структурно-функционального состояния сердца зависели от степени и длительности дефицита тиреоидных гормонов. Причем при субклиническом гипотиреозе выявляются такие же нарушения работы сердца и сосудов, как при выраженном гипотиреозе. Обнаружено, что у пациентов с незначительным дефицитом гормонов щитовидной железы наблюдалось нарушение диастолической функции ЛЖ, в частности удлинение периода изоволюметрической релаксации миокарда желудочков и нарушение диастолического наполнения ЛЖ [79]. Тиреоидные гормоны влияют на активность аденилатциклазы, клеточный транспорт кальция и модулируют состав изоферментов АТФ-азы в кардиомиоцитах [80]. В связи с этим при их дефиците миокарду требуется больше энергии и времени для осуществления процессов расслабления и наполнения, что и находит отражение в нарушении показателей диастолической функции сердца. Установлено, что при гипотиреозе выявляется снижение минутного объема сердца вследствие уменьшения ударного объема сердца и ЧСС [81]. В случае СН и анемии пульс, напротив, может быть даже учащен.
Снижение систолической и диастолической функции в покое и при физической нагрузке приводит к ухудшению качества жизни больных [82]. Диастолическая дисфункция и снижение ОЦК являются причиной уменьшения преднагрузки на сердце, при этом сердечный выброс поддерживается на субнормальном уровне или снижается на 30-40% от исходного. Для гипотиреоза характерно существенное повышение ОПСС (до 30% от нормальных значений), что приводит к повышению уровня диастолического АД [83]. Продемонстрировано, что тиреоидные гормоны участвуют в процессах ангиогенеза, стимулируют рост артериол в сердце взрослых пациентов, а также после перенесенного инфаркта миокарда [84]. Соответственно, низкие уровни свободного Т3 будут ингибировать неоваскуляризацию в сердце после острого инфаркта миокарда, способствуя ускорению патологического ремоделирования ЛЖ и развитию СН, внося коррективы в краткосрочный и долгосрочный прогноз развития неблагоприятных сердечно-сосудистых событий [85, 86].
Установлено, что при микседеме размеры сердца могут быть значительно увеличены за счет расширения полостей, интерстициального отека миокарда и скопления муцинозной жидкости в полости перикарда; в миокарде определяются диффузные изменения в виде выраженного отека интерстиция и мышечных волокон, вакуолизации части мышечных волокон, пикноза ядер, частичного исчезновения поперечной исчерченности; в ряде случаев можно обнаружить очаги фиброза [87]. Классическими признаками микседемы являются: увеличение размеров сердца, брадикардия, пульс слабого наполнения и напряжения, артериальная гипотония, глухость сердечных тонов, низкий вольтаж зубцов на электрокардиограмме (ЭКГ), плотные на ощупь отеки подкожной клетчатки – голеней, лица (кожа над ними не собирается в складку), признаки СН.
В полости перикарда может накапливаться транссудат, его количество, как правило, небольшое (15-150 мл) [88]. Частота выявления перикардиального выпота у больных с тяжелым гипотиреозом составляет 30-80%, а при легкой форме гипотиреозе – 3-6% [89, 90]. Накопление в тканях и серозных полостях белка и жидкости обусловлено усиленной экстравазацией белков плазмы и недостаточностью лимфооттока. При перикардиальном выпоте у пациентов с гипотиреозом на ЭКГ определяются низковольтажные комплексы QRS, депрессия сегмента PR, смещение сегмента ST, изменения зубца Т и электрические альтерации.
Установлено, что у больных с гипотиреозом, включая субклинический гипотиреоз, отмечается увеличение дисперсии интервала QT [91]. Данные клинических исследований [92, 93] свидетельствуют о том, что, несмотря на существенное удлинение интервала QT, у пациентов с гипотиреозом редко встречаются такие осложнения, как злокачественные желудочковые аритмии и внезапная смерть. Однако вероятность возникновения последних повышается при сочетании увеличенной дисперсии интервала QT с гипокалиемией, гипомагниемией и синдромом удлиненного QT. Среди других изменений на ЭКГ возможно выявление неполной или полной блокады правой ножки пучка Гиса, снижение амплитуды зубца Р, уплощение или инверсия зубца Т на фоне низкого вольтажа всех комплексов ЭКГ [92].
Вследствие снижения скорости почечного кровотока, клубочковой фильтрации снижается диурез. Нарушения функции почек и секреции антидиуретического гормона могут приводить к гипонатриемии.
Сердечная недостаточность при гипотиреозе
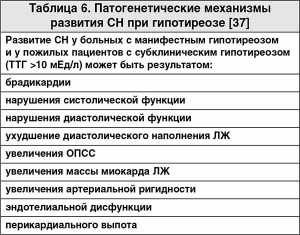
Изменения со стороны сердечно-сосудистой системы при гипотиреозе полностью противоположны таковым при тиреотоксикозе. Наиболее часто встречаемые: снижение сердечного выброса и сократительной способности миокарда, повышение уровня диастолического АД, увеличение ОПСС и нарушения ритма, а также нарушение систолической и диастолической функции ЛЖ в покое и при физической нагрузке [94]. Характерное для гипотиреоза увеличение ОПСС предположительно связано как с прямым воздействием Т3 на гладкомышечные клетки сосудов, так и нарушением эндотелийзависимой вазодилатации, ассоциированным с уменьшением синтеза и секреции оксида азота при дефиците Т3 [79]. Отмечается снижение преднагрузки, обусловленное развитием диастолической дисфункции и снижением ОЦК, а увеличение постнагрузки, уменьшение инотропной и хронотропной функций сердца способствуют снижению сердечного выброса (табл. 6) [95, 96].
Кроме того, при гипотиреозе происходит снижение потребления кислорода тканями, а также снижение расходования энергии и утилизации энергетических субстратов. Характерно снижение термогенеза, которое клинически проявляется непереносимостью холода и зябкостью. Уровень основного обмена снижается на 35-40% от исходного [94].
Следует отметить, что эффекты Т3 в клетках сердца, его стимулирующее влияние на Na+/K+-АТФ-азу и Са2+-АТФ-азу саркоплазматического ретикулума определяют хронотропный ответ клеток предсердия и растяжение мышцы сердца в диастолу. Развитие диастолической и систолической дисфункции ЛЖ, дилатация камер сердца и ухудшение миокардиального кровотока способствуют развитию ХСН у больных с гипотиреозом (рис. 2)
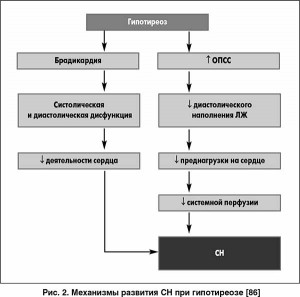 .
.
Следует подчеркнуть, что тиреоидные гормоны влияют на синтез N-терминального предшественника мозгового натрийуретического пептида (NT-pro-BNP) – маркера наличия и тяжести течения ХСН [97, 98]. В ряде клинических исследований [99-101] отмечено, что содержание NT-pro-BNP в сыворотке крови существенно увеличивалось у пациентов с гипертиреозом и уменьшалось у больных с гипотиреозом. Установлена существенная положительная корреляционная связь между содержанием NT-pro-BNP в сыворотке крови и уровнями свободного Т4 (r=0,549; р=0,012) у пациентов с гипертиреозом [99]. Многофакторный регрессионный анализ продемонстрировал, что повышение уровня свободного Т4 было независимо связано с высокими уровнями NT-pro-BNP в сыворотке крови [99, 100]. Установлено, что у больных гипотиреозом применение левотироксина приводило к увеличению концентрации NT-pro-BNP в сыворотке крови (p<0,001) [102]. На фоне терапии у пациентов с гипертиреозом выявлено существенное снижение концентрации NT-pro-BNP в сыворотке крови (p=0,05), поэтому оценивать его содержание в крови целесообразно в состоянии эутиреоза [102].
В исследовании А.С. Карась [32] продемонстрировано, что в большинстве случаев дистиреоидизма преобладающей кардиальной нозологией является метаболическая тиреоидная кардиомиопатия. Особенностями клинических, инструментальных и лабораторных изменений у больных с нарушенной функцией щитовидной железы являются: для гипотиреоза – преобладание лиц женского пола, стертость субъективной симптоматики, тенденция к повышению уровня систолического АД, отсутствие значимой дислипидемии, дисгликемии, кардиоцитолиза и гепатоцитолиза. Недостаток гормонов щитовидной железы ассоциирован с повышением гетерогенности процессов реполяризации миокарда: субклинический гипотиреоз сопровождается нарушением процессов реполяризации и развитием электрической гетерогенности миокарда желудочков, в то время как при явном гипотиреозе изменения в большей степени связаны с нарушением гомогенности проведения электрического импульса по предсердиям. Морфофункциональными особенностями поражения сердца при гипотиреозе являются развитие гипертрофии миокарда, увеличение полости левого предсердия, большая репрезентативность митральной недостаточности, укорочение раннего диастолического наполнения ЛЖ, зависимость процессов ремоделирования миокарда от уровня свободного тироксина, концентрации холестерина и ЛПНП.
В последнее время внимание исследователей приковано к начальным стадиям тиреоидных расстройств, в том числе к субклиническому гипотиреозу, поскольку уже на данном этапе заболевания выявляются особенности нарушения работы сердца и сосудов, свойственные выраженному гипотиреозу. В исследовании З.Н. Бланковой [38] отмечено, что у пациентов с ХСН и манифестным гипотиреозом частота встречаемости повышенного уровня NT-pro-BNP (>200 пг/мл) достоверно ниже, чем у таких же больных с субклиническим гипотиреозом (28,6 против 50,0% соответственно, p<0,05). Гормональная заместительная терапия левотироксином у пациентов с ХСН и с сопутствующим как манифестным, так и субклиническим гипотиреозом приводит к достоверному улучшению их клинического и функционального состояния, диастолической функции ЛЖ, эндотелиальной функции. Выявлено, что лечение левотироксином больных с ХСН и с сопутствующим гипотиреозом сопровождается не снижением, а увеличением уровня NТ-рroBNP, что свидетельствует не об обострении ХСН, а связано с непосредственным повышающим влиянием левотироксина на уровень NТ-рroBNP [38].
Заключение
Наиболее частым и серьезным осложнением дисфункции щитовидной железы является поражение сердечно-сосудистой системы, поэтому данную проблему следует рассматривать не только как эндокринологическую, но и как кардиологическую. Часто патология сердечно-сосудистой системы при дисфункции щитовидной железы является ведущей в клинической картине заболевания: различные сложные нарушения ритма сердца, АГ, тиреоидные кардиомиопатии с развитием ХСН, которые нередко приводят к утрате трудоспособности, а при тяжелом течении – и к смерти у указанной категории пациентов.
Дифференциальная диагностика функциональных и органических поражений миокарда при нарушении функции щитовидной железы с прогнозированием развития ХСН актуальна и требует динамического изучения всего спектра клинических проявлений поражения сердечно-сосудистой системы на фоне тиреоидной дисфункции. Развитие минимальных структурных и функциональных изменений миокарда у больных с дисфункцией щитовидной железы должно настораживать в плане вероятности развития сердечной патологии, осложнением которой является прогрессирование ХСН и нарушений ритма сердца.
Понимание клеточных механизмов действия тиреоидных гормонов на сердечно-сосудистую системы, а также особенностей патогенеза ХСН при дистиреоидизме позволяет не только скорректировать диагностический алгоритм обследования пациентов, включающий исследование уровня тиреоидных гормонов, но и определить дальнейшую тактику ведения больных с ХСН.
Литература
1. Воронков Л.Г. Пацієнт із ХСН в Україні: аналіз даних популяції пацієнтів, обстежених у рамках першого національного зрізового дослідження UNIVERS // Серцева недостатність. – 2012. – С. 6-13.
2. Hunt S.A., Abraham W.T., Chin M.H., for the American College of Cardiology, American Heart Association Task Force on Practice Guidelines, American College of Chest Physicians, International Society for Heart and Lung Transplantation, Heart Rhythm Society ACC/AHA 2005 guideline update for the diagnosis and management of chronic heart failure in the adult: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure): developed in collaboration with the American College of Chest Physicians and the International Society for Heart and Lung Transplantation: endorsed by the Heart Rhythm Society // J Am Coll Cardiol. – 2005. – Vol. 46. – P. e1-e82.
3. Jessup M., Abraham W.T., Casey D.E., 2009 focused update: ACCF/AHA guidelines for the diagnosis and management of heart failure in adults. A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines // J Am Coll Cardiol. – 2009. – Vol. 53. – P. 1343-1382.
4. Lloyd-Jones D., Adams R.J., Writing Group Members American Heart Association Statistics Committee and Stroke Statistics Subcommittee Heart disease and stroke statistics-2010 update: a report from the American Heart Association // Circulation. – 2010. – Vol. 121. – P. e46-e215.
5. Go A.S., Mozaffarian D., Roger V.L. et al. Heart disease and stroke statistics – 2014 update: a report from the American Heart Association. Circulation 2014; 129: e28-292.
6. Heidenreich P.A., Albert N.M., Allen L.A. et al., American Heart Association Advocacy Coordinating Committee, Council on Arteriosclerosis Thrombosis and Vascular Biology, Council on Cardiovascular Radiology and Intervention, Council on Clinical Cardiology, Council on Epidemiology and Prevention, Stroke Council. Forecasting the impact of heart failure in the United States: a policy statement from the American Heart Association // Circ Heart Fail. – 2013. – Vol. 6. – P. 606-619.
7. McMurray J.J., Adamopoulos S., Anker S.D. еt al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC // Eur J Heart Fail. – 2012. – Vol. 14. – P. 803-869.
8. Helfand M. Screening for subclinical thyroid dysfunction in nonpregnant adults: a summary of the evidence for the U.S. Preventive Services Task Force // Ann Intern Med. – 2004. – Vol. 140. – P. 128-141.
9. Canaris G.J., Manowitz N.R., Mayor G., Ridgway E.C. The Colorado thyroid disease prevalence Study // Arch Intern Med. – 2000. – Vol. 160. – P. 526-34.
10. Garmendia M., Santos Palacios S., Guillеn-Grima F., Galofrі J.C. The incidence and prevalence of thyroid dysfunction in Europe: a meta-analysis // J Clin Endocrinol Metab. – 2014. – Vol. 99(3). – P. 923-31.
11. Stone M.B., Wallace R.B. Medicare Coverage of Routine Screening for Thyroid Dysfunction // Washington (DC): National Academies Press (US); 2003 http://www.ncbi.nlm.nih.gov/books/NBK221544/
12. Hollowell J.G., Staehling N.W., Flanders W.D. et al. Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III) // J Clin Endocrinol Metab. – 2002. – Vol. 87. – P. 489-99.
13. Jameson J. Harrison's Principles of Internal Medicine. 17th ed. New York: McGraw-Hill; 2008.
14. Surks M.I., Ortiz E., Daniels G.H. et al. Subclinical thyroid disease: scientific review and guidelines for diagnosis and management // JAMA. – 2004. – Vol. 291. – P. 228-38.
15. Rugge J., Bougatsos C., Chou R. Screening and Treatment of Thyroid Dysfunction: An Evidence Review for the U.S. Preventive Services Task Force // Ann Intern Med. – 2015. – Vol. 162(1). – P. 35-45.
16. Cappola A.R., Fried L.P., Arnold A.M., Thyroid status, cardiovascular risk, and mortality in older adults // JAMA. – 2006. – Vol. 295. – P. 1033-1041
17. Rodondi N., den Elzen W.P., Bauer D.C. et al. Thyroid Studies Collaboration. Subclinical hypothyroidism and the risk of coronary heart disease and mortality // JAMA. – 2010. – Vol. 304. – P. 1365-74.
18. Heeringa J., Hoogendoorn E.H., van der Deure W.M., High-normal thyroid function and risk of atrial fibrillation // Arch Intern Med. – 2008. – Vol. 1168. – P. 2219-2224.
19. Ochs N., Auer R., Bauer D.C. et al. Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality // Ann Intern Med.- 2008. – Vol. 148. – P. 832-45.
20. Gencer B., Collet T.H., Virgini V. et al. Thyroid Studies Collaboration. Subclinical thyroid dysfunction and the risk of heart failure events: an individual participant data analysis from 6 prospective cohorts // Circulation. – 2012. – Vol. 126. – P. 1040-9.
21. Collet T.H., Gussekloo J., Bauer D.C. et al. Thyroid Studies Collaboration. Subclinical hyperthyroidism and the risk of coronary heart disease and mortality // Arch Intern Med. – 2012. – Vol. 172. – P. 799-809.
22. Razvi S., Weaver J.U., Butler T.J., Pearce S.H. Levothyroxine treatment of subclinical hypothyroidism, fatal and nonfatal cardiovascular events, and mortality // Arch Intern Med. – 2012. – Vol. 172. – P. 811-7.
23. Mitchell J.E., Hellkamp A.S., Mark D.B. et al. Thyroid Function in Heart Failure and Impact on Mortality // JCHF. 2013; 1(1): 48-55.
24. Bardy G.H., Lee K.L., Mark D.B., for the SCD-HeFT Investigators Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005; 352: 225-237
25. Pearce E.N., Yang Q., Sawin C.T., Vasan R.S. Relation of thyroid hormone status to incident cardiovascular disease and mortality in the Framingham Heart Study. Proceedings of the Endocrine Society 88th Annual Meeting; Boston, MA; 24-27 June 2006; Endocrine Society Press, Chevy Chase, MD; 2006; abstract 42-1.
26. Nanchen D., Gussekloo J., Westendorp R.G.J. et al. Subclinical Thyroid Dysfunction and the Risk of Heart Failure in Older Persons at High Cardiovascular Risk // JCEM. – 2011. – Vol. 97, Issue 3. – doi.org/10.1210/ jc.2011-1978.
27. Pilo A., Iervasi G., Vitek F. еt al. Thyroidal and peripheral production of 3,5,3'-triiodothyronine in humans by multicompartmental analysis // Am J Physiol 1990. – Vol. 258(4 Pt 1). – P. E715-E726.
28. Bianco A.C., Salvatore D., Gereben B. et al. Biochemistry, cellular and molecular biology, and physiological roles of the iodothyronine selenodeiodinases // Endocr Rev. – 2002. – Vol. 23. – P. 38-89
29. Голицын C.П., Бакалов С.А., Свириденко Н.Ю., Платонова Н.М., Молашенко Н.В., Сердюк С.Е. Кардиальные и эндокринные аспекты применения амиодарона в современной практике лечения нарушений ритма сердца.
30. Everts M.E., Verhoeven F.A., Bezstarosti K. et al. Uptake of thyroid hormones in neonatal rat cardiac myocytes // Endocrinology. – 1996. – Vol. 137. – P. 4235-4242
31. Sabatino L., Iervasi G., Pingitore A. Thyroid hormone and heart failure: from myocardial protection to systemic regulation // Expert Rev. Cardiovasc. Ther. 2014. – P. 1-10.
32. Карась А.С., Обрезан А. Г. Влияние гормонов щитовидной железы на сердце: молекулярные, клеточные, тканевые и органные аспекты (обзор литературы) // Вестник СПбГУ. – 2009. – Сер. 11, вып. 4. – С. 28-35
33. Bianco A.C. Cracking the code for thyroid hormone signaling. Trans Am Clin Climatol Assoc. 2013; 124: 26-35.
34. Senese R., Federica Cioffi F., de Lange P., Goglia F., Lanni A. Thyroid: biological actions of 'nonclassical' thyroid hormones. J Endocrinol. 2014; 221: R1-R12.
35. Vargas-Uricoechea H., Sierra-Torres C.H. Thyroid hormones and the heart // Horm Mol Biol Clin Investig. 2014; 18: 15-26.
36. Kahaly G.J., Dillmann W.H. Thyroid hormone action in the heart // Endocr Rev. 2005; 26: 704-28.
37. Biondi В. Mechanisms in endocrinology: Heart failure and thyroid dysfunction // Eur J Endocrinol. – 2012. – Vol. 167. – P. 609-618.
38. Бланкова З.Н., Агеев Ф.Т., Середенина Е.М. и др. Гипотиреоз и сердечно-сосудистые заболевания // РМЖ. – 2014. – № 13. – С. 980-987.
39. Sawin C.T., Geller A., Wolf P.A. et al. Low serum thyrotropin concentrations as a risk factor for atrial fibrillation in older persons // N Engl J Med. 1994 Nov 10; 331(19): 1249-52.
40. Grais I.M., Sowers J.R. Thyroid and the heart // Am J Med. – 2014. – Vol. 127 (8). – P. 691-8.
41. Trivalle C.I., Doucet J., Chassagne P. et al. Differences in the signs and symptoms of hyperthyroidism in older and younger patients // J Am Geriatr Soc. 1996 Jan; 44(1): 50-3.
42. Аметов А.С., Кониева М.Ю., Лукьянова И.В. Сердечно-сосудистая система при тиреотоксикозе // Consilium Medicum. – 2003. – № 11.
43. Петунина Н.А. Особенности терапии заболеваний щитовидной железы у пациентов с кардиальной патологией // РМЖ. Эндокринология. – 2005. – № 28. – С. 1927-1932.
44. Kim B., Carvalho-Bianco S.D., Larsen P.R. Thyroid hormone and adrenergic signaling in the heart // Arq. Bras. Endocrinol. Metabol. 2004. – V. 48. – № 10. – Р. 171-175.
45. Dahl P., Danzi S., Klein I. Thyrotoxic cardiac disease. Curr Heart Fail Rep. 2008; 5170-6.
46. Pearce E.N., Yang Q., Benjamin E.J., Aragam J., Vasan R.S. Thyroid function and left ventricular structure and function in the Framingham Heart Study. Thyroid. 2010; 20: 369-73.
47. Triggiani V., Iacoviello M. Thyroid disorders in chronic heart failure: from prognostic set-up to therapeutic management. Endocr Metab Immune Disord Drug Targets. 2013; 13: 22-37.
48. Giamouzis G., Pappas D., Simeonidis N. et al. Acute Experimental Hyperthyroidism Does Not Affect Basal and Volume-Induced Atrial Natriuretic Peptide Secretion in Healthy Subjects // Cardiol Res Pract. 2011; 2011: 381865.
49. Коноплева Л.Ф. Хроническая правожелудочковая сердечная недостаточность: дифференцированный подход к лечению // Серце і судини. – 2014. – № 3. – С. 102-110.
50. Воронков Л.Г. Хроническая сердечная недостаточность: Пособие для кардиологов в таблицах и схемах. – К.: ТОВ «Инфо-Ф», 2002. – 136 с.
51. Marvisi M., Balzarini L., Mancini C., Mouzakiti P. Thyroid gland and pulmonary hypertension. What's the link? // Panminerva Med. 2013 Mar; 55(1): 93-7.
52. Hegazi M.O., El Sayed A. El Ghoussein H. Pulmonary hypertension responding to hyperthyroidism treatment // Respirology. 2008 Nov; 3(6): 23-5.
53. Vоke H. Schwahn C. Wallaschofski H., Dоrr M. Review: the association of thyroid dysfunction with all-cause and circulatory mortality: is there a causal relationship? Journal of Clinical Endocrinology and Metabolism. – 2007; 92 2421-429.
54. Brandt F., Green A., Hegedus L., Brix T.H. A critical review and meta-analysis of the association between overt hyperthyroidism and mortality // Eur J Endocrinol. 2011 Oct; 165(4): 491-7.
55. Biondi B. Should we treat all subjects with subclinical thyroid disease the same way? European Journal of Endocrinology 2008; 159; 343-45.
56. Yang L.B., Jiang D.Q., Qi W.B., Zhang T. еt al. Subclinical hyperthyroidism and the risk of cardiovascular events and all-cause mortality: an updated meta-analysis of cohort studies // Eur J Endocrinol. 2012 Jul; 167(1): 75-84.
57. Frost L., Vestergaard P. & Mosekilde L. Hyperthyroidism and risk of atrial fibrillation or flutter: a population-based study. Archives of Internal Medicine 2004;164 1675-1678.
58. Siu C.W., Yeung C.Y., Lau C.P. et al. Incidence, clinical characteristics and outcome of congestive heart failure as the initial presentation in patients with primary hyperthyroidism // Heart. – 2007. – Vol. 93. – P. 483-487.
59. Squizzato A., Gerdes V.E., Brandjes D.P., Buller H.R. & Stam J. Thyroid diseases and cerebrovascular disease // Stroke. – 2005. – Vol. 36. – P. 2302-2310.
60. Lin H.C., Yang L.Y. & Kang J.H. Increased risk of pulmonary embolism among patients with hyperthyroidism: a 5-year follow-up study // J. Thrombosis and Haemostasis. – 2010. – Vol. 8. – P. 2176-2181.
61. Biondi B. & Kahaly G.J. Cardiovascular involvement in patients with different causes of hyperthyroidism. Nature Reviews. Endocrinology 2010; 6; 431-443.
63. Шульгина В.Ю., Фадеев В.В., Мельниченко Г.А. Поражение миокарда при тиреотоксикозе: особенности течения, исходы, отдаленный прогноз // Клин. и экспер. тиреодол. – 2006. – Т. 2, № 4. – С. 21-30.
64. Шульгина В.Ю., Мельниченко Г.А., Сыркин А.Л и соавт. Прогностические факторы неблагоприятного исхода тиреотоксической кардиомиопатии // Кардиология. – 2007. – № 11. – С. 21-30.
65. Гома Т.В., Хамнуева Л.Ю., Орлова Г.М. Клинико-иммунологические аспекты поражения сердечно-сосудистой системы у больных с болезнью Грейвса и хронической сердечной недостаточностью // Клиническая и экспериментальная тиреодолошия. – 2011. – № 3. – С. 42-47.
66. Galli E., Pingitore A., Iervasi G. The role of thyroid hormone in the pathophysiology of heart failure: clinical evidence. Heart Fail Rev. 2010; 155-69.
67. Forfar J., Muir A.L., Sawers S.A. & Toft A.D. Abnormal left ventricular function in hyperthyroidism: evidence for a possible reversible cardiomyopathy. New England Journal of Medicine 1982; 307; 1165-1175.
68. Soh M.C., Croxson M. Fatal thyrotoxic cardiomyopathy in a young man. BMJ 2008; 337: 531.
69. Платонова Н.М., Молашенко Н.В., Абдулхабирова Ф.М., Трошина Е.А. Йодиндуцированные заболевания щитовидной железы // Consilium medicum. – 2013. – Т. 15, № 4. – С. 67-69.
70. Calо L., De Ruvo E., Sette A. et al. Tachycardia-induced cardiomyopathy: mechanisms of heart failure and clinical implications // J Cardiovasc Med (Hagerstown). – 2007. – Vol. 8 (3). – P. 138-43.
71. Зубкова С.Т. Актуальные проблемы сердечно-сосудистых нарушений при тиреотоксикозе // Здоров'я України. Темат. номер «Эндокринология». – 2014. – № 3. – С. 44-45.
72. Карась А.С. Изменение метаболизма, структуры и функции сердца при гипотиреозе и гипертиреозе // Автореф... канд. мед. н. – Санкт-Петербург, 2011. – 26 с.
73. Fazio S., Palmieri E.A., Lombardi G. & Biondi B. Effects of thyroid hormone on the cardiovascular system // Recent Progress in Hormone Research. – 2004. – Vol. 59. – P. 31-50.
74. Mourouzis I., Forini F. Thyroid Hormone and Cardiac Disease: From Basic Concepts to Clinical Application // J. Thyroid Research. – 2011. – Vol. 2011 http://www.hindawi.com/journals/jtr/2011/958626/
75. Monzani F., Caraccio N., Kozakowa M., Dardano A., Vittone F., Virdis A. et al. Effect of levothyroxine replacement on lipid profile and intima-media thickness in subclinical hypothyroidism: a double-blind, placebo-controlled study // J Clin Endocrinol Metab. 2004; 89 (5): 2099-106.
76. Пeтунинa Н.A., Трухинa Л.В. Бoлeзни щитoвиднoй жeлeзы. – М., 2011. – 216 c.
77. Tang Y.D., Kuzman J.A., Said S. et al. Low thyroid function leads to cardiac atrophy with chamber dilatation, impaired myocardial blood flow, loss of arterioles, and severe systolic dysfunction // Circulation. – 2005. – Vol. 112. – P. 3122-3130.
78. Fatourechi V. Subclinical hypothyroidism: an update for primary care physicians // Mayo Clin Proc. – 2009. – Vol. 84(1). – P. 65-71.
79. Klein I. Endocrine disorders and cardiovascular disease In: Bonow R.O., Mann D.L., Zipes D.P., Libby P. Braunwald's Heart Disease: а textbook of cardiovasculae medicine, 8th ed. Philadelphia: Saunders Elsevier, 2008. Рp. 2033-47.
80. Тарасова А.А. Особенности состояния сердца у детей при заболеваниях щитовидной железы // Вестник Российского научного центра рентгенорадиологии. – 2007. – Вып. 7.
81. Петунина Н.А. Сердечно-сосудистая система при заболеваниях щитовидной железы // Сердце. – 2003. – Т. 2. – № 6 (12). – С. 272-279.
82. Мадиярова М.Ш., Моргунова Т.Б., Фадеев В.В. и др. Особенности клинической картины, показателей качества жизни и когнитивных функций у пациенток с гипотиреозом разной этиологии // клиническая и экспериментальная тиреоидология. – 2014. – Т. 10, № 1. – С. 44-54.
83. Бланкова З.Н. Влияние терапии левотироксином на клинический, гемодинамический и нейрогуморальный статус больных хронической сердечной недостаточностью с сохранной систолической функцией левого желудочка в сочетании с субклиническим гипотиреозом // Автореф… канд. мед. н., Москва, 2012, 25 с.
84. Liu Y., Sherer B.A., Redetzke R.A., Gerdes Am. M. Regulation of arteriolar density in adult myocardium during low thyroid conditions // Vascular. Pharmacol. 2010. Vol. 52. P. 146-150.
85. Pol C.J., Muller A., Zuidwijk M.J. et al. Left-ventricular remodeling after myocardial infarction is associated with a cardiomyocyte-specific hypothyroid condition // Endocrinology. 2011 Feb; 152(2): 669-79.
86. Hernando V.U., Eliana M.S. Role of thyroid hormones in different aspects of cardiovascular system // Endocrinol Metab Synd. – 2015. – Vol. 4. – P. 1-13.
87. Василенко В.Х., Фельдман С.Б., Хитров Н.К. Миокардиодистрофия. – «Медицина», 1989, 272 с.
88. Бирюкова Е.В. Гипотиреоз: как вовремя диагностировать и эффективно лечить? // Справочник поликлинического врача. – 2013. – № 11.
89. Kabadi U.M., Kumar S.P. Pericardial effusion in primary hypothyroidism // Am Heart J. 1990 Dec; 120 (6 Pt 1): 1393-5.
90. Tudoran C., Tudoran M., Avram R. et al. Particularities of pericardial effusion in patients with hypothyroidism // Journal of Experimental Medical & Surgical Research. – 2011. – № 4. – P. 176-179.
91. Bakiner O.1., Ertorer M.E., Haydardedeoglu F.E. et al. Subclinical hypothyroidism is characterized by increased QT interval dispersion among women // Med Princ Pract. 2008; 17 (5): 390-4.
92. Galetta F., Franzoni F., Fallahi P., et al. Changes in heart rate variability and QT dispersion in patients with overt hypothyroidism. Eur J Endocrinol 2008; 158: 85-90.
93. Yadav B.S., Gupta B., Bharani A.K. Long QT interval and torsades de pointes in hypothyroidism. Indian Heart J 1995; 47: 261-262.
94. Вербовой А.Ф. Синдром гипотиреоза // Фарматека. – 2015. – № 10. – С. 8-11.
95. Rhee C.M., Curhan G.C., Alexander E.K., et al. Subclinical hypothyroidism and survival: the effects of heart failure and race // J Clin. Endocrinol. Metab. – 2013. – Vol. 98. – P. 2326-2336.
96. Gerdes A.M., Iervasi G. Thyroid replacement therapy and heart failure // Circulation. – 2010. – Vol. 122. – P. 385-393.
97. Lee S.C., Stevens T.L., Sandberg S.M. et al. The potential of brain natriuretic paptide a biomarker for New York Heart Association class during the outpatient treatment of heart failure // J. Card. Fail. – 2002. – Vol. 8. – P. 149-154.
98. Christ-Crain M., Morgenthaler N.G., Meier C. et al. Pro-A-type and N-terminal pro-B-type natriuretic peptides in different thyroid function states // Swiss Med Wkly. – 2005. – Vol. 135 (37-38). – P. 549-554.
99. Ozmen B., Ozmen D., Parildar Z. Serum N-terminal-pro-B-type natriuretic peptide (NT-pro-BNP) levels in hyperthyroidism and hypothyroidism // Endocr. Res. – 2007. – Vol. 32 (1-2). – P. 1-8.
100. Schultz M., Faber J., Kistorp C. et al. N-terminal-proB-type natiuretic peptide (NT-pro-BNP) in different thyroid function states // Clin. Endocrin. – 2004. – Vol. 60. – P. 54-59.
101. Manuchehri A.M., Jayagopal V., Kilpatrick E.S., Atkin S.L. The effect of thyroid dysfunction on N-terminal pro-B-type natriuretic peptide concentrations // Ann. Clin. Biochem. – 2006. – Vol. 43 (Pt 3). – P. 184-188.
102. Custro N., Scafidi V., Lo Baido R. et al. A. Subclinical hypothyroidism resulting from autoimmune thyroiditis in female patients with endogenous depression // J. Endocrinol. Iinvestig. – 1994. – Vol. 17. – № 8. – P. 641-646.