18 травня, 2016
Сучасні можливості функціональної діагностики в кардіологічній практиці
17 березня відбулася IV Науково-практична конференція «Функціональна діагностика серцево-судинних хвороб», організована кафедрою функціональної діагностики Національної медичної академії післядипломної освіти ім. П.Л. Шупика та ДУ «Інститут серця МОЗ України».
У конференції взяли участь понад 260 лікарів з переважної більшості областей України.
Конференцію відкрив генеральний директор ДУ «Інститут серця МОЗ України», член-кореспондент НАМН України, професор кафедри функціональної діагностики НМАПО ім. П.Л. Шупика Борис Михайлович Тодуров. У першій частині конференції провідні вітчизняні фахівці представили доповіді, присвячені відомим, але недооціненим проблемам кардіології, а також клінічні випадки, які ілюструють роль функціональних методів у диференційній діагностиці коморбідної серцево-судинної патології.
 Завідувач кафедри променевої діагностики факультету післядипломної освіти Львівського національного медичного університету ім. Данила Галицького, президент Української асоціації фахівців з електрокардіографії, доктор медичних наук, професор Юрій Андрійович Іванів висвітлив ехокардіографічні та клінічні аспекти феномена відкритого овального вікна (ВОВ).
Завідувач кафедри променевої діагностики факультету післядипломної освіти Львівського національного медичного університету ім. Данила Галицького, президент Української асоціації фахівців з електрокардіографії, доктор медичних наук, професор Юрій Андрійович Іванів висвітлив ехокардіографічні та клінічні аспекти феномена відкритого овального вікна (ВОВ).
Відкрите овальне вікно – це щілина між первинною та вторинною частинами міжпередсердної перегородки (МПП), які накладаються одна на одну, але не зрощені між собою. Фізіологічне значення ВОВ у періоді внутрішньоутробного розвитку пов’язане з особливостями кровообігу плода і полягає у пропусканні артеріальної оксигенованої крові (яка надходить від плаценти) з правого передсердя у ліві відділи серця. Після народження тиск у лівому передсерді підвищується, овальне вікно закривається і в більшості випадків заростає. У дорослих незарощене овальне вікно виявляють у 10-18% випадків, за даними ехокардіографії (ЕхоКГ) з контрастуванням. Ознакою ВОВ на трансторакальній ЕхоКГ (ТТЕ) є перпендикулярний до МПП струмінь крові між передсердями, частіше спрямований зліва направо, відповідно до градієнта тиску. Переваги черезстравохідної ЕхоКГ (ТЕЕ) перед ТТЕ беззаперечні: за даними A.C. Pearson (1991), серед 238 обстежених осіб із застосуванням контрасту при ТЕЕ виявили ВОВ у 22% випадків, тоді як при ТТЕ – у 8%.
Доповідач застеріг від гіпердіагностики ВОВ, яка спостерігається у повсякденній практиці. За нормального градієнта тиску між передсердями ВОВ не має клінічного значення, хоча в реальному житті лікарі часто рекомендують таким пацієнтам обмеження фізичної активності. Діагноз ВОВ, встановлений дитині, викликає занепокоєння батьків, і вони шукають можливості оперативного лікування, хоча досить часто у процесі спостереження ВОВ спонтанно закривається.
Міжпередсердне сполучення може ставати небезпечним щодо розвитку тромбоемболій лише за наявності право-лівого шунтування крові. Це відбувається тоді, коли тиск у правому передсерді вищий, ніж у лівому. Причинами можуть бути легенева гіпертензія, правошлуночкова недостатність з підвищеним кінцево-діастолічним тиском, інфаркт міокарда (ІМ) правого шлуночка (ПШ), подібні до проби Вальсальви ситуації: продування «закладених» вух, сечовипускання або дефекація з напруженням, кашель, чхання.
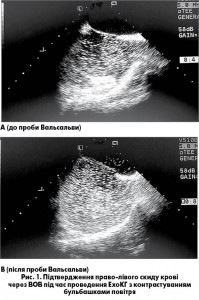
Підтвердити право-лівий скид крові допомагає бульбашкове контрастне ЕхоКГ-дослідження. Через периферичну вену у кровообіг вводиться 8 мл фізіологічного розчину, який збовтали разом з 1 мл крові пацієнта й 1 мл повітря. У цей момент візуалізують МПП і ліве передсердя. Хворого просять покашляти або натужитися (проба Вальсальви). Якщо протягом трьох спроб після заповнення бульбашками правого передсердя 2-5 бульбашок з’являються у лівому передсерді, наявність право-лівого шунтування слід вважати підтвердженою (рис. 1А та 1В).
Рідкісна знахідка на ЕхоКГ – тромб, що застряг у овальному вікні на межі передсердь. Зазвичай він має видовжену форму, і його вільні кінці звиваються за потоками крові. Це ургентний стан: тромб потребує якнайшвидшого видалення, оскільки в будь-який момент його частинки можуть відірватися і потрапити у велике коло кровообігу.
Парадоксальна емболія тромбами, які потрапляють з венозного русла у велике коло кровообігу крізь ВОВ, може бути причиною ішемічних інсультів та артеріальних емболій іншої локалізації, а також часто виникає одночасно з тромбоемболією легеневої артерії. За даними американських дослідників, ВОВ з парадоксальною емболією є причиною 20-30% криптогенних інсультів, тобто тих, для яких не встановлено інші причини емболізації мозкових судин. Враховуючи, що криптогенні інсульти становлять 35-40% у етіопатогенетичній структурі мозкових катастроф, парадоксальною емболією може бути зумовлений кожний десятий випадок інсульту.
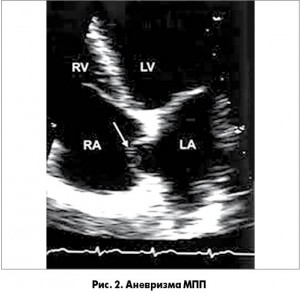
Ще один ЕхоКГ-феномен – аневризма МПП. Частота його виявлення при ТТЕ оцінюється у 0,2%, при ТЕЕ – 3-8%. Аневризма візуалізується як завелика і дуже рухлива мембранозна частина МПП, яка випинається в те передсердя, де тиск менший (рис. 2). Розмір основи має становити не менше 15 мм, випинання – не менше 10 мм. Аневризми МПП у 77% випадків поєднуються з ВОВ чи дефектом МПП, і лише тоді вони становлять загрозу як причина парадоксальної емболії.
Тяжкість вади і показання до лікування чи оперативного втручання з метою усунення дефекту МПП визначаються ступенем гемодинамічних розладів та/або несприятливим прогнозом, а не лише фактом наявності сполучення між передсердями. Іншими словами, важливим є не розмір дефекту, а кількість крові, яка шунтується за серцевий цикл. У реальній практиці ВОВ дуже рідко потребує закриття оклюдерами. Але у разі право-лівого скиду крові та за наявності умов тромбоутворення у венозному руслі ВОВ становить реальну загрозу розвитку тромбоемболічних подій.
 Доцент кафедри променевої діагностики НМАПО ім. П.Л. Шупика, кандидат медичних наук Наталія Миколаївна Носенко охарактеризувала можливості сучасних методів функціональної діагностики в пошуку причин ішемічних інсультів, керуючись положеннями виданого на початку цього року керівництва Американського товариства ехокардіографії з пошуку серцевих джерел емболії (J Am Soc Echocardiogr 2016; 29: 1-42).
Доцент кафедри променевої діагностики НМАПО ім. П.Л. Шупика, кандидат медичних наук Наталія Миколаївна Носенко охарактеризувала можливості сучасних методів функціональної діагностики в пошуку причин ішемічних інсультів, керуючись положеннями виданого на початку цього року керівництва Американського товариства ехокардіографії з пошуку серцевих джерел емболії (J Am Soc Echocardiogr 2016; 29: 1-42).
У структурі ішемічних інсультів від 15 до 40% становлять кардіоемболічні інсульти (КІ). Для КІ характерні висока смертність, гірший потенціал відновлення та високий ризик рецидиву, тому важливо знайти джерела емболії для розробки плану вторинної профілактики. Серед причин КІ левову частку (50%) становить фібриляція передсердь (ФП), приблизно по 10% – хронічна ревматична хвороба серця, тромби лівого шлуночка (ЛШ) і гострий інфаркт міокарда (ГІМ). Ще 5% КІ зумовлені тромбозом протезованих клапанів, решта 15% – іншою патологією серця (розшаровуюча аневризма аорти, синдром слабкості синусового вузла та ін.).
Під час збору анамнезу та клінічного обстеження на користь кардіогенної емболії можуть вказувати попередні епізоди ФП, дисфункція синусового вузла, ознаки застійної серцевої недостатності (СН), тромбози глибоких вен, перенесений ІМ (ризик розвитку церебральних емболій максимальний у перші 4 тижні), супутні захворювання (системний червоний вовчак, ендокардит Лібмана-Сакса, новоутворення).
Усім пацієнтам із КІ обов’язково слід виконати ультразвукове дослідження судин голови та шиї, електрокардіографію (ЕКГ) та холтерівське моніторування ЕКГ протягом 24 год, незалежно від ритму і наявності чи відсутності скарг, для виявлення порушень ритму, у тому числі асимптомних і прихованих, які можуть бути причиною інсульту.
При ЕхоКГ одні знахідки слід інтерпретувати як можливі причини КІ, а інші мають менше значення. З високим ризиком тромбоемболії асоціюються ФП, ГІМ, кардіоміопатії, аневризма ЛШ з тромбозом та інші внутрішньосерцеві утворення (пухлини, фіброеластома), ревматичні ураження клапанів (мітральний стеноз), протезовані клапани, інфекційний ендокардит (ІЕ), атеросклеротичні бляшки дуги аорти. З невисоким ризиком тромбоемболії пов’язані пролапс мітрального клапана, кальциноз мітрального кільця, кальцинований аортальний стеноз, розростання Lambl (ниткоподібні утворення на шлуночковому боці аортального і мітрального клапанів), нетромбована аневризма ЛШ, ВОВ або аневризми МПП за відсутності шунтування крові справа наліво. Для перерахованих станів і утворень зв’язок із розвитком КІ не доведено або він незначний. Але слід пам’ятати, що при поєднанні патологічних станів, прогресуванні дилатації порожнин і систолічної дисфункції серця або приєднанні ФП ризик розвитку тромбоемболій різко зростає. Високий ембологенний потенціал має поєднання аневризми МПП із ВОВ і право-лівим скидом крові. Золотий стандарт діагностики ВОВ – черезстравохідна ЕхоКГ або бульбашковий тест при ТТЕ. Доцільність оперативного закриття ВОВ з метою профілактики інсультів залишається суперечливою, оскільки метааналіз досліджень із застосуванням оклюдерів не продемонстрував користі (B.S. Wessler et al., 2015).
У хворих на ГІМ умови тромбоутворення та емболії є дуже варіабельними. У перші 10 днів внутрішньопорожнинний тромбоз виявляють у 5-40% випадків, здебільшого при передньому чи верхівковому ураженні (тромбоутворенню сприяє порушення скоротливості міокарда). Ризик зростає при систолічній дисфункції, повторному ІМ, за наявності великого рубця. При хронічній аневризмі ЛШ тромб формується у половині випадків. У діагностиці тромбів ЛШ вищу чутливість має трансторакальна ЕхоКГ порівняно з трансезофагеальною. Контрастування та тривимірний режим покращують візуалізацію. Ризик емболізації периферичних судин, імовірно, є вищим при більших розмірах тромба, при виступаючих у порожнину шлуночка мобільних тромбах. Такі хворі мають отримувати антикоагулянти. Слід враховувати, що протягом перших місяців після ГІМ близько 40% тромбів змінюють свою форму, 29% змінюють рухливість, відповідно, змінюється і ризик емболій.
ЕхоКГ має бути виконана у хворих із відомою або підозрюваною кардіоміопатією (КМП). Високий ризик розвитку КІ асоціюється з дилатацією і дисфункцією ЛШ, спонтанним контрастуванням. Дилатаційна КМП (ДКМП) часто супроводжується ФП, яка є фактором високого ризику розвитку інсульту. При ендоміокардіальному фіброзі тромб може утворюватися навіть за нормальної рухливості стінки і в ПШ, і в ЛШ. Частота емболій при ДКМП сягає 18%. Тромбоутворення також можливе при гіпертрофічній КМП (ГКМП) із дискінезом верхівки. Пацієнтам з ГКМП навіть при синусовому ритмі обов’язково необхідно проводити холтерівський моніторинг ЕКГ протягом 48 год 1 раз на 6 міс для виявлення епізодів ФП, які розвиваються внаслідок дилатації лівого передсердя.
Джерелом тромбоемболії можуть бути штучні клапани серця. Незважаючи на прийом антикоагулянтів, тромбоз механічних клапанів спостерігається з частотою 1-2% на рік, біопротезів – 0,5-1% на рік. До тромбозу більш схильні мітральний та тристулковий клапани, тоді як ІЕ частіше уражається клапан аорти. Першим кроком діагностичного пошуку у хворих із протезованими клапанами при емболічній події (інсульті) має бути трансторакальна ЕхоКГ, а при нейтральному результаті показана черезстравохідна ЕхоКГ. Повторні ТТЕ або ТЕЕ рекомендуються після тромболітичної або антикоагулянтної терапії.
Частота емболій у пацієнтів з ІЕ сягає 43%. ТТЕ має низьку чутливість, але високу специфічність у діагностиці ІЕ. ТЕЕ має бути виконана при негативних результатах ТТЕ за наявності клінічних ознак ІЕ, також черезстравохідному дослідженню слід віддавати перевагу у хворих із протезованими клапанами. Повторні ТТЕ або ТЕЕ рекомендуються через 7 днів у разі негативних результатів первинного обстеження і збереження клінічної підозри на ІЕ.
ТТЕ або ТЕЕ дозволяють встановити чіткі предиктори емболізації у хворих на ІЕ:
- вегетації на клапанах (погано візуалізуються вегетації до 2 мм, а також за наявності пролапсу мітрального клапана з ущільненням);
- формування абсцесу;
- виражена рухливість вегетацій, розмір вегетацій >10-15 мм.
У хворих, що перенесли інсульт, частіше виявляють ураження мітрального клапана, особливо передньої стулки. Частіше призводить до інсульту ІЕ в комбінації з ВОВ (відкритий шлях для потрапляння емболів у велике коло). Високий ризик емболізації характерний для ІЕ, викликаних Streptococcus bovis, Streptococcus aureus, грибами. Ризик розвитку нових емболій найвищий протягом перших днів антибактеріальної терапії і зменшується після 2 тижнів.
Таким чином, ретельний збір анамнезу, клінічне обстеження, застосування методів холтерівського моніторингу ЕКГ та ЕхоКГ у більшості випадків дозволяють ідентифікувати джерела емболії та запобігати повторенню тромбоемболічних ускладнень.
 Доцент кафедри променевої діагностики ФПО Львівського національного медичного університету ім. Данила Галицького, кандидат медичних наук Михайло Степанович Сороківський охарактеризував клінічні та електрокардіографічні прояви синдрому електрокардіостимулятора (ЕКС).
Доцент кафедри променевої діагностики ФПО Львівського національного медичного університету ім. Данила Галицького, кандидат медичних наук Михайло Степанович Сороківський охарактеризував клінічні та електрокардіографічні прояви синдрому електрокардіостимулятора (ЕКС).
Синдром ЕКС – це комплекс симптомів, причиною яких є низка клінічних, гемодинамічних чи електрофізіологічних розладів, пов’язаних із тривалою електричною стимуляцією серця. Переважна більшість зарубіжних публікацій щодо синдрому ЕКС стосується однокамерної стимуляції в режимі VVI (стимуляція ПШ на вимогу), оскільки саме однокамерні пристрої історично були першими й упродовж тривалого часу домінували у клінічній практиці. У наш час більшість брадиаритмій для свого лікування потребують двокамерної передсердно-шлуночкової стимуляції (DDD або DDDR – з функцією частотної адаптації), а єдиним показанням до стимуляції VVI залишається брадисистолічна ФП. Однак в Україні за відсутності страхової медицини та за умов недостатнього бюджетного фінансування закупівель медичних приладів нерідко пацієнтам доводиться самостійно сплачувати за ЕКС. Більшість хворих за власний кошт можуть дозволити собі лише однокамерні пристрої, тому проблема синдрому ЕКС, зумовленого недоліками режиму VVI, для нас залишається актуальною. За даними Львівського обласного кардіологічного центру, які навів доповідач, співвідношення встановлених однокамерних ЕКС до двокамерних у 2015 році становило 3:2.
Причини розвитку синдрому ЕКС, пов’язані з недоліками стимуляції VVI, – це асинхронність роботи передсердь і шлуночків, некоректно підібрана базова (мінімальна) частота серцевих скорочень (ЧСС), відсутність частотної адаптації (не в усіх приладах).
Симптоми і скарги хворих при синдромі ЕКС можна розділити на групи:
- неврологічні – запаморочення, передсинкопальні стани;
- психічні – апатія, дратівливість, тривога;
- ознаки зниження серцевого викиду та СН – втомлюваність, задишка, ортопное, пароксизмальна нічна ядуха, задишка, набряки нижніх кінцівок;
- симптоми гіпотензії – пітливість, ортостатичні реакції;
- гемодинамічні ознаки – пульсація в шиї, животі, відчуття серцебиття або перебоїв у роботі серця;
- інші – головний біль, біль у нижній щелепі, у грудній клітці.
Доповідач зауважив, що всі перераховані клінічні прояви є неспецифічними і потребують диференційної діагностики. Симптоми можуть бути зумовлені прогресуванням СН, яке не пов’язане з роботою ЕКС, змінами в лікуванні (наприклад, збільшенням дози антигіпертензивних препаратів), пароксизмами фібриляції/тріпотіння передсердь.
Патофізіологічними причинами синдрому ЕКС є втрата передсердного вкладу у серцевий викид (у нормі 15-20%), скорочення передсердь при закритих атріовентрикулярних (АВ) клапанах, підвищення тиску в передсердях, підвищена продукція натрійуретичних пептидів, ретроградне АВ проведення, нефізіологічний спосіб активації міокарда ПШ (електрод імплантується у верхівку).
Під час об’єктивного обстеження можна виявити такі ознаки синдрому ЕКС: гіпотензія, тахіпное, зниження сатурації кисню, варіабельність наповнення пульсу, нестабільні показники при повторних вимірюваннях артеріального тиску, видиме потовщення і пульсація шийних вен, застійні хрипи в легенях, шуми регургітації та варіабельність серцевих тонів, відчуття пульсації печінки, її збільшення, чутливість при пальпації, пастозність і набряки нижніх кінцівок.
Частоту виникнення синдрому ЕКС різні автори оцінюють від 7 до 18%, чутливість залежить від оцінки симптомів (Furman, 1985; M.S. Link et al., 2004). Найчастіше синдром ЕКС проявляється у перший рік після встановлення пристрою. За даними D. Heldman і співавт. (1990), під час ретельного опитування симптоми, характерні для синдрому ЕКС, було зареєстровано у 83% пацієнтів з однокамерним стимулятором у режимі VVI. N. Sulke і співавт. (1992) спостерігали покращення стану у 75% пацієнтів після заміни стимулятора VVI на DDD.
Синдром ЕКС також може виникати при стимуляції в режимі DDD. Причинами можуть бути некоректно підібраний час АВ затримки, пейсмейкерна тахікардія за механізмом re-entry, некоректно встановлена мінімальна або максимальна ЧСС. Крім того, не завжди є можливість частотної адаптації стимулятора.
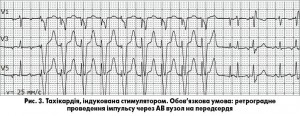
Найчастіше виникає тахікардія, індукована стимулятором (рис. 3).
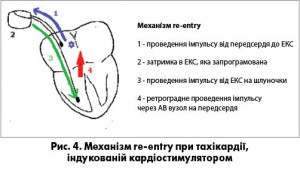
Обов’язкова умова – ретроградне проведення імпульсу через АВ вузол на передсердя. Механізм має чотири етапи (рис. 4).
Лектор наголосив на ЕКГ-особливостях тахікардії, індукованої ЕКС:
- форма комплексів QRS аналогічна таким, як при нормальній роботі ЕКС;
- перед кожним QRS тахікардії є спайк стимулятора;
- ЧСС становить переважно 120-140 уд/хв.
Клінічні особливості тахікардії, індукованої ЕКС:
- виявляється рідко, зазвичай при холтерівському моніторуванні ЕКГ;
- відносно легко переноситься пацієнтом;
- припиняється спонтанно;
- потребує диференційної діагностики з іншими тахікардіями з широким комплексом QRS;
- найкраще лікується зміною налаштувань ЕКС.
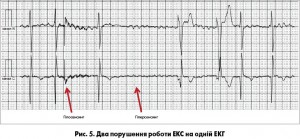
Синдром ЕКС слід відрізняти від порушень функції стимулятора. Найчастіше це гіпосенсинг: стимулятор не сприймає спонтанного імпульсу, і стимулюючий розряд (спайк на ЕКГ) з’являється там, де його не має бути. Можливий також гіперсенсинг: стимулятор сприймає як імпульс іншу подію, і спайк не з’являється там, де він має виникнути. Інколи обидва порушення можна спостерігати на одній ЕКГ (рис. 5).
До порушень роботи ЕКС належить відсутність нав’язування, коли за нормальним вчасним імпульсом стимулятора немає відповідного скорочення міокарда. Розпочинати лікування таких станів потрібно з перепрограмування ЕКС, яке в більшості випадків є ефективним.
Таким чином, під час огляду пацієнта з ЕКС лікаря має найбільше цікавити самопочуття пацієнта. За відсутності порушень роботи стимулятора, захворювань та станів, які можуть зумовити відповідні симптоми, слід запідозрити синдром ЕКС. Більшість випадків синдрому ЕКС можна усунути шляхом перепрограмування пристрою або заміни на двокамерний ЕКС.
 Головний позаштатний спеціаліст з функціональної діагностики Харківської області, завідувач відділення функціональної діагностики Харківської обласної клінічної лікарні Тетяна Олександрівна Загубіженко доповіла про результати впровадження дистанційної діагностики ЕКГ за системою «Телекард».
Головний позаштатний спеціаліст з функціональної діагностики Харківської області, завідувач відділення функціональної діагностики Харківської обласної клінічної лікарні Тетяна Олександрівна Загубіженко доповіла про результати впровадження дистанційної діагностики ЕКГ за системою «Телекард».
Діагностичний комплекс «Телекард» складається з портативного електрокардіографа та пристрою зв’язку для передачі даних (мобільний або стаціонарний телефон). Запис ЕКГ передається з місця надання первинної медичної допомоги (фельдшерсько-акушерський пункт, амбулаторія, районна поліклініка) до закладів вторинного або третинного рівня – районних лікарень та обласної лікарні, де встановлено базові станції прийому ЕКГ і чергують лікарі, здатні надавати консультативну допомогу. Портативні телеметричні пристрої також використовують сімейні лікарі та бригади швидкої медичної допомоги під час роботи на викликах.
Дистанційна передача ЕКГ допомагає вирішувати такі завдання:
- рання діагностика гострого коронарного синдрому, швидке прийняття рішення про евакуацію хворого з ГІМ та проведення тромболізису;
- оперативне вирішення питання про госпіталізацію хворих до лікувальних закладів відповідного рівня;
- вибір тактики лікування на місцях та контроль її ефективності за даними повторних ЕКГ;
- адміністративні: контроль кількості зареєстрованих серцево-судинних подій, особливостей їх перебігу, своєчасності та якості надання допомоги;
- навчальні: спільний розбір діагностично складних випадків.
У Харківській області телемедицина впроваджується з 2013 року. На сьогодні діють 804 діагностичні комплекси «Телекард». 2013 року за допомогою дистанційної передачі ЕКГ було діагностовано 1111 інфарктів – половина всіх ІМ, які діагностували в області. 2015 року діагностовано 606 ІМ, а всього виконано 18 850 передач ЕКГ. Завершуючи доповідь, фахівець висловила думку, що подальший розвиток телемедицини має стати одним із пріоритетів удосконалення кардіологічної допомоги в Україні.
Асистент кафедри функціональної діагностики НМАПО ім. П.Л. Шупика Наталія Юріївна Васильєва на клінічних прикладах продемонструвала можливості електроенцефалографії (ЕЕГ) у пошуку причин синкопальних станів, які супроводжують порушення серцевого ритму та інші захворювання серця.
 Причини істинного синкопе різноманітні: близько 60% випадків зумовлені вазовагальними рефлексами, 15% є ортостатичними, 10% пов’язані з аритміями, 5% – з патологією серця та легенів, але причина 10% випадків короткочасної втрати свідомості залишається не встановленою. У клінічній практиці найчастіше потребують диференційної діагностики скарги на запаморочення та короткочасну втрату свідомості, які не відповідають критеріям судомного нападу, виникають за відсутності органічного ураження мозку і не пояснюються наявними порушеннями серцевого ритму чи іншими захворюваннями.
Причини істинного синкопе різноманітні: близько 60% випадків зумовлені вазовагальними рефлексами, 15% є ортостатичними, 10% пов’язані з аритміями, 5% – з патологією серця та легенів, але причина 10% випадків короткочасної втрати свідомості залишається не встановленою. У клінічній практиці найчастіше потребують диференційної діагностики скарги на запаморочення та короткочасну втрату свідомості, які не відповідають критеріям судомного нападу, виникають за відсутності органічного ураження мозку і не пояснюються наявними порушеннями серцевого ритму чи іншими захворюваннями.
Це ілюструє наведений нижче клінічний випадок. Хвора 1936 року народження, пенсіонерка, звернулася до клініки Інституту серця за направленням з поліклініки за місцем проживання зі скаргами на біль у ділянці серця стискаючого характеру, який супроводжується відчуттям тривоги (тривалість нападів 1-2 хв, купіруються валідолом), задишку під час фізичного навантаження, запаморочення.
За результатами обстеження було встановлено клінічний діагноз: ішемічна хвороба серця (стенокардія напруги IIІ функціонального класу), дифузний кардіосклероз, недостатність мітрального та трикуспідального клапанів І ступеня, повна АВ блокада, гіпертонічна хвороба II стадії, 3 ступеня, ризик 3 (високий), СН ІІА стадії зі збереженою ФВ (56%).
Періодичні епізоди втрати свідомості були розцінені як напади Морганьї-Адамса-Стокса, зумовлені повною АВ блокадою (частота скорочень передсердь 60/хв, шлуночків – 35/хв). Після успішної імплантації двокамерного ЕКС з режимом стимуляції DDD, корекції антигіпертензивної та антиангінальної терапії хвора була виписана з покращенням стану. Але через 6 тижнів вона знову звернулася зі скаргами, типовими для стенокардії, та з приводу повторних епізодів втрати свідомості. При більш детальному розпитуванні хвора повідомила неврологу, що напади почастішали до 6 разів за останні 1,5 міс і навіть призвели до падіння та травми голови. Ознак гострої вогнищевої патології ЦНС невролог не виявив. Під час повторного кардіологічного обстеження було встановлено неефективність роботи штучного водія ритму внаслідок дислокації шлуночкового ендокардіального електрода. Проведено репозицію електрода, і ЕКС переведено в режим DDDR. Залишилося невизначеним, чим саме зумовлені синкопальні напади і чому вони почастішали. На фоні нормально працюючого ЕКС і регулярного ритму з частотою 60 уд/хв хвора знову втратила свідомість, тому їй було призначено ЕЕГ-дослідження.
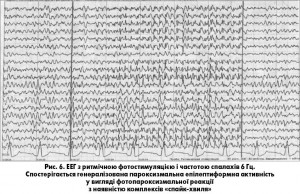
На фоновій ЕЕГ у стані спокою зафіксовано дезорганізацію домінуючого альфа-ритму з одиничними повільнохвильовими спалахами тета-діапазону в лобних ділянках. На тлі ритмічної фотостимуляції при пред’явленні стимулу 6 Гц 5 с було зареєстровано генералізовану пароксизмальну епілептиформну активність у вигляді фотопароксизмальної реакції з наявністю SW-комплексів (спайк-хвиля), які клінічно можуть викликати синкопальні стани (рис. 6). На паралельному каналі ЕКГ при цьому реєструються регулярні шлуночкові комплекси з частотою 70/хв (ритм, нав’язаний ЕКС), тобто аритмічна причина синкопе виключена.
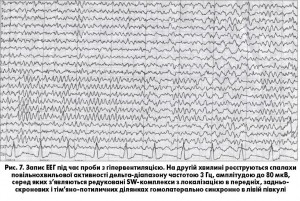
Під час проби з гіпервентиляцією на другій хвилині реєструються спалахи патологічної повільнохвильової активності дельта-діапазону у скроневій і парієнтальній ділянках лівої півкулі (рис. 7).
Таку картину мультифокальної енцефалопатії у пацієнтки можна пояснити тривалим анамнезом артеріальної гіпертензії 3 ступеня і брадиаритмії. Крім того, на фоні гіпервентиляції спостерігалася короткочасна втрата свідомості з тоніко-клонічним судомним компонентом. Таким чином, причиною синкопальних станів у цієї хворої була пароксизмальна епілептиформна активність зі схильністю до генералізації, яку майже неможливо описати клінічно через коротку тривалість нападів. За результатами ЕЕГ-дослідження невролог рекомендував консультацію в центрі епілепсії, і пацієнтка отримала призначення карбамазепіну з титрацією дози до 300 мг/добу. Протягом наступного року спостереження синкопальні напади не повторювалися.
 Президент Української асоціації медицини сну, головний лікар Лабораторії сну, кандидат медичних наук Юрій Несторович Погорецький звернув увагу лікарів на проблему порушень дихання під час сну. Синдром обструктивного апное сну (СОАС) – один із найбільш значущих і поширених факторів ризику розвитку серцево-судинних захворювань. Гіпоксія – головний тригер патологічних станів при СОАС. При тяжких формах СОАС може реєструватися до 400-500 зупинок дихання за ніч загальною тривалістю 3-5 год, що призводить до гострої і хронічної нестачі кисню. Нормальне насичення крові киснем становить 96-98%, критичний рівень – 85%, а у хворих із СОАС цей показник знижується до 50 і навіть 10%. Крім того, СОАС унеможливлює перехід у глибоку фазу сну і нормальне фізіологічне відновлення. Патологічна структура сну – це чергування фаз поверхневого сну і зупинок дихання тривалістю від кількох секунд до хвилин. Відсутність фізіологічного відпочинку, хронічна гіпоксія і порушення синтезу мелатоніну зумовлюють розвиток та прогресування багатьох захворювань – від серцево-судинних до онкологічних. За даними Лабораторії сну, 78% пацієнтів з артеріальною гіпертензією мають середню або тяжку форму СОАС. За наявності СОАС і хропіння в одного члена сім’ї завжди спостерігаються порушення сну та погіршення здоров’я в інших.
Президент Української асоціації медицини сну, головний лікар Лабораторії сну, кандидат медичних наук Юрій Несторович Погорецький звернув увагу лікарів на проблему порушень дихання під час сну. Синдром обструктивного апное сну (СОАС) – один із найбільш значущих і поширених факторів ризику розвитку серцево-судинних захворювань. Гіпоксія – головний тригер патологічних станів при СОАС. При тяжких формах СОАС може реєструватися до 400-500 зупинок дихання за ніч загальною тривалістю 3-5 год, що призводить до гострої і хронічної нестачі кисню. Нормальне насичення крові киснем становить 96-98%, критичний рівень – 85%, а у хворих із СОАС цей показник знижується до 50 і навіть 10%. Крім того, СОАС унеможливлює перехід у глибоку фазу сну і нормальне фізіологічне відновлення. Патологічна структура сну – це чергування фаз поверхневого сну і зупинок дихання тривалістю від кількох секунд до хвилин. Відсутність фізіологічного відпочинку, хронічна гіпоксія і порушення синтезу мелатоніну зумовлюють розвиток та прогресування багатьох захворювань – від серцево-судинних до онкологічних. За даними Лабораторії сну, 78% пацієнтів з артеріальною гіпертензією мають середню або тяжку форму СОАС. За наявності СОАС і хропіння в одного члена сім’ї завжди спостерігаються порушення сну та погіршення здоров’я в інших.
Розпитування пацієнтів про якість і тривалість сну має бути обов’язковим пунктом під час збору анамнезу в практиці лікарів усіх спеціальностей. Особливу увагу слід приділяти скаргам на зупинки дихання та хропіння, які зазвичай пред’являє не сам хворий, а його родичі. Полісомнографія – золотий стандарт діагностики порушень сну й основа підбору індивідуальної терапії. Крім того, необхідно ширше впроваджувати метод скринінгових досліджень для виявлення хворих, яких слід направляти в спеціалізовану клініку для проведення полісомнографії. В останні роки для цього розроблено портативні прилади реєстрації дихання та насичення киснем, які хворий може використовувати в амбулаторних умовах.
Під час конференції проведено координаційно-методичну нараду головних спеціалістів та представників кафедр, на яких здійснюється викладання функціональної діагностики. На нараді обговорено стан підготовки нормативної документації з функціональної діагностики. Головний позаштатний спеціаліст МОЗ України, професор О.Й. Жарінов доповів, що проекти наказів МОЗ України про організацію та роботу системи функціональної діагностики, а також про кваліфікаційні характеристики фахівців з функціональної д іагностики пройшли громадське обговорення. З урахуванням зроблених зауважень і побажань відбулася підсумкова експертиза цих проектів на засіданні робочої групи МОЗ України. Крім того, разом із суміжними кафедрами здійснюється значна освітня робота, регулярно проводяться школи-семінари з функціональної діагностики у регіонах України.
У другій частині конференції фахівці кафедри функціональної діагностики НМАПО ім. П.Л. Шупика провели майстер-клас «Діагностика та сучасні підходи до лікування аритмій серця».
Підготував Дмитро Молчанов