16 травня, 2016
Ефективність розувастатину в пацієнтів з ішемічною хворобою серця: результати відкритого проспективного дослідження «Чисті судини»
Історія застосування статинів налічує вже чверть століття. За цей час препарати даного класу вийшли на перше місце у світі за частотою призначень та стали одними з найбільш вивчених ліків. Результати численних досліджень, що загалом охоплюють 1 млн пацієнто-років, надають переконливі аргументи щодо ефективності статинів у вторинній та первинній профілактиці серцево-судинних захворювань (ССЗ).
Безсумнівним є прогнозмодифікуюче значення статинотерапії у пацієнтів з ішемічною хворобою серця (ІХС). Суттєве зниження ризику серцево-судинних ускладнень (інфаркту міокарда, коронарної реваскуляризації, серцево-судинної смерті та смерті від усіх причин) у таких хворих під впливом статинів продемонстровано в дослідженнях 4S, CARE, TNT (4S Group, 1994; Sacks F. M., 1996; LaRosa J.C., 2004). Більш того, у пацієнтів зі стабільною ІХС застосування високих доз статинів сприяє сповільненню прогресування та навіть регресу коронарного атеросклерозу, що підтверджено результатами щойно опублікованого метааналізу Lipid and Blood Pressure Meta-analysis Collaboration (LBPMC) Group (Banach М., 2015). Його результати свідчать про достовірне зменшення об’єму атеросклеротичної бляшки, яке вперше було зафіксоване в дослідженні ASTEROID та відбулося на тлі значного (на 53%) зниження рівня атерогенного холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) під впливом розувастатину (Nissen S. E., 2006).
Ефективність статинотерапії у попередженні ССЗ напряму пов’язана з величиною зниження рівня ХС ЛПНЩ. Стратегія статинотерапії, яку нині застосовують у Європі, передбачає досягнення цільового рівня ХС ЛПНЩ, що визначається ступенем ризику ССЗ. Для пацієнтів дуже високого ризику, до яких відносяться хворі на ІХС, цільовим рівнем ХС ЛПНЩ є 1,8 ммоль/л. У США принцип застосування статинів ґрунтується на виборі інтенсивності терапії. Хворим на ІХС показана інтенсивна статинотерапія, що передбачає використання аторвастатину в дозах 40-80 мг/добу та розувастатину 20-40 мг/добу незалежно від вихідного рівня ХС ЛПНЩ. Такі дози найпотужніших статинів забезпечують зниження ХС ЛПНЩ на ≥50%, що дозволяє досягти цільових значень.
Проте попри наявні аргументи щодо необхідності й ефективності статинотерапії в пацієнтів з ІХС ситуація з призначенням цих препаратів, а отже, й з досягненням цільових рівнів ХС ЛПНЩ залишається погано контрольованою. Так, за результатами дослідження EUROASPIRE IV, у країнах Європи 87% пацієнтів дуже високого ризику отримують статини для вторинної профілактики ССЗ, проте тільки 21% з них мають ХС ЛПНЩ <1,8 ммоль/л (Kotseva K., 2015). За даними цього ж огляду, в Україні з 79% хворих дуже високого ризику, які застосовують статини, цільових значень ХС ЛПНЩ досягли лише 15% (Коваленко В. М., 2015). З одного боку, така ситуація зумовлена лікарською інерцією, яка полягає в переважному використанні низьких і помірних доз статинів, що не дозволяє досягти цільового ліпідзнижувального ефекту. Також спостерігається низька прихильність пацієнтів до статинотерапії, що пояснюється як системними чинниками (відсутність інститутів медичного страхування, самозабезпечення ліками та ін.), так і безпосередньо пов’язаними з пацієнтом факторами (Casula М., 2012). Відомо, що протягом року близько 50% хворих припиняють прийом призначених статинів. За результатами одного з опитувань, проведеного в США, переважна більшість пацієнтів, які припинили лікування, не були впевнені в користі цих ліків (81,7%) та поінформовані щодо їх значення для прогнозу (72,5%), а також не знали про необхідність їх тривалого застосування (97,7%) (McGinnis В., 2007). Дані цього анкетування свідчать про необхідність більш тісної й ефективної взаємодії між лікарем та пацієнтом для поширення знань та усвідомлення необхідності застосування статинів.
Одним із заходів подолання системних чинників є використання якісних генеричних статинів. У масштабному аналізі даних з реальної клінічної практики, який включив 13 799 пацієнтів (Ломбардія, Італія), було встановлено, що генеричні форми не поступаються брендовим статинам в аспекті ефективності та переносимості терапії. Частота відміни препарату (ВР 0,98; 95% ДІ 0,94-1,02) та ризик серцево-судинних ускладнень (ВР 0,98; 95% ДІ 0,79-1,22) були ідентичними у групах генеричних і брендових статинів (Corrao G., 2014).
Вітчизняний ринок статинів нещодавно поповнився генеричним розувастатином – препаратом Клівас. Компанією «Фарма Старт» було проведено скринінгову програму «Чисті судини», метою якої було вивчити ефективність переведення хворих на ІХС з інших статинів (при їх недостатній ефективності) на розувастатин (Клівас). У дослідженні брали участь 435 лікарів-кардіологів як амбулаторної, так і стаціонарної ланки державних і приватних закладів охорони здоров’я з обласних центрів та інших міст України (дослідженням було охоплено всі регіони, за винятком Донецької, Луганської областей та АР Крим). Критеріями включення були документована ІХС та попереднє призначення статинотерапії. У рамках програми дослідження виконували первинне обстеження, яке передбачало оцінку результативності попередньої статинотерапії (регулярність прийому, назва статину, переносимість терапії) та визначення показників ліпідного спектра крові на тлі застосованої терапії. На цьому ж візиті хворих переводили на розувастатин (Клівас) у дозі 20 мг/добу. Вибір дози ґрунтувався на рекомендаціях Американської колегії кардіологів / Американської асоціації серця (2013), в яких хворим на ІХС з метою вторинної профілактики рекомендовано застосовувати високоінтенсивну статинотерапію (у випадку розувастатину – 20-40 мг). Оцінка ефективності та переносимості терапії розувастатином (препаратом Клівас) проводилася через 4 тиж лікування. За принципом повноти даних на всіх етапах дослідження для остаточного аналізу було відібрано результати обстеження 9317 хворих на ІХС, середній вік яких становив 62,5±9,5 років (усі дані представлені у вигляді М±σ). У когорті обстежених переважали чоловіки (72,6%), у 64,4% учасників спостерігали поєднання ІХС та артеріальної гіпертензії.
За результатами аналізу попередньої статинотерапії, більшість (68,5%) пацієнтів застосовували аторвастатин, розувастатин використовували 19,4% хворих, симвастатин – 12,1% учасників. Найчастіше лікарі обирали для лікування хворих на ІХС помірно інтенсивну статинотерапію: аторвастатин в дозі 20 мг (у 58,5% випадках), розувастатин у дозі 10 мг (у 74,8% осіб); високі дози статинів застосовувалися всього в 16,4% учасників групи аторвастатину (40 мг – 13,2%; 80 мг – 3,4%) та 25,2% пацієнтів групи розувастатину (20 мг – 19,8%; 40 мг – 5,4%). За результатами опитування, 79,6% хворих приймали статини регулярно (критерієм регулярного застосування вважали тривалість прийому 9 міс протягом року), при цьому 3,3% пацієнтів пов’язували з терапією статинами такі побічні явища, як нудота, здуття, дискомфорт в епігастрії та правому підребер’ї.
Аналіз показників ліпідного спектра крові продемонстрував недостатню ефективність статинотерапії в обстежених хворих на ІХС. Рівень загального холестерину (ЗХС) у середньому становив 5,09±0,84 ммоль/л, переважно за рахунок атерогенної фракції ХС ЛПНЩ (3,13±0,89 ммоль/л). Слід зазначити, що цільового рівня ХС ЛПНЩ (1,8 ммоль/л) вдалося досягти лише в 10,4% учасників, тобто приблизно в кожного 10-го хворого на ІХС. Це засвідчує низьку ефективність статинотерапії щодо контролю ХС ЛПНЩ за допомогою застосування низьких та помірних доз статинів у пацієнтів з ІХС в умовах реальної клінічної практики. Гіпертригліцеридемія спостерігалась у 32,2% пацієнтів, уміст тригліцеридів (ТГ) у середньому становив 1,87±0,98 ммоль/л. Рівень антиатерогенної фракції холестерину ліпопротеїнів високої щільності (ХС ЛПВЩ) у жінок відповідав значенням 1,24±0,83 ммоль/л, у чоловіків – 1,08±0,71 ммоль/л.
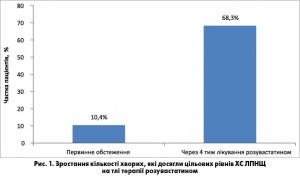
Обстеження пацієнтів через 4 тиж лікування розувастатином (препаратом Клівас) показало позитивну динаміку показників ліпідного спектра за рахунок як зниження вмісту атерогенних фракцій, так і зростання рівня ХС ЛПВЩ. На тлі застосування розувастатину спостерігали додаткове зменшення вмісту ЗХС на 13,2% (з 5,09±0,84 до 4,42±0,78 ммоль/л; р<0,001) з вираженим зниженням рівня ХС ЛПНЩ (на 20,6%: з 3,13±0,89 до 2,47±0,87 ммоль/л; р<0,001). Кількість осіб, які досягли цільового рівня ХС ЛПНЩ, суттєво зросла: при первинному обстеженні частка таких пацієнтів становила 10,4%, натомість через 4 тиж вона збільшилась до 68,3% (рис.).
Таким чином, перехід на високоінтенсивну терапію розувастатином 20 мг (препаратом Клівас) супроводжувався значним збільшенням кількості хворих на ІХС з ефективним контролем ХС ЛПНЩ. Поряд з цим відзначалися зменшення вмісту ТГ на 10,1% (з 1,87±0,98 до 1,67±0,95 ммоль/л; р<0,001) і додаткове зростання концентрації ХС ЛПВЩ на 4,2% в осіб чоловічої статі (з 1,08±0,71 до 1,14±0,82 ммоль/л; р<0,001) і на 4,3% у жінок (з 1,24±0,83 до 1,29±0,92 ммоль/л; р<0,001).
Більшість пацієнтів відмітили хорошу переносимість лікування розувастатином.
Кількість зареєстрованих побічних ефектів становила лише 1,2%, при цьому небажані явища мали переважно загальний характер (нудота, головний біль, слабкість) і не потребували відміни лікування.
Проведена скринінгова програма надає чіткі свідчення доцільності використання у хворих на ІХС розувастатину (препарату Клівас) у дозі 20 мг, що забезпечує зростання ліпідзнижувального ефекту та кількості осіб, які досягають цільового рівня ХС ЛПНЩ. Безумовно, частина пацієнтів дуже високого ризику потребують більш інтенсивної статинотерапії, проте розувастатин (препарату Клівас) у дозі 20 мг/добу надає можливість ефективного контролю ХС ЛПНЩ на рівні ≤1,8 ммоль/л у 68% хворих на ІХС. Результати програми з оцінки використання генеричного розувастатину (Клівас) зіставні з даними дослідження STELLAR, предметом якого було вивчення ефективності розувастатину в порівнянні з іншими статинами. Результати STELLAR засвідчили перевагу розувастатину над аторвастатином та симвастатином щодо ліпідзнижувального ефекту і, як наслідок, щодо кількості пацієнтів із цільовим зниженням ХС ЛПНЩ. Застосування розувастатину в дозі 20 мг/добу дозволило досягти цільового рівня ХС ЛПНЩ у 77% пацієнтів, проте варто зазначити, що на той час цей показник становив 2,6 ммоль/л (Jones P. H., 2003).
Досягнення цільового рівня атерогенної фракції ХС ЛПНЩ є надзвичайно важливим завданням статинотерапії з точки зору попередження розвитку серцево-судинних ускладнень. Більше того, в дослідженні K.H. Lee (2011) у пацієнтів з гострим інфарктом міокарда і рівнем ХС ЛПНЩ <1,8 ммоль/л подальше зниження вмісту останнього в крові за допомогою статина сприяло значному (на 42%) зменшенню числа випадків досягнення комбінованої кінцевої точки (кількість серйозних побічних явищ протягом року, включно з летальним випадком, повторним інфарктом міокарда, плановою реваскуляризацією та аортокоронарним шунтуванням).
Здатність статинів сповільнювати прогресування атеросклерозу також залежить від вираженості зниження ХС ЛПНЩ. У дослідженні ASTEROID за участю 500 хворих на ІХС застосування розувастатину в дозі 40 мг/добу протягом 2 років сприяло достовірному зменшенню об’єму атеросклеротичної бляшки коронарних артерій за даними внутрішньосудинного УЗД, що відбулося на тлі значного покращення показників ліпідного спектра крові з вираженим (у середньому на 53%) зниженням рівня ХС ЛПНЩ (Nissen S.E., 2006). Водночас у дослідженнях з аторвастатином, симвастатином та правастатином зафіксовано менш виражений ліпідзнижувальний ефект (Nissen S.E., 2004; Nicholls S. J., 2007), що, ймовірно, стало причиною менш значимого порівняно з таким розувастатину (дослідження ASTEROID) впливу на об’єм атеросклеротичної бляшки в коронарних артеріях.
Безумовно, не можна обійти питання переносимості та безпеки статинотерапії ще й тому, що міфи з цього приводу суттєво впливають на прихильність пацієнтів до лікування. За даними опитування хворих, які припинили статинотерапію, найчастіше (42,2%) причиною відмови були побічні ефекти, друге місце (12,7%) посідало хвилювання з приводу можливої їх появи (McGinis В., 2007).
Останнім часом широко обговорюється зростання ризику розвитку цукрового діабету при тривалому використанні статинів, яке, за даними метааналізу N. Satar (2010), становить 9%. Проте експерти переконані, що користь від застосування статинів у вигляді суттєвого зменшення серцево-судинних ускладнень (зниження ХС ЛПНЩ на 3 ммоль/л асоціюється зі зниженням ризику серцево-судинної смерті на 50%) значно перевищує їх потенціальний діабетогенний ефект. Результати численних досліджень, зведені в метааналізі CTT, свідчать про незначний ризик розвитку міопатії (<1/1000 випадків) та зростання активності трансаміназ (0,5-2%) на тлі застосування статинів (CTT Collaboration, 2010). Найбезпечнішим з точки зору печінкових та м’язових побічних ефектів є розувастатин, на користь чого свідчать результати аналізу H.B. Brewer (2003), де міопатію зареєстровано менш ніж у 0,3% учасників, а зростання активності аланінамінотрансферази – у 0,2% пацієнтів, які отримували розувастатин у дозі 10-40 мг/добу. Хороший профіль безпеки та переносимості продемонстрував розувастатин (Клівас) й у всеукраїнському дослідженні: кількість побічних ефектів становила лише 1,2%.
Таким чином, результати скринінгової програми «Чисті судини» підтверджують доцільність переводу пацієнтів з ІХС на терапію розувастатином (у випадку неефективної статинотерапії). Експерти вважають, що його потужний ліпідзнижувальний потенціал та хороший профіль безпеки сприятимуть підвищенню прихильності хворих до терапії та зростанню кількості осіб з ефективним контролем ХС ЛПНЩ.
Список літератури знаходиться в редакції.