3 березня, 2016
Прагматичный подход к выбору антигипертензивного препарата у пациентов с АГ и коморбидной патологией в амбулаторной практике
По материалам XVI Национального конгресса кардиологов Украины (23-25 сентября 2015 года, г. Киев)
Артериальная гипертензия (АГ) – заболевание, которое длится многие годы, и если в самом начале ее развития можно замедлить и даже прервать сердечно-сосудистый континуум, то на более поздних этапах изменения в органах-мишенях становятся необратимыми. Поэтому, подбирая терапию пациенту с АГ, врачу следует использовать прагматичный подход и максимально сократить количество шагов к главной цели – снижению сердечно-сосудистого риска.
 О приоритетных задачах ведения больных АГ и об эффективных методах их решения рассказала в ходе своего выступления доктор медицинских наук, профессор Елена Акиндиновна Коваль (Днепропетровская государственная медицинская академия).
О приоритетных задачах ведения больных АГ и об эффективных методах их решения рассказала в ходе своего выступления доктор медицинских наук, профессор Елена Акиндиновна Коваль (Днепропетровская государственная медицинская академия).
Назначая пациенту с АГ антигипертензивную терапию, врач должен быть нацелен на выполнение нескольких основных задач.
- Достижение и удержание целевого уровня артериального давления (АД) с сохранением его физиологических биоритмов.
- Поиск причин и обязательное преодоление резистентности к терапии в случаях, если она возникает.
- Предупреждение или замедление поражений органов-мишеней.
- Обеспечение высокой приверженности пациента к терапии.
У пациентов с АГ и коморбидной патологией решение этих задач затруднено, что связано с влиянием сопутствующих заболеваний (например, сахарного диабета – СД) на контроль АД и с возможными ограничениями в применении некоторых антигипертензивных средств.
Исходя из этих задач, важным моментом является правильный выбор препарата, который будет служить основой антигипертензивной терапии. Наиболее часто среди рекомендуемых препаратов первой линии антигипертензивной терапии, используются средства, модулирующие активность ренин-ангиотензин-альдостероновой системы (РААС), а именно: ингибиторы ангиотензинпревращающего фермента (ИАПФ) и блокаторы рецепторов ангиотензина II (БРА).
Выбираемый врачом препарат должен соответствовать следующим требованиям:
- иметь выраженный и длительный (не менее 24 ч) антигипертензивный эффект;
- обладать доказанными органопротекторными свойствами;
- отличаться хорошей переносимостью и отсутствием негативного влияния на течение коморбидной патологии.
Круг поиска такого препарата может быть значительно сужен, если мы сосредоточим свое внимание на современных представителях класса БРА. В исследованиях последних лет получены ответы на многие важные вопросы в области применения БРА. Основные выводы, которые были сделаны международными экспертами в отношении этих препаратов, можно представить следующим образом.
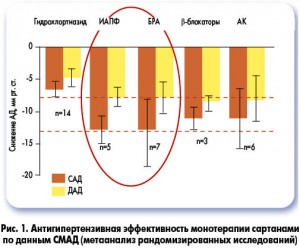
БРА не уступают ИАПФ в эффективности в снижении АД и, следовательно, в уменьшении сердечно-сосудистого риска у больных АГ (рис. 1) (F. J Am. Messerli, 2011).
БРА имеют дополнительные протекторные механизмы, которые могут иметь значение в определенных клинических ситуациях (VAL-HeFT Trial, 2001).
БРА хорошо изучены и продемонстрировали эффективность и безопасность при применении у пациентов с АГ и различными сопутствующими состояниями, в том числе с сердечной недостаточностью (СН), хроническими заболеваниями почек, СД 2 типа (Drug Saf., 2015, 38:33-54). Это особенно важно, учитывая, что наличие данных заболеваний значительно влияет на эффективность контроля АД (MARVAL Study, 2002; RENAAL, 2001).
БРА эффективны в лечении пациентов с диабетической нефропатией, что отражено в современных рекомендациях по лечению пациентов с СД 2 типа. В руководстве Американской диабетической ассоциации (ADA, 2011) БРА наряду с ИАПФ рекомендованы для лечения пациентов с диабетической нефропатией (за исключением беременных) в качестве основных медикаментозных средств для уменьшения/ликвидации альбуминурии (МА). БРА предлагается использовать для лечения больных СД 2 типа с повышенным АД и МА как препараты, которые могут замедлить прогрессирование МА. Отмечено также, что у этой категории пациентов при наличии почечной недостаточности (уровень креатинина крови ≥133 мкмоль/л) БРА способствуют замедлению прогрессирования нефропатии.
Плавное, но выраженное и устойчивое снижение АД на фоне приема БРА может обеспечивать дополнительные преимущества в виде положительного влияния на когнитивные функции и риск развития цереброваскулярных осложнений (M. Levi et al., 2013).
Вопросы о возможном повышении риска развития инфаркта миокарда и опухолевых заболеваний на фоне терапии БРА закрыты после получения результатов крупных метаанализов, свидетельствующих о том, что эти риски не превышают таковые при применении антигипертензивных препаратов других классов (H.M.A. Abraham, C.M. White, W.B. White, 2015).
БРА характеризуются благоприятным профилем безопасности и отличной переносимостью, поэтому их использование значительно повышает шансы на формирование высокой приверженности пациентов к лечению (H.M.A. Abraham, C.M. White, W.B White, 2015).
На последнем пункте хотелось бы остановиться более подробно, поскольку именно высокая приверженность пациентов является одним из главных условий успешной терапии АГ, как и любого другого заболевания. В исследовании P.R. Conlin и соавт. (2010) показано, что к терапии БРА сохраняется наиболее высокая приверженность – 67% в начале лечения и 51% через 4 года приема. Все основные классы антигипертензивных препаратов, в том числе ИАПФ, уступают БРА в этом отношении (Conlin et al., 1999-2010).
Тот факт, что хорошая приверженность к приему препаратов является важным преимуществом антигипертензивной терапии, подтвердили результаты исследования итальянских ученых, проведенного в крупной когорте больных Ломбардии (почти 500 тыс.), принимавших различные классы антигипертензивных средств. В данном исследовании только БРА продемонстрировали лучшую приверженность к терапии по сравнению с ИАПФ, и это ассоциировалось со снижением суммарной частоты неблагоприятных исходов АГ (Corrao, 2008, Lombardia Data-basa).
Следует отметить, что хорошая переносимость антигипертензивных препаратов, назначаемых для постоянного приема, особенно важна для пациентов с удовлетворительным состоянием и самочувствием, без сердечно-сосудистых осложнений в анамнезе. Таким больным трудно осознать, что повышение АД – это реальная угроза развития тяжелых осложнений, поэтому даже небольшое ухудшение качества жизни, обусловленное побочными эффектами антигипертензивного средства, будет поводом для самостоятельного прекращения терапии.
Помимо вышеперечисленных, «базисных» уже хорошо известных преимуществ БРА, нельзя не задуматься и о дополнительных «бонусах», которые мы можем получить при назначении этих препаратов у некоторых категорий пациентов.
Например, БРА можно рассмотреть в качестве предпочтительных препаратов для лечения больных АГ с сопутствующим активным хроническим обструктивным заболеванием легких (ХОЗЛ). У таких пациентов назначение ИАПФ может быть нежелательным, учитывая накопление при этом в тканях брадикинина (одного из медиаторов воспаления) и роль воспаления в патогенезе ХОЗЛ (Br J Pharmacol, 2002).
Значительный интерес представляют результаты исследования Mitsuyasu Terashima и соавт. (JACC, 2012), в котором сравнивали возможности одного из современных БРА и антагониста кальция (АК) в снижении выраженности эндотелиальной дисфункции у пациентов, которым были имплантированы стенты с лекарственным покрытием (DES). В этом исследовании БРА продемонстрировал сопоставимый с АК вазопротекторный эффект, уменьшив выраженность эндотелиальной дисфункции и спазма стентированного сосуда в ответ на пробу с ацетилхолином. Авторы исследования также сделали вывод о том, что терапия БРА не оказывает негативного влияния на коллатеральный коронарный кровоток после имплантации DES.
Известно, что эндотелиальная дисфункция у пациентов с DES ассоциируется с развитием вазоспазма и различными осложнениями: инфарктом миокарда, жизнеугрожающими аритмиями, внезапной кардиальной смертью (B.C. Brott, A.S. Anayiotos et al., 2006), тромбозами стентов (М. Togni et al., 2005), и, следовательно, играет ключевую роль в ухудшении долгосрочного прогноза у этих больных (J.E. Deanfield, 2007). Таким образом, можно говорить о дополнительных основаниях для назначения современных БРА пациентам с АГ и различными формами ишемической болезни сердца (ИБС), перенесшим стентирование коронарных артерий. Такой подход поможет без увеличения количества препаратов базисной терапии одновременно обеспечить эффективный контроль АД у гипертензивных пациентов, уменьшить выраженность эндотелиальной дисфункции и снизить риск возникновения спастической стенокардии.
Итак, БРА открывают нам все новые и новые возможности для получения дополнительных полезных эффектов у различных категорий кардиологических пациентов. В современных международных и национальных рекомендациях по лечению АГ БРА рассматриваются как класс препаратов, обладающих совокупными органопротекторными свойствами, выраженность которых отличается у разных препаратов, что, однако, не изменяет подходы к решению клинических ситуаций для различных представителей класса.
Тем не менее на существование значительных фармакологических отличий между представителями класса БРА и возможность влияния этих отличий на сердечно-сосудистые исходы указывали эксперты в ходе недавних международных конгрессов.
Так, например, разница во влиянии БРА на исходы АГ подтверждена в шведском ретроспективном исследовании, в котором сравнили результаты применения двух БРА – лозартана и кандесартана в период с 1999 по 2007 г. по данным 72 клинических центров (S.E. Kjeldsen et al., 2009).
Было установлено, что при сопоставимом снижении АД применение кандесартана приводило к большему снижению частоты сердечно-сосудистых событий по сравнению с лозартаном. Авторы исследования сделали вывод, что различные БРА имеют дополнительные протекторные возможности, помимо снижения АД, и отличия в исходах при использовании разных представителей этого класса очевидны.
Кандесартан, продемонстрировавший преимущества во влиянии на сердечно-сосудистые исходы у кардиологических пациентов перед другими БРА, является предшественником нового, улучшенного представителя этого класса – азилсартана (в Украине зарегистрирован как Эдарби®). Данные препараты имеют сходную структуру, за исключением наличия в молекуле азилсартана 5-членного окси-оксадиазольного кольца вместо тетразольного кольца.
Уникальность азилсартана заключается в том, что его химическая структура, в отличие от всех других одобренных сегодня к применению БРА, обеспечивает наиболее стойкую связь с рецепторами ангиотензина ІІ 1 типа (АТ1-рецепторами) и наиболее медленную диссоциацию комплекса блокатор/АТ1-рецептор (М. Ojima et al., 2011), что и определяет в значительной степени длительность и мощность антигипертензивного эффекта препарата.
Для азилсартана накоплена достаточно убедительная доказательная база в отношении эффективности и профиля безопасности – его эффекты изучали в клинических исследованиях, в том числе сравнительных, с общей численностью >7 000 пациентов.
Азилсартан продемонстрировал преимущества в снижении и контроле АД в сравнительных исследованиях с ИАПФ рамиприлом, широко используемым во всем мире валсартаном и новым БРА олмесартаном (W.B. White et al., 2011; G. Bonner et al., 2013).
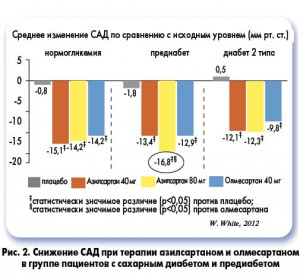
Антигипертензивная эффективность азилсартана предоставляет дополнительные «бонусы» в контроле АД у больных с предиабетом и СД 2 типа (W. White, 2012) (рис. 2), тем более, что этот препарат, как и другие БРА, обладает благоприятным метаболическим профилем.
Азилсартан относится к мультифункциональным БРА, являясь частичным агонистом ядерных рецепторов PPARγ, которые регулируют метаболизм липидов и углеводов, и антагонистом рецепторов АТR1. Антагонизм к рецепторам ATR1 – один из механизмов повышения чувствительности тканей к инсулину. Установлено также, что азилсартан увеличивает потребление глюкозы инсулинчувствительными тканями у больных с СД (Iwai et al., 2007).
Таким образом, азилсартан одновременно оказывает выраженный антигипертензивный эффект и благоприятно влияет на метаболические показатели.
Учитывая распространенность сочетания АГ и ИБС, важными являются экспериментальные данные о способности азилсартана уменьшать ремоделирование после острого инфаркта миокарда (Y. Nakamura, Suzuki, Biological & Pharmaceutical Bulletin, 2013). В прямом эксперименте азилсартан при использовании во всех концентрациях снижал экспрессию ингибитора тканевого активатора плазминогена (РАІ) в стенке аорты (C.J. French, A.K. Zaman, B.E. Sobel, 2011). Данный эффект приводит к увеличению уровня тканевого активатора плазминогена в местах повреждения сосуда, способствуя уменьшению образования фибрина и, как следствие, – снижению риска развития атерогенных и протромботических изменений в сосудах, стабилизации атеросклеротической бляшки.
Резюмируя вышесказанное, можно заключить, что азилсартан (Эдарби) является мощным оружием в борьбе с АГ на фоне коморбидных состояний.
Азилсартан демонстрирует преимущества в снижении АД перед другими БРА, сохраняя все позитивные черты класса: благоприятный метаболический профиль; кардио-, нефро- и вазопротекторный эффекты.
Таким образом, назначение азилсартана с первых шагов лечения АГ позволит выполнить главное условие для снижения сердечно-сосудистого риска – эффективно контролировать АД, причем у наиболее трудных пациентов – с коморбидными состояниями, которые часто встречаются в реальной практике.
Подготовила Наталья Очеретяная
UA/AZI/1215/0003