17 лютого, 2016
Інсулінорезистентність при хронічній серцевій недостатності (огляд літератури та власні дані)

Серцева недостатність (СН) – це прогресуючий клінічний синдром, який характеризується венозним застоєм, нейрогормональною дизрегуляцією і системною запальною відповіддю в умовах насосної дисфункції серця [3, 35, 59]. Ці зміни асоційовані з порушенням обміну речовин в інших органах, зокрема жировій тканині, скелетних м’язах та ендокринній системі. Одним із наслідків вказаних розладів є інсулінорезистентність (ІР). Незважаючи на потенційне патогенетичне значення цього феномена при хронічній СН (ХСН), на сьогодні його клінічна роль при зазначеному синдромі є недостатньо вивченою [19, 34].
Інсулінорезистентність – це порушення біологічної дії інсуліну, що супроводжується зниженим засвоєнням глюкози тканинами (переважно скелетними м’язами) і призводить до розвитку хронічної компенсаторної гіперінсулінемії (ГІ) [10]. Основою ІР є зниження чутливості м’язової, жирової та печінкової тканин до інсуліну.
М’язова ІР характеризується зниженим надходженням глюкози з крові у кардіоміоцити та клітини скелетної мускулатури [17, 51]. У разі недостатності глюкози в міокарді відбувається заміна субстрату обміну речовин для підвищення енергоефективності. Компенсаторна ГІ, яка спрямована на уникнення зазначеної адаптативної реакції, може, навпаки, зумовлювати подальше ушкодження міокарда шляхом посилення ліпотоксичності, активації запалення, оксидантного стресу та фіброзоутворення [50]. Так, в експериментальних моделях було виявлено існування інсулінорезистентної кардіоміопатії, яка характеризується неефективним енергетичним обміном [62]. Крім того, під впливом ГІ в осіб з ІР посилюється симпатична активація, стимулюється гіпертрофія міокарда, спостерігається затримка натрію і води, підвищується жорсткість судин [10, 11]. Погіршення периферичного кровообігу при СН призводить до функціональної неспроможності скелетних м’язів. Поступове зменшення кількості капілярів у скелетній мускулатурі зумовлює зниження засвоєння глюкози м’язами, а це – додатковий фактор формування системної ІР [17, 51].
Проявом ІР жирової тканини є розвиток резистентності до антиліполітичної дії інсуліну (блокування ліпази в адипоцитах і попередження гідролізу тригліцеридів), у результаті чого накопичуються вільні жирні кислоти (ВЖК) і гліцерин. Останні беруть участь в утворенні ліпопротеїдів дуже низької щільності. Синтез лептину в адипоцитах стимулюється інсуліном, дещо меншою мірою – катехоламінами. Лептин підвищує чутливість клітин печінки та м’язової тканини до дії інсуліну [52, 61]. Існують дані про те, що надлишок лептину сприяє розвитку ІР інсулінозалежних тканин [16]. На підставі результатів багатьох досліджень встановлено основні закономірності порушень обміну лептину й адипонектину при ожирінні та метаболічному синдромі (МС) [36, 46, 52]. Утім, опубліковано лише поодинокі дослідження, присвячені вивченню стану адипокінів у пацієнтів із ХСН [22, 56].
ІР печінкової тканини характеризується зниженням синтезу глікогену й активацією глікогенолізу, внаслідок чого збільшується надходження глюкози в плазму крові, яке зумовлює тривалу компенсаторну ГІ [14,15].
Серед хворих із ХСН поширеність феномена ІР, яку оцінювали за індексом НОМА [13], коливається в різних дослідженнях від 30 до 49% [26, 47, 59]. Як критерій ІР у зазначених дослідженнях використовували значення індексу НОМА >2,5; ≥2,7; ≥2,77 і ≥3 [60, 26, 47]. Серед обстежених нами 107 пацієнтів із ХСН ІІ-ІV функціонального класу (ФК) за NYHA (Нью-Йоркська асоціація серця) з фракцією викиду (ФВ) лівого шлуночка (ЛШ) ≤40% на фоні ішемічної та дилатаційної кардіоміопатії ІР виявлялася у 45 хворих (42%). Медіана (Ме) за індексом НОМА у пацієнтів з ІР становила 3,58 (2,96; 5,74) на противагу 1,85 (0,95; 2,31) у хворих без ІР (р<0,001). У близько 1/3 пацієнтів (33 із 107) значення індексу НОМА становило ≥3,0.
Нами було проаналізовано клініко-демографічні дані та результати рутинного інструментального обстеження (електрокардіографія, ехокардіографія) хворих із ХСН залежно від наявності ІР. За статевим розподілом, етіологічним фактором ХСН, кількістю пацієнтів із перенесеним інфарктом міокарда, постійною/персистуючою формами фібриляції передсердь, розподілом на ФК за NYHA групи пацієнтів істотно не відрізнялися (для всіх порівнянь р>0,05). Не виявлено й відмінностей за середнім віком, антропометричними показниками (індекс маси тіла, окружність талії та біцепса), частотою серцевих скорочень, рівнем систолічного та діастолічного артеріального тиску, а також розрахунковими величинами швидкості клубочкової фільтрації (для всіх порівнянь р>0,05).
До найбільш обговорюваних у науковій літературі механізмів розвитку ІР при ХСН належать порушення механізмів регуляції кровообігу в скелетних м’язах [9, 48], зміни з боку гормонів жирової тканини [1, 53], системне запалення [12, 35] й оксидантний стрес [21, 42]. Як фундаментальний потенційний фактор виникнення ІР розглядають ендотеліальну дисфункцію (ЕД), яка зумовлює погіршення перфузії скелетних мязів на фоні знижених можливостей регуляції периферичного кровообігу [31]. Припускають, що перманентна периферична вазоконстрикція при ХСН призводить до розвитку «метаболічного хибного кола», яке може спричиняти більш тяжкий перебіг ХСН внаслідок порушення метаболізму та резистентності периферичних тканин до інсуліну [53]. Одним із механізмів регуляції периферичного кровообігу є ендотелій-опосередкована вазодилатація [18, 31], патогенетична роль якої, як і порушень периферичного кровотоку, при ХСН є доведеною [8, 37].
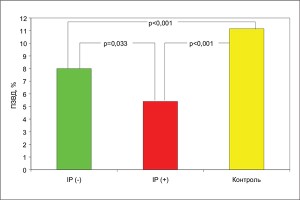
Достовірних відмінностей між показниками магістрального периферичного кровообігу у спокої в групах з ІР та без ІР нами не виявлено [5]. Утім, функціональний тест, який характеризує вазодилататорну здатність ендотелію (проба з реактивною гіперемією), дав змогу виявити значне зниження потікзалежної вазодилататорної відповіді (ПЗВД) плечової артерії (ПА) в «інсулінорезистентних» хворих (рис. 1). На відповідний зв’язок між зниженням ПЗВД та наявністю у наших пацієнтів ІР не впливали інші фактори (провідні клінічні характеристики, гемодинамічні та структурні особливості ЛШ, характер лікування), оскільки за відповідним спектром характеристик групи з ІР і без ІР виявилися співставними.
Ендотеліальна дисфункція спричиняє порушення механізму дії інсуліну шляхом зміни транскапілярного проходження інсуліну до тканин-мішеней. Зниження кровообігу в мікроциркуляторному руслі метаболічно активних тканин і збіднення мережі капілярів зумовлюють порушення стимульованого інсуліном метаболізму глюкози і ліпідів [25].
На сьогодні існують відомості про залежність між рівнем альдостерону та чутливістю тканин до інсуліну, яка асоціюється з підвищеною нейрогормональною активністю, погіршенням ендотеліальної функції, зниженим кровопостачанням скелетних м’язів [26, 59]. Останнє може зумовлювати подальше обмеження фізичної активності внаслідок погіршення функції скелетних м’язів і, можливо, сприяти прогресуванню ХСН [8, 28].
Одним із патогенетичних механізмів розвитку ІР є системне запалення. Разом із накопиченням надлишку ВЖК і проміжних продуктів їх метаболізму в інсулінзалежних клітинах (скелетних м’язах, кардіоміоцитах, гепатоцитах, адипоцитах) спостерігається паралельне зростання рівня цитокінів [30, 44]. Прозапальні цитокіни (TNF-α, IL-6), які при ХСН утворюються і циркулюють у крові в підвищених концентраціях, можуть істотно впливати на формування ІР у таких хворих [24, 62]. Встановлено зв’язок між маркерами запалення та резистентністю до інсуліну. Зокрема, J. Chen, R.P. Wildman, L.L. Hamm, P. Muntner та співавт. провели дослідження, в якому взяли участь 5959 практично здорових осіб. Рівні феритину, сечової кислоти, кількість лейкоцитів, фібриногену і C-реактивного білка були значно більшими у пацієнтів з вищим індексом HOMA [24]. Згідно з отриманими нами даними [4] рівень циркулюючого ТNF-α у хворих із ХСН та супутньою ІР виявився значно вищим порівняно з групою пацієнтів без ІР (р=0,041).
TNF-α, катехоламіни й ангіотензин-ІІ (АТ-II) є посередниками активації ліполізу та формування ІР [2, 45, 62]. Підвищена секреція лептину та/або знижена продукція адипонектину посилює акумуляцію макрофагів у жировій тканині та їх адгезію до ендотеліальних клітин [30, 57], зумовлюючи поглиблення ЕД в умовах зниженого периферичного кровообігу при ХСН.
При цьому високий рівень адипонектину (як наслідок адипонектинрезистентності) виступає предиктором смертності у хворих із ХСН [39, 44]. Це узгоджується з тим, що високий індекс маси тіла і, відповідно, низький рівень адипонектину асоціюються з вищою виживаністю у термінальній стадії СН [20, 27]. Також виявлено, що високий рівень адипонектину в плазмі крові асоціюється з нижчою функціональною активністю у пацієнтів із ХСН [23]. Утім, клінічні наслідки адипонектинрезистентності у хворих із ХСН поки що не з’ясовані.
Результати дослідження стану адипокінів продемонстрували, що у пацієнтів із ХСН та супутньою ІР реєстрували значно вищий рівень лептину в плазмі крові порівняно з хворими з ХСН без ІР (р=0,044). У якості підтвердження зв’язку між ІР і лептинутворюючою функцією жирової тканини при ХСН можна розглядати виявлену нами пряму кореляційну залежність (rho=0,294; p=0,002) між індексом НОМА та рівнем лептину в сироватці крові у пацієнтів з ХСН [4].
Оксидантний стрес (ОС) посідає вагоме місце серед неспецифічних ланок патогенезу ХСН. ОС характеризується підвищенням рівня вільних радикалів, які ушкоджують кардіоміоцити й ендотелій, і зниженням активності клітинних антиоксидантних систем [21, 58].
Ми спостерігали істотно вищий рівень сечової кислоти в плазмі крові у пацієнтів з ХСН та ІР. Відомо, що рівень сечової кислоти в плазмі крові розглядається як маркер вираженості системного оксидантного стресу, оскільки біопродуктами реакції розпаду ксантину під дією ксантиноксидази є, з одного боку, сечова кислота, а з іншого – супероксидний аніон [54]. Зважаючи на зв’язок між системним оксидантним стресом та імунозапальною відповіддю [42], зазначений факт узгоджується із підвищенням рівня циркулюючого імунозапального фактора TNF-α в обстежених нами хворих з ХСН.
У доступній літературі ми не знайшли досліджень, присвячених визначенню предикторів розвитку ІР при ХСН. На основі кластерного аналізу нами було визначено, що інформативними предикторами ІР (рис. 2) у пацієнтів з ХСН і систолічною дисфункцією (СД) ЛШ за даними лабораторно-інструментальних досліджень виявилися рівні циркулюючого TNF-α (відношення шансів [ВШ] 3,900; 95% довірчий інтервал [ДІ] 1,257-12,102), сечової кислоти (ВШ 3,200; 95% ДІ 1,276-8,027), лептину (ВШ 3,117; 95% ДІ 1,196-8,126), відношення лептин/адипонектин (ВШ 3,030; 95% ДІ 1,106-8,30), середній тиск у легеневій артерії – ЛА (ВШ 3,048; 95% ДІ 1,360-6,831), ПЗВД ПА (ВШ 2,884; 95% ДІ 1,160-7,171) [6].
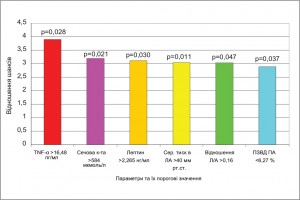 Рис. 2. Результати кластерного аналізу незалежних змінних, які впливають на розвиток ІР у хворих із хронічною систолічною СН
Рис. 2. Результати кластерного аналізу незалежних змінних, які впливають на розвиток ІР у хворих із хронічною систолічною СНПідвищений рівень TNF-α у наших пацієнтів із ХСН та ІР узгоджується з даними клінічних й експериментальних досліджень, у яких описано зв’язок активності гормонів жирової тканини з підвищенням експресії TNF-α у хворих з ожирінням [32, 33, 49]. Введення екзогенного TNF-α тваринам може індукувати резистентність до інсуліну, тоді як його нейтралізація може підвищити чутливість до останнього [63]. Зазначені механізми впливу TNF-α здійснює через порушення регуляції генів, які відповідають за біологічну дію інсуліну, підвищення рівня вільних жирних кислот через стимуляцію ліполізу, інгібуючий вплив на рецептори, які активують проліферацію пероксисом (peroxisome proliferator-activated receptors – PPAR) [55, 62].
Описаний раніше зв’язок ЕД із погіршенням периферичного кровообігу [18, 37] може бути справедливим і для наших пацієнтів, оскільки хворі із приростом діаметра плечової артерії у фазі реактивної гіперемії <6,27 % мають майже в 3 рази вищі шанси на виникнення ІР (рис. 2).
Як обгрунтування зв’язку розвитку ІР із підвищенням рівня середнього тиску в ЛА можна розглядати погіршення ендотеліальної функції у хворих з ІР. Відомо, що ЕД асоціюється із посиленням констрикторної активності дрібних і середніх гілок системи ЛА [29].
У результаті дослідження довготермінового клінічного прогнозу пацієнтів із систолічною ХСН нами було встановлено, що медіана досягнення комбінованої критичної точки (госпіталізація або смерть внаслідок серцево-судинних причин) у групі хворих з ІР становила 5,5 міс, а в групі пацієнтів без ІР – 11,7 міс. Відмінність між групами за лог-ранговим тестом достовірна – р=0,003 (рис. 3).
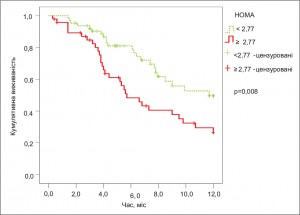 Рис. 3. Криві настання комбінованої критичної точки у пацієнтів з ХСН і СДЛШ залежно від наявності ІР
Рис. 3. Криві настання комбінованої критичної точки у пацієнтів з ХСН і СДЛШ залежно від наявності ІРШанси на досягнення критичної клінічної події зростають удвічі у хворих з ІР (ВШ 2,257; 95% ДІ 1,309-3,889) порівняно з пацієнтами без зазначеного феномена.
Ці дані збігаються з результатами поодиноких досліджень, у яких хворі з ХСН та ІР мали несприятливий прогноз щодо виживаності (р<0,001) порівняно з пацієнтами без ІР [7].
Специфічні підходи до корекції ІР при ХСН на сьогодні відсутні. Становлять інтерес результати пілотного дослідження щодо впливу метформіну на ІР і фізичну активність у хворих із ХСН [64]. У подвійному сліпому плацебо-контрольованому дослідженні взяли участь 62 пацієнти з ІР і ХСН без цукрового діабету (ЦД). Середній вік становив 65,2±8,0 років; 90% обстежених – чоловіки; ФВ ЛШ – 32,6±8,3%; розподіл на ФК за NYHA I, II, III, IV – 11, 45, 6 і 0 пацієнтів відповідно. Учасників рандомізували на прийом протягом 4 міс метформіну (n=39, добова доза 2 г) або плацебо (n=23). ІР визначалась за критерієм індексу резистентності до інсуліну (натще) НОМА ≥2,7. Толерантність до фізичних навантажень за даними кардіопульмонального навантажувального тесту і НОМА оцінювались одразу та через 4 міс спостереження. Порівняно з плацебо, на тлі терапії метформіном знизився індекс НОМА (з 5,8±3,8 до 4,0 ±2,5; р<0,001), і це поєднувалось зі зниженням маси тіла на 1,9 кг (р<0,001). Первинна кінцева точка дослідження – пік споживання кисню (VO2), не відрізнялася між групами. Проте застосування метформіну асоціювалося із покращенням вторинної кінцевої точки – зниженням відношення хвилинної вентиляції до продукції вуглекислого газу (VE/VCO2 slope) з 32,9±15,9 до 28,1±8,8 (р=0,034). У групі, якій терапія проводилась метформіном, НОМА був достовірно пов’язаний зі зменшенням VE/VCO2 slope (R=0,41; p=0,036). Отже, у хворих з ХСН та ІР лікування метформіном сприяло зменшенню ІР і VE/VCO2 slope та значному зниженню маси тіла, але без покращення пікового споживання кисню, тобто первинної кінцевої точки дослідження. Обмеженням цього дослідження є невелика кількість пацієнтів і необхідність оцінки впливу фізичних навантажень за наявності ІР у хворих з ХСН із застосуванням метформіну і без використання зазначеного препарату. Очевидно, що дослідження в цьому напрямі доцільно продовжувати.
Клінічно важливим залишається питання щодо реального впливу лікарських засобів, які використовуються у стандартній схемі лікування пацієнтів із ХСН, на чутливість до інсуліну у таких хворих. Основою дискусії є доцільність надання переваги β-адреноблокаторам (БАБ) з вазодилатуючою дією у пацієнтів з ХСН та ІР.
Опубліковано дані про те, що БАБ ІІІ покоління (такі як карведилол, небіволол), зменшуючи периферичний опір судин і посилюючи периферичний кровообіг, потенційно покращують доставку інсуліну до тканин і поглинання глюкози тканинами [38, 40, 41, 43]. У нашому дослідженні не виявлено достовірних відмінностей між часткою хворих з ХСН у групах з ІР та без ІР, які застосовували карведилол або бісопролол (р=0,158). Порівняльний аналіз величини індексу НОМА у пацієнтів, яких лікували карведилолом, і хворих, яким терапія проводилась бісопрололом, не виявив достовірних відмінностей між зазначеними групами пацієнтів (р=0,633). Можливо, цей факт асоціюється з обмеженістю досліджуваної вибірки (84 хворих з ішемічною кардіоміопатією і 23 – з дилатаційною кардіоміопатією). Водночас отримані дані свідчать, що поступове покращення функціональної активності у пацієнтів із ХСН призводить до зменшення індексу НОМА або до його нормалізації [6]. За даними проспективного 3-місячного спостереження 23 хворих із клінічно контрольованим «титруванням вгору» нейрогуморальних антагоністів (у тому числі БАБ до максимальних доз), виявлено достовірне зниження індексу НОМА (рис. 4) і збільшення частки пацієнтів з його нормальними значеннями: з 12 вихідних «інсулінорезистентних» хворих через 3 міс контрольованого лікування нормалізація індексу НОМА спостерігалася у 8 випадках (р=0,008). При цьому тип БАБ, який застосовувався, не мав значення.
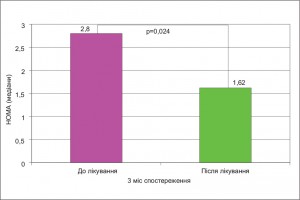 Рис. 4. Величина індексу НОМА на початку та наприкінці 3-місячного контрольованого амбулаторного лікування пацієнтів з ХСН і СДЛШ (n=23)
Рис. 4. Величина індексу НОМА на початку та наприкінці 3-місячного контрольованого амбулаторного лікування пацієнтів з ХСН і СДЛШ (n=23)Отже, ефективне стандартне лікування хворих з ХСН, згідно з нашими даними, сприяє зменшенню ІР.
Таким чином, ІР – об’єктивний феномен, який спостерігається майже у половини пацієнтів з ХСН без супутнього ЦД, має специфічні патофізіологічні риси та негативно впливає на клінічний прогноз. Контрольоване амбулаторне лікування хворих з ХСН, яке базується насамперед на «титруванні вгору» дози нейрогуморальних антагоністів, може бути передумовою до подолання ІР.
Список літератури знаходиться в редакції.