30 квітня, 2020
Формування й оптимальна корекція зовнішньосекреторної панкреатичної недостатності у дітей
 Основною особливістю дитячої гастроентерології порівняно з лікуванням захворювань травного тракту у дорослих є те, що педіатри, на відміну від лікарів-терапевтів, значно обмежені у виборі як діагностичних методик, так і лікарських препаратів, оскільки не всі підходи, які використовуються в гастроентерологічній практиці у дорослих, можна застосувати у дітей. І особливо яскраво ці відмінності проявляються при захворюваннях підшлункової залози (ПЗ).
Основною особливістю дитячої гастроентерології порівняно з лікуванням захворювань травного тракту у дорослих є те, що педіатри, на відміну від лікарів-терапевтів, значно обмежені у виборі як діагностичних методик, так і лікарських препаратів, оскільки не всі підходи, які використовуються в гастроентерологічній практиці у дорослих, можна застосувати у дітей. І особливо яскраво ці відмінності проявляються при захворюваннях підшлункової залози (ПЗ).
На сьогодні захворювання ПЗ залишаються найменш вивченою темою у загальній гастроентерології. Це насамперед зумовлено тим, що ПЗ, яка виконує функцію основної сполучної ланки між ендокринною і травною системами, є унікальним органом навіть для такої складної багаторівневої біологічної системи, як організм людини. Саме ПЗ виконує функції контролю енергетичного обміну, надходження пластичних речовин і синтезу енергії від моменту споживання їжі до моменту внутрішньоклітинного синтезу АТФ і, відповідно, відіграє важливу роль у регулюванні захисно-пристосувальних механізмів. Потенційна дисфункція ПЗ із формуванням гострої або хронічної внутрішньо- та зовнішньосекреторної недостатності у пацієнтів із патологією будь-якого ґенезу є додатковою прогностичною несприятливою ознакою для збереження життєздатності людського організму у будь-який віковий період. При цьому анатомо-топографічні особливості розташування такого важливого органа є досить несприятливими для рутинного медичного спостереження та інструментального обстеження – секрет ПЗ отримати складно, а методи дослідження є глибокоінвазивними. Це неабияк ускладнює діагностику, особливо у дітей, у яких застосування інвазивних і потенційно травматичних методів дуже обмежене.
Крім цього, в дитячому віці особливості патології ПЗ мають свою специфіку, про яку слід пам’ятати як педіатрам, так і лікарям сімейної медицини. Так, клінічні симптоми ураження ПЗ у дітей часто не є класичними, значно відрізняються від клінічних проявів у дорослих і не завжди вкладаються у пропедевтичні канони. Для дітей не характерні яскраві клініко-лабораторні прояви, зовнішньосекреторна панкреатична недостатність переважно клінічно не проявляється. Це можна пояснити надзвичайно великими компенсаторними можливостями ПЗ, що дозволяють компенсувати недостатність ферментів аж до 90% втрати функціональності [1].
Існують також об’єктивні труднощі інтерпретації отриманих результатів лабораторних, функціональних та інструментальних досліджень ПЗ у дітей. Цьому сприяють і вже згадана неможливість одержання матеріалу для морфологічного дослідження органа, і труднощі діагностики захворювання на ранніх етапах. Слід пам’ятати, що через своє анатомічне розташування ПЗ легко залучається у будь-який патологічний процес, який відбувається у шлунково-кишковому тракті [1, 2]. Ця особливість теж є досить характерною саме для педіатричної практики – однією з важливих характеристик будь-яких захворювань травної системи у дітей є їх поєднаний характер, або залучення у патологічний процес одночасно декількох відділів шлунково-кишкового тракту. Зокрема, в 86% випадків хронічні захворювання ПЗ у дітей є вторинними, тобто розвиваються на тлі іншої соматичної патології [2]. Частково цьому сприяють деякі анатомо-фізіологічні особливості дитячого віку, зокрема, висока васкуляризація, яка характерна для дітей і визначає потенційні мікроциркуляційні порушення, що виникають при багатьох патологічних станах і зумовлюють розвиток транзиторних розладів. І навпаки – зниження екзокринної функції, що навіть має транзиторний характер, призводить до виникнення мальасиміляції та визначає виникнення потенційних метаболічних розладів. Тому багато захворювань у дітей, навіть безпосередньо не повязаних з ураженням травної системи (наприклад, алергічна патологія), можуть супроводжуватися порушеннями травлення і всмоктування різного ступеня вираженості.
Розлад діяльності ПЗ також може бути наслідком інших чинників – перенесеної інтоксикації, аутоімунних захворювань, систематичного порушення характеру і режиму харчування. Не останнє місце посідають різного роду ятрогенні фактори – вплив антибіотикотерапії, прийом протимікробних засобів, різні медикаментозні отруєння, а також наявність глистяної інвазії з локалізацією в протоках ПЗ, травми живота і спини, падіння з висоти.
З огляду на характерну для дитячого віку коморбідність захворювань травної системи, до порушень екзокринної функції ПЗ (крім можливих аномалій розвитку проток ПЗ) можуть призвести атрофічний гастрит, дуоденіт, гострий і хронічний холецистит, холелітіаз і навіть наявність дисахаридазної недостатності [1].
Все вищенаведене висуває особливі вимоги до педіатрів: необхідні знання основних причин ураження ПЗ, підходів до призначення ферментотерапії, а також властивостей, складу та переваг сучасних ферментних препаратів.
Зовнішньосекреторна недостатність ПЗ є класичним патологічним синдромом, який характеризується абсолютним або відносним дефіцитом ферментів, екскретованих ПЗ у просвіт дванадцятипалої кишки, і клінічно проявляється ознаками мальдигестії та мальабсорбції [3, 4].
Екзокринна недостатність ПЗ переважно є результатом загального зниження вироблення ферментів. Така ситуація характерна для гострого і хронічного панкреатиту, муковісцидозу, травм ПЗ, первинного склерозивного холангіту, аномалій розвитку ПЗ. Крім цього, екзокринна недостатність ПЗ може бути результатом ізольованого зниження продукції ферментів – не дуже часто, але періодично доводиться стикатися з вродженою недостатністю ліпази або трипсину, або амілази. Ще рідше трапляється екзокринна недостатність без істинної ферментної недостатності, що є винятково наслідком порушення активації ферментів у тонкій кишці. Відомо, що більшість ферментів перебувають у неактивній формі і становлять собою проензими, які активуються в дванадцятипалій кишці під впливом ентерокіназ.
Отже, дефіцит у дванадцятипалій кишці ентерокіназ та інших ферментів, які беруть участь у процесі активації, може викликати розвиток клінічного симптомокомплексу, характерного для зовнішньосекреторної недостатності навіть при безперебійній роботі ПЗ.
Небагато авторів описують поширеність і наслідки перенесеного в дитячому віці гострого панкреатиту. Як правило, цією патологією займаються дитячі хірурги. За даними North American Society for Pediatric Gastroenterology, Hepatology and Nutrition (NASPGHAN), частота гострого панкреатиту у дітей становить
Разом з вищенаведеними нозологіями українські педіатри часто послуговуються терміном «реактивний панкреатит», правомірність якого є предметом жвавих дискусій серед дитячих гастроентерологів. Відповідно до сучасної офіційної класифікації, серед нозологічних форм ураження ПЗ значаться тільки гострий і хронічний панкреатит, аномалії та вади розвитку ПЗ, функціональні розлади, представлені дисфункцією сфінктера Одді за панкреатичним типом. Діагноз реактивний панкреатит, як і раніше, залишається напівофіційним спрощеним визначенням вторинного характеру ураження структури ПЗ.
На думку багатьох дитячих гастроентерологів, типовий для дорослих симптомокомплекс при панкреатиті в педіатричній практиці зустрічається досить рідко. Набагато частіше йдеться про патологію ПЗ вторинного характеру (насамперед про захворювання гастродуоденальної зони) і патологію, пов’язану з різноманітними розладами панкреатичної секреції, кровообігу, підвищенням тиску в системі проток, дуоденостазом. Реактивний панкреатит у дітей може бути різновидом панкреатиту, спровокованого якимось запальним процесом в організмі дитини (гостра респіраторна інфекція, грип, ангіна). Іноді захворювання може маніфестувати після надмірного вживання продуктів, що чинять підвищену подразливу дію на травну систему. Морфологічним субстратом таких реактивних змін є інтерстиціальний набряк тканин ПЗ, що зазвичай має зворотний характер [1].
В останнє десятиліття спостерігається несприятлива тенденція. Зокрема, така патологія, як хронічний панкреатит, не тільки все частіше діагностується в педіатричній практиці [4], а й має значно тяжчий перебіг, ніж у дорослих. При цьому досліджень, результати яких дають відповіді на всі фундаментальні питання, що стосуються дитячого панкреатиту, в світі досить мало. І незважаючи на величезний досвід щодо патофізіології, етапів розвитку, особливостей клінічної картини та діагностики цієї патології у дорослих, слід дотримуватися обережності при екстраполюванні цих даних на хворих дітей, оскільки панкреатит у них має іншу ніж у дорослих етіологію, різні прояви та наслідки [4, 5].
На жаль, прогресування зовнішньосекреторної недостатності призводить до порушення травлення, всмоктування жирів і жиророзчинних вітамінів, дефіциту поживних речовин, який може стати причиною затримки росту, формування прогресуючого абдомінального больового синдрому. При цьому розвиток патологічних порушень при зовнішньосекреторній недостатності ПЗ відбувається в такому порядку: мальдигестія та мальабсорбція, стеаторея і порушення статусу харчування пацієнта (мальнутриція). Остання стадія є основною причиною розвитку ускладнень і навіть передчасної смерті дорослих пацієнтів [7, 8]. Безумовно, для максимальної мінімізації ризику розвитку тяжких ускладнень зовнішньосекреторної панкреатичної недостатності необхідно не тільки вчасно її виявити, ретельно з’ясувати причину порушення функції ПЗ, а й максимально адекватно скоригувати порушення травлення та всмоктування. Особливе значення це має в дитячому віці, коли будь-які, навіть незначні похибки в харчуванні та засвоєнні харчових інгредієнтів можуть призвести до розвитку тяжкої мальнутриції [2, 9, 10]. Тому саме в педіатрії пріоритетом у виборі терапевтичної тактики є призначення ферментної терапії та підбір адекватної дози ферментного препарату.
З цього приводу існують певні розбіжності в публікаціях вітчизняних авторів і зарубіжних рекомендаціях.
Згідно з усталеними традиціями, в українській педіатричній практиці дозу ферментного препарату підбирають індивідуально протягом перших тижнів лікування залежно від наявності та ступеня вираженості екзокринної недостатності ПЗ. При цьому тривалість терапії визначають індивідуально, а прийом препарату припиняють у разі зникнення клінічних (поліпшення стану хворого) і копрологічних (зникнення поліфекалії, зменшення або зникнення діарейного синдрому, наростання темпів збільшення маси тіла, зникнення креатореї, амілореї та стеатореї) ознак мальдигестії та мальабсорбції. У більшості описаних випадків повідомлялося про короткочасне (не більше 2-3 тижнів) призначення ферментів переривчастими курсами. Дозування ферментного препарату розраховують за ліпазою. Рекомендованою стартовою дозою для дітей віком до 4 років є 1000 ОД ліпази на 1 кг маси тіла на добу, а для дітей старше 4 років – 500 ОД ліпази на 1 г жирів у добовому об’ємі їжі. Дітям шкільного віку та підліткам рекомендується 10 000-25 000 ОД на прийом їжі [11]. За відсутності ефекту дозу препарату поступово збільшують. При тяжкій екзокринній недостатності використовують 4000-5000 ОД ліпази на 1 кг маси тіла на добу [12].
Зарубіжні рекомендації та протоколи пропонують іншу тактику: згідно з консенсусними рекомендаціями ESPGHAN/NASPGHAN (2015) [13], дозу ферментного препарату розраховують за ліпазою, починаючи з 1000 ОД ліпази на 1 кг маси тіла на прийом їжі для дітей молодше 4 років і 500 ОД ліпази на 1 кг маси тіла на прийом їжі для дітей старше 4 років. Немовлятам рекомендують давати від 2000 до 4000 ОД ліпази на 120 мл дитячої суміші або на одне годування грудним молоком.
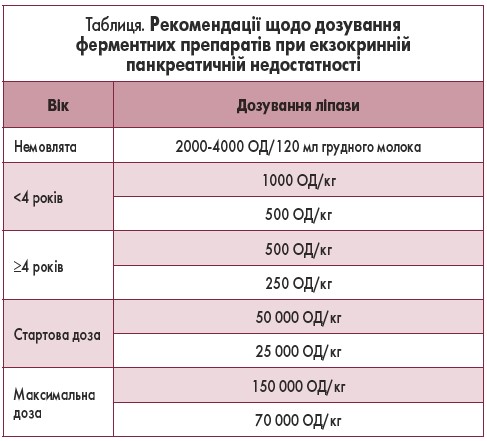 У дітей старшого віку рекомендована доза становить 10 000-25 000 ОД на прийом їжі й половина дози – на перекуси. Дітям молодше 4 років із муковісцидозом зазвичай потрібно від 1000 до 2500 ОД на 1 кг маси тіла на прийом їжі, для дітей старше 4 років використовується від 500 до 2500 ОД ліпази на 1 кг маси тіла, а для підлітків – від 25 000 до 40 000 ОД ліпази [14]. Сучасні рекомендації з дозування ферментних препаратів у пацієнтів різного віку наводяться у зведеній таблиці керівництва з екзокринної панкреатичної недостатності (2017) [15].
У дітей старшого віку рекомендована доза становить 10 000-25 000 ОД на прийом їжі й половина дози – на перекуси. Дітям молодше 4 років із муковісцидозом зазвичай потрібно від 1000 до 2500 ОД на 1 кг маси тіла на прийом їжі, для дітей старше 4 років використовується від 500 до 2500 ОД ліпази на 1 кг маси тіла, а для підлітків – від 25 000 до 40 000 ОД ліпази [14]. Сучасні рекомендації з дозування ферментних препаратів у пацієнтів різного віку наводяться у зведеній таблиці керівництва з екзокринної панкреатичної недостатності (2017) [15].
Дозування і тривалість прийому ферментів є складними аспектами лікування захворювань ПЗ у дітей, оскільки різні мікросфери з ентеросолюбільним покриттям не є біоеквівалентними in vitro і все ще недостатньо клінічних досліджень для визначення біодоступності препаратів in vivo.
Крім того, існують інші, відмінні від вітчизняних, погляди на критерії компенсації стану дитини. Тоді як в Україні вони ґрунтуються на клінічних і копрологічних аспектах, що досить відносно з урахуванням неспецифічності симптомів ураження ПЗ, то за рекомендаціями ESPGHAN/NASPGHAN, діти з хронічним панкреатитом мають проходити скринінг на екзокринну недостатність ПЗ через кожні 6-12 місяців із дослідженнями рівня фекальної еластази або 72-годинного фекального збору жиру (рекомендація 3.5а, сильна рекомендація; докази низької якості) [5].
Таким чином, сучасна статистика та дані численних публікацій доводять, що захворювання ПЗ є серйозною медико-соціальною проблемою, зумовленою великою кількістю чинників, у тому числі й тенденцією до зростання запальних захворювань ПЗ і різних ускладнень.
У сучасній педіатричній панкреатології все ще залишається багато невирішених питань.
На жаль, досі не розроблені єдині й універсальні критерії діагностики хронічного панкреатиту, як і не існує загальноприйнятого підходу до обстеження дітей із ризиком розвитку або з наявною панкреатичною недостатністю. Відсутні прості достовірні діагностичні методи – функціональні проби не стандартизовані, багато спеціалізованих відділень використовують власні модифікації проб і критерії оцінювання їх результатів. На сьогодні провідні експерти-панкреатологи активно працюють над розробленням уніфікованих алгоритмів, які враховували б основні характеристики наявних методів діагностики: економічну доступність, чутливість і специфічність діагностичних тестів, інвазивність діагностики, складність виконання та інші важливі моменти.
Ще одним перспективним напрямом у сучасній панкреатології є розроблення адекватних принципів нутритивної підтримки пацієнта із зовнішньосекреторною панкреатичною недостатністю, що розвивається або вже розвинулася, принципів адекватної корекції та комплексної терапії хронічного панкреатиту в педіатрії, застосування системного підходу в процесі поетапної терапії.
Література
- Белоусова О.Ю. Заболевания поджелудочной железы у детей, сопровождающиеся развитием экзокринной недостаточности: тактика обследования и возможности коррекции // Сучасна гастроентерологія. – 2014. – № 3. – С. 51-58.
- Abu-El-Haija M., Kumar S., Quiros J.A., Balakrishnan K., Barth B., Bitton S. et al. Management of Acute Pancreatitis in the Pediatric Population: A Clinical Report From the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition Pancreas Committee. Journal of pediatric gastroenterology and nutrition. 2018; 66 (1): 159-176; doi: 10.1097/MPG.0000000000001715.
- Ильченко А.А. Внешнесекреторная недостаточность поджелудочной железы и ее коррекция // Русский медицинский журнал. – 2013. – Т. 21, № 13. – С. 741-744.
...
15. Struyvenberg M.R., Martin C.R., Freedman S.D. Practical guide to exocrine pancreatic insufficiency – Breaking the myths. BMC Med. 2017; 15: 29. doi: 10.1186/s12916-017-0783-y.
Повний список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (55) 2020 р.


