1 травня, 2020
Патогенетически обоснованная стратегия лечения ФГИР: фокус на прокинетики
.jpg) Функциональные гастроинтестинальные расстройства (ФГИР) рассматриваются как наиболее распространенная патология желудочно-кишечного тракта (ЖКТ), в основе которой лежат комбинированные морфологические и физиологические отклонения, связанные с висцеральной гиперчувствительностью, нарушениями моторики ЖКТ, защитного слизистого барьера, иммунной функции и состава кишечной микробиоты, наличием микровоспаления, а также расстройствами со стороны центральной и энтеральной нервной системы.
Функциональные гастроинтестинальные расстройства (ФГИР) рассматриваются как наиболее распространенная патология желудочно-кишечного тракта (ЖКТ), в основе которой лежат комбинированные морфологические и физиологические отклонения, связанные с висцеральной гиперчувствительностью, нарушениями моторики ЖКТ, защитного слизистого барьера, иммунной функции и состава кишечной микробиоты, наличием микровоспаления, а также расстройствами со стороны центральной и энтеральной нервной системы.
ФГИР составляют 40% диагнозов гастроэнтерологического профиля, они являются одной из основных причин для направления в отделения неотложной помощи, тем самым истощая значительные объемы ресурсов здравоохранения. Отсутствие неинвазивных, дешевых, легко доступных биомаркеров для диагностики функциональной диспепсии и/или синдрома раздраженного кишечника делает врачей неуверенными в отношении клинического подхода к этим состояниям, несмотря на значительные успехи в понимании их патофизиологических механизмов и относительные терапевтические улучшения за последние десятилетия. Ряд традиционных диагностических исследований часто повторяются, несмотря на отрицательные результаты, что не дает надлежащих объяснений природы симптомов и оставляет пациентов разочарованными и обеспокоенными своими «странными» клиническими проблемами. Как следствие, пациенты обращаются за новыми (часто бесполезными) консультациями [22, 25, 27].
ФГИР не представляют угрозы для жизни пациентов, но значительно ухудшают ее качество.
Среди функциональных желудочно-кишечных расстройств ведущие позиции сохраняют синдром функциональной диспепсии (ФД), синдром раздраженного кишечника (СРК), дисфункция сфинктера Одди, для которых патогномоничными являются нарушения моторики, часто по спастическому типу.
Патофизиологические механизмы развития ФГИР, уточненные диагностические критерии и практические алгоритмы ведения пациентов были изложены в Римских критериях IV.
К основным патогенетическим факторам ФГИР, которые можно считать доказанными в настоящее время, относятся нарушения моторики ЖКТ. Это определяет целесообразность использования в базисной терапии данных заболеваний лекарственных препаратов, воздействующих на моторную функцию ЖКТ и препятствующих антиперистальтическим сокращениям гладких мышц, объединенных в группу прокинетиков.
Доказано, что у пациентов с ФГИР механизмы физиологической регуляции существенно изменены. Нарушения моторики ЖКТ (наследственные, приобретенные или вызванные лекарственными препаратами) могут, таким образом, оказывать существенное влияние на потребление питательных веществ, транспорт, эвакуацию, всасывание и дальнейший транзит кишечного содержимого. При ФД и СРК с запором нарушена ритмическая регуляция ЖКТ в покое: снижены частота мигрирующего моторного комплекса кишечника и формирование пропульсивной перистальтики.
По современным представлениям, в регуляции моторно-эвакуаторной функции ЖКТ и сложной координационной деятельности всех его отделов участвуют энтеральная нервная система (ЭНС), интерстициальные клетки Кахаля, мигрирующий миоэлектрический комплекс. ЭНС локализуется в стенке пищеварительной трубки от пищевода до прямой кишки, состоит из множества нейронов, образующих ауэрбаховское и мейсснеровское сплетения. Регуляция ЭНС осуществляется на центральном, сегментарном и местном уровне – в самой пищеварительной трубке. Основными медиаторами ЭНС являются гормоны, нейротрансмиттеры (инсулин, нейротензин, холецистокинин, гастрин, глюкагоноподобные пептиды, глюкозозависимый инсулинотропный полипептид, ацетилхолин, норадреналин, серотонин, мотилин, допамин, оксид азота, энкефалины), которые прямо или через сложные рефлекторные взаимодействия и рецепторный аппарат влияют на тонус гладкомышечной клетки и тем самым регулируют моторику всех отделов ЖКТ.
Важнейшим мессенджером в регуляции двигательной функции желудка является допамин, который секретируется в желудочной стенке, действует на расположенные в ней специфические допаминовые рецепторы и оказывает ингибирующее действие на моторику желудка.
Интерстициальные клетки Кахаля образуют сеть функционально связанных клеток в мышечном слое ЖКТ, где они генерируют и передают электрическую активность, которая контролирует функцию гладких мышц. Они являются водителями устойчивого ритма разных отделов ЖКТ, выполняют роль интермедиаторов нейромышечной трансмиссии (передачи импульсов от нервной ткани на гладкомышечные клетки).
В соответствии с экспериментальными данными, при различных нарушениях моторики были выявлены наследственные и приобретенные потенциально обратимые изменения. В недавних исследованиях поднимались вопросы о потенциальной роли макрофагов как модуляторов моторики ЖКТ. Эти макрофаги образуют трехмерную сеть внутри мышечных слоев и продуцируют различные медиаторы, которые могут изменять функцию кишечника [7]. Совокупность упомянутых факторов обеспечивает двигательную функцию желудка – перистальтику, тонус гладких мышц, пропульсивную активность.
Мигрирующий миоэлектрический комплекс представляет собой высокоамплитудные потенциалы, которые возникают в двенадцатиперстной кишке и распространяются в дистальном направлении по толстой и тонкой кишке. Функциональная роль мигрирующего миоэлектрического комплекса заключается в изменении секреторной и двигательной активности соответствующего отдела ЖКТ, запуск пропульсивной перистальтики, во время которой происходит активная эвакуация кишечного содержимого.
Иннервация играет важную роль в регуляции моторики ЖКТ. Внутренняя, или кишечная нервная система образует мицеллярное сплетение с ганглиями, расположенными между круговым и продольным слоями мышечных волокон. Локализованные аномалии, такие как наследственный аганглионоз прямой кишки (болезнь Гиршпрунга) или приобретенная потеря ганглиозных клеток при ахалазии, нарушают нормальный характер активности и в контексте этих нарушений сфинктерических структур задерживают или даже блокируют прохождение содержимого просвета. Изменения в кишечных нейронах, нарушения их функций также могут способствовать возникновению различных расстройств, характеризующихся аномальной моторикой, таких как дисфункция пищевода при синдроме Шегрена, гастропарез, псевдообструкция или хронический запор.
Механизмы физиологической регуляции двигательной активности ЖКТ могут нарушаться при повреждении нейронов и ганглиев вследствие уменьшения их количества и дегенеративных изменений, функциональной недостаточности нейронов и ганглиев, при повреждении гладких мышц и интерстициальных клеток Кахаля.
Нарушение двигательной функции кишечника может выражаться усилением или ослаблением перистальтических и локальных (сегментирующих и маятникообразных) движений и быть обусловлено несостоятельностью нейрогуморальной регуляции, нарушением баланса нейротрансмиттеров и регуляторных пептидов, контролирующих основные функции кишечника. Одновременно у пациентов с ФГИР резко снижена толерантность ЭНС к растяжению и восприятию боли (висцеральная гиперчувствительность), что является основной причиной абдоминальной боли при СРК.
Формирование висцеральной гиперчувствительности большинство исследователей с современных позиций рассматривают как результат стрессорной нейромодуляции и изменений в оси мозг – ЖКТ – сенсибилизации ЭНС и ЦНС под влиянием психологического хронического стресса и стрессорных факторов внешней среды. При этом развивается относительный дефицит защитных стресс-лимитирующих систем ЖКТ (нейромедиаторные антагонисты ацетилхолина: норадреналин, серотонин, допамин и др.). Подавляя активность холинергических нейронов, стресс-лимитирующие системы уменьшают секрецию, подвижность и расслабляют сфинктеры, увеличивая болевой порог в оси мозг – ЖКТ.
У пациенов с ФГИР хронический стресс приводит к стойкой активации гипоталамо-гипофизарной оси, относительному дефициту стресс-лимитирующих систем. Хронический стресс у данных пациентов является причиной стереотипной нейромодуляции в оси мозг – ЖКТ, направленной в сторону уменьшения толерантности к восприятию боли и формирования висцеральной гиперчувствительности. По данным клинических исследований, нарушенное восприятие нормальных стимулов наблюдается у 60-96% пациентов с СРК [5]. Установлено, что стрессогенные факторы способны влиять на иммунную реактивность, а измененная иммунная реактивность – на восходящие сигналы ЦНС.
Принимая во внимание концептуальную важность взаимодействий между мозгом и кишечником, в будущих исследованиях необходимо определить, в какой степени эти корреляции являются следствиями измененной физиологии и связаны ли эти изменения в основном с соматическими проявлениями эмоциональных либо других психических проблем.
Патогенетические механизмы ФД разнообразны и могут включать психосоциальные факторы, нарушение аккомодации желудка, замедление эвакуации из желудка, измененную миоэлектрическую активность, расстройство моторики тонкой кишки. Нарушение аккомодации (адаптивного расслабления в ответ на поступление пищи в желудок) наблюдается у 41% пациентов с ФД.
Появляется все больше свидетельств того, что нарушение регуляции моторики желудка, характеризующееся расстройством желудочной релаксации вместе с антральной гипомобильностью, представляет собой ключевой механизм развития синдрома ФД. Гипотония антрального отдела может вызвать задержку опорожнения желудка, тогда как нарушения проксимальной функции (наличие каналов с транзиентным рецепторным потенциалом (TRP), особенно TRPA1 и TRPC, которые преимущественно экспрессируются в областях дна/тела желудка, ответственных за тоническую или спастическую активность органа) приводят к нарушению расслабления дна и тела с последующей гиперчувствительностью к растяжению.
Нарушение каждого компонента двигательной активности желудка вызывает появление соответствующей клинической симптоматики. Расстройства аккомодации желудка обусловливают появление раннего насыщения, тошноты, отрыжки. Ослабление моторики антрального отдела желудка и нарушение антродуоденальной координации вызывают ощущение тяжести и переполнения в эпигастрии после приема пищи. Данные нарушения наиболее характерны для такой разновидности ФД, как постпрандиальный дистресс-синдром. Изжога, отрыжка, ощущение горечи во рту возникают вследствие гастроэзофагеального и дуоденогастрального рефлюксов. Изменение моторики желудка и замедление эвакуации приводят к появлению тошноты и рвоты (синдром циклической рвоты и синдром хронической тошноты согласно Римским критериям ІV), функциональному дуоденостазу.
Транзит пищевого химуса по толстой кишке осуществляется в основном благодаря особенностям ее перистальтики: это быстрые непропульсивные сокращения в отдельных сегментах, которые уплотняют содержимое кишки, создают условия для всасывания и отвечают за формирование нормальных каловых масс, а также высокоамплитудные перистальтические сокращения, перемещающие содержимое по кишке. Сокращение кишечной стенки в разных ее отделах зависит также и от ретропульсивных, пропульсивных неперистальтических, тонических сокращений. Моторика толстой кишки стимулируется холинергическим влиянием, которое, в свою очередь, модулируется миоэлектрической активностью. Нарушение каждого вида сокращений стенки толстой кишки может приводить к появлению как запоров, так и диареи [13].
При функциональных заболеваниях кишечника нарушение моторной функции толстой кишки является ведущим фактором в патогенезе таких симптомов, как боль, метеоризм, запор, диарея. Среди пациентов с функциональными заболеваниями кишечника и запором 30% имеют диссинергию тазового дна с замедлением кишечного транзита, а около 5% – инертную толстую кишку вследствие потери нейронов или интерстициальных клеток Кахаля [27].
Таким образом, координированное действие стимулирующих и ингибирующих факторов обеспечивает нормальную перистальтику пищевода, желудка, двенадцатиперстной и толстой кишки.
В качестве ключевых факторов патогенеза СРК рассматривают генетическую предрасположенность, психоэмоциональный стресс, кишечные инфекции, повышение проницаемости слизистой оболочки и активации в ней иммунных процессов, пищевую непереносимость, нарушение всасывания желчных кислот, расстройства энтероэндокринной регуляции и др.
СРК связан с нарушением регуляции моторики кишечника, что выражается изменением «привычек» кишечника, спазмами кишечника и болью в животе. По результатам исследований у пациентов с СРК по сравнению с практически здоровыми лицами был усиленный моторный ответ на различные раздражители окружающей среды, такие как психологический стресс, пептидные гормоны или жирная пища [7]. Подвижность может быть увеличена или уменьшена в зависимости от особенностей пациента и индивидуального подтипа СРК.
Появляется все больше доказательств того, что ФД и СРК могут быть связаны с низким уровнем воспаления, вызывая соответствующие изменения моторики и висцеральной чувствительности. Особенно висцеральная гиперчувствительность может быть вызвана местным воспалением, изменениями плотности тучных клеток и их близости к окончаниям висцерального нерва. Сообщалось, что воспалительные и тучные клетки связаны с клинической тяжестью и симптомами СРК. Вопрос о том, вызван ли этот эффект бактериями (такими как Helicobacter pylori либо другими кандидатами в измененном микробиоме) или обусловлен специальными пищевыми компонентами и лекарствами, остается не решенным [7].
Клиницисту с учетом многообразия и изменчивости клинической картины функциональных нарушений приходится часто корректировать лечение, в том числе при сочетанных функциональных нарушениях, например СРК + ФД, СРК + билиарная дисфункция, ФД + билиарная дисфункция, а также при смене клинического варианта СРК. Все это требует пересмотра подхода к терапии и заставляет врача постоянно изменять тактику лечения.
Лечение ФГИР представляет собой нерешенную медицинскую проблему. Актуальной является оптимизация фармакотерапии, подразумевающая приоритет применения селективных препаратов с доказанной эффективностью, обладающих мультитаргетным действием, влияющих одновременно на несколько патогенетических звеньев этих заболеваний (в том числе при перекрестных сочетанных функциональных заболеваниях) или же оказывающих благоприятное действие при наличии коморбидной патологии и безопасных при длительном применении.
Учитывая высокую значимость нарушений моторики у пациентов с ФГИР, важно определять конкретный тип расстройств для последующего проведения патогенетической фармакотерапии.
Лечение функциональных расстройств ЖКТ предполагает длительный (4-8 недель) основной курс с последующим переходом на терапию в режиме «по требованию» в течение 6-12 месяцев.
Одним из широко применяемых современных и хорошо изученных препаратов, представленных компанией АТ «Киевский витаминный завод», является прокинетический препарат итоприда гидрохлорид – Мотоприд [27].
Механизм прокинетического действия итоприда гидрохлорида заключается в блокаде D2-допаминовых рецепторов, антихолинэстеразном эффекте, модулирующем влиянии на гормональную систему, благодаря чему осуществляется комплексный контроль моторики верхних отделов ЖКТ по сравнению с другими представителями класса прокинетиков, которые, как правило, не ингибируют ацетилхолинэстеразу (рис.).
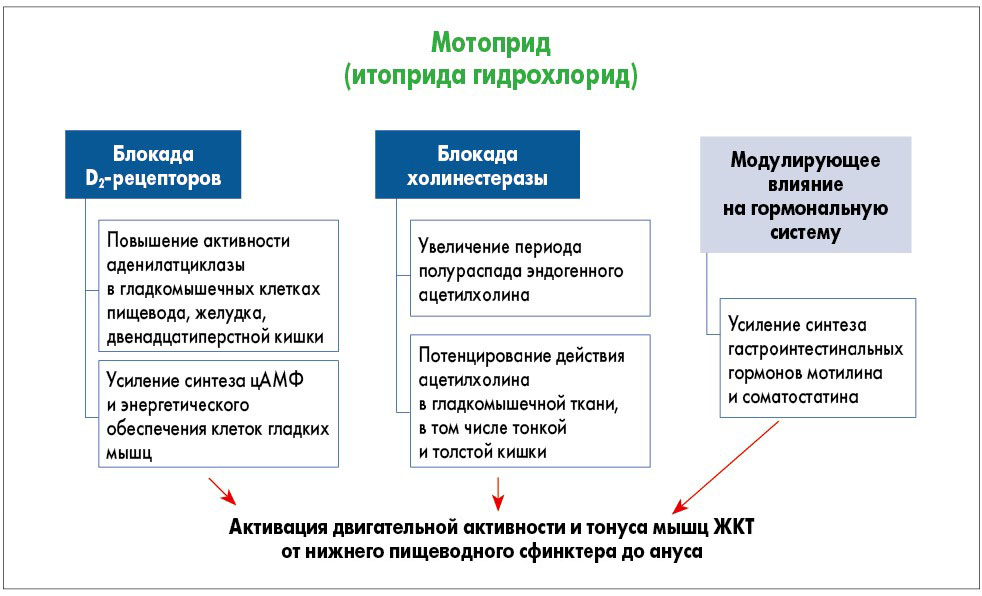 Рис. Патогенетические фармакологические эффекты препарата Мотоприд
Рис. Патогенетические фармакологические эффекты препарата Мотоприд
Блокируя D2-рецепторы, итоприд повышает активность аденилатциклазы и уровень цАМФ в гладких мышцах пищевода, желудка, двенадцатиперстной кишки, усиливает пропульсивную моторику, двигательную функцию и опорожнение желудка, ускоряет эвакуацию из него. Это дает основание рассматривать итоприда гидрохлорид в качестве препарата первой линии в лечении двигательных нарушений желудка.
Приоритетной прокинетической особенностью итоприда является его способность повышать перистальтическую активность мышц тонкой и толстой кишки, уменьшать время транзита пищевых масс по тонкой кишке, что обусловлено активацией пролонгированного высвобождения эндогенного ацетилхолина, модулированием и усилением кишечного транзита.
Отличительной особенностью итоприда является отсутствие межлекарственных взаимодействий. Он метаболизируется флавинзависимой монооксигеназой, a не энзимной системой, связанной с цитохромом Р450 (CYP450), т.е. итоприд не влияет ни на одну из CYP-опосредованных реакций в микросомах печени.
Отсутствие ингибирования цитохрома CYP450 свидетельствует и о минимальном гепатотоксичном действии препарата, что позволяет избежать нежелательного лекарственного взаимодействия и использовать его вместе с другими лекарственными препаратами, которые метаболизируются при помощи системы CYP450, без изменения фармакологических свойств последних, в том числе с ингибиторами протонной помпы, варфарином, диазепамом, диклофенаком натрия, нифедипином и др.
Итоприда гидрохлорид ингибирует преходящие расслабления нижнего пищеводного сфинктера и повышает его тонус, при этом уменьшая вероятность возникновения гастроэзофагеального рефлюкса и регургитации, что дает основание использовать его при гастроэзофагеальном рефлюксе, гастроэзофагеальной рефлюксной болезни (ГЭРБ) и ее неэрозивной форме.
Многообразные фармакологические эффекты итоприда проявляются в следующем:
- обладает противорвотным действием за счет взаимодействия с D2-рецепторами, находящимися в триггерной зоне, обусловливает дозозависимое подавление рвоты, вызванной апоморфином;
- не оказывает влияния на сывороточные концентрации гастрина;
- не влияет на длину интервала PQ, не оказывает кардиотоксического воздействия;
- обладает благоприятным профилем безопасности (в том числе для пациентов с сердечно-сосудистыми заболеваниями), что позволяет рекомендовать его при функциональных нарушениях органов пищеварения; можно сочетать с антисекреторными и ферментными препаратами, алгинатами, антацидами, урсодезоксихолевой кислотой;
- не проникает через гематоэнцефалический барьер, практически не дает побочных эффектов в виде центральных экстрапирамидных и нейроэндокринных расстройств; оказывает модуляторное влияние на гипоталамо-гипофизарно-адреналовую систему благодаря повышению концентрации соматостатина, мотилина и снижению уровня холецистокинина и адренокортикотропного гормона;
- отличается хорошей переносимостью и высоким профилем безопасности.
Для взрослых рекомендуемая доза составляет 150 мг в сутки (по 1 таблетке (50 мг) 3 раза в сутки перед приемом пищи). Указанную дозу можно снизить с учетом возраста пациента и редукции симптомов. Продолжительность приема в клинических исследованиях – до 8 недель.
Лечение больных с ФГИР проводится с учетом клинического варианта течения заболевания и предполагает назначение препаратов, нормализующих моторику верхних отделов ЖКТ (прокинетиков), антисекреторных препаратов. С учетом доказанной эффективности и высокого профиля безопасности наиболее предпочтительным препаратом из группы прокинетиков в лечении больных с ФД в настоящее время также является итоприда гидрохлорид. Мотоприд представляет собой препарат выбора при сочетанной ФД и СРК как наиболее частой ассоциации нарушений моторики.
Собрана большая доказательная база клинической эффективности итоприда гидрохлорида на основании результатов мультицентровых исследований, проведенных в разных странах.
Результаты метаанализа 10 исследований свидетельствовали о более высокой эффективности прокинетиков при лечении ФД по сравнению с блокаторами Н2-гистаминовых рецепторов и плацебо [23]. Согласно результатам метаанализа, проведенного в более поздние сроки, в котором были обобщены данные 14 исследований, включавших 1053 больных с ФД, эффективность прокинетиков в лечении этой патологии составила 61%, значительно превысив эффективность плацебо (41%). Показатель NNT при лечении прокинетиками был равен 4 (уровень доказательности IА) [6, 12, 23].
Xuan Huang и соавт. (2012) оценили терапевтическую эффективность итоприда у пациентов с ФД по сравнению с другими лекарственными средствами (домперидон, мозаприд, плацебо). Было включено 9 рандомизированных клинических исследований, в которых зарегистрировано 2620 случаев ФД; 1372 пациента получали лечение итопридом, а 1248 – плацебо или другими препаратами (контрольные группы). По сравнению с контрольными группами в группе итоприда были превосходные значения относительного риска – 1,11 (95% доверительный интервал – ДИ – 1,03-1,19; P=0,006), 1,21 (95% ДИ 1,03-1,44; P=0,02) и 1,24 (95% ДИ 1,01-1,53; P=0,04) для общей оценки состояния пациента, переполнения после приема пищи и раннего насыщения соответственно. Для оценки по опроснику Лидса по диспепсии средневзвешенное отклонение составило -1,38 (95% ДИ -1,75-1,01; P<0,01). Частота побочных эффектов была одинаковой в группе принимавших итоприд и в контрольной группе. Итоприд обладает хорошей эффективностью с точки зрения общей оценки пациентов, устраняет ощущения переполнения после приема пищи и раннего насыщения при ФД и показывает низкий уровень побочных реакций. Авторы заключили, что итоприд может значительно улучшить оценку ФД [5].
Y.S. Kim и соавт. (2005) сообщали о результатах пилотного исследования эффективности итоприда у 26 пациентов с легкой формой ГЭРБ (класс Савари – Миллера I, II степень) в дозе 150 и 300 мг в сутки на протяжении 30 дней. Авторы сделали вывод о том, что итоприд в дозе 300 мг был значительно эффективнее, чем 150 мг, при уменьшении общего процента времени с pH <4, общего времени с pH <4 и показателями по шкале DeMeester. Никаких серьезных побочных эффектов во время исследования не наблюдалось. Рекомендовано использовать итоприд по 100 мг 3 раза в день для купирования патологического рефлюкса у пациентов с ГЭРБ [8].
О.В. Крапивная и соавт. (2014) сообщали о терапевтической эффективности итоприда в комбинации с лактулозой при коморбидной патологии (сочетании ГЭРБ, ФД и СРК с запорами) у 60 пациентов в течение 4 недель. Авторы считают, что при назначении итоприда стало возможным успешно контролировать клинические симптомы ГЭРБ, ее неэрозивной формы, ФД, уровень рН в пищеводе и количество эпизодов гастроэзофагеального рефлюкса. Отмечали достоверное (Р<0,05) повышение частоты дефекации до 3 раз в неделю. Итоприд усиливает пропульсивную моторику пищевода, желудка и кишечника [24].
Перспективным направлением использования итоприда гидрохлорида является коррекция нарушений моторики у пациентов с гипомоторной дисфункцией желчного пузыря, желчевыводящих путей, сфинктера Одди [25, 26].
На сегодняшний день получены экспериментальные и клинические данные о стимулирующем влиянии итоприда гидрохлорида на моторику кишечника, что позволит использовать его при лечении пациентов с нарушением двигательной функции кишечника [16].
По результатам исследования итоприда гидрохлорид, в отличие от других прокинетиков, стимулирует как перистальтику, так и сегментарную активность кишечника путем повышения давления в толстой кишке, стимулирует контрактильную активность – от желудка до толстой кишки, что позволяет использовать его для лечения функционального запора [9]. В ряде исследований отмечено, что препарат ускоряет не только опорожнение желудка, но и уменьшает время транзита пищевых масс по тонкой кишке [26, 28]. Выявлено снижение выраженности кишечных симптомов при использовании итоприда гидрохлорида в ходе подготовки пациентов к колоноскопии [11].
Tadashi Tsubouchi и соавт. (2003) исследовали влияние итоприда гидрохлорида на двигательную активность толстой кишки in vitro и in vivo в сравнении с бензамидами, цизапридом и мозапридом. Итоприд стимулировал перистальтическую и сегментарную подвижность, вызванную изменением внутрипросветного давления в изолированной ободочной кишке in vivo. Хотя цизаприд и мозаприд усиливали сегментарную подвижность, они заметно снижали перистальтическую подвижность. У экспериментальных животных с имплантированными датчиками силы тензометрического измерения итоприд стимулировал сократительную активность ЖКТ от желудка до толстой кишки. Цизаприд стимулировал сократительную активность в антральном отделе желудка, подвздошной и восходящей ободочной кишке. Мозаприд стимулировал сократительную активность только в антральном отделе желудка и подвздошной кишке. In vivo итоприд ускорял транзит содержимого в толстой кишке, в то время как цизаприд и мозаприд не смогли его усилить.
Эти результаты показывают, что итоприд оказывает стимулирующее действие на перистальтику толстой кишки, отличное от такового у цизаприда и мозаприда. Авторы заключили, что итоприд может быть эффективным для лечения функциональных расстройств кишечника, таких как функциональный запор [17].
Xiaoling Zhang и соавт. (2019) в двойном рандомизированном исследовании с участием 80 пациентов с СРК, диареей и вздутием живота выявили, что у 40 пациентов основной группы, получавших итоприд в течение 6 недель исследования, отмечалось значительное улучшение абдоминальных симптомов по сравнению с группой контроля (40 больных). У пациентов, принимавших итоприд, отмечались более высокие эффективность терапии и общие показатели по сравнению с контрольной группой (P<0,05). Авторы делают вывод о том, что итоприд может облегчить клинические симптомы, улучшить качество жизни и психическое здоровье пациентов с СРК и диареей, сопровождающимися вздутием живота [18].
Собственное исследование, включавшее 30 пациентов с ФГИР (в соответствии с Римскими критериями IV, из них с СРК – 14 пациентов, с СРК + ФД – 12 пациентов, с СРК + ФД + дуоденогастральный рефлюксом – 4 пациента), продемонстрировало высокую терапевтическую эффективность препарата Мотоприд в дозе 150 мг в сутки в течение 2 недель. На фоне лечения препаратом Мотоприд у 27 (90%) больных отмечалась четкая положительная динамика клинических симптомов. У 14 (70%) из 20 пациентов исчезла боль в животе (у 6 пациентов слабая и умеренная боль исчезла к 20-му дню лечения, после выписки из гастроэнтерологического стационара и продолжения лечения на амбулаторном этапе). Полностью купированы ощущения тяжести, распирания и переполнения в эпигастрии, тошнота и метеоризм. К концу лечения (на 14-й день) дуоденогастральный рефлюкс не определялся у всех 4 пациентов при проведении фиброгастродуоденоскопии.
Отмечена значительная положительная динамика в опорожнении кишечника. У 23 (76,6%) пациентов дефекация нормализовалась, что проявилось полнотой опорожнения, нормализацией формы и консистенции кала. Частота дефекации изменилась с 1,5-2 раз в неделю до 3,5-5 раз в неделю, что позволяло уменьшить прием слабительных препаратов. Пять (21,7%) пациентов отмечали, что дефекация стала самостоятельной, но через 2-3 дня, а у 2 больных запоры сохранялись (эти пациенты не были привержены диетическим рекомендациям, принимали антидепрессанты, которые тормозят кишечный транзит).
На фоне лечения препаратом Мотоприд отмечалась положительная тенденция к улучшению качества жизни пациентов с ФД и СРК. Общая эффективность препарата Мотоприд была оценена как отличная у 19 (63,3%) пациентов; хорошая – у 9 (30%), удовлетворительный эффект отмечен у 2 (6,6%) пациентов, неудовлетворительный – не отмечен. Клинический опыт использования препарата Мотоприд подтвердил его безопасность.
Таким образом, назначение препарата Мотоприд в составе комплексной терапии обеспечивало регрессирование симптомов ФД, ДГР и запоров, что позволило считать препарат средством патогенетической терапии при ФГИР, протекающих с нарушениями моторной функции пищевода, желудка и кишечника.
Приоритетным является то, что прокинетик Мотоприд с двойным механизмом действия стимулирует перистальтику, сегментарную, пропульсивную и контрактильную активность кишечника. Это обосновывает целесообразность его назначения при запоре у пациентов с СРК, а в некоторых случаях и при СРК с диареей.
С позиций коморбидности, клинической эффективности и лекарственной безопасности Мотоприд (итоприда гидрохлорид) является приоритетным прокинетиком в лечении ФГИР, их перекрестов и других сопутствующих им заболеваний.
Мотоприд выгодно отличается от других прокинетиков по трем основным параметрам: наличию двойного механизма действия, отсутствию лекарственных взаимодействий и серьезных побочных эффектов.
Появление на отечественном фармацевтическом рынке препарата Мотоприд повышает доступность эффективной и безопасной терапии ФГИР у взрослых пациентов.
Литература
- Andreasson A., Talley N.J., Forsberg A.M. et al. Functional dyspepsia has doubled over two decades: 23 year prospective, longitudinal study of 1847 randomly selected subjects from the general population in Sweden. Gastroenterol. 2018; 154. (6,, suppl. 1): 8-14.
- Camilleri M., Ford A.C. Pharmacotherapy for irritable bowel syndrome. J. Clin. Med. 2017; 6 (11).
- Carbone F., Vandenberghe A., Holvoet L. et al. The therapeutic outcome of itopride in functional dyspepsia postprandial distress syndrome: a double-blind randomized, multicentre, placebo-controlled study. Gastroenterology. 2018. 154 (6, suppl. 1): S-91.
- Allescher H.D. et al. Mechanism of Action of STW 5 in Functional Dyspepsia and IBS. Dig. Dis. 2017; 35 (suppl. 1): 18-24.
- Huang H., Lv B., Zhang S. et al. Itopride therapy fir functional dyspepsia: A meta-analysis. Word J. Gastroenterol. 2012; 18: 7371-7377.
- Holtmann G., Talley N.J., Liebgrets T. et al. A placebocontrolled trial of itopride in functional dyspepsia. N. Engl. J. Med. 2006; 354: 832-840.
- Furness J.B. The enteric nervous system and neurogastroenterology. Gastroenterology & Hepatologу. 2012; 9: 286-294.
- Kim Y.S., Kim T.H., Choi C.S. et al. Effect of itopride, a new prokinetic, in patients with mild GERD: a pilot study. World J. Gastroenterol. 2005; 11 (27): 4210-4214.
- Kim H.J., Kim T.O., Shin B.C. et al. Efficacy of prokinetics with a split-dose of polyethylene glycol in bowel preparation for morning colonoscopy: a randomized controlled trial. Digestion. 2012; 86 (3): 194-200.
- Lim H.C., Kim Y.G., Lim J.H., Kim H.S., Park H. Effect of itopride hydrochloride on the ileal and colonic motility in guinea pig in vitro. Yonsei Med. J. 2008 Jun 30; 49 (3): 472-478.
...
28. Трухан Д.И. Функциональные гастроинтестинальные расстройства: выбор прокинетика с позиций коморбидности, клинической эффективности и лекарственной безопасности // Медицинский совет. – 2017. – № 5. – С. 108-115.
Полный список литературы находится в редакции.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (55) 2020 р.


