28 липня, 2015
Неиспользованные возможности в лечении артериальной гипертензии
 Несмотря на признание Комитетом экспертов ВОЗ более 10 лет назад того факта, что «артериальная гипертензия является основной причиной смерти в мире», и огромного интереса к этой проблеме со стороны медицинской общественности и производителей фармацевтических препаратов, нам не удалось достичь больших успехов в контроле артериальной гипертензии (АГ) за последние годы.
Несмотря на признание Комитетом экспертов ВОЗ более 10 лет назад того факта, что «артериальная гипертензия является основной причиной смерти в мире», и огромного интереса к этой проблеме со стороны медицинской общественности и производителей фармацевтических препаратов, нам не удалось достичь больших успехов в контроле артериальной гипертензии (АГ) за последние годы.
Об отсутствии значительного прогресса в контроле АГ в Украине свидетельствует тот факт, что за последние годы не удалось существенно уменьшить количество церебральных инсультов, которое, с точки зрения экспертов Европейского общества кардиологов, является суррогатным маркером контроля АГ в популяции.
Очевидно также, что проблема лечения АГ не связана с высокими технологиями, а определяется рутинной клинической практикой. Прежде всего речь идет о корректной диагностике указанного заболевания и повышении приверженности больных к приему антигипертензивных препаратов.
Несмотря на прогресс в диагностике АГ, в большинстве случаев диагностические решения принимаются так же, как и в конце XIX века. При всей кажущейся простоте, диагностика АГ до настоящего времени претерпевает процесс усовершенствования. Только в последнее время были даны основанные на доказательствах рекомендации в отношении того, где и как корректнее измерять артериальное давление (АД). В настоящее время предложены три варианта: измерение АД в медицинских учреждениях (офисное АД), измерение АД в домашних условиях (домашнее мониторирование АД) и измерение АД в течение суток с помощью специальных устройств (амбулаторное мониторирование АД). Какой из этих методов предпочтителен с точки зрения прогностического значения уровня АД и принятия решения о терапии?
До настоящего времени многие врачи во всем мире уделяют большее внимание офисному измерению АД для принятия решения о терапии, хотя домашнее мониторирование АД имеет большее прогностическое значение и позволяет во многих случаях избежать неоправданного назначения медикаментозной терапии в случае гипертензии белого халата.
Наиболее высокая частота выявления гипертензии белого халата отмечается у пожилых больных, беременных, пациентов с сахарным диабетом, у которых она достигает 25%, и домашнее самоизмерение АД имеют при этом наибольшее значение.
Домашнее измерение АД больными получает все большее распространение не только по этой причине, но прежде всего вследствие простоты и доступности. Тем не менее оно требует обучения пациента или тех, кто измеряет АД больному в домашних условиях. Ошибочно полагать, что офисное измерение АД лишено ошибок и погрешностей, основными из которых являются: игнорирование подготовки пациента к измерению АД, использование неверифицированного и некалиброванного оборудования, использование манжеты несоответствующего размера, округление значения АД до ближайшей цифры, кратной 5 или 10 мм, и, наконец, самая частая причина ошибок – общение врача или медсестры при измерении АД с больным.
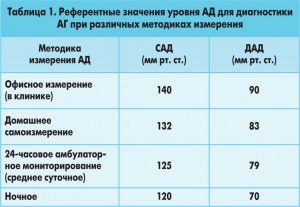
Следует также учитывать разницу в референтных значениях АД при различных видах измерений, полученную по данным исследования PAMELLA (табл. 1).
При домашнем измерении значения АД существенно ниже, чем при офисном. В том случае, когда врач при домашнем измерении ориентируется на референтное значение 140/90 мм рт. ст. (как при офисном), это приводит к тому, что у больных не диагностируется АГ, но делается ложный вывод о наличии гипертензии белого халата.
При наличии у пациента истинной гипертензии белого халата, то есть нормального АД по данным как домашнего измерения, так и амбулаторного мониторирования, в случае повышения АД при офисном измерении дополнительный сердечно-сосудистый риск увеличивается незначительно по сравнению с лицами без АГ. Однако у больных с частичной гипертензией белого халата, то есть при нормальном уровне АД по данным одного из двух вариантов измерения внеофисного АД (домашнего либо амбулаторного мониторирования), сердечно-сосудистый риск незначительно отличается от риска у больных АГ, повышаясь в 2,76 раза по сравнению с лицами, имеющими нормальное АД.
Очевидным преимуществом амбулаторного мониторирования АД является также возможность выявления замаскированной АГ, которая современными рекомендациями определяется как наличие у больного с нормальным или высоким нормальным АД при измерении в клинике внеофисного АД в дневное время ≥135/85 мм рт. ст. или ночного АД ≥120/70 мм рт. ст., или 24-часового среднего АД ≥130/80 мм рт. ст.
По результатам популяционного исследования IDACO, основанного на анализе баз данных 11 стран (n=9691), из общего числа пациентов, в отношении которых проводилось амбулаторное мониторирование, замаскированная АГ выявлялась у 18% больных, не получавших антигипертензивную терапию, и значительно чаще – у нормотензивных пациентов с сахарным диабетом (около 30%), причем риск кардиоваскулярных событий в течение 11 лет наблюдения у них был такой же, как у больных АГ 1 степени.
В этом же исследовании была выявлена еще более важная проблема: у пациентов с АГ, получавших терапию антигипертензивными препаратами, частота выявления замаскированной АГ достигала 30% у больных без сопутствующего сахарного диабета и 42% при сопутствующем сахарном диабете. Фактически это означает, что, по данным офисного измерения АД, у трети пациентов без сахарного диабета и почти у половины больных с сопутствующим сахарным диабетом достигнут целевой уровень АД, при этом у пациента остается высокий риск кардиоваскулярных катастроф.
Кроме того, согласно результатам большинства исследований диагностическая чувствительность и прогностическое значение при домашнем измерении АД выше по сравнению с офисным.
Так, по данным исследования, в котором у 1789 лиц из общей популяции сравнивалось прогностическое значение двукратного скринингового офисного измерения АД с домашними измерениями в течение 4 недель, при наблюдении в течение 6,6 года прогностическим значением в отношении риска сердечно-сосудистой смертности обладало только систолическое АД (САД) при домашнем измерении. Увеличение САД при домашнем измерении на 1 мм рт. ст. повышало риск сердечно-сосудистой смертности на 2,1%.
С другой стороны, исследование PAMELLA, проведенное с участием 2048 жителей г. Монца (Италия), при наблюдении в течение 16 лет не позволило выявить достоверных различий офисного и внеофисного измерения АД в отношении риска сердечно-сосудистых событий и смертности.
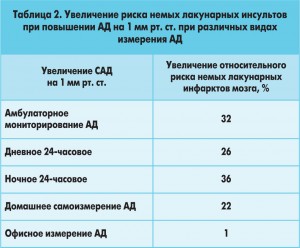
Во всех популяционных исследованиях было показано прогностическое преимущество внеофисного измерения АД в отношении риска развития повреждения органов-мишеней и немых лакунарных повреждений мозга (табл. 2).
Преимущества амбулаторного мониторирования очевидны и в диагностике циркадных колебаний АД.
Хорошо известно, что большинство кардиоваскулярных катастроф происходят в утренние часы, в период от 5 до 11 часов, в связи с чем существует предположение, что это может быть связано с утренним подъемом АД после просыпания.
В исследовании PAMELLA была предпринята попытка проверить эту гипотезу. У 2051 пациента в течение 16-летнего периода наблюдения по данным амбулаторного мониторирования определялось прогностическое значение среднего уровня АД на протяжении 2 часов до просыпания и в течение 2 часов после него. Среднее АД после просыпания коррелировало со среднесуточной вариабельностью АД, в том числе с разницей ночного и дневного АД, и обладало слабым достоверным прогностическим значением в отношении кардиоваскулярной и общей смертности. Также среднее значение АД после просыпания коррелировало с развитием гипертрофии миокарда левого желудочка. Среднее АД в течение 2 часов до просыпания не было связано с вариабельностью АД и не обладало прогностическим значением. В целом, по данным исследования PAMELLA, утреннее АД в момент просыпания не дало той прогностической информации, которая позволила бы использовать его для принятия терапевтических решений.
Другой вопрос заключается в том, на какой из методов измерения ориентироваться при принятии терапевтических решений. Сравнение офисного и домашнего измерения в специально спланированном исследовании THOP показало, что при ориентации на домашнее измерение больные принимали в начале лечения меньшее количество препаратов, что позволило избежать излишней терапии и существенно уменьшить затраты, однако через год контроль АД был хуже у тех пациентов, решения у которых принимались на основе домашнего измерения. Кроме того, среди тех больных, у которых решения принимались на основе домашнего измерения АД, значительно большее число пациентов прекратили терапию (25,6 vs 11,3%; р<0,001).
В другом исследовании TASMIN-SR, оценивающем АД на основании домашнего измерения, контроль САД был лучше в группе пациентов, корректировавших терапию самостоятельно на основе домашнего измерения АД.
По-видимому, самостоятельное принятие решений о коррекции лечения самим больным повышает его приверженность к терапии. Эти исследования еще раз подчеркнули важность приверженности больных к лечению, поскольку если пациент не принимает антигипертензивные препараты, то не стоит ожидать результата от такой терапии.
Среди европейских стран наибольшие успехи в контроле АГ достигнуты во Франции. В 2015 г. кардиологами в этой стране поставлена задача достигнуть контроля АГ у 50% больных. По данным скрининговых исследований, в Украине на сегодняшний день АГ контролируется примерно у 15% пациентов.
Сложно или невозможно повлиять на ряд факторов, которые снижают приверженность больных к терапии, таких как проживание в сельской местности, низкий уровень образования и доходов, короткий период от момента постановки диагноза АГ или относительно молодой возраст больных (от 35 до 60 лет).
Однако приверженность пациентов с АГ к терапии во многом зависит и от врача. Помимо вовлечения больного в процесс контроля АД и самокоррекции терапии, создание мотивации к приему антигипертензивных препаратов, назначаемая терапия также влияют на то, принимает пациент антигипертензивные препараты или нет.
Хорошо известно, что увеличение количества лекарственных средств и кратности приема антигипертензивных препаратов ухудшает приверженность к терапии. Именно поэтому национальные и европейские рекомендации подчеркивают, что «необходимо отдавать предпочтение лекарственным средствам, антигипертензивный эффект которых длится более 24 часов при приеме 1 раз в сутки».
В связи с этим вызывает удивление, что в Украине до настоящего времени неоправданно широко используются такие препараты, как каптоприл, эналаприл и их фиксированные комбинации с диуретиками, требующие дву- и трехкратного применения в течение суток, поскольку они имеют короткий период полувыведения, не обеспечивающий достаточного антигипертензивного эффекта на протяжении суток. А использование препаратов с дву- и трехкратным приемом в течение суток значительно ухудшает приверженность больных к лечению.
Кроме того, наблюдаются значительные различия в приверженности пациентов к приему антигипертензивных препаратов различных классов. Метаанализ 17 исследований с участием 935 920 больных, которым для контроля АГ назначались диуретики, β-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента (ИАПФ) или сартаны (БРА II), показал, что приверженность к терапии варьировала от 28% при использовании β-блокаторов до 65% при применении сартанов (БРА II). Использование сартанов (БРА II) обеспечивало максимальную приверженность пациентов к терапии, превосходившую таковую к приему ИАПФ на 33%, антагонистов кальция – на 57% и в 2 раза приверженность к приему диуретиков и β-блокаторов.
Еще большая разница по сравнению с рандомизированными исследованиями в приверженности к антигипертензивной терапии различными классами препаратов наблюдается в реальной клинической практике.
Проведенное в Италии специально спланированное популяционное исследование у больных АГ, которым была впервые назначена антигипертензивная терапия, показало, что при использовании диуретиков на 83% повышается вероятность отмены или смены препарата при сравнении с ИАПФ, на 64% – при использовании β-блокаторов и на 8% – антагонистов кальция (рис. 1).
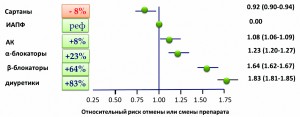 Рис. 1. Относительный риск отмены или смены препарата при назначении различных классов антигипертензивных средств (при сравнении с ИАПФ)
Рис. 1. Относительный риск отмены или смены препарата при назначении различных классов антигипертензивных средств (при сравнении с ИАПФ)
Наименьшую вероятность отмены или смены препарата демонстрировали сартаны (БРА II) – на 8% меньше по сравнению с ИАПФ.
Аналогичные результаты были получены при оценке приверженности к терапии в течение 12 месяцев от момента назначения антигипертензивных препаратов с помощью регистров больных АГ (суммарно более 350 тыс. пациентов). Самая низкая приверженность наблюдалась в том случае, если в качестве стартовой терапии больным АГ назначались диуретики: только 10% пациентов демонстрировали среднюю приверженность к лечению, у остальных она была либо плохой (15% больных), либо очень плохой (75% пациентов) (рис. 2).
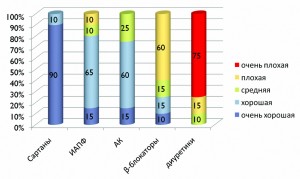 Рис. 2. Приверженность к терапии больных АГ (данные реестров через 12 месяцев от назначения препаратов)
Рис. 2. Приверженность к терапии больных АГ (данные реестров через 12 месяцев от назначения препаратов)Также при назначении β-блокаторов плохая приверженность терапии отмечалась у большинства больных (60%), и только четвертая часть пациентов (25%) показали хорошую или очень хорошую приверженность к терапии. Гораздо лучше больные принимали антагонисты кальция. Три четверти пациентов (75%) демонстрировали хорошую или очень хорошую приверженность терапии и только у 25% больных были незначительные проблемы. При применении ИАПФ 10% пациентов имели плохую приверженность к терапии, связанную с побочными эффектами, в основном с появлением кашля. В том случае, когда в качестве стартовой терапии использовались сартаны (БРА II), очень хорошую приверженность к приему препаратов демонстрировали 90% больных, хорошую – 10%.
В целом все исследования (рандомизированные, когортные и популяционные) давали одинаковый результат: наименьшая приверженность к терапии пациентов с АГ имела место в том случае, если в качестве стартовой терапии назначаются диуретики или β-блокаторы. Наиболее высокая вероятность того, что больной будет длительно принимать антигипертензивные препараты, наблюдается в том случае, если назначаются сартаны (БРА II).
Европейские эксперты рекомендуют начинать терапию пациента с АГ и высоким сердечно-сосудистым риском при АД выше 140/90 мм рт. ст. с комбинации двух антигипертензивных препаратов, одним из которых должен быть блокатор ренин-ангиотензиновой системы, а вторым – либо диуретик, либо антагонист кальция (табл. 3).
При сравнении приоритетных комбинаций антигипертензивных препаратов наибольшая приверженность больных к терапии будет в том случае, если используется комбинация сартана (БРА II) с антагонистом кальция, а наименьшая – при назначении комбинации ИАПФ с диуретиком.
Учитывая тот факт, что контроль АГ стал одним из наиболее эффективных инструментов (вклад которого составил 20%) в снижении сердечно-сосудистой заболеваемости и смертности в индустриально развитых странах в период с 1980 по 2000 г., мы имеем большой неиспользованный потенциал в контроле АГ в Украине. Прежде всего, речь идет о корректной диагностике и выявлении АГ. Второй, не менее важной задачей является увеличение количества больных, которые постоянно принимают антигипертензивные препараты и контролируют уровень АД. И то, и другое не требует внедрения дорогостоящих высоких технологий, а во многом определяется нашими подходами в повседневной клинической практике.
Список литературы находится в редакции.