1 квітня, 2015
Диагностика сердечной недостаточности у детей и подростков
В XXI веке хроническая сердечная недостаточность (ХСН) остается одним из важнейших проблемных разделов современной медицины и имеет огромное социальное значение в связи с широкой распространенностью, неуклонно прогрессирующим, прогностически неблагоприятным течением и высокими экономическими потерями [1]. Характерной чертой нынешнего состояния этой проблемы является значительное увеличение числа больных с ХСН. В США и странах Западной Европы подобная динамика наблюдается в связи с увеличением в общей популяции доли лиц пожилого и старческого возраста, а также c удлинением клинической эволюции наиболее распространенных сердечно-сосудистых заболеваний – ишемической болезни сердца и артериальной гипертензии – за счет их более или менее адекватного лечения [2].
Поскольку большинство проспективных клинических исследований были проведены у пожилых лиц, очень мало известно о распространенности, этиологии и особенностях ХСН у молодых пациентов. Данные о распространенности ХСН в детском возрасте противоречивы, что связано с большим количеством этиологических факторов, проблемами ее выявления и регистрации, а также с динамическим характером заболевания. В результате возникают значительные колебания показателей в разных странах. Установлено, что частота первой госпитализации по причине сердечной недостаточности (СН) составляет 0,87 случая на 100 тыс. детей, причем этот показатель не включает увеличивающуюся популяцию пациентов с врожденными пороками сердца (ВПС) [3]. В 2006 г. в США было зарегистрировано около 14 тыс. случаев госпитализации детей с СН [4]. Частота госпитализаций в связи с ухудшением течения СН составила почти 18 на 100 тыс. детей [4], что сопоставимо с таковой при тяжелом сепсисе [5]. Смертность госпитализированных детей с СН остается высокой. Так, госпитальная смертность составляет 7%, что превышает показатель у госпитализированных взрослых с СН – 4% [6]. У детей с ХСН и сопутствующими заболеваниями, в частности с почечной недостаточностью, сепсисом или инсультом, госпитальная смертность может превышать 20%, однако риск летального исхода остается высоким и после выписки из стационара. Так, в исследовании S.A. Hollander и соавт. [7] отмечено, что после первой госпитализации в связи с СН только у 21% детей удалось избежать повторной госпитализации, летального исхода или трансплантации.
Этиология
В педиатрической практике немало заболеваний, возникающих на фоне кардиальной, а также экстракардиальной патологии, которые могут привести к формированию ХСН (табл. 1).
 Причины ХСН у детей достаточно гетерогенны, зависят от возраста (табл. 2) и, что очень важно, принципиально отличаются от таковых у взрослых.
Причины ХСН у детей достаточно гетерогенны, зависят от возраста (табл. 2) и, что очень важно, принципиально отличаются от таковых у взрослых.
 Так, у новорожденных и детей раннего возраста основными причинами СН являются ВПС [9]. У 78% детей с ВПС СН исчезает после операции. В дошкольном и школьном возрасте причинами СН являются идиопатические и воспалительные заболевания сердца: инфекционные эндокардиты, миокардиты, кардиомиопатии, первичная легочная гипертензия, перикардит. В последнее время увеличилось количество случаев поражений миокарда при системных заболеваниях соединительной ткани, васкулитах, особенно при болезни Кавасаки [8]. Поражение сердца при различных генетических синдромах, нервно-мышечных заболеваниях, митохондриальной патологии часто сопровождается развитием ХСН. Также имеют значение заболевания, обусловливающие хроническую перегрузку миокарда вследствие его интенсивной работы (тахиаритмии) или повышения периферического сопротивления сосудов (артериальная гипертензия).
Так, у новорожденных и детей раннего возраста основными причинами СН являются ВПС [9]. У 78% детей с ВПС СН исчезает после операции. В дошкольном и школьном возрасте причинами СН являются идиопатические и воспалительные заболевания сердца: инфекционные эндокардиты, миокардиты, кардиомиопатии, первичная легочная гипертензия, перикардит. В последнее время увеличилось количество случаев поражений миокарда при системных заболеваниях соединительной ткани, васкулитах, особенно при болезни Кавасаки [8]. Поражение сердца при различных генетических синдромах, нервно-мышечных заболеваниях, митохондриальной патологии часто сопровождается развитием ХСН. Также имеют значение заболевания, обусловливающие хроническую перегрузку миокарда вследствие его интенсивной работы (тахиаритмии) или повышения периферического сопротивления сосудов (артериальная гипертензия).
Патогенез
Патогенез формирования ХСН у детей включает: гемодинамические, нейрогуморальные, иммунологические механизмы развития ХСН, а также эндотелиальную дисфункцию и нарушения клеточного энергообмена. Сохранение этиологического фактора способствует прогрессированию ХСН с морфофункциональными проявлениями поздней дезадаптации или декомпенсации в виде застоя в легких, отечного синдрома, апоптоза и некроза клеток со снижением сердечного выброса и развитием аритмий.
Классификация
Классифицировать ХСН у детей достаточно сложно, что связано с принципиальными отличиями в этиологии ХСН в детском возрасте, а также с трудностями субъективной оценки своего состояния детьми, резко различающейся физической активностью в одном и том же возрасте у разных индивидуумов. При оценке тяжести ХСН должны сохраняться 2 принципа: оценки стадии (на основании клинических проявлений) и функционального состояния пациента.
В клинической практике у детей раннего возраста наиболее удобной для определения стадии ХСН с учетом право- и левожелудочковой недостаточности с четкими клиническими критериями является классификация, предложенная Н.А. Белоконь (табл. 3).  Изолированная оценка право- и левожелудочковой недостаточности особую важность приобретает в детском возрасте, так как позволяет дифференцированно подойти к лечению этих пациентов.
Изолированная оценка право- и левожелудочковой недостаточности особую важность приобретает в детском возрасте, так как позволяет дифференцированно подойти к лечению этих пациентов.
Наибольшие трудности в детской кардиологии представляет определение функционального класса (ФК) ХСН, особенно у детей раннего и дошкольного возраста. С этой целью используется классификация R.D. Ross (табл. 4).  Недостатком этой классификации является оценка гемодинамической перегрузки только малого круга кровообращения, без четких количественных критериев.
Недостатком этой классификации является оценка гемодинамической перегрузки только малого круга кровообращения, без четких количественных критериев.
У детей школьного возраста и подростков используется классификация ХСН Ассоциации кардиологов Украины (2012), которая предусматривает объединение существующей в настоящее время классификации по стадиям (В.Х. Василенко и Н.Д. Стражеско; табл. 5), а также по варианту ФК СН (классификация Нью-Йоркской ассоциации сердца – NYHA).

Варианты СН:
– с систолической дисфункцией левого желудочка (ЛЖ): фракция выброса (ФВ) ЛЖ ≤45%;
– с сохраненной ФВ ЛЖ (>45%).
Во многих странах мира используется функциональная классификация Нью-Йоркской ассоциации сердца (NYHA) (табл. 6), принятая в 1964 г.  В ее основу положена оценка способности больного выполнять обычную физическую нагрузку [12]. Преимуществами классификации являются высокая валидность, удобство применения (оценка проводится по одному критерию), гибкость (учитывает влияние современного лечения), возможность математической обработки [13]. Однако все эти преимущества «перевешивает» очень серьезный недостаток – субъективизм и низкая воспроизводимость [14]. ФК по классификации NYHA не учитывают доклинической стадии заболевания [15].
В ее основу положена оценка способности больного выполнять обычную физическую нагрузку [12]. Преимуществами классификации являются высокая валидность, удобство применения (оценка проводится по одному критерию), гибкость (учитывает влияние современного лечения), возможность математической обработки [13]. Однако все эти преимущества «перевешивает» очень серьезный недостаток – субъективизм и низкая воспроизводимость [14]. ФК по классификации NYHA не учитывают доклинической стадии заболевания [15].
В клинической педиатрии также используется классификация А.С. Сенаторовой и И.М. Галдиной (2004), в основу которой положены объективные данные ультразвуковой диагностики систолической и диастолической функций сердца [16] (табл. 7). 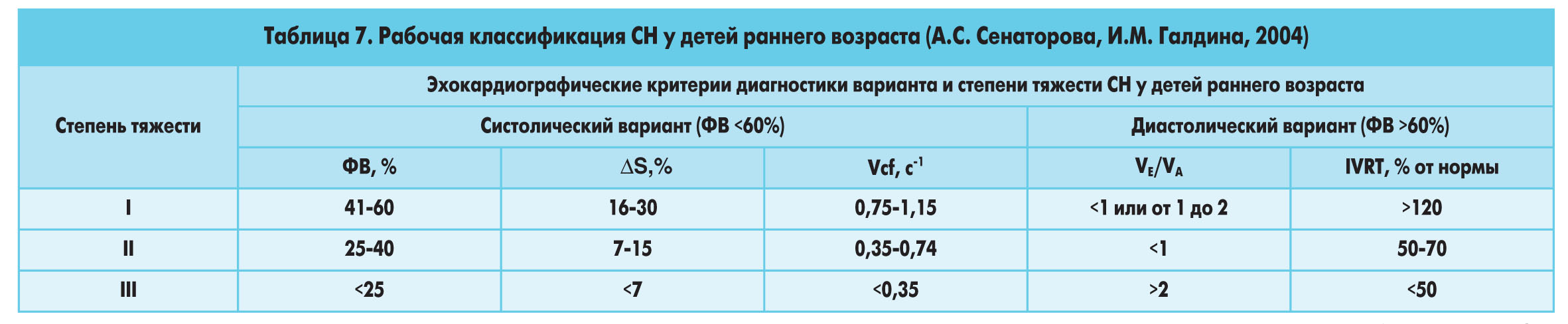
Клинические проявления ХСН
Опорными точками в установлении диагноза ХСН являются:
1) характерные симптомы СН;
2) данные физикального обследования (осмотра, пальпации, аускультации) или клинические признаки;
3) данные объективных (инструментальных) методов обследования.
Значимость клинических симптомов и клинических признаков чрезвычайно велика, поскольку именно они заставляют врача заподозрить наличие у больного СН. При преимущественном поражении одного из желудочков симптомы несколько различаются (табл. 8).
Левожелудочковая недостаточность
Жалобы на ранних стадиях неспецифичны (быстрая утомляемость, потливость, снижение аппетита) или могут отсутствовать. Главным проявлением левожелудочковой недостаточности является одышка. Вначале она отмечается только при физической нагрузке, затем появляется ортопноэ (неспособность находиться в горизонтальном положении из-за ощущения нехватки воздуха), далее могут возникнуть более выраженные проявления – сердечная астма и отек легких.
Объективно: положение ортопноэ (полусидячее, связанное с усилением одышки в горизонтальном положении), напряжение и раздувание крыльев носа, втяжение податливых мест грудной клетки (из-за участия в акте дыхания вспомогательной мускулатуры), тахипноэ, реже диспноэ (затруднение вдоха и удлинение выдоха вследствие ригидности легких), тахикардия, реже развитие брадикардии, влажные разнокалиберные хрипы в легких (сначала в нижнебоковых отделах легких и/или преимущественно слева из-за сдавления левого легкого увеличенным сердцем, затем над всей поверхностью легких), сердечный горб, расширение границы относительной сердечной тупости влево, глухость сердечных тонов (за счет снижения сократительной способности миокарда) и появление дополнительных тонов – III протодиастолического (вследствие повышения давления в левых отделах сердца и снижения тонуса миокарда) и IV пресистолического (вследствие повышения давления в левом предсердии становится слышна систола предсердий), акцент II тона (характерен для легочной гипертензии), возможен суммационный ритм галопа (так как III и IV тоны на верхушке сердца нередко сливаются), шумы над областью сердца (чаще всего связанные с клапанной патологией или внутрисердечным шунтированием крови).
В терминальной стадии СН может развиться дыхательная недостаточность с появлением характерного признака – цианоза кожи и слизистых оболочек. Основная причина цианоза – увеличение содержания в крови восстановленного гемоглобина >5 г%. У больных с СН цианоз может быть центральным или периферическим. Первый носит диффузный характер, не является следствием СН, но может утяжелять ее течение. Его основными причинами являются: нарушение оксигенации крови в легких (при артериовенозных шунтах) и смешивание артериальной и венозной крови (при некоторых пороках синего типа (тетрада Фалло). Периферический цианоз (акроцианоз) связан с повышенной утилизацией кислорода тканями, возникает при замедлении кровотока или венозном застое и появляется на губах, кончике носа, концевых фалангах. Степень выраженности акроцианоза обычно соответствует тяжести нарушения кровообращения.
Правожелудочковая недостаточность
Жалобы на ранних стадиях неспецифичны или могут отсутствовать. Проявляется признаками венозного застоя в большом круге: повышение уровня пульсации и набухание шейных вен, увеличение печени, периферические отеки. Могут отмечаться асцит, гидроторакс вплоть до анасарки. В чистом виде правожелудочковая недостаточность встречается довольно редко, в основном при легочном сердце. В большинстве случаев одновременно имеется и левожелудочковая недостаточность. Кроме того, даже при изолированной левожелудочковой недостаточности могут быть заметны периферические отеки вследствие нарушения функции почек и задержки жидкости. Клинические признаки венозного застоя в большом круге отмечаются также при констриктивном перикардите и тампонаде сердца.
Объективно: отмечается набухание вен (особенно яремных), сердечный горб, расширение границ относительной сердечной тупости вправо, пульсация в эпигастрии (обусловленная гипертрофией или объемной перегрузкой правого желудочка – ПЖ), увеличение размеров и болезненность при пальпации печени (по консистенции печень вначале мягкая, с ровной поверхностью и закругленным краем, при хроническом течении заболевания становится плотной, а при развитии кардиального фиброза ее размеры уменьшаются), нарушения функции печени (повышение уровня билирубина и сывороточных трансаминаз, диспротеинемия, симптом Плеша (набухание шейных вен при надавливании на область печени), умеренное увеличение селезенки (характерно для детей раннего возраста), диарея/ запор, тошнота, рвота, связанные с застоем крови в мезентериальных сосудах и застойным гастритом, периферические отеки (на стопах, затем лодыжках, голенях, у лежачих больных в области крестца, обычно увеличивающиеся к вечеру, чаще у детей старшего возраста, так как у детей первых лет жизни отеки не видны из-за высокой гидрофильности тканей), гидроторакс и/или асцит (появляются позднее периферических отеков), изменения II тона во втором межреберье слева (расщепление, а затем акцентуация при наличии легочной гипертензии), систолический шум трикуспидальной регургитации, периферический цианоз (вследствие венозного застоя), центральный цианоз (у пациентов с септальными дефектами вследствие повышения давления в правых отделах сердца и сброса крови справа налево).
Практические рекомендации
– Симптомы и признаки и лево- и правожелудочковой СН (тахипноэ, одышка – как при физической нагрузке, так и без нее, ортопноэ, потоотделение, увеличение печени, набухание яремных вен и отеки) также могут быть начальным проявлением рестриктивной кардиомиопатии.
– Миокардит может проявляться желудочковой эктопической активностью и классическими симптомами острой СН [17]. Возможно прогрессивное ухудшение состояния вплоть до молниеносной формы, характеризующейся внезапным началом с быстро развивающимися (в течение нескольких часов) СН и кардиогенным шоком [18]. Показано, что при прогрессировании заболевания большинство смертельных случаев отмечается в ранние сроки; предполагается, что степень тяжести заболевания влияет на прогноз [19]. Таким образом, необходимо тщательное наблюдение за пациентами, у которых предполагается миокардит, даже при выявлении легкой степени тяжести при первичном осмотре.
– Кардиомегалия при остром миокардите обычно не определяется, что необходимо учитывать при оценке данных рентгенографии грудной клетки. Миокардит следует включить в перечень заболеваний для дифференциальной диагностики у детей, поступающих с патологией желудочно-кишечного тракта (болью в животе и рвотой) или гриппоподобными симптомами, поскольку в начале заболевания существуют трудности при проведении дифференциальной диагностики с внекардиальной патологией.
Диагностический поиск у пациентов с СН зависит от:
– возраста больных;
– наличия или отсутствия ВПС;
– наличия системных нарушений;
– степени тяжести СН.
Пациенты с симптомами и признаками ХСН должны быть осмотрены детским кардиологом. В зависимости от клинического статуса ребенка оценка может проводиться в амбулаторных условиях в течение нескольких дней. Кроме того, в случае впервые возникшей СН или ухудшения ее течения больных необходимо обследовать в отделении интенсивной терапии в течение нескольких часов.
Методы инструментальной диагностики ХСН
Среди инструментальных методов диагностики ХСН наиболее распространены электрокардиография (ЭКГ) в 12 отведениях, рентгенография органов грудной клетки и эхокардиография (ЭхоКГ), причем последняя является наиболее полезным методом оценки ВПС и функции ЛЖ. Цель инструментальной диагностики – предоставить объективные доказательства наличия дисфункции сердца у больного с подозрением на ХСН.
ЭКГ позволяет получить данные о наличии факторов, нарушающих функцию сердца, однако специфических признаков, соответствующих СН, не существует. При анализе ЭКГ можно выявить признаки перегрузки или гипертрофии предсердий либо желудочков сердца, патологическое отклонение электрической оси сердца влево или вправо, нарушения сердечного ритма и проводимости, нарушения процесса реполяризации миокарда и др.
Суточное мониторирование ЭКГ имеет диагностический смысл лишь при наличии (вероятно, связанных с аритмией) субъективных ощущений перебоев, сопровождающихся головокружениями, обмороками в анамнезе и др. Холтеровское мониторирование позволяет судить о характере, частоте возникновения и продолжительности предсердных и желудочковых аритмий, которые могут вызывать появление симптомов СН или усугублять ее течение [20-22]. Кроме того, при холтеровском мониторировании возможно выявление эпизодов безболевой ишемии миокарда, которые могут стать причиной возникновения симптомов СН и их последующего нарастания. Показаниями к проведению данного исследования являются миокардиты и кардиомиопатии, поскольку они очень часто сопровождаются опасными нарушениями ритма сердца и относятся к группе заболеваний с высоким риском внезапной сердечной смерти. Аритмиями нередко сопровождаются и ВПС. Использование холтеровского мониторирования у больных с ВПС способно выявить пред- и послеоперационные, в том числе жизнеугрожающие, нарушения ритма сердца.
Рентгенография органов грудной клетки. Рентгенологическое исследование в кардиологии является скрининговым и выполняется всем больным на начальном этапе обследования. Стандартная рентгенография органов грудной клетки хорошо отражает легочное кровообращение и является базисным методом визуализации сердца [23]. Исследование следует выполнять в переднезадней и боковой проекциях. С помощью рентгенографии можно определить выраженность кардиомегалии, уровень накопления жидкости в легких и плевральной полости. С целью оценки размеров сердца вычисляют кардиоторакальный индекс, верхняя граница нормы которого в грудном возрасте составляет 0,55, начиная c 3 лет – 0,50 [8]. Следует помнить, что нормальные размеры сердца не исключают наличия диастолических расстройств как причины ХСН.
Рентгенологический метод имеет особое значение в диагностике легочной патологии, позволяет уточнить генез одышки [24]. Кроме того, рентгенография позволяет выявить ряд ВПС, в частности коарктацию аорты, на доклинической стадии и определить тактику дальнейшего обследования и лечения пациента [25]. С помощью этого метода можно оценить динамику течения заболевания, результаты хирургической коррекции пороков сердца, направление процессов ремоделирования.
Для оценки состояния больных с ХСН в арсенале клиницистов имеются различные неинвазивные методы визуализации сердечно-сосудистой системы. К ним относятся ЭхоКГ, радионуклидные исследования, позитронно-эмиссионная томография, а также магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография и др. Эти методы позволяют провести анализ структурно-функциональных характеристик сердца, оказывающих влияние на прогноз и лечение пациентов с СН. Они также могут быть полезны при сопутствующей патологии клапанного аппарата сердца. Следует отметить, что с помощью указанных методов можно оценить прогрессирование ремоделирования ЛЖ и последующее обратное ремоделирование после начала медикаментозной терапии. Наиболее важным является то обстоятельство, что с помощью методов визуализации сердца можно уточнить этиологию дисфункции ЛЖ и выбрать наиболее оптимальную стратегию лечения.
ЭхоКГ. Трансторакальная ЭхоКГ считается методом первой линии для диагностики и последующего наблюдения ВПС у детей и подростков. ЭхоКГ позволяет выявить различные структурные нарушения со стороны миокарда и клапанов сердца, другие возможные кардиальные причины СН. Особое значение при проведении ЭхоКГ у детей имеет динамическая оценка размеров и функции камер при различной патологии: нарушениях ритма, кардиомиопатиях, воспалительных заболеваниях. Диагностическая точность оценки структурно-функциональных показателей сердца очень высокая – в частности, отмечено менее 100 ошибок в более чем 50 тыс. эхокардиограмм [26]. Грамотное применение ЭхоКГ позволяет уменьшить необходимость в инвазивных методах, таких как катетеризация.
Выраженность изменений камер сердца и сосудов является количественным параметром, качество оценки которого достигается использованием стандартных подходов для измерений. Места и фазы стандартных измерений, линейных и объемных показателей четко определены рекомендациями Американского общества эхокардиографии (ASE) [27]. Большинство показателей ЭхоКГ разработаны и утверждены для оценки морфологии и функционального состояния ЛЖ. В то же время важно подчеркнуть, что для оценки функционирования ЛЖ у детей часто применяются методики, правомерные для взрослых пациентов, и данные часто экстраполируются в педиатрии без всестороннего обоснования в многочисленной когорте детей или в соответствии со слепыми проспективными исследованиями. Гетерогенность ВПС, анатомические варианты строения сердца в норме, влияние роста ребенка и вариабельность данных исследований по оценке гемодинамики усложняют правильную интерпретацию многих функциональных переменных. Большинство исследователей для оценки функционального состояния ПЖ применяют качественный (субъективный) анализ. Однако гемодинамическая функция ПЖ физиологически отличается от таковой ЛЖ, в частности по толщине стенок за счет мышечного слоя, что объясняется большей работой ЛЖ [28], меньшей постнагрузкой на ПЖ (легочное сосудистое сопротивление) и более низким систолическим давлением в ПЖ по сравнению с левым.
При выполнении ЭхоКГ у детей большинство исследователей используют возрастные нормативы размеров (как правило, это поперечники камер для М-режима), предложенные в различных методических рекомендациях [29]. Реже применяются различные номограммы, основанные на уравнениях регрессии между антропометрическими данными (рост, вес или площадь тела – BSA) и диаметром сосудов, поперечниками ЛЖ и ПЖ [30-31]. У детей для определения объемов камер сердца чаще всего используется ЭхоКГ в М-режиме с применением известной формулы Teichholz [30]. С помощью пакета программ определяют диастолический и систолический объемы ЛЖ и показатели сократимости (ФВ) и насосной функции (ударный объем) [29]. Следует помнить, что использование одномерной ЭхоКГ приводит к завышению объемов ЛЖ до 18-20%, причем формула расчета объема ЛЖ (Teichholz) при изменении его формы (сферификации) значительно искажает реальный результат. Эталонным методом, не отличающимся по точности от МР-методики, считается трехмерная ЭхоКГ [32]. Другим точным способом определения конечнодиастолического объема ЛЖ является двухпроекционный метод Симпсона [29].
В исследовании Г.И. Марцинкевич и соавт. [33] изучены диагностические возможности одно-, двух- и трехмерной ЭхоКГ у здоровых детей разного возраста, а также проведена оценка возможностей индивидуального прогнозирования эхокардиографических показателей при изменении антропометрических данных. На основании результатов обследования 2600 детей в возрасте от 1 дня до 18 лет были определены уравнения линейной регрессии, позволяющие с точностью 80-97% выполнять индивидуальное прогнозирование значений объемных и линейных показателей двухмерной ЭхоКГ на основании антропометрических данных. Показано, что использование ЭхоКГ в М-режиме для определения объема ЛЖ абсолютно неприемлемо у детей в возрасте до 6 мес, нежелательно до 7 лет и дает ошибку до 124%. У детей в возрасте до 6 мес ЛЖ увеличен по длинной оси и менее сферичен по сравнению с его размерами в старших возрастных группах. Установлено, что нормированные значения конечнодиастолического объема ЛЖ у детей не являются постоянной величиной и увеличиваются вдвое в возрасте 1-2 лет по сравнению с детьми младше 1 мес. Долгосрочная динамическая оценка объемов камер сердца, линейных размеров и диаметров крупных сосудов у детей должна осуществляться не с использованием «возрастных норм», а с применением антропометрических нормативов. Показано, что использование пятикамерной позиции изображения ЛЖ у детей не уступает по точности двухпроекционному методу Симпсона.
Таким образом, ЭхоКГ позволяет выявить различные структурные нарушения со стороны миокарда и клапанов сердца, а также другие возможные кардиальные причины СН. Традиционными критериями дисфункции сердца являются дилатация его полостей (увеличение конечнодиастолического и конечносистолического размера и объема), гипертрофия стенок желудочков и межжелудочковой перегородки, а также увеличение массы миокарда, выходящие за рамки норм, определяемых по площади поверхности тела. В качестве вспомогательных критериев ориентируются также на гипо- или дискинезии стенок желудочков или межжелудочковой перегородки, увеличение объема предсердий, повышение среднего и систолического давления в легочной артерии.




