31 січня, 2017
Застосування карбамазепіну в лікуванні тригемінальної прозопалгії
Ураження трійчастого нерва, що супроводжуються тяжкими прозопалгіями, незважаючи на сучасні методи лікування, залишаються актуальною проблемою практичної медицини.
У наших дослідженнях серед пацієнтів із тригемінальною прозопалгією переважали жінки (67,6%), особливо після 50 років (80,0%) [1]. Тривалість захворювання становила від декількох тижнів до 40 років. У половині випадків початок захворювання припадав на вік старше 50 років.
Якщо причиною розвитку захворювання в 43,3% осіб молодше 40 років були одонтогенні ураження (травматичне видалення зубів і залишків коренів, що супроводжувалося травмою альвеолярного гребеня), то в більш старшому віці значну роль відігравала компресія тригемінального корінця патологічно звитою петлею верхньої мозочкової артерії або відповідної вени (27,0%) як прояв вікових судинних порушень. У цій групі спостерігалися: артеріальна гіпертензія (5,4%); перенесений інсульт (5,4%), цукровий діабет (5,4%); наслідки двостороннього кохлеоневриту (2,7%); синдром вегетативної дистонії (2,7%); черепно-мозкова травма (2,7%); гайморит (2,7%); скронево-щелепний артроз (2,7%).
Хворі пред’являли скарги на болі й відчуття печіння з іррадіацією по ходу уражених гілок трійчастого нерва, що мали виражений циклічний характер. Кількість пароксизмів – від 1-2 до 30 протягом дня. У низці випадків вони супроводжувалися болючими гіперкінезами. Напади провокувалися прийомом їжі, розмовою, сміхом, туалетом області лиця й зубів. Хворі намагалися зберігати маскоподібний вираз обличчя з метою максимального обмеження рухів мімічної мускулатури. У всіх спостереженнях відзначалася наявність тригерних зон, дотик до яких призводив до розвитку больового нападу.
Початок захворювання часто був пов’язаний з візитом до стоматолога й, як правило, з видаленням одного або декількох зубів. Так, хворій П., 76 років, було проведено протягом 1,5 місяця видалення 7 зубів на стороні болю. При цьому екстракція кожного зуба призводила до тимчасового припинення алгічних пароксизмів, вочевидь, внаслідок подразнення рецепторів глибокої чутливості навколозубних тканин, що викликало виділення гальмівного медіатора в ядрі спинального тракту стовбура мозку [2].
В 8,1% пацієнтів були зареєстровані двосторонні тригерні зони: в 2,7% уражена друга, а в 5,4% – всі гілки трійчастого нерва. В 43,2% спостережень тригерні зони розташовувалися ліворуч: в 27% були уражені всі гілки, в інших – різні комбінації. В 48,6% випадків виявлено правобічну локалізацію куркових зон, при цьому в 24,3% були уражені всі гілки. Тривале спостереження за хворими показало, що протисудомні препарати залишаються найбільш ефективними й обов’язковими в лікуванні цієї патології, незалежно від сторони ураження, віку й тривалості захворювання. Традиційні аналгетики малоефективні при невралгіях і невропатіях.
Європейські рекомендації з терапії постгерпетичної невралгії, тригемінальної невралгії, больових полінейропатій і центрального нейропатичного болю наведено нижче (табл. 1) [3, 4, 5, 6, 7].
Застосування антиконвульсантів при невралгії трійчастого нерва засновано на гальмуванні поширення судомноподібних розрядів із джерела патологічно посиленого порушення, що виникло в оральному відділі ядра трійчастого нерва під впливом патологічної імпульсації з периферії.
Карбамазепін – протиепілептичний лікарський засіб, що належить до групи похідних карбоксаміду. У клінічній практиці переважно використовується в якості протисудомного препарату при великих судомних нападах (тоніко-клонічних нападах) і при фокальній епілепсії. Також має помірну нормотимічну дію. Механізм дії карбамазепіну подібний до протиепілептичних препаратів групи похідних гідантоїну. За своєю структурою карбамазепін близький до трициклічних антидепресантів (має структурну подібність до іміпраміну). У готових лікарських формах карбамазепін може бути представлений у вигляді дигідрату. Карбамазепін відкритий в 1953 р. хіміком Вальтером Шиндлером (Швейцарія). Вальтером був отриманий патент на синтез цього препарату. В 1962 році карбамазепін став першим на ринку препаратом для лікування невралгії трійчастого нерва.
При дослідженні ефективності карбамазепіну для лікування ідіопатичної невралгії трійчастого нерва карбамазепін застосовували у 61 пацієнта з підозрою на невралгію трійчастого нерва. Всім пацієнтам було виконано магнітно-резонансну (МРТ) або комп’ютерну (КТ) томографію головного мозку. Остаточний діагноз був поставлений щелепно-лицьовим хірургом і нейрохірургом. З 61 пацієнта 50 був поставлений остаточний діагноз «невралгія трійчастого нерва», шістьом – атипічні лицьові болі. Карбамазепін був ефективний як аналгетик у 45 з 50 пацієнтів (90%) з невралгією трійчастого нерва та у 5 з 11 пацієнтів (45%) з іншими головними болями [8].
У Китаї було проведено порівняльний аналіз ефективності топірамату й карбамазепіну при лікуванні невралгії трійчастого нерва. У цілому шість рандомізованих контрольованих досліджень із недостатньою методологічною якістю були включені в дослідження Q.P. Wang і співавт., (2011) [9]. У цілому вони містили в собі аналіз лікування 354 пацієнтів з невралгією трійчастого нерва. Результати аналізу показали, що топірамат був більш ефективний, ніж карбамазепін при тривалості лікування більше 2 місяців (відносний ризик 1,20, 95% довірчий інтервал 1,04, 1,39, р=0,01). Проте ніяких розходжень в ефективності лікування після 1 місяця не було виявлено (ВР 1,00, 95% ДІ 0,87, 1,14, р=0,94), у тривалості ремісії після лікування навпротязі 1 місяця (ВР 1,06, 95% ДІ 0,83, 1,36, р=0,63), у тривалості ремісії після лікування протягом 2 місяців (ВР 1,31, 95% ДІ 0,96, 1,80, р=0,09) або побічних ефектах при порівнянні топірамату з карбамазепіном. Авторами зроблено висновок про те, що всі сучасні дослідження, які порівнюють топірамат з карбамазепіном, мають неналежну методологічну якість. Аналіз цих досліджень показав, що загальна ефективність і переносимість топірамату не відрізняються від карбамазепіну при лікуванні класичної невралгії трійчастого нерва. Результати були обмежені через низьку методологічну якість і географічну локалізацію рандомізованих контрольованих досліджень. Таким чином, необхідні подальші великі міжнародні, добре сплановані і проведені рандомізовані контрольовані дослідження для оцінки відносної ефективності й переносимості топірамату й карбамазепіну.
Проведено порівняльний аналіз ефективності габапентину й карбамазепіну при лікуванні невралгії трійчастого нерва. Для того щоб оцінити безпеку й ефективність габапентину порівняно з карбамазепіном при лікуванні невралгії трійчастого нерва, було виконано аналіз рандомізованих контрольованих досліджень [10]. Два дослідники незалежно один від одного вибирали дослідження, оцінювали якість дослідження й отримані дані. Було оцінено 16 рандомізованих контрольованих досліджень, які включали 1331 пацієнта. Аналіз показав, що загальна ефективність у групі габапентину була подібною до ефективності в групі карбамазепіну (ВР 1,600, 95% ДІ 1,185, 2,161, p=0,002). Ефективність терапії габапентином протягом 4 тижнів була вищою, ніж ефективність терапії карбамазепіном (ВР 1,495, 95% ДІ 1,061, 2,107, р=0,022), поліпшення задоволеності життям також переважало в групі, що приймала габапентин після 4-тижневого лікування (БМБ=0,966, 95% ДІ 0,583, 1,348, р<0,001). Аналіз показав, що несприятливі побічні ефекти в групі, що одержувала терапію габапентином, були вірогідно нижче, ніж у групі, що приймала карбамазепін (ВР 0,312, 95% ДІ 0,240, 0,407, р<0,001).
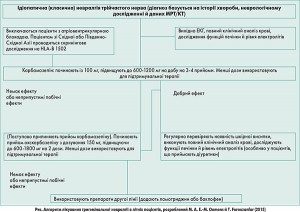
У той же час дослідження, що порівнюють габапентин з карбамазепіном, є недосконалими з погляду методологічної якості. На підставі наявних даних не представляється можливим зробити висновки щодо ефективності й побічних ефектів габапентину порівняно з карбамазепіном. Вивчено особливості застосування карбамазепіну у літніх пацієнтів з невралгією трійчастого нерва. У роботі М.А. Е.-М. Ооmens й Т. Forouzanfar (2015) для першої лінії лікування тригемінальної невралгії рекомендується використання алгоритму, що представлений на нижченаведеному рисунку. Призначають протиепілептичні препарати в людей похилого віку з особливою обережністю й звертають увагу на лікарські взаємодії й побічні ефекти. У літературі існує дефіцит досліджень проблеми ідіопатичної тригемінальної невралгії у людей похилого віку. Подальші дослідження мають бути спрямовані на вивчення ефективності й безпеки альтернативних варіантів нехірургічного лікування. Літні пацієнти та хворі із супутніми захворюваннями й супутньою терапією повинні бути включені в подальші дослідження для забезпечення узагальнених наукових висновків [11].
У Кокранівському огляді P.J. Wiffen і співавт. від 2014 року проаналізовано результати десяти досліджень (11 публікацій) із загальною кількістю у 480 пацієнтів з невралгією трійчастого нерва, діабетичною нейропатією і постінсультним больовим синдромом [12]. Дев’ять досліджень використовували перехресний дизайн, у десятому використовувався паралельний дизайн. Більшість досліджень були нетривалими, тривалістю чотири тижні або менше. У жодному з досліджень не було представлено доказів ефективності першого або другого ряду. Відповідно до доказів третього ряду, як правило, карбамазепін краще полегшував біль, ніж плацебо в трьох роботах, з деякою вказівкою на зменшення болю головним чином у короткостроковій перспективі, але з недостатньо достовірними результатами, неповною звітністю, а також у невеликої кількості учасників. Не було достатньо даних у дослідженнях, що порівнюють карбамазепін з іншими препаратами, щоб зробити які-небудь висновки.
У чотирьох дослідженнях у 65% (113/173) учасників спостерігалася принаймні одна побічна дія карбамазепіну й у 27% (47/173) – побічна дія плацебо; на кожні п’ять пролікованих пацієнтів відзначалося два побічних ефекти, які не спостерігалися у пацієнтів, що приймали плацебо. У восьми дослідженнях 3% (8/268) учасників припинили лікування через побічні ефекти, пов’язані з карбамазепіном, і жоден (0/255) із групи плацебо. Про серйозні побічні ефекти не повідомлялося; висипання на шкірі були пов’язані з карбамазепіном. Чотири смертельних випадки спостерігалися у пацієнтів, що приймали карбамазепін, і не були асоційовані із прийомом медикаментів.
Часто існуюча необхідність багаторічного й постійного прийому карбамазепіну при лицьових болях обумовлює обов’язкову оцінку можливих побічних дій.
Імовірність розвитку гіперчутливості до карбамазепіну становить 1,0-4,0 на 10 тис. випадків застосування препарату [13]. Пацієнтам з ідіосинкразичною реакцією на карбамазепін протипоказане застосування етосуксиміду, окскарбазепіну, фенобарбіталу, фенітоїну, зонізаміду, тому що існує перехресна чутливість [14]. Гідної альтернативи застосуванню антиконвульсантів у лікуванні нейропатичного болю дотепер не знайдено. Карбамазепін залишається препаратом першого вибору при тригемінальній прозопалгії.
Необхідно нагадати ще про декілька можливостей застосування карбамазепіну.
Застосування карбамазепіну при мігрені. В огляді M. Linde із співавторами (2013), присвяченому застосуванню протиепілептичних препаратів для профілактики мігрені у дорослих, було виявлено профілактичну дію карбамазепіну [15]. В одному проспективному рандомізованому подвійному сліпому одиночному перехресному дослідженні 48 пацієнтів було продемонстровано значну перевагу карбамазепіну порівняно з плацебо (ВР 11,77; 95% ДІ від 3,92 до 35,32).
Застосування карбамазепіну при вестибулярних пароксизмах. Вестибулярні пароксизми визначаються як пароксизмальні, короткочасні, чутливі до застосування карбамазепіну запаморочення [16, 17]. У дослідженні K. Hufner і співавт. (2008) вивчався стан 32 пацієнтів з рецидивуючими короткими періодами запаморочення з діагнозом «вестибулярні пароксизми», середній строк спостереження становив 31,3 місяця [18]. В 28% хворих напади виникали винятково в стані спокою, в 22% випадків вони регулярно викликалися певним рухом, найчастіше поворотом голови (60%). Найпоширенішим супутнім симптомом було хитке положення тіла й порушення ходи (75%). МРТ (n=23) показала принаймні одну ділянку нейросудинної компресії в усіх, крім одного пацієнта. Калоричне тестування показало помірне збільшення вестибулярного дефіциту із часом, індукований гіпервентиляцією ністагм було виявлено в 70% обстежених хворих (n=23). Більшість пацієнтів одержували карбамазепін (середня доза 568 мг/добу) або окскарбазепін (середня доза 870 мг/добу). Лікування призвело до значного зниження частоти атак до 10% від вихідного рівня (95% ДІ, 6,69-14,96%), інтенсивності атак до 15% (95% ДІ 11,57-19,63%), а також скорочення тривалості атак до 11% (95% ДІ 6,72-17,40).
Карбамазепін також ефективний для лікування вестибулярних пароксизмів у дітей [19]. N. Lehnen і співавт. (2015) описують трьох дітей (одна дівчинка 12 років; два хлопчики 8 й 9 років), які мали типові короткочасні атаки запаморочення кілька разів на день. Під час нападів спостерігався ністагм. МРТ показала компресію артерією восьмого черепного нерва. Атаки припинилися після введення низьких доз карбамазепіну (2-4 мг/кг на день).
Карбамазепін у лікуванні алкоголізму. У сімох дослідженнях, що охоплювали 612 пацієнтів, карбамазепін продемонстрував значне зменшення симптомів при синдромі скасування алкоголю. Проте у порівняльних випробуваннях з бензодіазепіновими агентами здатність карбамазепіну запобігати судомам, що виникають при скасуванні алкоголю (ВР 0,93; 95% ДІ 0,06-14,97, р – статистично незначущий) і алкогольного делірію (ВР 1,25; 95% ДІ 0,28-5,64, p – статистично незначущий), була невизначена в результаті недостатньої кількості пацієнтів. У трьох дослідженнях карбамазепіну не вдалося зменшити симптоми синдрому скасування алкоголю, можливо, у результаті несвоєчасного введення, неадекватного дозування або недостатнього розміру вибірки. При добових дозах 800 мг протягом 5-9 днів карбамазепін добре переносився, був безпечним для застосування, коли концентрація алкоголю в крові падала нижче 0,15%. Карбамазепін продемонстрував безпеку, переносимість й ефективність у лікуванні помірних і тяжких симптомів синдрому скасування алкоголю в стаціонарних умовах. Однак, як повідомляють автори, дослідження карбамазепіну не забезпечують остаточних доказів у плані профілактики судом, що виникають при синдромі скасування прийому алкоголю порівняно з бензодіазепінами.
Карбамазепін у лікуванні шизофренії. Огляд S. Leucht і співавт. (2014) був присвячений вивченню ефективності карбамазепіну у пацієнтів, що страждають на шизофренію [20]. Пошук у регістрі Кокранівської групи з вивчення шизофренії був проведений до липня 2012 року. У нього були включені десять досліджень, у яких у цілому брали участь 283 пацієнта. Карбамазепін порівнювався із плацебо, з антипсихотичними засобами. Проте всі 10 досліджень були невеликими, і інформація, що містилася в них, не була стандартизована. Отже, має місце відсутність доказів того, що карбамазепін зменшує симптоми у пацієнтів, що страждають на шизофренію. Перш ніж карбамазепін може бути рекомендований для лікування пацієнтів, що страждають на шизофренію, необхідні масштабні добре продумані дослідження для забезпечення більш переконливих доказів.
Карбамазепін у лікуванні нецукрового діабету використовується в основному у випадку неефективності інших препаратів [21, 22].
Література:
1. Горанский Ю.И. Опыт диагностики и лечения лицевых болей // Вісник стоматології. – 2000. – 4. – С. 32-33.
2. Степанченко А.В. Типичная невралгия тройничного нерва. – М.: Медицина, 1994. – 210 с.
3. Attal N., Cruccu G., Haanpaa M. et al. EFNS guidelines on pharmacological treatment of neuropathic pain. European Journal of Neurology, 2006, 13: 1153-1169.
4. Freynhagen R., Strojek K., Griesing T. et al. Efficacy of pregabalin in neuropathic pain evaluated in a 12 – week, randomised, double-blind, multicentre, placebo-controlled trial of fable-and fixeddose regimens. Pain, 2005 Jun; 115(3): 254-63.
5. Gilron I., Bailey J.M., Tu D. et al. Morphine, gabapentin, or their combination for neuropathic pain. N Engl J Med, 2005. Mar 31; 352(13): 1324-34.
6. Saarto T., Wiffen P. Antidepressants for neuropathic pain. Cochrane Database of Systemic Reviews, 2005. 20: CD005454.
7. Siddall P.J., Cousins M.J., Otte A., et al. Pregabalin in central neuropathic pain associated with spinal cord injury: a placebo-controlled trial. Neurology, 2006. Nov 28; 67(10): 1792-800
8. Sato J., Saitoh T., Notani K. et al. Diagnostic significance of carbamazepine and trigger zones in trigeminal neuralgia. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2004 Jan; 97 (1): 18-22.
9. Wang Q.P., Bai M. Topiramate versus carbamazepine for the treatment of classical trigeminal neuralgia: a meta-analysis. CNS Drugs. 2011 Oct 1; 25(10): 847-57.
10. Yuan M., Zhou H.Y., Xiao Z.L. et al. Efficacy and Safety of Gabapentin vs. Carbamazepine in the Treatment of Trigeminal Neuralgia: A Meta-Analysis. Pain Pract. 2016 Feb 19.
11. Oomens M.A., Forouzanfar T. Pharmaceutical Management of Trigeminal Neuralgia in the Elderly. Drugs Aging. 2015 Sep; 32 (9): 717-26.
12. Wiffen P.J., Derry S., Moore R.A. et al. Carbamazepine for chronic neuropathic pain and fibromyalgia in adults. Cochrane Database of Systematic Reviews 2014, Issue 4. Art. No.: CD005451.
13. Kothare S.V., Kaleyias J. The adverse effects of antiepileptic drugs in children. Expert Opin Drug Saf, 6(3): 251-65 2007.
14. Panayiotopoulos C.P. The Epilepsies. Seizures, Syndromes and Management.Blandon Medical Publishing; Oxfordshire; 2005; p. 497-500.
15. Linde M., Mulleners W.M., Chronicle E.P. et al. Antiepileptics other than gabapentin, pregabalin, topiramate, and valproate for the prophylaxis of episodic migraine in adults. Cochrane Database of Systematic Reviews 2013, Issue 6. Art. No.: CD010608.
16. Brandt T., Dieterich M. Vestibular paroxysmia: vascular compression of the eighth nerve? Lancet 1994; 343: 798-799.
17. Brandt T., Dieterich M. Vlllth nerve vascular compression syndrome: vestibular paroxysmia. Baillieres Clin Neurol 1994; 3: 565-575.
18. Hufner K., Barresi D., Glaser M. et al. Vestibular paroxysmia: diagnostic features and medical treatment. Neurology 2008; 71: 1006-1014.
19. Lehnen N., Langhagen T., Heinen F. et al. Vestibular paroxysmia in children: a treatable cause of short vertigo attacks. Dev Med Child Neurol. 2015 Apr; 57 (4): 393-6.
20. Leucht S., Helfer B., Dold M. et al. Carbamazepine for schizophrenia. Cochrane Database of Systematic Reviews 2014, Issue 5. Art. No.: CD001258.
21. Wales J.K. Treatment of diabetes insipidus with carbamazepine. Lancet. 1975 Nov 15; 2 (7942): 948-51.
22. Kalra S., Zargar A.H., Jain S.M. et al. Diabetes insipidus: The other diabetes. Indian J Endocrinol Metab. 2016 Jan-Feb; 20(1): 9-21.