31 січня, 2017
Раціональні підходи до лікування невропатії лицевого нерва у дітей: сучасний стан проблеми

Однією з проблем сучасної клінічної медицини є своєчасна діагностика депресивних розладів та надання спеціалізованої допомоги. За даними Всесвітньої організації охорони здоров’я (ВООЗ), депресивні розлади займають провідне місце серед 10 основних хвороб, які призводять до інвалідизації населення. Депресія набула у світі такої популярності, що вже з початку 2010 р. ВООЗ прирівняла її до епідемії, що поширилася на все людство.
Система «лицевий нерв – мімічні м’язи» є високоорганізованим спеціалізованим еферентним нейро-моторним механізмом спілкування та вираження емоцій, тому порушення її функції серйозно впливає на якість життя [24]. Найбільш яскравий клінічний прояв ураження системи – параліч Белла – зустрічається з частотою 20-32 випадки на 100 тис. населення на рік з однаковою частотою в представників обох статей [36]. В історичному аспекті паралічем Белла тривалий час називали ураження лицевого нерва у формі так званої ідіопатичної невропатії лицевого нерва. На сьогодні парез чи плегію мімічних м’язів (прозопопарез) визначають як тяжкий клінічний синдром, що вимагає ретельного вивчення етіопатогенезу і диференційної діагностики, а параліч Белла не завжди є синонімом ідіопатичної невропатії лицевого нерва, хоча у 50% випадків прозопопарез є ідіопатичним [46].
У дітей невропатія лицевого нерва є найбільш частим захворюванням черепних нервів, яке виникає гостро та посідає перше місце серед захворювань периферичної нервової системи. Її поширеність становить 5-7 випадків на 100 тис., з однаковою частотою серед хлопчиків та дівчаток [1, 2, 46].
Більшість дослідників вважають невропатію лицевого нерва поліетіологічним монопатогенетичним захворюванням [1, 2, 9].
Існують анатомічні особливості, які сприяють ураженню лицевого нерва:
• лицевий нерв є філогенетично найбільш молодим та вразливим черепним нервом;
• він має складний хід у вузькому кістковому каналі, займаючи від 40 до 70% його поперечного перерізу, причому діаметр каналу звужується з наближенням до шилососкоподібного отвору;
• магістральні судини системи кровопостачання лицевого нерва в умовах жорсткого кісткового ложа ведуть себе як судини кінцевого типу, не маючи можливості розширюватися, що сприяє первинній та вторинній ішемії;
• сукупність лімфатичних вузлів у місці виходу нерва з шилососкоподібного отвору.
Окрім того, значна кількість досліджень анатомії лицевого нерва засвідчує індивідуальні особливості топографічного розміщення лицевого нерва у фаллопієвому каналі, а також товщини стовбура лицевого нерва, кількісного та якісного складу пучків, ступеня розвитку сполучної тканини. Комплекс всіх анатомо-топографічних особливостей будови лицевого нерва визначає різну його стійкість та водночас високу уразливість при дії різноманітних пошкоджувальних факторів [1, 2, 6, 7, 9].
Етіологічними чинниками невропатії лицевого нерва можуть виступати отогенні, травматичні, компресійні фактори, судинні захворювання, інтоксикації, аномалії розвитку внутрішнього вуха і пухлинні процеси в ділянці мосто-мозочкового кута, вірусні ураження колінчатого ганглія [1, 5, 6, 7]. Значно рідше, в основному у дорослих, зустрічаються інші причини ураження лицевого нерва, такі як цукровий діабет, артеріальна гіпертензія, СНІД, хвороба Лайма, саркоїдоз, синдром Шегрена, амілоїдоз, синдром Рамзея-Ханта, ятрогенні чинники [1, 2, 6, 8, 9, 10, 17]. Невропатія лицевого нерва може виникати як клінічно ізольований синдром при розсіяному склерозі і у дорослих, і у дітей [3, 51].
В дослідженнях останніх років показано, що в сироватці крові хворих виявляються підвищені титри антитіл до вірусів простого герпесу, Епштейна-Барр, грипу, аденовірусів, що свідчить про важливу роль вірусної інфекції в ґенезі цієї форми невропатії лицевого нерва [2, 10, 11]. Провокуючим чинником, як правило, є переохолодження [5, 7, 11]. Холод призводить до подразнення рецепторів шкіри обличчя і судин краніо-цервікального відділу і розвитку рефлекторних судинних порушень у формі спазму судин, які кровопостачають стовбур лицевого нерва. Інфекційний агент, завдяки його місцевій та загальній дії, призводить до гострих минаючих розладів кровообігу в системі vasa nervorum у стовбурі лицевого нерва та у тканинах фаллопієвого каналу, що сприяє їх набряку та компресії нерва у вузькому жорсткому фаллопієвому каналі [1, 2, 5].
В дитячому віці найбільшу питому частку становлять хворі, у яких захворювання виникає на тлі переохолодження, загальної інфекції або ж в формі так званої ідіопатичної невропатії лицевого нерва, механізми розвитку якої залишаються ще не до кінця з’ясованими.
Стосовно патогенезу невропатії лицевого нерва тривалий час виділяли декілька теорій, серед них найперше слід зазначити судинну, запальну тощо [1, 2, 4, 5]. Останнім часом дослідники зійшлися на єдиній схемі змін, що відбуваються: ішемія – набряк – компресія або ж первинна ішемія – набряк – компресія – вторинна ішемія. Патоморфологічно виділяють 5 ступенів пошкодження нерва: від нейропраксії (втрата мієліну) і аксонотмезису до тяжкого невротмезису з валеровським переродженням та втратою пери- і епіневрію. Ступінь пошкодження корелює з вираженістю клініки і несприятливим прогнозом відновлення функції [2]. В низці експериментальних робіт показано, що при холодовій невропатії лицевого нерва відбуваються фазні зміни внутрішньостовбурового мікроциркуляторного русла і структури нервових волокон із порушенням організації компонентів сполучнотканинних оболонок нерва. Початкова фаза триває 10-15 діб та відображає реактивно-набряково-дистрофічні зміни [4]. Наступна фаза, яка триває з 15-ї по 30-ту добу, віддзеркалює переважання деструктивних процесів, поглиблення структурних змін у нервових волокнах. З 30-ї доби поряд із деструктивними змінами включаються початкові репаративні процеси. Фаза компенсаторно-адаптаційних змін із залишковими явищами, яка триває 30-60 діб, характеризується зменшенням набряку, активацією ремієлінізацї, виникають заново сформовані нервово-м’язові зв’язки, зменшується і наближається до норми діаметр просвіту судин [4].
Слід зазначити, що у дітей невропатія лицевого нерва розвивається на тлі інтенсивних процесів росту нервів та мієлінізації нервових волокон, що зумовлює особливості перебігу та завершення хвороби [2].
Захворювання розпочинається гостро протягом кількох годин, рідше 3-10 днів [1, 2, 5, 6, 9]. Провідним синдромом є прозопопарез чи прозопоплегія, що проявляється наступними симптомами: асиметрія обличчя в спокої, обмеження рухів брови, лагофтальм, згладженість носогубної складки, асиметрія при оскалюванні зубів, неможливість надути щоки. У 60% випадків прозопопарезу передує біль у завушній ділянці пекучого чи ниючого характеру. Залежно від рівня ураження також можуть зустрічатися додаткові симптоми (табл. 1): сльозотеча, сухість ока, гіперакузія, порушення смаку на передніх 2/3 язика.
Хоча діагноз невропатії лицевого нерва є нескладним, виникає необхідність оцінки тяжкості ураження лицевого нерва, а також динаміки відновлення втрачених функцій.
Для клінічної оцінки ступеня ураження лицевого нерва і моторної дисфункції мімічних м’язів запропоновано чимало вітчизняних та зарубіжних шкал [2, 3, 6, 7, 8, 9, 10, 11, 14, 15, 26, 31, 37, 38, 40, 47, 48, 49].
Найчастіше використовуються наступні шкали:
• Botman and Jongkees;
• May;
• Peitersen;
• K. Rosler grading Scale;
• House-Brackmann;
• Smith Scale;
• Yanagihara Scale;
• Janssen’s Scale;
• Sunnybrook Scale.
Значна частина із цих шкал, зокрема Botman and Jongkees, Peitersen, K. Rosler, є 5-ступеневими та передбачають такі ступені:
0 ст. – нормальна активність мімічних м’язів;
I ст. – легкий парез: асиметрії немає в спокої і при розмові, лагофтальму немає, деяка асиметрія при посмішці та свисті;
II ст. – помірний парез: асиметрії немає в спокої, асиметрія помітна при розмові та посмішці, лагофтальм;
III ст. – тяжкий парез: асиметрія в спокої, дисфункція при рухах;
IV ст. – параліч: атонія, повна втрата функції.
Шкала May окрім 5-ступеневої характеристики тяжкості дисфункції мімічних м’язів включає також етіологічний чинник та прогноз відновлення. Згідно із цією шкалою ІІ ст. (легкий парез) відображає неповне ураження нерва при паралічі Белла, герпетичному ураженні, отитах, переломах скроневої кістки, чудовий та добрий прогноз для відновлення.
ІІІ-V ст. (відповідно помірний, тяжкий або критичний парез із слабкістю, спазмами, синкінезіями) відображають повне пошкодження нерва, наприклад, на ґрунті травми, пухлини. Прогноз для відновлення при ІІІ ст. – відносно сприятливий, при ІV ст. – несприятливий (симетрія обличчя лише в спокої), при V ст. лікування неуспішне, мають місце стійкі залишкові явища.
Визначають наступні недоліки цих шкал: неможливість тонко відрізняти прояви дисфункції та зміни рухової функції при відновленні; недостатня надійність оцінки; ймовірність помилки дослідника; не враховуються вторинні дефекти.
Серед вітчизняних шкал найбільшої уваги заслуговує шкала Я.С. Балабана, згідно з якою наявні клінічні прояви аналізуються на основі 5-бальної оцінки, виходячи з того, що фізіологічна норма отримує максимальну кількість – 5 балів.
Оцінку 4 бали отримує стан, коли хворий може закрити око, насупити і підняти брови, наморщити чоло, проте з меншою силою, ніж на здоровій стороні; при оскалі видно 4-5 зубів, рот ледь помітно перетягується в здорову сторону; хворий надуває щоку, але з меншою силою, ніж з протилежної сторони; при електронейроміографічному (ЕНМГ) дослідженні кінцева латенція становить 4,5-5,0 мс.
Оцінка 3 бали – хворий може замружити око, але має місце позитивний симптом «вій»; може насупити і підняти брови, наморщити чоло, проте меншою мірою і з меншою силою, ніж на здоровій стороні, при цьому не може здолати опір дослідника. При оскалі видно 3-4 зуба; хворий погано складає губи для свисту й із затрудненням свистить; надуває щоку, але не може здолати опір дослідника. При ЕНМГ-дослідженні кінцева латенція 5,0-5,5 мс.
Оцінка 2 бали – око повністю не закривається – лагофтальм становить 1-2 мм; чоло хворий наморщує злегка, при спробі насупити брови відмічаються незначні рухи; при оскалі видно 2-3 зуба, надування щоки слабке; свистіти не може. При ЕНМГ-дослідженні кінцева латенція сягає 5,5-6,0 мс.
Оцінка в 1 бал виставляється, коли око повністю не закривається, лагофтальм становить 3-5 мм, пацієнт не може насупити і підняти брови, надути щоки і свистіти; при оскалі видно 1-2 зуба. При ЕНМГ-дослідженні кінцева латенція понад 6 мс.
Оцінка в 0 балів характеризує повний параліч мімічної мускулатури – хворий не закриває око (лагофтальм понад 5 мм), не може насупити і підняти брови, оскалити зуби, кут рота на стороні ураження нерухомий; пацієнт не може скласти губи для свисту, рот різко перекошений в здорову сторону. При стимуляційній ЕНМГ М-відповідь не викликається.
За шкалою Я.С. Балабана 3-4 бали відповідають легкому перебігу, 2 бали – середній тяжкості, 0-1 балів свідчать про тяжкий перебіг захворювання.
Валідність і об’єктивність шкали Я.С. Балабана суттєво підвищується визначенням і оцінкою показників стимуляційної ЕНМГ. Тут необхідно зауважити, що, за даними літератури та власних досліджень [16, 18, 19], нормалізація ЕНМГ-показників відбувається повільніше, ніж відновлення функції мімічних м’язів клінічно, що вимагає коректного співставлення їх динаміки та дещо затруднює використання шкали на етапах відновлення системи «лицевий нерв – мімічні м’язи».
Виділяють також групу так званих реґіонарних шкал, серед яких найбільш вживані шкали Smith, Yanagihara, Janssen’s, Sunnybrook.
Так, за шкалою Smith оцінюють функцію мімічної мускулатури у відсотках для кожної ділянки окремо, а саме – в спокої і рухову активність фронтального черевця фронто-окципітального м’яза, колових м’язів ока та рота. Зокрема, 0 ст. відповідає 0% функції, I ст. – 0-25%, II ст. – 25-50%, III ст. – 50-75%, IV ст. – 75-100%. Наступний крок цього методу – оцінку функції м’язів у відсотках переводять у бали – від 0 (відсутність функції) до 4 балів (норма) та вираховують середнє арифметичне із оцінок кожної частини.
За допомогою шкали Yanagihara оцінюють функцію мімічних м’язів за 10-ма параметрами, згідно з такими станами: в спокої, зморшки на чолі, мигання, легке змикання повік, щільне змикання повік, змикання ока лише на ураженій стороні, зморшки на носі, свист, посмішка, слабкість нижньої губи. Оцінка здійснюється в балах в наступному напрямку: 4 бали – норма, 3 – легкий парез, 2 – помірний парез, 1 – тяжкий парез, 0 – плегія.
Ця шкала є зручною для відображення функції мімічних м’язів у балах на етапах лікування.
Шкала Janssen’s дає можливість роздільно оцінити функцію мімічних м’язів окремих ділянок, зокрема, стан обличчя в спокої, рухову активність фронтального черевця фронто-окципітального м’яза, колових м’язів ока та рота у %. Наступний крок – % функції кожної зони множать на ваговий коефіцієнт, який становить 0,3 для обличчя в спокої, ока та рота і 0,1 для чола. Сумують % кожної із окремих ділянок та отримують сумарний результат.
Недоліками цих трьох шкал є те, що вони не враховують вторинні дефекти при невропатії лицевого нерва, досить високий рівень варіабельності результатів у різних дослідників, складність оцінки функції мімічних м’язів у %.
Оцінка функції системи «лицевий нерв – мімічні м’язи» за шкалою Sunnybrook Scale проводиться в 4 етапи:
• 1-й етап – оцінка мімічних м’язів в балах обличчя в спокої для ділянок ока, щоки, рота (0-2), бали сумуються, результат множиться на 5;
• 2-й етап – оцінка мімічних м’язів в балах (1-5) при довільних рухах, зокрема, рухи брови, легке змикання повік, посмішка, оскалювання, зморщування губ, бали сумуються, результат множиться на 4;
• 3-й етап – оцінка синкінезій при рухах брови, легкому змиканні повік, посмішці, оскалюванні, зморщуванні губ (0-3), бали сумуються;
• 4-й етап – від балу по шкалі довільних рухів віднімають бал оцінки обличчя в спокої та віднімають бал оцінки синкінезій. Проте ця шкала затратна щодо часу на виконання, а також має виражений ступінь суб’єктивності в оцінках.
Найбільш вживаною в практичному аспекті на сьогодні залишається шкала House-Brackmann, яка включає 5 рівнів оцінки дисфункції мімічних м’язів. Кожному рівню відповідають показники м’язової слабкості, симетричності, наявності синкінезій і контрактур мімічних м’язів [9, 15]:
І ступінь – нормальна функція всіх гілок;
ІІ ступінь – легка дисфункція:
а) легка слабкість, можливі незначні синкінезії;
б) обличчя в спокої симетричне, звичайний вираз;
в) незначні рухи брови, очна щілина повністю змикається при зусиллі;
г) незначна асиметрія рота;
ІІІ ступінь – помірна дисфункція:
а) очевидна, проте не спотворююча асиметрія;
б) невиражені синкінезії;
в) незначні рухи брів, очна щілина повністю змикається при зусиллі, легка асиметрія рота при максимальному зусиллі;
IV ступінь – дисфункція середньої тяжкості:
а) очевидна слабість чи спотворююча асиметрія;
б) рухи брови відсутні, очна щілина змикається неповністю;
в) асиметрія рота при максимальному зусиллі;
V ступінь – тяжка дисфункція:
а) ледь помітні рухи мімічних м’язів;
б) обличчя асиметричне в спокої;
VI ступінь – тотальний параліч.
В порівняльному аспекті шкала House-Brackmann видається найбільш оптимальною в комплексній оцінці вираженості прозопопарезів для пацієнтів в гострому періоді та при неповному відновленні функції лицевого нерва, коли в клінічній картині нерідко має місце розвиток патологічних синкінезій і контрактур мімічних м’язів [1].
Таким чином, використання шкал оцінки дисфункції системи «лицевий нерв – мімічні м’язи» дозволяє об’єктивізувати та уніфікувати результати досліджень, що суттєво підвищує їх валідність і можливість порівняльного аналізу, уніфікованого підходу до діагностики, оцінки ефективності лікування, реабілітації та прогнозу. Основними вимогами до «ідеальної» шкали клінічної оцінки ступеня ураження лицевого нерва, як витікає із розглянутих джерел, повинні бути: універсальність, відтворюваність та низька варіабельність отриманих результатів при використанні різними дослідниками; оцінка в балах статичних та динамічних параметрів функції мімічних м’язів; врахування регіонарної оцінки, оскільки волокна лицевого нерва уражаються нерівномірно, і дисфункція різних мімічних м’язів може мати різний ступінь вираженості; врахування вторинних дефектів; зручність використання, мінімальні затрати часу та коштів.
Враховуючи вищенаведене, при лікування невропатії лицевого нерва необхідно враховувати етіологію, тяжкість дисфункції мімічних м’язів та період захворювання.
Більшість методів лікування невропатії лицевого нерва є патогенетично спрямованими. Їх можна розділити на консервативні, серед яких виділяють медикаментозні, фізіотерапевтичні та оперативні. До оперативних методів лікування належать декомпресія, трансмастоїдальне шунтування з подальшим введенням медикаментів, зшивання нерва, вільна трансплантація, невротизація [5]. Останні три використовуються при травматичному пошкодженні, після оперативних втручань. Декомпресія застосовується при досить широкому спектрі невропатій лицевого нерва, в тому числі при паралічі Белла. За даними низки авторів, зниження амплітуди М-відповіді на 90% протягом перших 5-7 днів є показом до невідкладної декомпресії [5].
При консервативному лікуванні підхід має бути диференційованим залежно від періоду захворювання: гострий, ранній відновний (10-30 днів від початку захворювання), пізній відновний (30 днів – 6 місяців), період стійких резидуальних змін (понад 6 місяців).
В гострому періоді необхідно досягнути усунення набряку нерва і, таким чином, його компресії в каналі. З цією метою застосовують сечогінні препарати, нестероїдні протизапальні препарати та кортикостероїди [4, 5, 9], а також препарати, що впливають на судинну ланку (нікотинова кислота, дротаверин, теофілін, бенциклан, вінпоцетин) та покращують мікроциркуляцію (актовегін) [2, 5]. На ділянку виходу лицевого нерва можна призначати аплікацію дімексиду, здатного проникати глибоко в тканини і викликати протинабряковий, протизапальний і судинорозширювальний ефекти. Дискутабельним залишається питання доцільності застосування противірусної терапії, зокрема препаратів ацикловіру [27, 32, 33, 35, 41, 42, 44]. Так, проведені рандомізовані дослідження порівняльної ефективності лікування невропатії лицевого нерва із використанням кортикостероїдів та препаратів ацикловіру засвідчили, що використання кортикостероїдів, особливо у перші 48-72 години, підвищує можливість повного відновлення функції мімічних м’язів в терміни від 3 до 9 місяців. При використанні препаратів ацикловіру у монотерапії та в комбінації із кортикостероїдами не встановлено достовірної різниці порівняно із плацебо [35].
В ранньому відновному періоді продовжується терапія, спрямована на зменшення набряку, відновлення регіонарного кровотоку, а також на покращення провідності нерва. Відновлення регіонарного кровотоку досягається призначенням актовегіну, ефективність якого була підтверджена даними клінічних та ЕНМГ-досліджень, згідно з якими вона зростала при ранньому лікуванні і виявлялася скороченням термінів повного відновлення до 7-10 днів, що зумовлено антигіпоксантною, антиоксидантною дією, нормалізацією ендотелійзалежних реакцій і зниженням периферичного судинного опору, збільшенням вироблення ендотелієм власних антикоагулянтів та антиагрегантів [14]. Є дані про ефективність введення в схему лікування препарату альфа-ліпоєвої кислоти [2]. З метою відновлення невральної провідності використовують вітаміни групи В [5], антихолінестеразні препарати [2, 8]. Стосовно термінів застосування антихолінестеразних препаратів єдиної точки зору немає, проте від застосування прозерину поступово відмовляються, оскільки вважається, що це сприяє формуванню локальних гіпертонусів мімічних м’язів і, як наслідок, постпаралітичної контрактури [5]. За іншими даними, прозерин навпаки сприяє усуненню нервово-м’язового блоку [8]. Результатом таких розбіжностей стало подальше клінічне вивчення при невропатії лицевого нерва ефективності препаратів із антихолінестеразною дією, зокрема іпідакрину. Встановлено, що застосування іпідакрину в комплексному лікуванні невропатії лицевого нерва прискорює відновлення рухових функцій вдвічі, а в поєднанні із антиоксидантною терапією – у 2,5 рази. До того ж на відміну від прозерину іпідакрин не сприяє розвитку контрактур [2, 8]. Протягом всього відновного і навіть починаючи з кінця гострого періоду доцільним є застосування моніторингової електростимуляції мімічного нейро-моторного апарату, що сприяє вираженій позитивній динаміці денерваційно-ренерваційних процесів, як за даними клініко-неврологічного обстеження, так і за ЕНМГ-даними [8, 9].
На підставі проведеного на базі Івано-Франківської обласної дитячої клінічної лікарні дослідження 122 хворих з невропатією лицевого нерва нами запропоновано методику лікування цієї нозології у гострому періоді із включенням в схему терапії препаратів тіотриазоліну та нуклеотидів.
За способом лікування хворі були розподілені на 4 групи. 30 хворих І групи отримували стандартне лікування, яке проводилось згідно з додатком до наказу МОЗ № 502 від 28.12.2002 «Тимчасові нормативи надання медичної допомоги» за напрямом дитяча неврологія, у 31 хворого ІІ групи стандартна терапія поєднувалася із використанням вітчизняного препарату тіотриазолін у формі 2,5% розчину внутрішньом’язово протягом 10 днів. Хворим ІІІ групи (31 пацієнт) в схему терапії включали препарат нуклеотидів перорально по 1 капсулі двічі на добу протягом 20 днів. 30 хворих IV групи в комплексному лікуванні одночасно отримували препарати тіотриазолін та нуклеотиди.
За тяжкістю ураження системи «лицевий нерв – мімічні м’язи» у 12 (9,8%) дітей мала місце помірна дисфункція лицевого нерва – ІІІ ступінь за шкалою House-Brackmann, у 97 (79,5%) дітей – дисфункція середньої тяжкості – ІV ступінь за шкалою House-Brackmann, у 13 (10,7%) дітей – тяжка дисфункція – V ступінь за шкалою House-Brackmann.
В результаті проведеного лікування відмічалася позитивна клінічна динаміка у всіх обстежених: глибина прозопопарезу зменшувалася, проте його ступінь та швидкість відновлення функції мімічних м’язів відрізнялися у групах лікування. У І групі лікування 40,00% хворих були виписані з одужанням, у 60,00% випадків стаціонарне лікування було припинене для перерви, серед яких ступінь дисфункції мімічних м’язів на момент виписки відповідав рівню ІІ ступеня за шкалою House-Brackmann у 72,20%, ІІІ ступеня – у 16,70%, IV ступеня – у 11,10%. Середній термін стаціонарного лікування в цій групі становив 19,70±1,18 днів. При контрольному огляді через 2 тижні у 43,30% хворих констатовано повне відновлення функції мімічних м’язів. У 16,70% пацієнтів цієї групи перебіг захворювання набув затяжного характеру, було проведено повторні курси лікування. Надалі у 6,7% хворих сформувалася постневритична контрактура мімічних м’язів.
У ІІ групі 61,30% хворих були виписані з одужанням, у 38,70% випадків стаціонарне лікування було припинене для перерви, ступінь дисфункції мімічних м’язів на момент виписки відповідав ІІ ступеню за шкалою House-Brackmann. Середній термін стаціонарного лікування у цій групі становив 13,45±0,69 днів. На контрольному огляді через 2 тижні встановлено повне відновлення функції мімічних м’язів.
У ІІІ групі 48,40% хворих були виписані з одужанням, у 51,60% випадків стаціонарне лікування було припинене для перерви. У цих хворих дисфункція мімічних м’язів на момент виписки відповідала ІІ ступеню за шкалою House-Brackmann у 56,30% хворих, ІІІ ступеню – у 31,30%, IV ступеню – у 12,50%. Середній термін стаціонарного лікування в цій групі становив 20,77±1,15 днів. Серед виписаних з покращенням у 19,35% хворих функція мімічних м’язів відновилася повністю через 2 тижні після виписки, у 12,90% – через місяць. У 19,35% пацієнтів цієї групи перебіг захворювання набув затяжного характеру, було проведено повторні курси лікування. Надалі у 6,45% хворих сформувалася постневритична контрактура мімічних м’язів.
У IV групі повне відновлення мало місце у 63,30% хворих. У 36,70% випадків стаціонарне лікування було припинене для перерви, дисфункція мімічних м’язів на момент виписки відповідала ІІ ступеню за шкалою House-Brackmann. Середній термін стаціонарного лікування в цій групі становив 14,40±1,03 днів. У 20% дітей функція мімічних м’язів відновилася повністю через 2 тижні після виписки, у 13,37% – через місяць. У 1 пацієнта цієї групи (3,33%) перебіг захворювання набув затяжного характеру, було проведено повторний курс лікування, після якого функція мімічних м’язів відновилася повністю.
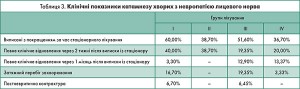
Загальна оцінка клінічної ефективності проведеного стаціонарного лікування хворих та даних катамнезу відображена в таблицях 2 та 3.
Отримані клінічні дані також підтверджені виявленими біохімічними змінами вмісту рівня лактату та пірувату у крові хворих з невропатією лицевого нерва, які корелювали із тяжкістю дисфункції мімічних м’язів. На початку лікування найбільш виражено лактат зростав при тяжкій дисфункції системи «лицевий нерв – мімічні м’язи» (V ступінь за House-Brackmann), виявлено прямий кореляційний зв’язок середньої сили між ступенем тяжкості прозопопарезу та рівнем лактату, про що свідчить значення коефіцієнту Пірсона + 0,35. Рівень пірувату на початку захворювання при тяжкому прозопарезі значно знижувався (табл. 4, 5), виявлено сильний прямий кореляційний зв’язок (коефіцієнт Пірсона + 0,82).
Зростання рівня лактату та низький рівень пірувату у хворих з невропатією лицевого нерва можна пояснити тим, що при дефіциті кисню глюкоза в більшій мірі перетворюється в лактат з утворенням 2 молекул АТФ замість 34 при метаболізмі в циклі Кребса. При довгостроковому утриманні анаеробних умов лактат не окислюється до пірувату через брак НАД. Отримані біохімічні зміни, особливо у взаємозв’язку із ступенем дисфункції лицевого нерва за шкалою House-Brackmann, свідчать про значну роль порушення окисно-відновних процесів у визначенні особливостей динаміки перебігу захворювання і ступеня дисфункції лицевого нерва.
На 14-й день лікування встановлено зниження вмісту лактату у всіх групах обстежених: у І групі на 60,9%, у ІІ – на 84%, у ІІІ – на 61,9%, у IV – на 87,5%, проте у І та ІІІ групах рівня достовірності досягнуто не було. Рівень пірувату зростав у І групі на 8,7%, у ІІ – на 22,6%, у ІІІ – на 9,6%, у IV – на 18,1%, достовірними ці зміни були у ІІ та ІV групах (табл. 6, 7).
Отже, виявлено значне зниження рівня молочної кислоти та зростання пірувату, особливо у хворих, які отримували тіотриазолін, що свідчить про його виражений вплив на окисно-відновні процеси, одним із механізмів реалізації якого є активації лактатдегідрогеназної реакції, внаслідок чого лактат трансформується в необхідний для гліколізу піруват і рівень його знижується, що приводить до зменшення явищ набряку і ацидозу, важливих патогенетичних ланок в розвитку невропатії лицевого нерва.
Отримані результати є підставою для включення в комплексну терапію невропатії лицевого нерва тіотриазоліну, який при ішемічному ушкодженні тканин нормалізує утилізацію запасів глюкози й глікогену в клітині, активність глюкозо‑6-фосфатдегідрогенази, підвищує співвідношення НАД/НАДН та активність цитохром-С-оксидази, збільшує рівень пірувату, одночасно зменшуючи гіперпродукцію лактату. Позитивно впливаючи на утилізацію відновлених форм піридиннуклеотидів, тіотриазолін значно гальмує шляхи утворення активних форм кисню та активує окислювальне фосфорилювання зі збільшенням утворення АТФ. Захисна дія тіотриазоліну при ішемії реалізується шляхом активації малат-аспартатного «човникового» механізму, що забезпечує протонами електронно-транспортний ланцюг. В ішемізованих клітинах і тканинах тіотриазолін суттєво гальмує процес накопичення вільних амінокислот, збільшує рівень РНК, активізує процес протеїнового синтезу, що вказує на ініціювання реакцій адаптації в клітинах, які забезпечують перебудову метаболізму в тканині в умовах гіпоксії без підвищення потреби в кисні та утворення вільних радикалів.
Практичне значення методики підтверджено отриманими патентами України на корисну модель [12, 13], а також інформаційним листом (Інформаційний лист № 381-2012 / М.І. Пітик, І.І. Ліскевич. Оптимізація комплексного лікування невропатії лицевого нерва у дітей та підлітків. – Київ: Укрмедпатентінформ МОЗ України. – 4 с.).
Найважчим в плані нейрореабілітації є період резидуальних змін, оскільки можливості відновлення функції нерва в цьому періоді практично вичерпані. В цьому періоді рекомендовано оперативне усунення косметичного дефекту при повній відсутності ефекту відновного лікування або реабілітація за індивідуальною відновною програмою при частковому відновленні, яка розрахована в середньому на 14 днів і включає препарати групи міорелаксантів (толперизон, баклофен), в тому числі методом ультрафонофорезу, карбамазепін, а також немедикаментозні методи лікування, зокрема тренування методом електроміографічного зворотного зв’язку, лазеро-магнітна терапія, постізометрична релаксація за методом Г.А. Іваничева [2, 5]. Слід зазначити, що в гострому періоді відновлення йде за рахунок покращення невральної провідності, а в періоді резидуальних змін – за рахунок покращення кровопостачання мімічних м’язів, зниження збудливості м’язових рецепторів, що веде до зменшення м’язових контрактур.
Що стосується фізіотерапевтичних методів, які є невід’ємною складовою відновного лікування невропатії лицевого нерва, то їх застосовують з 7-10-го дня захворювання: УВЧ в нетеплових і слабкотеплових дозуваннях на завушну ділянку, електромагнітні коливання, магнітотерапію змінним і постійним магнітним полем, лазеротерапію, масаж, фонофорез з гідрокортизоном, електрофорез з еуфіліном, дибазолом, карипазимом за Бергон’є, ЛФК, гіпербаричну оксигенацію, фотохромотерапію, голкорефлексотерапію, гірудотерапію, озонотерапію, ДЕНС-терапію, локальну гіпотермію [2, 8]. У відновному періоді рекомендують масаж, ЛФК, рефлексотерапію, фонофорез лідази, грязелікування, гірудотерапію, акупунктуру, гіпербаричну оксигенацію. При ранніх клінічних ознаках формування контрактури стимулюючі види фізіотерапії відміняють, окрім електрофорезу із міорелаксантами. На санаторно-курортному етапі рекомендують грязелікування та бальнеопроцедури із міцними хлоридно-натрієвими, йодо-бромними та радоновими водами [1, 8]. В пізньому відновному періоді перебіг невропатії лицевого нерва часто ускладнюється розвитком постпаралітичної контрактури, частота виникнення якої становить 16-32% випадків [1, 4, 8]. Тому актуальним є пошук методики лікування, яка, з одного боку, не викликає переродження тканин обличчя, а з іншого – забезпечує достатній лікувальний ефект при ускладненому перебігу невропатії лицевого нерва. Такою методикою є поєднане застосування низькоінтенсивного інфрачервоного випромінювання, яке покращує мікроциркуляцію і стимулює репаративні процеси в тканинах, і локальної гіпотермії за типом кріомасажу, що має знеболювальний, протизапальний і вазотропний ефекти. При цьому для визначення початкових ознак контрактури мімічних м’язів можна використовувати метод термографії обличчя. Протягом останніх кількох років з’явилися нові напрацювання з використанням препарату ботулотоксину з метою усунення контрактур на ураженій стороні та гіпертонусу м’язів обличчя на здоровій стороні, оскільки останні поглиблюють асиметрію обличчя [4, 24].
В поглядах на використання електростимуляції також немає однозначності щодо термінів її застосування та поглядів стосовно її сприяння для розвитку контрактури. Частина досліджень доводять, що застосування диференційованої електростимуляції в комплексному лікуванні невропатії лицевого нерва є патогенетично обґрунтованим і ефективним методом відновлення рухових функцій на основі стимуляції регенерації та ремієлінізації нервових волокон лицевого нерва, відновлення провідності нервовими волокнами та електрозбудливості нейром’язового апарату, покращення тканинної трофіки та кровообігу [22]. Повідомлялося про ефективне застосування динамічної електронейростимуляції, причому чим раніше був розпочатий курс лікування, тим раніше вдавалося досягти позитивної динаміки.
На різних етапах лікування може застосовуватися рефлексотерапія, яка є сумісною з більшістю інших методів. Її суттєвою перевагою є можливість застосування в гострому періоді. Висока ефективність цього методу зумовлена позитивним впливом на мікроциркуляцію, ішемію, гіпоксію нерва, порушення тканинного метаболізму, а також міорелаксуючою, міотонізуючою, аналгезуючою, седативною, імуномодулюючою дією.
Список літератури знаходиться в редакції.