10 травня, 2016
Алфлутоп у лікуванні больових синдромів в області спини
Больові синдроми в області спини (БСВОС) наразі є однією з найбільш частих причин звернення за медичною допомогою. Протягом життя БСВОС зустрічаються в 70-90% населення [1, 2]. При цьому майже в половині випадків біль рецидивує, а його хронізація відбувається у кожного 5-го мешканця Європи [3-5].
В етіологічній структурі БСВОС провідна роль належить патології м’язів і міофасціальним синдромам, однак важливим підґрунтям для хронізації больової симптоматики є прогресування дегенеративних змін у хребцево-рухових сегментах.
Остеохондроз хребта (грецьк. osteon – кістка і chondros – хрящ) вважається дистрофічним захворюванням, що характеризується переважним ураженням міжхребцевих дисків; може супроводжуватися розростанням остеофітів, артрозом міжхребцевих суглобів, протрузіями і грижами диска, їх секвестрацією з компресією корінців спинномозкових нервів, спинного мозку і його оболонок, залученням у патологічний процес зв’язок, фасцій і сухожилків м’язів [1, 6].
Сьогодні погляди на вертебральні дегенеративні процеси дещо змінились: остеохондроз розглядають у контексті природних процесів старіння людини, які починаються з моменту її народження. Надмірна дегенерація структур хребцево-рухових сегментів супроводжується появою клінічних симптомів нейронрефлекторного, компресійно-ішемічного і дистрофічного характеру. Причинами цього можуть бути травми хребта, надмірні виробничі і спортивні навантаження, часті загострення вісцеральної патології, емоційні розлади, що супроводжуються тривалим м’язово-тонічним напруженням; запальні процеси в суглобах хребта локального та системного характеру, порушення обміну речовин, а також захворювання, асоційовані з перерозподілом навантаження на хребет і суглоби (вроджені і набуті деформації останніх, спондилолістез, плоскостопість та ін.). Так, останнім часом у патогенезі клінічних проявів остеохондрозу хребта багато уваги приділяється саме ролі запальних процесів у грудній і черевній порожнинах, органах малого таза. Унаслідок запалення та періодичних загострень вісцеральної патології іритація по аферентних провідниках тривалий час передається у відповідні сегменти спинного мозку і викликає рефлекторний спазм сегментарних м’язів, а також, передаючись на синувертебральний нерв, порушує трофічну іннервацію окістя хребцевого каналу, зв’язок і відповідного міжхребцевого диска. Унаслідок цього порушується трофіка диска, він втрачає рідину і пружно-еластичні властивості. При цьому відбуваються деформація і стоншення фіброзного кільця, а також втрата гідрофільності пульпозним ядром. Розриви волокон фіброзного кільця, причина так званих прострілів, супроводжуються утворенням протрузій – випинань пульпозного ядра за межі тіл хребців <5 мм для поперекового і <2 мм для шийного відділів хребта. У подальшому за наявності осьових і радіальних навантажень та збереження причин прискореної дегенерації в дегідратованому фіброзному кільці збільшуються кількість і глибина розривів з наступною секвестрацією і випадінням мас зміненого пульпозного ядра в просвіт спино-мозкового каналу та міжхребцевого отвору. Частіше кили міжхребцевих дисків розташовуються в найбільш слабкому задньобоковому (дорзо-латеральному) відділі фіброзного кільця з відповідною компресією корінців спинномозкових нервів, кровоносних судин, простору спинномозкового каналу та його вмісту. Зміни в міжхребцевих дисках супроводжуються дистрофічними і запальними процесами в дуговідросткових суглобах, зв’язках хребта, сухожилках м’язів та ін. (фасетковий синдром, ентезити, лігаментити, спондиліт та ін.) [6].
Персистенція клінічно розгорнутої або навіть субпорогової тривоги викликає генералізацію м’язово-тонічного напруження, унаслідок чого потужні м’язи хребта зміщують хребці по відношенню один до одного в тих хребцево-рухових сегментах, структури яких дегенерували найбільш сильно та створили умови для розвитку нестабільності.
Насправді етіопатогенетичні механізми дегенеративних процесів у хребцево-рухових сегментах при остеохондрозі хребта набагато складніші і супроводжуються розвитком запальних, ішемічно-набрякових і, досить часто, аутоімунних процесів. Однією з ключових позицій у патогенезі дегенеративно-
дистрофічних уражень міжхребцевих дисків є так звана хондроїтинсульфатна теорія, згідно з якою в тканинах дисків знижується кількість хондроїтинсульфату при відносному зростанні кератансульфату і глікопротеїну, зменшується кількість сірки і здатність до її засвоєння. Це, у свою чергу, призводить до втрати сполучнотканинним матриксом пружно-еластичних властивостей, зниження активності хондроцитів та порушення регенеративних можливостей хрящової тканини.
Традиційно консервативне лікування проводять за допомогою методів, спрямованих на усунення больового синдрому, порушень функції спинномозкових корінців і попередження прогресування дистрофічних змін у структурах хребта. Важливо відзначити, що відповідно до сучасної нормативної бази в терапії БСВОС, спричинених диско-радикулярним конфліктом, вважається недоцільним використання режиму обмеженої рухової активності. Комплексна консервативна терапія проводиться на тлі зниження осьових навантажень на хребет і включає застосування протезно-ортопедичних засобів, фізіотерапевтичних процедур і лікарських препаратів з метою розслаблення м’язів, усунення набряку, запалення і болю. За наявності сегментарних неврологічних симптомів випадіння використовують препарати регенеративної спрямованості (α-ліпоєву кислоту, нуклеотиди, комплекси вітамінів групи В) та антихолінестеразні засоби.
Сьогодні в комплексній схемі лікування БСВОС важливе значення надається хондропротекторній терапії [7, 8]. У схемах лікування дегенеративних захворювань опорно-рухового апарату хондропротекторні засоби віднесені до групи SYSADOA (Symptomatic slow acting drugs for osteoarthritis) – симптоматичних засобів уповільненої дії, ефективність яких у терапії ноцицептивних больових синдромів, за даними останніх метааналізів, характеризується рівнем доказів ІА-В. Дослідження останніх років, виконані з урахуванням сучасних вимог доказової медицини, довели наявність у хондропротекторів не тільки позитивної симптоматичної дії, а й здатності змінювати перебіг захворювання у разі застосування їх як засобів базисної (хворобомодифікуючої) терапії [9, 10].
Перспективність групи SYSADOA в лікуванні дегенеративно-запальних захворювань хребта і суглобів полягає у відсутності значної кількості гастроінтестінальних і кардіоваскулярних ускладнень, що супроводжують тривале використання нестероїдних (НПЗП) і стероїдних протизапальних препаратів. На відміну від них хондропротектори позитивно впливають на регенеративні властивості хрящової тканини.
Одним з найвідоміших ін’єкційних представників групи SYSADOA є Алфлутоп – очищена, знежирена і позбавлена білків витяжка з 4 видів морських риб, що містить мукополісахариди, кальцій, магній, мідь, цинк, залізо, калій, деякі амінокислоти, дерматансульфат і пептиди. Головні складові Алфлутопу – хондроїтинсульфат, глюкуронова кислота і протеоглікани. Це базисні речовини, що забезпечують компенсацію дефіциту глікозаміногліканів, захист хряща від дегенерації та виявляють протизапальну і вторинну знеболювальну дію.
Відомо, що біодоступність ін’єкційних форм істотно вища за таку пероральних. Так, для глюкозаміну сульфату вона становить 26% при пероральному прийомі і 95% при парентеральному. Пероральна біодоступність хондроїтинсульфату дорівнює лише 13% [11, 12]. Ін’єкційні форми хондропротекторів є універсальними і можуть використовуватися як у рамках ініціальної терапії для індукції ремісії, так і для системного лікування захворювання. За даним літератури, паравертебральне введення Алфлутопу при захворюваннях, що супроводжувалися болем у нижній частині спини, дозволило суттєво скоротити терміни перебування хворих у стаціонарі, зменшити дози нестероїдних та стероїдних аналгетиків, а також пришвидшити відновлення рухової активності і покращити якість життя пацієнтів.
Метою нашого дослідження було вивчити ефективність і безпеку застосування Алфлутопу в лікуванні хворих із БСВОС, спричиненим дегенеративно-дистрофічними та запальними процесами в міжхребцевих дисках, унко-вертебральних суглобах, зв’язках, фасціях і сухожилках м’язів.
Матеріали та методи
Обстежено пацієнтів (n=42) з різноманітними проявами остеохондрозу попереково-крижового відділу хребта: 25 чоловіків і 17 жінок віком від 37 до 62 років. Тривалість захворювання в більшості учасників перевищувала 5 років. Лікування здійснювалося відповідно до клінічного протоколу надання медичної допомоги хворим на дорсалгію (МКХ‑10: М 54), затвердженого наказом МОЗ України від 17.08.2007 р. № 487, і включало використання НПЗП, міорелаксантів, комплексів вітамінів групи В, протинабрякових препаратів, седативних засобів та місцевої терапії в гострий період хвороби. Хворі розподілялися на 2 групи по 21 особі в кожній: учасники основної разом із вищеописаним комплексним лікуванням отримували Алфлутоп, натомість пацієнти контрольної – лише комплексну терапію. Афлутоп призначався внутрішньом’язово паравертебрально в дозі 1,0 мл 1 р/день у ділянку найбільшої пальпаторної болючості курсом 10-12 ін’єкцій. Під час перебування в стаціонарі (10-12 днів) уникали призначень антиконвульсантів, місцевих анестетиків та кортикостероїдних препаратів.
Серед супутніх захворювань переважала в основному судинна патологія: дисциркуляторна енцефалопатія І-ІІ ст., гіпертонічна хвороба I-II ст., ішемічна хвороба серця. Рідше зустрічалися захворювання органів травлення: хронічний холецистит, панкреатит, стеатогепатит. У 2 пацієнтів було вперше виявлено цукровий діабет.
Для підтвердження діагнозу та вивчення стану попереково-крижового відділу хребта використовували рентгенографію, комп’ютерну і магнітно-резонансну томографію. Моніторинг стану хворих здійснювався шляхом контролю неврологічного та соматичного статусу, а також за допомогою рутинних методів лабораторно-інструментального обстеження.
Для оцінки больового синдрому послуговувалися візуальною аналоговою шкалою (ВАШ) від 1 до 10 см, модифікацією вербальної оціночної шкали, яку застосовували для оцінки загального стану пацієнтів, ефективності і переносимості лікування. Больові відчуття за ВАШ та вербальною шкалою оцінювалися як хворим, так і лікарем [13]. Використовуючи спеціальну ортопедичну лінійку, кількісно визначали вираженість симптому натягу Ласега: вимірювали кут між випрямленою ногою хворого під час появи або посилення больових відчуттів і горизонтальною площиною. Також оцінювали ступінь рефлекторного сколіозу, м’язового дефансу, об’єму рухів в ураженій ділянці.
Регіональний кровообіг поперекової області вивчали методом реолюмбографії, який згідно із стандартною методикою виконували на реоаналізаторі РА5-01. Оцінювали показники пульсового кровонаповнення – амплітуду реограми (АРГ) та реографічний показник (РП).
Критеріями виключення були гострі (не пов’язані з патологією опорно-рухового апарату) захворювання, вагітність, важкі функціональні ураження печінки та нирок, а також алергія до тестованого препарату. Точкою контролю був стан пацієнтів у 1-й та 10-й день перебування в стаціонарі.
Статистичну обробку цифрового матеріалу виконували за допомогою комп’ютерної програми Excel for Windows з обчисленням середніх значень показників (М) та похибок (m) для однорідних груп. Оцінку розбіжностей середніх значень проводили з використанням критерію Ст’юдента (t). При значенні р<0,05 відмінності вважали достовірними.
Результати та обговорення
На підставі клініко-неврологічного та інструментального методів обстеження у 18 (42,9%) пацієнтів діагностовано люмбалгію та люмбоішіалгію; у 24 (57,1%) – дискогенну радикулопатію з ураженням корінців L3-S1. У 37 хворих (88,1%) за результатами візуалізаційних досліджень були виявлені грижі міжхребцевих дисків L3-L4, L4-L5, L5-S1 без компресії простору і структур спинномозкового каналу.
Усі хворі страждали від больового синдрому різної інтенсивності, що значно обмежував їхню рухову активність. У спокої стан більшості пацієнтів покращувався, однак у 21 (50%) хворого зберігався тупий біль. Унаслідок больового синдрому в учасників погіршувався сон, спостерігалися порушення тривожно-депресивного спектра. Корінцевий синдром характеризувався розвитком порушень чутливості, слабкістю розгиначів пальців стопи (частіше великого пальця), гіпотрофією м’язів стегна і гомілки (в 11,9% пацієнтів). У 7 (16,7%) хворих спостерігалось оживлення колінного рефлексу, у 8 (19%) – зниження цього показника. У 19 (45,2%) пацієнтів мало місце зниження ахіллового рефлексу. У 10 (23,8%) хворих визначено гіперестезію больової чутливості в сегментах L3-S1, у 14 (33,3%) – гіпостезію. Об’єм активних рухів у поперековому відділі хребта був значно обмежений у більшості хворих. Спостерігалися виражений рефлекторний сколіоз, м’язовий дефанс, болісність при пальпації паравертебральних точок. У 83,3% обстежених визначалися симптоми натягу.
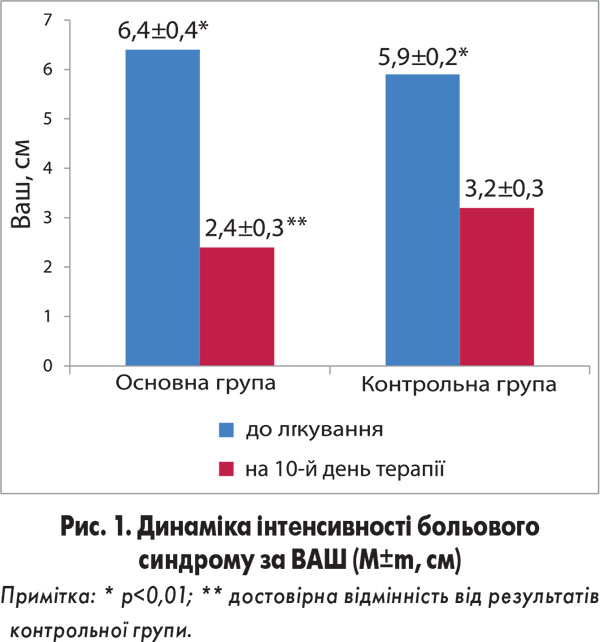
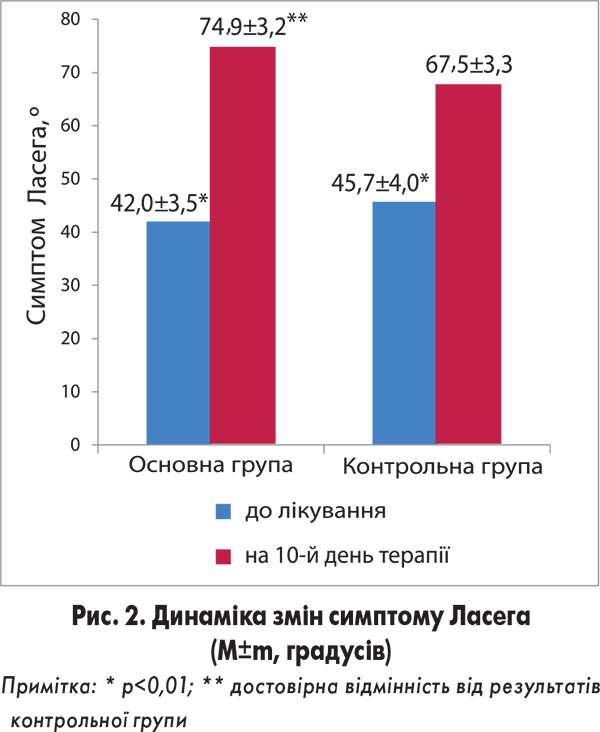
Унаслідок проведеного лікування в учасників дослідження зменшилася вираженість больової симптоматики та м’язового дефансу, збільшився об’єм рухів у поперековому відділі хребта та знизилася болючість паравертебральних м’язів. Регрес корінцевої симптоматики проявлявся зменшенням площі сенсорних розладів та інтенсивності симптомів натягу, збільшенням сили і відновленням функцій паретичних м’язів. Результати клініко-неврологічного обстеження до початку лікування та на 10-й день терапії представлені на рисунках 1 і 2.
Наведені на рисунках 1 і 2 дані демонструють статистично значиму ефективність терапевтичних комплексів, застосованих у лікуванні вертеброгенних БСВОС. Так, в обох групах відмічалися достовірне зниження інтенсивності больового синдрому за ВАШ і значне зменшення симптому натягу Ласега (збільшення кута підйому кінцівки). При цьому ступінь регресу больової симптоматики в пацієнтів основної групі виявився достовірно більшим, ніж в учасників групи контролю: зростання середніх значень показників ВАШ 4,0±0,5 і 2,7±0,4 см відповідно (р<0,05). Редукція симптому Ласега також була достовірно більшою в основній групі: збільшення кута підйому нижньої кінцівки в основній групі хворих становило 32,9±4,1°, натомість у пацієнтів групи контролю – 21,8±4,5° (р<0,01).
Зафіксована досить висока частка позитивних оцінок ефективності проведеного лікування як серед пацієнтів, так і серед лікарів – відповідно 79,0±6,4 і 80,9±5,9% в основній групі і 77,2±6,2 і 79,7±5,3% у контрольній. Однак статистично значимих відмінностей між групами порівняння за цими показниками отримано не було.
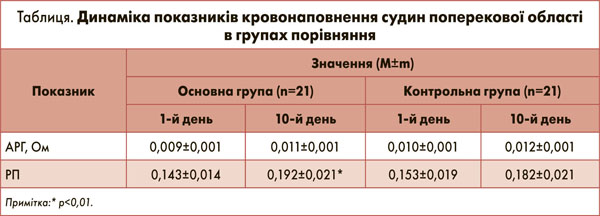
За результатами реолюмбографії було виявлено порушення гемодинаміки поперекової зони спини у вигляді зниження її кровонаповнення, на що вказували низькі значення показників АРГ та РП, динаміку яких до початку лікування та на 10-й день терапії представлено в таблиці.
Як видно з представленої таблиці, в учасників основної групі спостерігалося достовірне покращення кровонаповнення поперекової області за показником РП, приріст якого дорівнював 0,048±0,008 одиниць, у той час як у пацієнтів групи контролю – 0,028±0,01 (р<0,05).
Слід відмітити, що під час лікування у 3 (14,3%) хворих основної групи і 3 (14,3%) пацієнтів групи контролю були зареєстровані побічні явища у вигляді алергічних реакцій системного та місцевого характеру, підвищення температури тіла та артеріального тиску. Однак встановити зв’язок побічних реакцій з прийомом тестованого препарату в представленому дослідженні не вдалось, оскільки місцевої реакції на паравертебральне введення Алфлутопу в цих хворих виявлено не було.
Таким чином, результати проведеного дослідження демонструють більш високу ефективність терапевтичного комплексу, підсиленого натуральним ін’єкційним хондропротекторним засобом Алфлутоп, у лікуванні вертеброгенних БСВОС і дозволяють нам сформулювати такі висновки.
Висновки
1. Паравертебральне внутрішньом’язове введення натурального хондропротекторного препарату Алфлутоп достовірно підсилює ефективність терапевтичних комплексів, що застосовуються для лікування вертеброгенних БСВОС.
2. Важливим плейотропним ефектом Алфлутопу є здатність підвищувати гемодинаміку поперекової зони, що сприяє покращенню трофічних і репаративних процесів в уражених структурах хребцево-рухових сегментів і може бути однією з причин більш значимого регресу клінічної симптоматики.
Список літератури знаходиться в редакції.
P. S. Доповідь кандидата медичних наук С. Г. Сови під назвою «Біль у нижній частині спини: способи ефективного лікування» була представлена в рамках Winter Pain School (25-27 лютого, м. Яремче).
Медична газета «Здоров’я України 21 сторіччя» № 7 (380), квітень 2016 р.